桑黃子實(shí)體中多酚含量測(cè)定的方法學(xué)研究
孫雨晴,吳偉杰,鐘石,霍進(jìn)喜,朱儉勛,郜海燕,李有貴*
(浙江省農(nóng)業(yè)科學(xué)院 a蠶桑與茶葉研究所,b食品研究所,浙江 杭州 310021)
桑黃是寄生于桑樹(shù)等闊葉樹(shù)上的大型真菌,具有抗炎、抗腫瘤、調(diào)節(jié)免疫等多種功效[1-8]。多酚是其發(fā)揮抗炎、抗腫瘤活性的重要活性成分[8-10],因此,多酚含量是桑黃品質(zhì)及藥用價(jià)值的重要指標(biāo)。但是不同的提取和測(cè)定方法測(cè)得的桑黃多酚含量差異較大[10-11],導(dǎo)致桑黃品質(zhì)好壞的判定標(biāo)準(zhǔn)不統(tǒng)一,不同研究間的結(jié)果也難以相互比較。目前桑黃沒(méi)有收入藥典,前人對(duì)其多酚含量的測(cè)定多直接參照其他中藥材,缺乏針對(duì)桑黃本身的多酚測(cè)定方法學(xué)研究。本研究在參考前人研究方法的基礎(chǔ)之上,采用單因素考察實(shí)驗(yàn),逐一確定桑黃多酚的最佳提取方法,然后考察該提取測(cè)定方法的精密度、重復(fù)性、回收率、中間精密度等參數(shù),最后利用該方法測(cè)定浙江地區(qū)不同來(lái)源的桑黃樣品多酚含量,為桑黃的多酚含量測(cè)定提供方法依據(jù)和參考。
1 材料與方法
1.1 材料
桑黃子實(shí)體樣品由海寧宏欣農(nóng)業(yè)生物科技公司、浙江千濟(jì)方醫(yī)藥科技公司、淳安千島湖桑都食用菌合作社提供。其中桑黃多酚提取方法優(yōu)化研究中所用桑黃樣品均為海寧宏欣農(nóng)業(yè)生物科技公司提供。
ML-204分析天平(METTLER-TOLEDO,上海),HH-6恒溫水浴鍋(晶玻實(shí)驗(yàn)儀器公司),KQ-250E型超聲波清洗器(昆山超聲儀器有限公司),Cary60紫外-可見(jiàn)分光光度計(jì)(Agilent公司,美國(guó)),UV-2800紫外可見(jiàn)分光光度計(jì)(尤尼柯(上海)儀器有限公司,上海)。
沒(méi)食子酸(批號(hào):C12504577,純度99%)購(gòu)于上海麥克林生化科技有限公司,甲醇(分析純)購(gòu)于上海凌峰化學(xué)試劑有限公司,乙醇(分析純)購(gòu)于國(guó)藥集團(tuán)化學(xué)試劑有限公司,磷鉬鎢酸(分析純)購(gòu)于北京華科盛精細(xì)化工產(chǎn)品貿(mào)易有限公司,碳酸鈉(分析純)購(gòu)于蘭溪市屹達(dá)化工試劑有限公司。
1.2 方法
1.2.1 對(duì)照品溶液的制備
精密稱(chēng)取沒(méi)食子酸對(duì)照品50 mg,置于100 mL棕色量瓶中,加水溶解并稀釋至刻度,精密量取5 mL,置于50 mL棕色量瓶中,用水稀釋至刻度,搖勻。
1.2.2 標(biāo)準(zhǔn)曲線的繪制
精密量取對(duì)照品溶液0.5、1.0、2.0、3.0、4.0、5.0、6.0、7.0 mL,分別置25 mL棕色量瓶中,各加入磷鉬鎢酸試液l mL,再分別加水11.5、11、10、9、8、7、6、5 mL,用29%碳酸鈉溶液稀釋至刻度,搖勻,放置30 min,以相應(yīng)的試劑為空白,參照紫外-可見(jiàn)分光光度法,在760 nm的波長(zhǎng)處測(cè)定吸光度,以吸光度為縱坐標(biāo),濃度為橫坐標(biāo),繪制標(biāo)準(zhǔn)曲線。
1.2.3 供試品溶液的制備
在提取方法的考察實(shí)驗(yàn)中,供試品溶液采用不同考察方法下的操作步驟制備。最優(yōu)提取方法建立后,精密度、重復(fù)性、回收率、中間精密度以及不同樣品含量測(cè)定均采用所建立最優(yōu)提取方法制備。
1.2.4 供試品多酚含量的測(cè)定
精密量取供試品溶液2 mL,置25 mL棕色量瓶中,加入磷鉬鎢酸試液1 mL,加水10 mL,用29%碳酸鈉溶液稀釋至刻度,搖勻,放置30 min,離心,取上清液,以相應(yīng)的試劑為空白,在760 nm的波長(zhǎng)處測(cè)定吸光度。從標(biāo)準(zhǔn)曲線中讀出供試品溶液中沒(méi)食子酸的濃度,計(jì)算,即得。供試品溶液的多酚濃度超出標(biāo)準(zhǔn)曲線線性范圍時(shí),應(yīng)稀釋后再測(cè)。
1.2.5 粉碎粒度考察
取分別過(guò)三號(hào)篩、四號(hào)篩的粉末約1 g,精密稱(chēng)定,置錐形瓶中,加甲醇100 mL,稱(chēng)定質(zhì)量,超聲處理30 min,放冷,再稱(chēng)定質(zhì)量,用甲醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液2 mL,置10 mL量瓶中,用甲醇稀釋至刻度,搖勻,即得供試品溶液。按照1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.6 提取溶劑考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,分別加入水、50%乙醇、50%甲醇、甲醇100 mL,稱(chēng)定質(zhì)量,超聲處理30 min,放冷,再稱(chēng)定質(zhì)量,用相應(yīng)溶劑補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液2 mL,置10 mL量瓶中,用相應(yīng)溶劑稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.7 提取方式考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,加入50%乙醇100 mL,稱(chēng)定質(zhì)量,分別超聲處理30 min、70 ℃水浴回流1 h,冷卻,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液2 mL,置10 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.8 液料比考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,分別加入50%乙醇100、150、200 mL,稱(chēng)定質(zhì)量,70 ℃水浴回流1 h,放冷,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),分別精密量取濾液2、3、4 mL(對(duì)應(yīng)溶劑量,使最后濃度一致),置10 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.9 提取時(shí)間考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,加入50%乙醇100 mL,稱(chēng)定質(zhì)量,分別加熱回流1、2、3、4、5 h,冷卻,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液2 mL,置10 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.10 精密度考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,加入50%乙醇100 mL,稱(chēng)定質(zhì)量,加熱回流3 h,放冷,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液10 mL,置50 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。精密量取同一供試品溶液2 mL 6份,按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.11 重復(fù)性考察
取過(guò)三號(hào)篩的樣品粉末約1 g,精密稱(chēng)定,置錐形瓶中,加入50%乙醇100 mL,稱(chēng)定質(zhì)量,加熱回流3 h,放冷,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取續(xù)濾液2 mL,置10 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.12 回收率考察
取過(guò)三號(hào)篩的樣品粉末約0.5 g,精密稱(chēng)定,置錐形瓶中,加入一定量的沒(méi)食子酸(分別相當(dāng)0.5 g樣品含量的80%、100%、120%,各平行操作3份),加入50%乙醇100 mL,稱(chēng)定質(zhì)量,加熱回流3 h,放冷,再稱(chēng)定質(zhì)量,用50%乙醇補(bǔ)足減失的質(zhì)量,搖勻,濾過(guò),精密量取濾液2 mL,置10 mL量瓶中,用50%乙醇稀釋至刻度,搖勻,即得供試品溶液。按照方法1.2.4節(jié)供試品多酚含量的測(cè)定方法測(cè)定多酚含量。
1.2.13 中間精密度考察
由不同實(shí)驗(yàn)人員于不同時(shí)間取本品粉末約1 g,按重復(fù)性考察實(shí)驗(yàn),平行操作6份,分別于不同儀器上測(cè)定。
1.3 10批桑黃樣品的測(cè)定
按照重復(fù)性考察的方法,測(cè)定10批不同生產(chǎn)廠家的桑黃產(chǎn)品多酚含量,每個(gè)樣品平行操作2份。
2 結(jié)果與討論
2.1 標(biāo)準(zhǔn)曲線
標(biāo)準(zhǔn)曲線的回歸方程為y=3.379x+0.034 2,R=0.999 8,表明沒(méi)食子酸在25~350 μg線性關(guān)系良好。
2.2 粉碎粒度
通過(guò)三號(hào)篩粉末提取所測(cè)得的多酚含量為2.99%,通過(guò)四號(hào)篩的粉末所測(cè)得的多酚含量為2.74%,因此,選擇多酚含量更高的三號(hào)篩。
2.3 提取溶劑
結(jié)果表明,水、50%乙醇、50%甲醇、甲醇提取所測(cè)得的多酚含量分別為0.72%、5.48%、4.76%、3.26%,以50%乙醇為溶劑的提取效率顯著高于其他溶劑,所以選取50%乙醇作為提取溶劑。
2.4 提取方式
常溫超聲處理所測(cè)得的多酚含量為5.61%,70 ℃水浴回流處理所測(cè)得的多酚含量為7.38%,70 ℃回流處理的多酚含量顯著高于超聲處理,所以選取70 ℃水浴回流處理作為提取方式。
2.5 液料比
提取1 g桑黃樣品加入提取溶劑100、150、200 mL所測(cè)得多酚的含量分別為7.37%、7.38%、7.39%,提取溶劑用量對(duì)提取效率的影響差異并不顯著,因此,選用更加節(jié)省溶劑的100 mL作為提取溶劑的體積,即料液比為1∶100。
2.6 提取時(shí)間
提取時(shí)間1、2、3、4、5 h所測(cè)得多酚的含量分別為7.37%、7.67%、8.32%、8.35%、8.35%,提取效率到3 h以后變化不大,因此,選擇3 h作為提取時(shí)間。
2.7 精密度
在單因素考察提取方法后,確定了桑黃粉碎粒度為過(guò)三號(hào)篩、1 g桑黃粉加入100 mL 50%乙醇水浴加熱回流3 h的桑黃多酚提取方法。在該提取方法下提取的供試品溶液,經(jīng)磷鉬鎢酸顯色法測(cè)定6次,多酚含量分別為8.29%、8.27%、8.27%、8.41%、8.38%、8.27%,相對(duì)標(biāo)準(zhǔn)偏差(RSD)為0.76%,表明磷鉬鎢酸顯色法用于測(cè)定桑黃多酚精密度良好。
2.8 重復(fù)性
同一樣品經(jīng)同樣提取步驟平行操作6份,測(cè)得多酚含量分別為8.44%、8.05%、8.09%、8.00%、8.17%、8.24%,RSD為1.95%,結(jié)果表明,該提取和測(cè)定方法重復(fù)性良好。
2.9 回收率
表1顯示,本方法的加標(biāo)回收率在97.95%~106.46%,平均回收率102.11%,RSD為2.92%,表明本方法的準(zhǔn)確度良好。
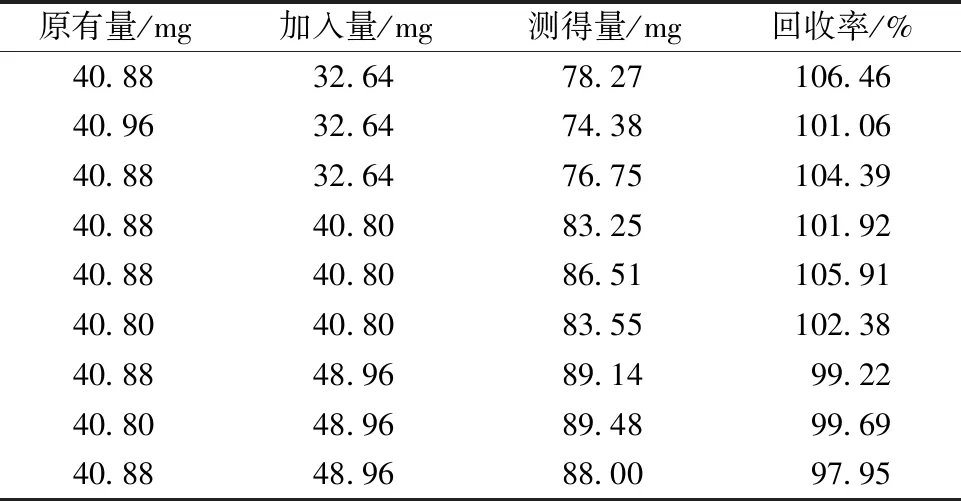
表1 沒(méi)食子酸加樣回收率(n=9)
2.10 中間精密度
2個(gè)實(shí)驗(yàn)人員的12份樣品多酚含量檢測(cè)結(jié)果(表2)表明中間精密度良好。
2.11 10批浙江省內(nèi)桑黃樣品多酚含量
在確定了本研究?jī)?yōu)化的方法具有良好的精密度、重復(fù)性、回收率之后,本研究測(cè)定了浙江省內(nèi)10份不同來(lái)源或不同批次的人工栽培桑黃子實(shí)體切片樣品中的多酚含量。結(jié)果顯示,10份樣品多酚含量在3.98%~8.54%(樣品干重百分比),不同廠家生產(chǎn)的桑黃子實(shí)體的多酚含量差異較大,多酚含量最高的是含量最低樣品的2倍多。同一公司不同生產(chǎn)批次的樣品多酚含量也存在差異,但是差異較小(表3)。
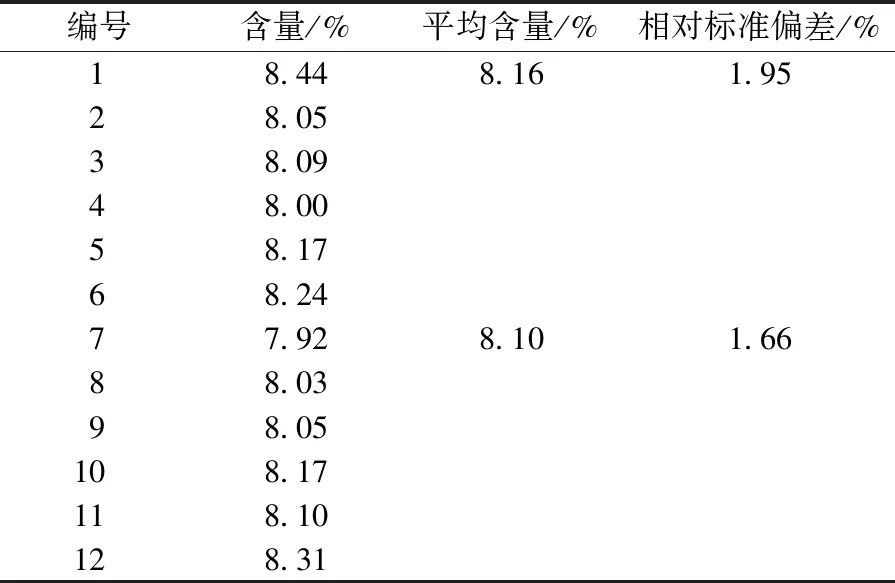
表2 中間精密度實(shí)驗(yàn)結(jié)果
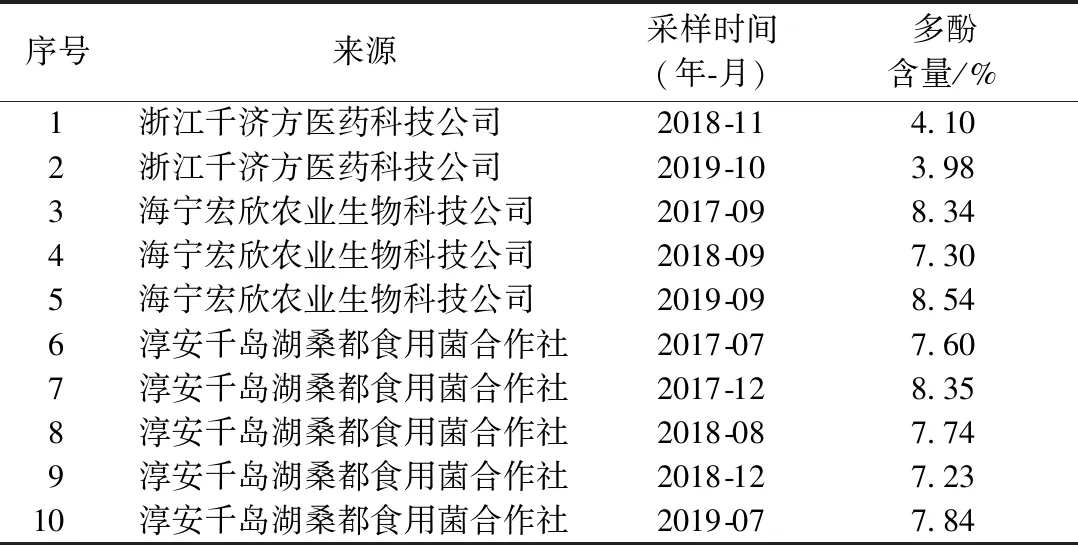
表3 10批浙江省不同廠家桑黃子實(shí)體樣品多酚含量
本研究測(cè)定的桑黃樣品多酚含量與其他文獻(xiàn)報(bào)道的桑黃多酚含量差異較大。雷萍等[11]將4 g桑黃樣品加入100 mL的70%乙醇55 ℃超聲提取60 min,提取2遍,用Folin-Ciocalteu比色法測(cè)定鮑姆桑黃5個(gè)品種(均來(lái)源于陜西省微生物研究所微生物技術(shù)研究中心)子實(shí)體,其多酚含量在1.11%~4.05%。《安徽省中藥飲片炮制規(guī)范(2019年版)》[12]采用方法為0.1 g樣品加入甲醇50 mL超聲處理30 min的提取方法,用磷鉬鎢酸顯色法測(cè)得的安徽省內(nèi)10份桑黃樣品的多酚含量為1.98%~4.77%。與其他文獻(xiàn)中報(bào)道的桑黃多酚含量相比,本研究中的桑黃多酚含量明顯提高。造成以上差異的原因,可能與提取方法、桑黃品種及產(chǎn)地、栽培方式等有關(guān)。
3 小結(jié)
本文開(kāi)展了桑黃子實(shí)體多酚含量測(cè)定的方法學(xué)研究。多酚測(cè)定方法以沒(méi)食子酸為標(biāo)準(zhǔn)品,采用磷鉬鎢酸顯色法測(cè)定,該法在多酚(以沒(méi)食子酸計(jì))含量25~350 μg范圍內(nèi)線性關(guān)系良好。依次考察了桑黃子實(shí)體的粉碎粒度、提取溶劑、提取方法、料液比、提取時(shí)間等提取條件對(duì)多酚含量的影響,最后確定了粉碎粒度為過(guò)三號(hào)篩、料液比1∶100、50%乙醇70 ℃水浴加熱回流3 h的多酚提取條件。經(jīng)方法學(xué)驗(yàn)證表明,該桑黃多酚提取測(cè)定方法精密度、重復(fù)性、回收率、中間精密度均良好。利用該方法測(cè)定了來(lái)自浙江省內(nèi)的10批桑黃樣品,其多酚含量在桑黃干重的3.98%~8.54%,其中不同生產(chǎn)廠家桑黃子實(shí)體多酚含量差異較大,同一廠家不同批次的桑黃多酚含量差異較小。本研究為桑黃多酚的提取測(cè)定提供方法學(xué)依據(jù),也為浙江省的桑黃中藥飲片炮制規(guī)范中多酚檢測(cè)限的制定提供重要依據(jù)。

