兔H-Y抗血清的制備和驗證
李孝初,袁秀芳,蘇菲,余斌,李軍星,葉十一,徐麗華*,肖琛聞*
(1.寧波鄞州中銘農業科技有限公司,浙江 寧波 315000;2.浙江省農業科學院 畜牧獸醫研究所,浙江 杭州 310021)
Eichwald和Silmsersl于1955年利用純系C57BL/6小鼠進行皮膚移植試驗時首次發現H-Y抗原[1]。這種抗原屬于次要組織相容性抗原,在哺乳動物中是雄性個體中特異基因的表達產物[2]。H-Y抗原的發現,引起了H-Y抗原對精子選擇和胚胎性別鑒定的廣泛研究[3]。雖然利用雜交瘤細胞技術獲取的H-Y單克隆抗體具有純度和效價高的優點,但由于H-Y抗原亞型多,單克隆抗體篩選的機遇性極大,研究周期長,技術難度大,因此難以成功[4]。在實際中,大多仍以動物制備多克隆抗H-Y抗體。本試驗探索以不同兔H-Y抗原的提取和免疫接種程序來制備兔H-Y抗血清,并用ELISA法測定抗血清效價,用所制備的抗血清以Western-blot技術檢測兔睪丸H-Y抗原組分。
1 材料與方法
1.1 試驗動物
從浙江省農業科學院種兔場選取2組同窩生新西蘭試驗兔8只(第1組1公3母;第2組2公2母),每只體重1.5~2.0 kg,3~4月齡。委托浙江省農業科學院種兔場進行常規飼養管理,試驗起始于1月,結束于7月。
1.2 睪丸H-Y抗原的制備
將公兔放血致死,無菌操作取出睪丸,立即置冰浴上剝離被膜和附睪,將睪丸剪成小塊,置無菌的5 mL玻璃勻漿器中,按1∶5加入預冷的0.01 mol·L-1PBS,冰浴制取勻漿,4 ℃ 2 000 r·min-1離心10 min,取上清用Lowery法測定蛋白濃度。分裝于1.5 mL小試管,-70 ℃保存備用。
1.3 免疫方法和程序
免疫前每只試驗兔分別采血約5 mL,分離血清,用作陰性血清對照,-70 ℃保存備用。每次免疫時從-70 ℃取出H-Y抗原適量,等量加入完全弗氏佐劑,用超聲波完全乳化備用。試驗共分2組,每組用公兔睪丸H-Y抗原免疫同窩母兔,以減少個體間抗原反應,提高獲取抗H-Y抗血清的可能性。
第1組試驗兔背部分2點皮下注射0.5 mL,然后每隔2周同法加強免疫一次,劑量相同,共免疫5次。將H-Y抗原加入等量不完全弗氏佐劑,用超聲波混合乳化完全,最后加強免疫一次,劑量同前,免疫后隔10 d,兔子采血致死,分離血清,每兔各得約20 mL抗血清,于-70 ℃保存備用。
第2組試驗兔第一次足墊注射免疫同窩2母兔,每只0.5 mL,然后每周皮下加強免疫一次,共免疫5次,劑量相同,最后一次免疫后,隔2周,分別采血致死,分離血清,每兔各得約20 mL抗血清,于-70 ℃保存備用。
1.4 H-Y抗血清的效價測定
從-70 ℃取出兔睪丸H-Y抗原,以NaHCO3/Na2CO3緩沖液稀釋至0.01 mg·mL-1,包被96孔酶標板,每孔100 μL,4 ℃過夜。取出酶標板,用5%脫脂奶粉封閉1 h。用pH 7.2的0.01 mol·L-1PBST洗滌3次。每孔加入1∶50稀釋的抗血清100 μL,37 ℃作用1 h,同法洗滌3次。再加入酶標SPA,37 ℃作用1 h后洗滌3次,用OPD+H2O2顯色,最后用2 mol·L-1H2SO4終止液(各50 μL)終止反應。用酶標儀于490 nm處測定D值,計算抗血清效價。
將上述取得的H-Y抗血清分別取15 mL,使用精子細胞毒性分析法測定H-Y抗血清的效價。
1.5 Western-blot檢測兔H-Y抗原組分
從-70 ℃取出睪丸H-Y抗原液適量,加入等量2×SDS上樣緩沖液混勻,煮沸3 min,高速離心后備用。同時制備12% SDS-PAGE,每孔上樣10 μL,120 V恒壓電泳2 h。電泳完畢,取出凝膠,立即進行電泳轉移至硝酸纖維素薄膜上,4 ℃ 30 V恒壓電泳過夜。
取出硝酸纖維素膜,用5%脫脂奶粉封閉1 h,用0.01 mol·L-1PBST洗滌3次,加入1∶50稀釋的抗血清,37 ℃作用1 h;同法洗滌3次,再用酶標SPA作用1 h,同法洗滌后用DAB+H2O2顯色。
2 結果與分析
2.1 睪丸H-Y抗原蛋白濃度
本研究選取的2窩試驗兔,分別取睪丸,研磨成勻漿,離心后用Lowery法測定蛋白濃度,第1組H-Y抗原蛋白濃度為28 mg·mL-1,第2組為24 mg·mL-1。
2.2 ELISA法測定兔H-Y抗血清效價
用提取的睪丸抗原包被酶標板后,分別用免疫前血清和免疫后血清進行倍比稀釋,按常規操作進行ELISA法檢測,最后于波長490 nm處測定D值。結果(圖1)表明,0830#兔子免疫前和免疫后D值變化較明顯,抗體效價在1∶100以上;其余4只試驗兔免疫前和免疫后D值變化不明顯。
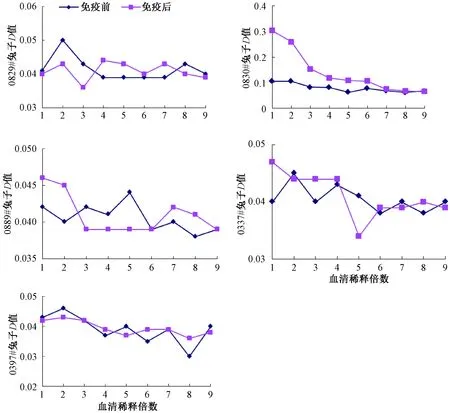
圖1 兔H-Y抗血清效價
用提取的睪丸抗原包被酶標板后,分別用免疫前血清和免疫后血清進行倍比稀釋,按常規操作進行ELISA法檢測,最后于波長490 nm處測定D值。結果表明,0830#兔子免疫前和免疫后D值變化較明顯,抗體效價在1∶100以上;其余4只試驗兔免疫前和免疫后D值變化不明顯。
2.3 Western-blot驗證
免疫的2組試驗兔,第1組有3只,抗血清編號為0829#、0830#、0889#;第2組有2只,抗血清編號為0337#、0397#。第1組試驗中,4次免疫后采血,進行瓊脂擴散試驗,無條帶,再加強免疫一次后采血。將5份抗血清分別進行Western-blot,最后顯色觀察,只有0830#兔抗血清作用的硝酸纖維素薄膜出現一條較弱的特異性條帶,另外的4個抗血清均無條帶出現(圖2)。
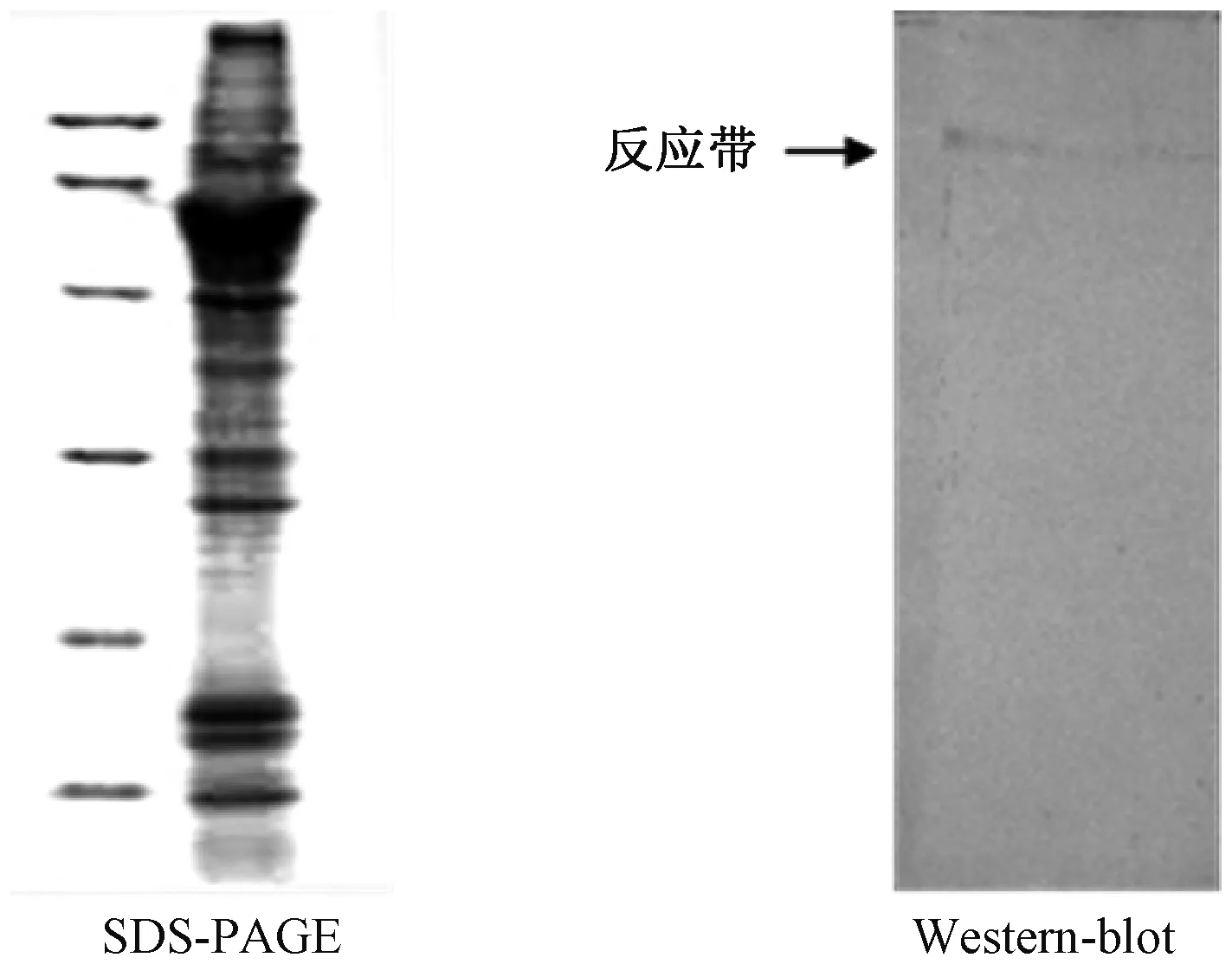
圖2 兔睪丸提取液的SDS-PAGE和Western-blot驗證
3 小結與討論
哺乳動物的性別由性染色體決定,雌性的性染色體為“XX”,雄性的性染色體為“XY”。根據這個特性,我們可以先分離X和Y精子,再通過人工授精的辦法有效地達到性別控制的目的。1955年在同一品系小鼠不同雌雄個體間進行皮膚移植時發現,雌性小鼠對雄性小鼠的皮膚移植有強烈地排斥反應[5],這種現象源于一種雄性特異性的抗原,稱之為Y染色體組織相容性抗原(Y-chromosomal histocompatibility antigen),簡稱“H-Y抗原”。Billingham等在1968年進一步證實,H-Y抗原是一種結合在細胞表面的糖蛋白,存在于所有哺乳動物含有Y染色體的雄性細胞表面。許多科學家對H-Y抗原的特異性進行了系統分析,結果推測H-Y抗原是一種弱抗原,由多個抗原表位組成,而每一個抗原表位僅有8~11個氨基酸。Greenfield等[6]報道,在小鼠上已經鑒定出4個H-Y抗原表位,其中2個H-Y抗原表位的編碼基因均為Smcy,一個編碼基因為Uty,第4個表位的編碼基因目前未知。其中Smcy和Uty表位基因在X染色體上的同源基因分別為Smcx和Utx,而在小鼠中這2個基因表達的抗原表位與H-Y基因的差異比較大。H-Y抗原表位在人類中鑒定出2個由Smcy編碼的H-Y抗原表位,其中一個表位與同源基因Smcx編碼的多肽僅差2個氨基酸。在精子中,H-Y抗原主要存在于精子頂體,附睪頭分離的精子其H-Y抗原主要分布于靠近精子的尾部,附睪尾分離的精子其抗原主要分布于頂體后端。很多試驗證實只有Y精子才能表達H-Y抗原。H-Y抗原的發現開辟了利用抗原抗體反應原理進行性別控制的新途徑,由H-Y抗體識別H-Y抗原,再通過一定分離程序將精子分離成X精子和Y精子,再選擇其中一種精子進行人工授精后得到所需性別的后代。
國內對H-Y單克隆抗體的研究已有多年歷史。小鼠H-Y抗原已被發現與多種動物發生交叉反應,包括人類、大鼠、兔、狗、鼴鼠、田鼠、鳥類、青蛙,甚至龍蝦、甲蟲、蟑螂和硬骨魚等無脊椎動物[7]。牛樹理等[8]采用間接ELISA條件提高靈敏度,建立檢測H-Y抗體的檢測方法。利用純系BALB/c公鼠免疫同系母鼠制備H-Y單抗,間接免疫熒光法鑒定胚胎性別PCR方法驗證準確率。結果表明,在18枚H-Y陽性胚胎中有15枚雄性胚胎和3枚雌性胚胎準確率為83%,在16枚H-Y陰性胚胎中有15枚雌性胚胎和1枚雄性胚胎準確率為94%。杭蘇琴等[9]以純系BALB/c雄性小鼠脾細胞腹腔注射免疫同系雌性小鼠9次,獲得的抗血清經雌、雄鼠脾細胞吸收后用于精子細胞毒性試驗,測得H-Y抗血清效價為1∶160。本次試驗選取體重相近的全同胞新西蘭兔,進行不同程序的免疫方式制備兔H-Y抗血清,結果5只受免疫的兔子中,只有0830#兔子產生較高效價的抗體滴度,并在Western-blot中出現一條較弱的特異性條帶。說明不同的免疫方法,其免疫效果也有很大差別。而同窩公兔睪丸提取液免疫同窩母兔,其產生抗血清的效價也不同,說明個體對H-Y抗原的敏感性也有很大的差異。
根據資料報道,H-Y抗原是一種弱組織相容性抗原,對不同動物的反應差異較大,免疫效果較差,產生的抗血清效價不高,一般獲得的效價只有1∶4~1∶16。而用本試驗所制備的兔H-Y抗原,以不同免疫程序,多點免疫,多次免疫,結合使用佐劑免疫等方法,最后獲取的效價較高,ELISA檢測效價在1∶100以上,兔H-Y抗血清制備獲得初步成功。對H-Y抗體效價的測定中,以往都是采用間接免疫熒光分析法、精子細胞毒性分析法和囊胚形成抑制法等方法,但這些方法都存在一定的不足之處。間接免疫熒光分析法準確率低,特異性差;精子細胞毒性分析法需要采集活精子進行試驗,眼觀判定精子活力,結果的重復性和準確性不強。而本試驗探索建立ELISA法,檢測H-Y抗血清的效價滴度,為H-Y抗血清效價的測定提供了一種新的檢測方法。
本試驗通過Western-blot技術,檢測到兔睪丸H-Y抗原有一條分子量約為90 ku的反應條帶。SDS-PAGE顯示兔睪丸提取液中蛋白成分極為復雜,而Western-blot僅檢測到一條顯色帶,特異性極強,該蛋白很可能就是H-Y抗原的主要成分。但據報道,人的H-Y抗原基因的mRNA為4 619 bp[10],鼠的H-Y抗原基因的mRNA為4 655 bp,其對應蛋白的理論分子量約為170 ku[11],與本試驗檢測到的分子量差異很大,造成此結果的原因有待進一步驗證,可能是因為在兔睪丸H-Y抗原制備過程中蛋白發生部分降解。

