一起牦牛巴氏桿菌病的診斷與治療
薛喜娟,王 亮,羅莉?qū)帲鞃槑V,尚立宏
(甘肅省動物疫病預(yù)防控制中心,甘肅 蘭州 730046)
多殺性巴氏桿菌可引起牦牛出血性敗血癥,簡稱“牛出敗”,其臨床特征主要表現(xiàn)為發(fā)熱、寒顫、流涎、咳嗽、呼吸困難、食欲廢絕等,慢性經(jīng)過表現(xiàn)為皮下組織、關(guān)節(jié)及各臟器化膿性炎癥[1-3]。該病多呈散發(fā)性或地方流行性特點,主要發(fā)生在牦牛飼養(yǎng)集中的高寒缺氧地區(qū),一年四季均可發(fā)生,但秋冬季節(jié)發(fā)病較多[4-7]。通過調(diào)查2018—2021年甘肅省甘南州牦牛巴氏桿菌病發(fā)病情況,發(fā)現(xiàn)該地牦牛多殺性巴氏桿菌病危害依然嚴(yán)重,4年間累計發(fā)生牦牛多殺性巴氏桿菌病29起,易感動物共2 100頭,發(fā)病260頭,病死62頭,病死率達(dá)23.85%,其中碌曲縣發(fā)病達(dá)14起,發(fā)病動物199頭,病死47頭,病死率達(dá)23.62%(表1)。本文通過對2020年9月甘南州碌曲縣某村發(fā)病牦牛進(jìn)行疾病診斷及治療,發(fā)現(xiàn)抗生素耐藥已經(jīng)在牧區(qū)廣泛存在,必須以藥敏試驗結(jié)果為依據(jù),合理規(guī)范用藥,同時交叉用藥,防止耐藥性產(chǎn)生[3]。
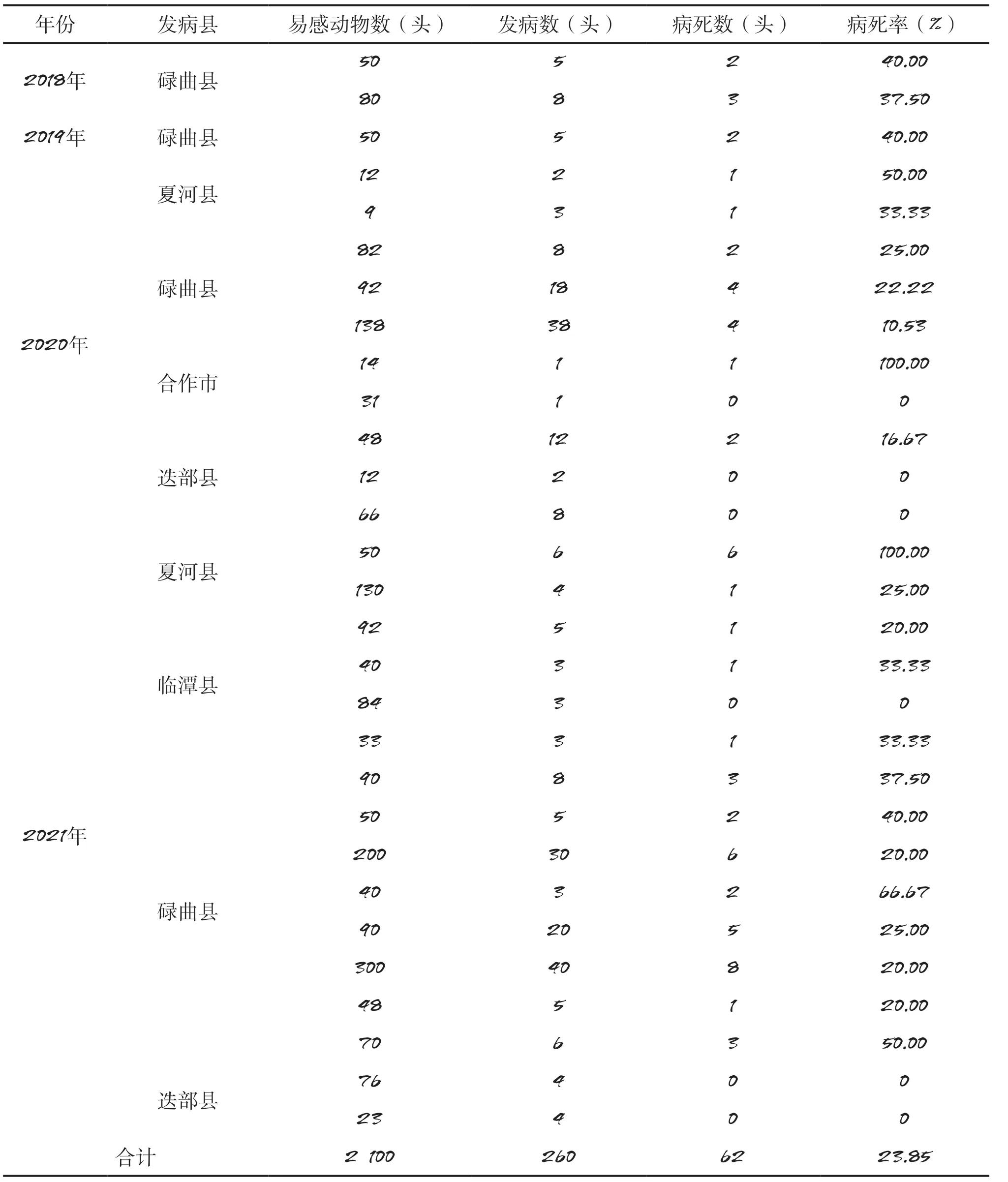
表1 2018—2021年甘南州牦牛巴氏桿菌病發(fā)病情況
1 發(fā)病情況
2020年9月下旬,甘南州碌曲縣某散養(yǎng)戶養(yǎng)殖的部分牦牛出現(xiàn)不同程度的發(fā)熱、咳嗽和腹瀉等癥狀,多為中等偏下膘情母牛發(fā)病。3 d內(nèi)死亡4頭,用青、鏈霉素和磺胺類藥物治療效果差,病情反復(fù)。為查明病原,更好地治療和預(yù)防該病,采集死亡牦牛的病料進(jìn)行分離鑒定和藥敏試驗。
2 臨床癥狀及剖檢病變
發(fā)病牦牛大多精神不振、被毛粗亂、鼻鏡干燥,采食下降或不食,反芻減弱。有的出現(xiàn)咳嗽、腹瀉、頭頸腫大、呼吸困難等癥狀。多呈急性經(jīng)過,體溫持續(xù)升高,可達(dá)41~42 ℃。3 d內(nèi)死亡4頭,其中1頭未見明顯癥狀,突然死亡;其余3頭呼吸高度困難,反芻停止,皮膚及可視黏膜發(fā)紺,眼角膜潮紅,伴有較多分泌物,鼻流帶血泡沫或膿性分泌物,舌伸出齒外,呈暗紅色。聽診有支氣管呼吸音及啰音。剖檢可見病牛頸部、咽部及胸前皮下組織漿液性浸潤伴有出血點,氣管內(nèi)點狀出血,淋巴結(jié)水腫出血,胸腔積液有纖維素性沉著,肺腫大,心包積液較為嚴(yán)重。
3 細(xì)菌分離鑒定及動物接種試驗
3.1 試驗材料
3.1.1主要試劑 普瓊培養(yǎng)基、血瓊脂平板、麥康凱瓊脂平板、營養(yǎng)肉湯培養(yǎng)基、革蘭氏染色液、瑞氏染色液、藥敏紙片、微量生化管,均購自杭州微生物試劑有限公司。
3.1.2實驗動物18~22 g健康小鼠,由中國農(nóng)業(yè)科學(xué)院蘭州獸醫(yī)研究所提供。
3.2 試驗方法及結(jié)果
3.2.1病料涂片鏡檢 無菌采集死亡牦牛肝、肺、脾病料制作觸片,革蘭氏染色可見大量革蘭氏陰性菌;瑞氏染色可見兩級濃染的橢圓形有莢膜的球桿菌。
3.2.2細(xì)菌分離培養(yǎng) 將病料接種于血瓊脂平板上,37 ℃培養(yǎng)18~24 h,可見露滴樣灰白色小菌落,半透明、不溶血、邊緣整齊、光滑濕潤。挑選典型的單個可疑菌落進(jìn)行純化,純化后分別接種于營養(yǎng)肉湯培養(yǎng)基、麥康凱瓊脂平板,37 ℃培養(yǎng)18~24 h。菌落在麥康凱瓊脂平板上未生長。將營養(yǎng)肉湯培養(yǎng)物革蘭氏染色后鏡檢,可見大量紅色球狀小桿菌。
3.2.3生化試驗 將純培養(yǎng)物分別接種于蔗糖、乳糖等9種微量生化管中,37 ℃培養(yǎng)48 h。觀察結(jié)果可見(表2),蔗糖、果糖、葡萄糖、甘露醇、硫化氫陽性,乳糖、麥芽糖、鼠李糖、山梨醇均為陰性。

表2 生化試驗結(jié)果
3.2.4動物接種試驗 取健康小鼠10只,平均分為5組,碾磨病料至糊狀,0.9%無菌氯化鈉溶液1∶10稀釋,腹腔注射前4組小鼠(0.5 ml/只)。第5組設(shè)為對照組。接種18~24 h后,第1~4組小鼠全部死亡,對照組未見死亡。剖檢死亡小鼠,可見皮下結(jié)締組織膠樣浸潤,肝、脾腫大,淤血,有出血點。胸腔含有大量黃色漿液纖維素性滲出物[3]。無菌采取死亡小鼠心血及肝脾作涂片鏡檢和分離培養(yǎng)。組織觸片和血涂片革蘭氏染色及瑞氏染色鏡檢結(jié)果與發(fā)病牦牛鏡檢結(jié)果一致,為紅色小桿菌,瑞氏染色可見兩端濃染。接種血瓊脂平板37 ℃培養(yǎng)18~24 h后,長出半透明、不溶血、邊緣整齊、光滑濕潤的露滴樣灰白色小菌落,與攻菌病料培養(yǎng)特性相同。
3.3 分析
死亡牦牛臨床癥狀符合多殺性巴氏桿菌引起的發(fā)熱、寒顫、流涎、咳嗽、呼吸困難、食欲廢絕等主要癥狀;病理剖檢病變符合多殺性巴氏桿菌剖檢病變。
病料細(xì)菌分離鏡檢可見革蘭氏陰性菌,瑞氏染色符合兩級濃染的特性;菌落形態(tài)可見露滴樣灰白色小菌落,半透明、不溶血、邊緣整齊、光滑濕潤。生化試驗符合巴氏桿菌特性。以上特征符合多殺性巴氏桿菌培養(yǎng)特性及生化指標(biāo)。
攻毒試驗致小鼠死亡,死亡小鼠剖檢病變及鏡檢結(jié)果符合目的菌特征。
綜合以上結(jié)果判斷,臨床癥狀、剖檢病變以及病原菌分離培養(yǎng)特性等均符合多殺性巴氏桿菌特征,確診該病為多殺性巴氏桿菌引起的牦牛出血性敗血癥。
4 藥敏試驗
參照WS/T 639-2018《抗菌藥物敏感性試驗的技術(shù)要求》,采用藥敏紙片擴(kuò)散法,測定此次分離的巴氏桿菌藥物敏感性。結(jié)果表明:此次分離的巴氏桿菌對氨芐青霉素、頭孢噻肟、恩諾沙星和強(qiáng)力霉素高敏,對慶大霉素和卡那霉素中敏,對青霉素G、鏈霉素和復(fù)方新諾明低敏。
5 治療
隔離病牛,對其余健康牛群緊急免疫。對發(fā)病牛群肌肉注射頭孢噻肟、氨芐青霉素和恩諾沙星等高敏感性抗菌藥物,1~2次/d,必要時兩種抗菌藥一起用以加強(qiáng)療效。治療過程中給予清潔飲水和易消化的飼料,同時口服電解多維。5~7 d后,大部分病牛康復(fù),無新增死亡病例,疫情得到控制。
6 討論
牦牛多殺性巴氏桿菌病感染率較高,已經(jīng)嚴(yán)重影響了我國牦牛產(chǎn)業(yè)的健康發(fā)展。巴氏桿菌屬于條件性致病菌,在健康牦牛呼吸道內(nèi)長期存在,通常由內(nèi)源性感染引發(fā)[8],如氣候劇變、長途運輸、營養(yǎng)不良、換料、疲勞、寄生蟲感染等應(yīng)激因素容易導(dǎo)致該病發(fā)生[9-10]。也可通過直接接觸患牛排泄物、分泌物等污染的草場、飼料、用具等發(fā)生感染[11]。此次疫情發(fā)生時間在9月下旬,正處于高原氣候季節(jié)性變化時間,因此建議養(yǎng)殖場(戶)在氣候多變季節(jié)加強(qiáng)飼養(yǎng)管理,注意補(bǔ)充精料、微量元素和維生素,減少擠奶頻次,降低牦牛應(yīng)激。發(fā)生此類疫病最有效的治療方法是抗生素治療,但隨著抗生素的濫用導(dǎo)致多殺性巴氏桿菌耐藥問題日漸凸顯[12]。因此建議治療以藥敏試驗結(jié)果為依據(jù),合理規(guī)范用藥,同時交叉用藥,避免耐藥性產(chǎn)生。由于巴氏桿菌可感染人,飼養(yǎng)人員和獸醫(yī)還需做好自身防護(hù),避免感染。
除了治療外,應(yīng)采取綜合防控措施。要堅持預(yù)防為主的原則,定期開展疫苗免疫接種。免疫接種注意區(qū)分不同體重牦牛免疫接種劑量,盡可能確保接種效果[13]。要開展劃區(qū)輪牧,結(jié)合牧民放牧習(xí)慣和疫病防控需要,將放牧牦牛群劃分為“兩大四小”牧場輪牧。兩個大區(qū)即夏秋、春冬牧場,四個小區(qū)即在兩個大區(qū)中按每年春、夏、秋、冬四季劃分。要充分利用高原紫外線殺菌、牦牛排泄物發(fā)酵殺菌等自然途徑預(yù)防本病,夏秋季節(jié)還應(yīng)注意避開過度陰濕草場放牧。對已經(jīng)發(fā)生疫情的圈舍及時開展圈灘場地消毒工作,并及時開展病死牦牛尸體、排泄物、乳、乳制品無害化處理工作[14]。

