前列腺癌術后RapidArc與IMRT放療計劃的劑量學比較
童鑄廷 周 駿 潘淑豪 李 銳 夏葉葉 朱倩倩
隨著我國人口逐步步入老齡化以及人們的生活方式和飲食結構的改變,前列腺癌的發病率呈現逐年快速增長的趨勢。目前前列腺癌在我國的發病率已經超過膀胱癌,成為男性泌尿生殖系統發病率最高的惡性腫瘤[1-2]。放射治療是前列腺癌重要的根治性治療手段。隨著調強放療設備在我國的普及,調強放射治療(intensity-modulated radiotherapy,IMRT)已經廣泛應用與前列腺癌的治療。但是,IMRT相較于傳統的二維放療具有更長的照射時間和更多的加速器跳數,這無形當中增加了患者患第二惡性的潛在風險[3]。快速旋轉容積調強放療(RapidArc)技術利用單弧或多弧設野,通過動態調控機架旋轉速度的過程中配合高速動態多葉光柵連續動態運動以及連續可變的輸出劑量率形成動態可變的束流,以達到靶區劑量適形的目的。相較于IMRT,RapidArc技術使危及器官的體劑量更低,理論上可降低放射性損傷發生率[4-6]。RapidArc技術在前列腺癌根治性放療中的優越性已在國外的研究[7-9]中報道,但是,目前關于其在前列腺癌術后輔助放療中優勢的相關研究相對比較少。本研究對14例前列腺癌術后或術后生化復發患者的RapidArc與IMRT計劃在靶區和危及器官(organs at risk,OAR)照射劑量分布進行比較分析,以期為前列腺癌術后輔助放療的放療計劃的設計提供劑量學參考。
1 資料與方法
1.1 一般資料 選取2020年7月至2022年2月在安徽醫科大學第一附屬醫院行術后行輔助放療或者術后生化復發行挽救性放療的前列腺癌患者14例。所有患者均經病理證實為前列腺癌,均無放療禁忌證,卡氏評分≥70分,年齡57~77歲,平均(67.14±6.02)歲。
1.2 方法與步驟
1.2.1 放療前準備和體位固定 患者放療前1小時排空膀胱和直腸,喝水憋尿充盈膀胱后再進行定位掃描和放療。患者仰臥位,采用真空負壓體袋固定體位后,用大孔徑螺旋CT模擬機(GE公司)進行定位掃描。掃描層厚為5 mm,掃描范圍從第1腰椎水平到坐骨結節下5 cm。掃描圖像經網絡傳送至eclipse 13.5 TPS計劃系統。
1.2.2 勾畫靶區 臨床靶區(clinical target volume,CTV)范圍為瘤床區域(包括膀胱頸、吻合口和直腸膀胱間隙)和盆腔淋巴結引流區域。計劃靶區(planning target volume,PTV)為CTV外放5mm,不含后方直腸壁。處方劑量為4 500~5 000 cGy;對與有前列腺包膜侵犯,切緣近或陽性等高危因素的患者,瘤床區縮野加量1 000~2 000 cGy。OAR包括膀胱、直腸及雙側股骨頭。所有靶區經過科室2位高年資醫師審核討論通過。
1.2.3 放射治療計劃設計 所有放療計劃都在Varian公司Eclipse 13.5 (Varian Medical Systems, Palo Alto, CA, USA)治療計劃系統上完成,分別為每例前列腺癌患者設計1個7野IMRT和1個RadpidArc治療計劃。為了方便對2種放療計劃進行劑量學比較,2種計劃采用相同的劑量約束條件和優化參數,2種計劃都要求靶區最小劑量不低于95%的處方劑量,最大劑量不高于107%的處方劑量。危及器官的劑量限制:膀胱V50<50%,V60<15%;直腸V50<50%,V60<10%;左右側股骨頭V40<5%。
1.3 放療計劃評估
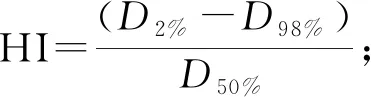
1.3.2 OAR劑量學評估 用V20、V30、V40,V50和平均劑量(Dmean)來評價膀胱和直腸;用D5%和Dmean來評價左右側股骨頭。
1.3.3 執行效率的評估 機器跳數(monitor unit,MU)定義為放療計劃中各個射野MU的總和;有效治療時間定義為患者完成擺位后,從加速器開始出束到出束全部結束所用時間。
2 結果
2.1 靶區劑量學比較 RapidArc計劃的D2%為(6 645.28±242.48)cGy,低于IMRT計劃,差異有統計學意義(P<0.05)。RapidArc計劃的靶區劑量HI優于IMRT計劃,差異有統計學意義(P<0.05)。見表1。典型前列癌患者的RapidArc計劃和IMRT計劃的橫斷位,冠狀位和矢狀位的劑量分布圖見圖1。

表1 14例患者2種放療計劃治療靶區劑量學參數比較

注:A為IMRT計劃橫斷位劑量分布,B為RapidArc計劃橫斷位劑量分布,C為IMRT計劃冠狀位劑量分布,D為RapidArc計劃冠狀位劑量分布,E為IMRT計劃矢狀位劑量分布,F為RapidArc計劃矢狀位劑量分布。
2.2 危及器官直腸劑量學比較 2種放療計劃直腸低劑量參數(V20和V30)以及Dmean進行比較,差異無統計學意義(P>0.05);RapidArc計劃的直腸V40為(32.95±13.19)%,IMRT計劃為(40.69±9.60)%,兩者差異無統計學意義(P>0.05),但RapidArc計劃較IMRT計劃有下降的趨勢;RapidArc計劃的直腸高劑量參數V50較IMRT計劃降低,差異有統計學意義(P<0.05)。見表2。

表2 14例患者2種放療計劃直腸劑量學比較
2.3 危及器官膀胱劑量學比較 2種放療計劃膀胱低劑量參數(V20和V30)以及Dmean的比較,差異無統計學差異(P>0.05)。RapidArc計劃在膀胱高劑量參數(V40和V50)劑量限制方面均優于IMRT計劃,差異有統計學意義(P<0.05)。見表3。

表3 14例患者2種放療計劃膀胱劑量學比較
2.4 危及器官左右側股骨頭劑量學比較 2種放療計劃左、右側股骨頭的Dmean進行比較,差異均無統計學意義(P>0.05)。RapidArc計劃兩側股骨頭D5%的劑量分別為(3 023.70±275.99)cGy和(2 896.15±230.74)cGy,均低于IMRT計劃,差異有統計學意義(P<0.05)。見表4。

表4 14例患者2種放療計劃雙側股骨頭劑量學比較
2.5 2種放療計劃執行效率的比較 RapidArc計劃的MU為(627.00±39.12),IMRT計劃為(1 132.78±116.26),2種放療計劃MU進行比較,差異有統計學意義(t=20.927,P<0.001)。RapidArc計劃的治療時間為(189.14±12.79)s,IMRT計劃為(394.64±19.59)s,差異有統計學意義(t=41.684,P<0.001)。
3 討論
目前常規的調強放射治療技術已經在我國廣泛的應用與前列腺癌臨床治療中,并且也能夠滿足臨床上對靶區劑量適形度和均勻度的要求。但是不同于頭頸部器官以骨性標志做參考,前列腺癌靶區由于受呼吸、膀胱和直腸的充盈程度等因素的影響,其位置變異很大,具有一定的不確定性。為了降低膀胱、直腸、小腸等危及器官的照射劑量和照射體積,前列腺癌患者在放療前一般常規需要進行充盈膀胱和排空直腸等準備工作。常規的調強放射治療的時間一般較長,在一定程度上會增加患者的不適感和患者的不自主運動。RapidArc技術在降低加速器MU及縮短治療時間上的優勢已經在其他瘤種的研究[11-12]中證實。但其在提高前列腺癌術后放療患者的靶區適形度和劑量均勻度,以及降低危及器官受量方面是否具有同樣的優勢,仍值得進一步的探討。
在靶區劑量學方面,本研究結果表明:相較于7野IMRT計劃,RapidArc計劃并不能顯著提高靶區劑量的適形度,但是可以降低靶區的D2%,從而提高靶區劑量的均勻度。這與Mellon等[13]在前列腺癌根治放療的研究中的結論類似,但是該研究未對靶區的D50%和Dmean進行比較,因此存在一定的局限性。在危及器官劑量學優劣性比較方面,目前的研究也主要集中在對前列腺癌根治性放療2種計劃的比較,術后輔助放療2種計劃危及器官劑量學的比較研究相對較少。本研究的結果顯示,RapidArc計劃對直腸和膀胱的低劑量區域參數(V20和V30)劑量限制并不優于甚至稍差于IMRT計劃,但是,RapidArc計劃對膀胱和直腸的高劑量區域參數(V40和V50)劑量限制均優于IMRT計劃,且這種優勢隨著劑量的增加越顯著,即RapidArc計劃對膀胱和直腸V50的保護優勢高于V40。膀胱和直腸的受量從低劑量區到高劑量區呈現先高后低的趨勢,這與RapidArc的旋轉布野方式導致照射體積的增加有關。RapidArc雖然在降低串聯器官(脊髓)最大劑量方面有優勢,但由于其照射路徑較寬,導致并聯器官(直腸和膀胱)低劑量區受照體積增大[11, 14]。Nguyen等[15]的研究結果顯示,RapidArc計劃較IMRT計劃顯著降低了直腸V50、V60和V70,對危及器官的保護更有優勢。而Poon等[16]的研究結果則認為,RapidArc計劃在靶區劑量適形度和均勻性方面均優于IMRT計劃,2種放療計劃在直腸,膀胱和股骨頭等危及器官保護方面的相似。但與本研究不同的是,這2項研究僅僅只對直腸和膀胱等危及器官的高劑量區域參數(V50、V60等)進行了比較,未對低劑量區域的劑量參數(V20和V30)進行比較。國內的研究[17]結果顯示,RapidArc技術較IMRT技術靶區適形指數和均勻性指數均有優勢,但RapidArc計劃中膀胱和直腸的V20、V30略高于IMRT計劃,與本研究的結論類似。
RapidArc計劃除了在降低危及器官高劑量的照射體積方面的優勢外,其最大的優勢是減少加速器的MU,大大減少患者的治療時間[18]。本研究中IMRT計劃和RapidArc計劃的MU分別為(1 132.78±116.26)MU和(627.00±39.12)MU,RapidArc計劃的機器平均MU僅為IMRT計劃的55.35%,幾乎下降了一倍。MU的減少,直接導致治療時間從IMRT的(394.64±19.59)s降低到(189.14±12.79)s,治療時間幾乎縮短了一半,大大提高了患者的治療效率。患者在3分鐘左右的時間就可以完成治療。這樣可以大大減小患者治療過程中位移變化、器官因呼吸導致位置變化以及由于患者不適如咳嗽緊張等不確定因素對放療精度的影響。此外,加速器MU的降低,意味著患者暴露的輻射減少,也可以有效的降低患者輻射誘發惡性腫瘤的風險[19-20]。
本研究屬于單中心的數據,樣本量較少,研究結果仍具有一定的局限性。要獲得更加精確的結論,仍需要開展更多的多中心、大樣本量的研究進行論證。
綜上所述,本研究通過對RapidArc和7野IMRT計劃的劑量學比較發現:RapidArc計劃在危及器官低劑量受照體積保護方面稍差于IMRT計劃,但在靶區劑量均勻度,危及器官高劑量受照體積限制,以及機器MU和治療時間方面均優于IMRT計劃。RapidArc可以作為一種常規方法在有條件的機構中應用于前列腺癌的治療。

