木犀草素對抗2 型糖尿病大鼠心肌纖維化的機制研究
黃 婷,唐建東,李真真,白 楊,劉惠雙,徐在革
(1.鄭州市第七人民醫院內分泌科,鄭州 450006;2.鄭州市第七人民醫院營養科,鄭州 450006)
糖尿病(diabetes mellitus,DM)是全球范圍內常見的流行病,發病率和病死率逐年增高,2 型糖尿病(type 2 diabetes mellitus,T2D)約占DM 患者死亡的90%以上[1-2]。糖尿病心肌病(diabetic cardiomyopathy,DCM)是DM 的主要并發癥,其特征是左室舒張和/或收縮功能障礙,目前普遍認為心肌肥大和心肌纖維化是其主要的病理特征[3-4]。
近年來,隨著中醫藥的快速發展,天然產物對疾病的預防效用成為研究熱點[5]。木犀草素(luteolin,LUT)是一種天然的常見黃酮類化合物,可在多種植物和草藥中提取,LUT 可作為一種抗氧化劑和抗炎劑,在多種疾病治療等方面均有報道[6-7]。研究[8]證實,LUT 可明顯抑制T2D 大鼠對胰島素的抵抗作用及炎癥反應。研究[9]發現,LUT 可明顯改善阿霉素引起的H9C2 心肌細胞損傷。但還未見LUT 與T2D 心肌纖維化關系的相關報道。以往研究發現,腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)-沉默信息調節因子3(sirtuin3,SIRT3)信號通路參與調控肝纖維化發展[10],研究[11]發現,運動可能通過激活AMPK-SIRT3 信號通路改善T2D 大鼠骨骼肌胰島素抵抗。關于AMPK-SIRT3 通路在T2D 心肌纖維化中的作用還未可知。筆者推測,LUT 可能通過激活AMPKSIRT3 信號對抗T2D 大鼠心肌纖維化,因此,本研究將通過體內和體外實驗共同驗證此猜想,并進一步探討LUT 潛在的抗T2D 心肌纖維化機制。
1 材料與方法
1.1 材料 健康雄性SPF 級Sprague-Dawley(SD)大鼠24 只,體質量180~220 g,購自北京科興中維生物技術有限公司,許可證號:SYXK(京)2020-0054。飼養期間自由進食飼料,自由飲水,12 h 晝夜循環,溫度23~26℃。鏈脲佐菌素(streptozocin,STZ,純度HPLC ≥98%)購自美國Sigma;LUT(純度HPLC≥98%)、AMPK通路抑制劑Compound C(純度HPLC ≥98%)購自上海aladdin;Masson 三色染色試劑盒購自北京Solarbio;RIPA 裂解液、CCK-8 細胞增殖檢測試劑盒購自北京YITA;一抗fibronectin、collagen I、α-SMA、p-AMPK、AMPK 和SIRT3 及 二抗HRP 標記的山羊抗兔均購自英國Abcam;H9C2細胞購自美國ATCC;DEME 培養基購自上海LMAI Bio;Annexin V-FITC/PI 凋亡檢測試劑盒購自北京BIOSIC;TUNEL 細胞凋亡檢測試劑盒(顯色法)購自上海Beyotime。BPH-9042 細胞培養箱購自上海一恒;Multiskan FC 酶標儀購自美國Thermo;CX43 生物顯微鏡、FV3000 激光掃描共聚焦顯微鏡購自日本Olympus;Gallios 流式細胞儀購自美國BECKMAN。
1.2 方法
1.2.1 大鼠分組及藥物處理 SD 大鼠適應性喂養7 d后,分為正常(Control)組,T2D 組,T2D+LUT 組,每組8 只。T2D 組和T2D+LUT 組SD 大鼠禁食12 h后通過腹腔注射1% 35 mg/kg STZ 誘導T2D 模型,注射后繼續喂食高脂高糖飼料,持續7 d 后,于大鼠尾部靜脈取血檢測血糖,當超過3 次隨機檢測血糖濃度≥16.7 mmol/L 則表明T2D 模型制備成功[12]。Control 組腹腔注射相同體積的檸檬酸鈉緩沖液,并一直使用普通飼料喂養。T2D+LUT 組大鼠于造模成功后第1 天開始灌胃給予40 mg/kg LUT[8],Control 組和T2D 組大鼠灌胃給予等體積生理鹽水,每天1 次,持續4 周。實驗結束后大鼠腹腔注射3% 50 mg/kg 戊巴比妥鈉麻醉,收集各組大鼠左心室心肌組織樣本,部分組織用4%多聚甲醛固定后制作4 mm 的石蠟切片;其余組織凍存于-80℃,用于Western blot 檢測。
1.2.2 Masson 染色觀察心肌組織病理學并測定心肌膠原容積分數 取1.2.1 中獲取的各組組織切片按照常規操作脫蠟,參照Masson 三色染色試劑盒說明書進行Masson 染色,大鼠心肌細胞染色呈紅色,間質膠原纖維呈藍色,使用光學顯微鏡觀察拍攝大鼠心肌結構及纖維化程度。通過Image Pro Plus 測定各組心肌膠原容積分數(collagen volume fraction,CVF),CVF(%)=膠原面積/視野總面積×100%。
1.2.3 Western blot 檢測心肌組織中纖維化標志蛋白及AMPK-SIRT3 通路相關蛋白水平 取出凍存的各組心肌組織,每100 mg 組織加入1 mL 預冷的RIPA 裂解液通過超聲破碎后離心提取上清液,使用BCA 試劑盒檢測各組蛋白濃度。按照1: 5 比例混合蛋白和上樣緩沖液后,在95℃煮沸15 min 使蛋白變性。按照40 mg總蛋白上樣,經SDS-PAGE 分離蛋白后經半干法將蛋白轉移至PVDF 膜上。使用5%牛血清白蛋白封閉1 h,洗去封閉液后添加一抗fibronectin、collagen I、α-SMA、p-AMPK、AMPK 和SIRT3(稀釋比例1: 1 000)4 ℃過夜孵育,隔天使用TBST 洗膜后,添加HRP 標記的山羊抗兔二抗(稀釋比例1: 5 000)在37 ℃孵育1 h,使用TBST 沖洗后,添加ECL 顯影,在凝膠成像系統中曝光,保存圖片。使用Image J 軟件分析各蛋白條帶的灰度值,β-actin 作為內參蛋白。目的蛋白的相對表達量=實驗組目的蛋白的灰度值/對照組蛋白的灰度值。
1.2.4 心肌細胞H9C2 培養 H9C2 細胞維持在DEME培養基中(含1%青霉素/鏈霉素和10%胎牛血清),在37℃培養箱中培養,至細胞融合度達到0%~90%,即可進行傳代培養。
1.2.5 LUT 濃度及干預時間選擇 取對數期且生長狀態良好的H9C2 細胞接種于6 孔板中(1×104個/孔),依次分為對照組(Control),高糖組(HG),高糖和不同濃度LUT 組[HG+LUT(5、10、15 mM)]。Control 組為常規培養條件添加5.5 mmol/L 葡萄糖,HG 組為常規培養條件下添加30 mmol/L 葡萄糖[13],HG+LUT(5、10、15 mM)組為常規培養條件下添加30 mmol/L 葡萄糖和不同濃度(5、10、15 mM)的LUT,分別干預處理24、48、72 h 后收集細胞,通過CCK-8 法檢測各組細胞的增殖情況。
1.2.6 細胞分組 取對數期且生長狀態良好的H9C2細胞接種于6 孔板中,依次分為Control 組、HG組、HG+LUT 組、AMPK通路抑制劑(Com.C)組(10 mM)[14]、高糖+LUT+AMPK通路抑制劑(HG+LUT+Com.C)組。Control 組,HG 組參照1.2.5中方法處理,HG+LUT 組為常規培養條件下添加30 mmol/L 葡萄糖和5 mM LUT,Com.C 組為常規培養條件下添加10 mM Compound C,HG+LUT+Com.C 組為常規培養條件下添加30 mmol/L 葡萄糖、5 mM LUT和10 mM Comound C,以上各組細胞均培養48 h。
1.2.7 流式細胞術檢測各組H9C2 細胞凋亡率 將按照1.2.6培養的各組H9C2細胞接種于96孔板中(1×106個/孔),添加200 mL 結合緩沖液重懸細胞,分別添加5 mL Annexin V-FITC 和碘化丙啶(PI),混勻后室溫避光孵育20 min,通過流式細胞儀檢測各組細胞凋亡率。
1.2.8 TUNEL 法檢測各組H9C2 細胞凋亡水平 收集按照1.2.6 培養的各組H9C2 細胞,使用4%多聚甲醛固定15 min,按照TUNEL 細胞凋亡檢測試劑盒說明操作,最后添加DAB 反應10 min。在熒光顯微鏡下觀察拍照,記錄每個視野下凋亡的細胞數量。TUNEL 陽性細胞率=單個視野下的凋亡細胞數量/單個視野下的總細胞數量×100%。
1.2.9 Western blot 檢測各組H9C2 細胞中纖維化標志蛋白及AMPK-SIRT3 通路相關蛋白水平 收集按照1.2.6 培養的各組細胞,通過RIPA 法提取總蛋白,參照1.2.3 方法分析各蛋白水平。
1.3 統計學方法 采用Graphpad Prism 9.0 對數據進行分析,多組間比較采用One-way ANOVA分析,組間兩兩比較采用SNK-q檢驗,以P<0.05 代表數據差異具有統計學意義。
2 結果
2.1 LUT 對STZ 誘導的糖尿病大鼠心肌纖維化和AMPK-SIRT3 通路的影響 與Control 組相比,T2D組大鼠心肌組織中細胞排列紊亂,間質膠原纖維分布增加,CVF 顯著增大;與T2D 組相比,T2D+LUT 組大鼠心肌組織中細胞排列紊亂及間質膠原纖維分布增加得到改善,CVF 顯著降低,見圖1;心肌組織中fibronectin、collagen I 和α-SMA 蛋白水平顯著增高,p-AMPK/AMPK 比值和SIRT3 蛋白水平顯著降低(P<0.05)。心肌組織中fibronectin、collagen I 和α-SMA 蛋白水平顯著降低,p-AMPK/AMPK 比值和SIRT3蛋白水平顯著增高(P<0.05)。結果見表1。
表1 各組相關蛋白水平比較(,n =3)

表1 各組相關蛋白水平比較(,n =3)
注:與Control 組比較,# P <0.05;與T2D 組比較,△P <0.05
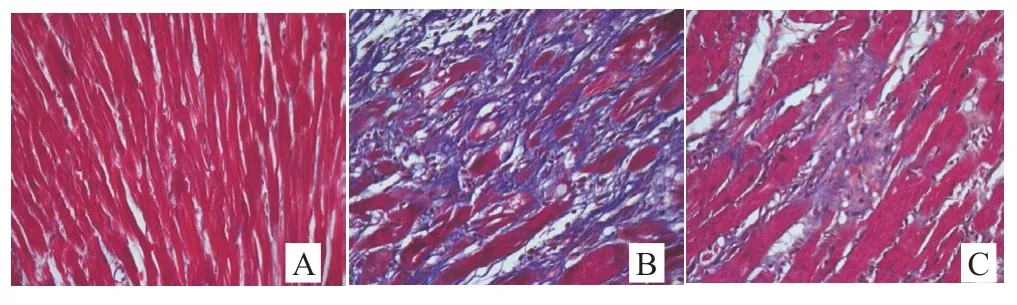
圖1 Masson 染色觀察心肌組織病理學
2.2 LUT 對HG 誘導的H9C2 細胞增殖活力的影響 HG 組H9C2 細胞增殖活力較Control 組明顯降低(P<0.05);在HG 處理的同時添加不同劑量的LUT 處理48 h 和72 h 后H9C2 細胞增殖活力較HG組得到明顯的改善(P<0.05),在處理24 h 時HG+LUT(5 mM)組H9C2 細胞增殖活力則與HG組無明顯差異(P>0.05)。因此,為避免較高濃度的LUT 對細胞生長產生不利影響,故而選擇5 mM 的LUT 處理48 h。結果見表2。
表2 LUT 促進HG 誘導的H9C2 細胞增殖(,n =3)
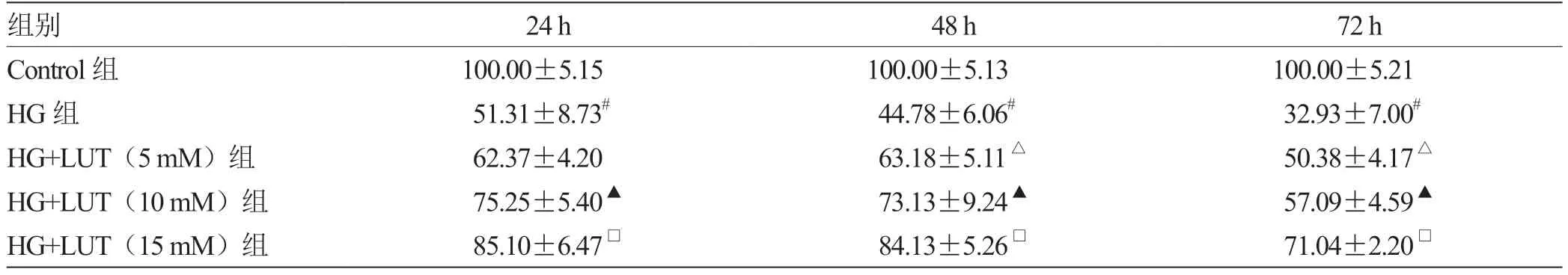
表2 LUT 促進HG 誘導的H9C2 細胞增殖(,n =3)
注:與Control 組比較,# P <0.05;與HG 組比較,△P <0.05;與HG+LUT(5 μM)組比較,▲P <0.05;與HG+LUT(10 μM)組比較,□P <0.05
2.3 LUT 對HG 誘導的H9C2 細胞凋亡、纖維化及AMPK-SIRT3 通路的影響 與Control 組相比,HG 組H9C2 細胞凋亡率和TUNEL 陽性細胞率明顯升高(P<0.05);與HG 組相比,HG+LUT 組H9C2 細胞凋亡率和TUNEL 陽性細胞率明顯降低(P<0.05)。見圖2,圖3。進一步研究發現,與Control 組相比,HG 組H9C2 細胞中fibronectin、collagen I 和α-SMA 蛋白水平明顯增高(P<0.05);此外,p-AMPK/AMPK比值和SIRT3 蛋白水平明顯降低(P<0.05);與HG組相比,HG+LUT 組H9C2 細胞中fibronectin、collagen I 和α-SMA 蛋白水平明顯降低(P<0.05);此外,p-AMPK/AMPK 比值和SIRT3 蛋白水平明顯升高(P<0.05),結果見表3。

圖2 流式細胞術檢測各組H9C2 細胞凋亡率
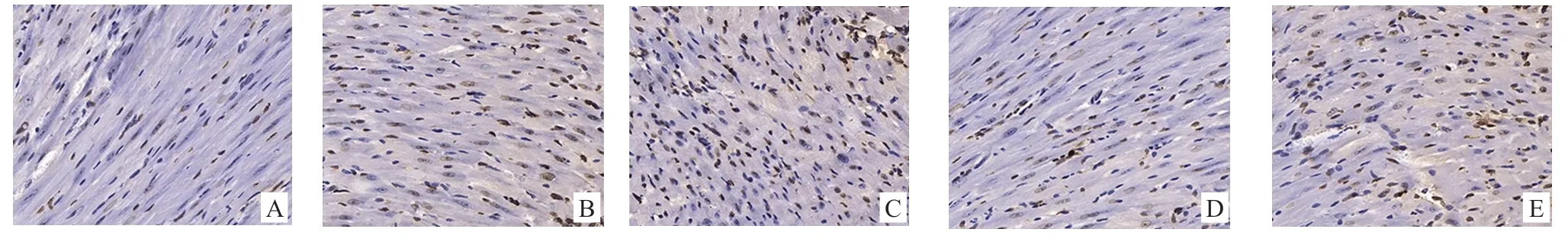
圖3 TUNEL 法檢測各組H9C2 細胞凋亡水平
表3 各組H9C2 細胞凋亡水平及蛋白表達比較(,n =3)
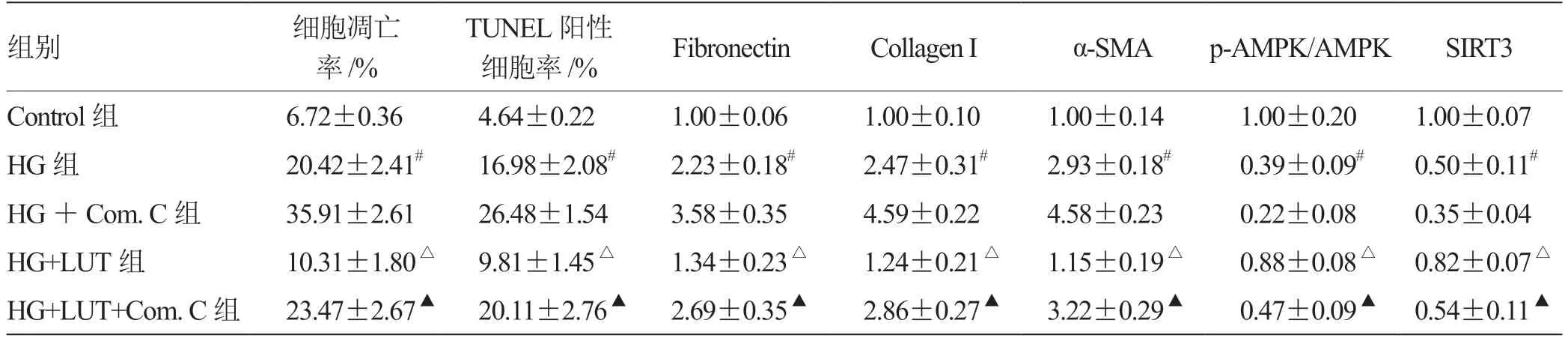
表3 各組H9C2 細胞凋亡水平及蛋白表達比較(,n =3)
注:與Control 組比較,# P <0.05;與HG 組比較,△P <0.05;與HG+LUT 組比較,▲P <0.05
2.4 AMPK 通路抑制劑可以逆轉LUT 的治療作用 與HG 組相比,Com.C 組H9C2 細胞凋亡率和TUNEL 陽性細胞率明顯增高;且細胞中fibronectin、collagen I 和α-SMA 蛋白水平明顯增高,p-AMPK/AMPK 比值和SIRT3 蛋白水平明顯降低(P<0.05)。與HG+LUT組相比,HG+LUT+Com.C 組H9C2 細胞凋亡率和TUNEL 陽性細胞率明顯增高;且細胞中fibronectin、collagen I 和α-SMA 蛋白水平明顯增高,p-AMPK/AMPK 比值和SIRT3 蛋白水平明顯降低(P<0.05)。
3 討論
心肌細胞纖維化是DCM 的突出病理特征之一,同時,T2D 心肌纖維化是導致心力衰竭的主要原因[15]。目前對DCM 的治療主要依賴部分化學藥物,如胰島素等,通常具有較大的副作用,效果不理想,缺乏針對性的DCM 治療方法。究其原因可能是因傳統化學藥物作用靶點單一。傳統的中藥具有多靶點協同作用的優勢,因此,有必要尋找新的、更安全有效的傳統中藥以控制和治療DCM[16]。本研究通過STZ 復制T2D 大鼠模型,后給予LUT 處理,發現LUT 可明顯改善T2D 大鼠心肌組織中細胞排列紊亂及間質膠原纖維分布增加情況,且CVF 亦顯著降低,此外,LUT 可明顯逆轉T2D 大鼠心肌組織中fibronectin、collagen I 和α-SMA的高表達。fibronectin、collagen I 和α-SMA 屬于纖維化標志蛋白,增加其表達,肝腎纖維化程度也顯著增加[17-18]。本研究結果表明,LUT 可能抑制STZ誘導的大鼠心肌組織纖維化。
纖維化是一個常見且復雜的病理生理過程,AMPK 是一個參與保持機體物質與能量平衡的重要分子。以往大量研究證實,AMPK 參與多種疾病的發生發展,且在調控纖維化的過程中發揮著重要的作用[19-20]。研究[21]發現,柚皮素可通過激活AMPK 相關通路增強抗氧化反應,減輕心肌纖維化進而明顯削弱DM 小鼠的心肌損傷。在多種疾病模型中,SIRT3已被報道為AMPK 的下游效應物,AMPK-SIRT3 信號的激活有助于改善線粒體功能,緩解疾病的進展[22-23]。研究[24]表明,雷公藤紅素可通過激活AMPK-SIRT3 信號促進抗炎作用,減輕肝纖維化。本研究結果顯示,在STZ 誘導T2D 模型中,大鼠心肌組織中p-AMPK/AMPK 比值和SIRT3 蛋白水平顯著降低,但經LUT 處理后,p-AMPK/AMPK比值和SIRT3蛋白水平明顯回升,以上結果表明,在體內,LUT 可能通過激活AMPKSIRT3 信號參與調控大鼠的心肌纖維化。
為進一步驗證LUT 是否通過激活AMPK-SIRT3 信號參與調控大鼠的心肌纖維化,本研究在體外培養心肌細胞H9C2。首先,通過檢測LUT 對H9C2 細胞增殖活力的影響,篩選LUT 合適的作用濃度和處理時間,發現LUT 可促進HG 誘導的H9C2 細胞增殖;其次,通過檢測LUT 對H9C2 細胞凋亡的影響,發現LUT可顯著降低HG 誘導的H9C2 細胞高凋亡率,表明LUT 參與調控H9C2 細胞增殖及凋亡過程。為進一步探究LUT 對心肌細胞纖維化的影響,本研究通過檢測fibronectin、collagen I 和α-SMA 蛋白水平發現,LUT可明顯降低HG 誘導的H9C2 細胞中高fibronectin、collagen I 和α-SMA 蛋白水平,同時,LUT 還可明顯改善HG對AMPK-SIRT3信號的抑制作用。以上結果表明,在體外,LUT 可能通過激活AMPK-SIRT3 信號參與調控心肌細胞纖維化,與體內結果一致。為更深入的探究LUT 與AMPK-SIRT3 信號的關系,本研究通過添加AMPK 抑制劑干預AMPK-SIRT3 信號,發現AMPK抑制劑與LUT 作用相反,且抑制AMPK-SIRT3 信號可逆轉LUT 對心肌細胞的治療作用。
綜上所述,LUT 通過激活AMPK-SIRT3 信號對抗T2D 大鼠心肌纖維化,本研究為臨床上使用LUT 治療T2D 心肌纖維化提供了理論依據。但本研究并未在大鼠體內使用通路抑制劑完善結論的可信度,且本研究僅是探究了LUT 對AMPK-SIRT3 信號的影響,并未對其他的作用靶點進行研究,故尚存在一定的局限性,仍需后續更深入的研究。

