rL-RVG抑制人小細胞肺癌細胞系NCI-H446的增殖及遷移
梁 冰,嚴玉蘭
(1.昆山市中醫醫院 呼吸科,江蘇 昆山 215300; 2.江蘇大學附屬人民醫院 呼吸科,江蘇 鎮江 212000)
小細胞肺癌(small cell lung cancer, SCLC)是惡性程度較高的惡性腫瘤之一,雖然目前免疫治療對其部分有效,但很多患者因經濟原因或其不良反應而無法耐受免疫治療。新城疫病毒(Newcastle disease virus,NDV)是最常見且最具潛力的溶瘤病毒之一[1]。NDV可以選擇性地殺死腫瘤細胞而不影響正常細胞,因它在癌細胞中復制效率是正常細胞的10 000倍[2]。前期實驗研究發現重組新城疫病毒rL-RVG[3]能夠抑制肺腺癌細胞系A549的增殖,并有促凋亡作用[4],而且rL-RVG能夠影響A549細胞系的遷移及活動減弱[5],但rL-RVG對人小細胞肺癌細胞系NCI-H446的作用機制不詳,本實驗主要探討rL-RVG對SCLC細胞增殖及遷移的影響。
1 材料與方法
1.1 材料
NDV LaSota系、rL-RVG(哈爾濱獸醫研究所);人小細胞肺癌細胞系NCI-H446(上海生命科學研究院細胞庫);胎牛血清、DMEM細胞培養基(維森特生物技術有限公司);HRP-兔抗雞二抗(Earthox公司);FITC-山羊抗鼠二抗、Cy3-山羊抗雞二抗(康為世紀生物科技股份有限公司);兔抗E-cadherin、兔抗MMP2 抗體(博士德生物工程有限公司);核熒光染料(Hoechst33342)、MTT(Sigma-Aldrich公司)。
1.2 方法
1.2.1 免疫熒光法檢測病毒蛋白的表達:將NCI-H446細胞接種在高溫滅菌后的蓋玻片上,將蓋玻片放入24孔細胞培養皿中培養,加入稀釋好的rL-RVG及NDV病毒液,恒溫箱過夜,洗滌,固定,再洗滌,封閉,加入雞抗NDV(1∶150)一抗或小鼠抗狂犬病毒糖蛋白(rabies virus glycoprotein,RVG)(1∶100)一抗,加入Cy3-山羊抗雞(1∶300)二抗或FITC-山羊抗鼠(1∶100)二抗,細胞核用0.2 μmol/L Hoechst 33342作用30 min,封片。于熒光顯微鏡下觀察細胞中的標志物:FITC(綠色)、Cy3(紅色)和Hoechst 33342(藍色)。
1.2.2 MTT法檢測細胞增殖:rL-RVG及NDV病毒液的滴度在雞胚半數感染量為109.8EID50/mL[3-5]。將rL-RVG和NDV用DMEM培養基(不含血清)稀釋至10-1、10-2、10-3和10-4濃度,將增殖期的NCI-H446細胞接種在96孔細胞培養皿,100 μL/孔,在rL-RVG組及NDV組分別加入相應的病毒稀釋液,PBS組為陰性對照組[4],詳細過程見參考文獻[5]。重復實驗3次。計算細胞增殖抑制率[4-5]:細胞活力值=(實驗組平均A值/空白對照組平均A值) ×100%。
1.2.3 細胞劃痕實驗檢測細胞遷移能力:根據參考文獻[5]中方法進行細胞處理,用無菌200 μL槍頭在細胞層中縱向劃線,將PBS、NDV(10-3稀釋度)、rL-RVG(10-3稀釋度)分別感染細胞24 h,光鏡下觀察劃痕寬度。
1.2.4 Transwell小室法檢測細胞遷移能力:在24孔板的Transwell上室內每孔加入100 μL增殖期NCI-H446細胞懸液,下室分別加入含rL-RVG(10-3稀釋度)、NDV(10-3稀釋度)的DMEM液600 μL,對照組加入DMEM液600 μL,37 ℃培養1 d,擦去Transwell上室聚碳酸酯膜表面的細胞,沖洗后用4%多聚甲醛固定上室細胞15 min,再次沖洗后用結晶紫染色20 min,選取5個不同視野,在倒置熒光顯微鏡下(×200)計數穿膜細胞,求平均值。
1.2.5 免疫熒光法檢測遷移途徑:按照1.2.1實驗步驟處理rL-RVG組、NDV組和對照組,后加入E-cadherin、MMP2一抗及對應的二抗,加核熒光抗體后在熒光顯微鏡下觀察。
1.3 統計學分析
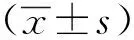
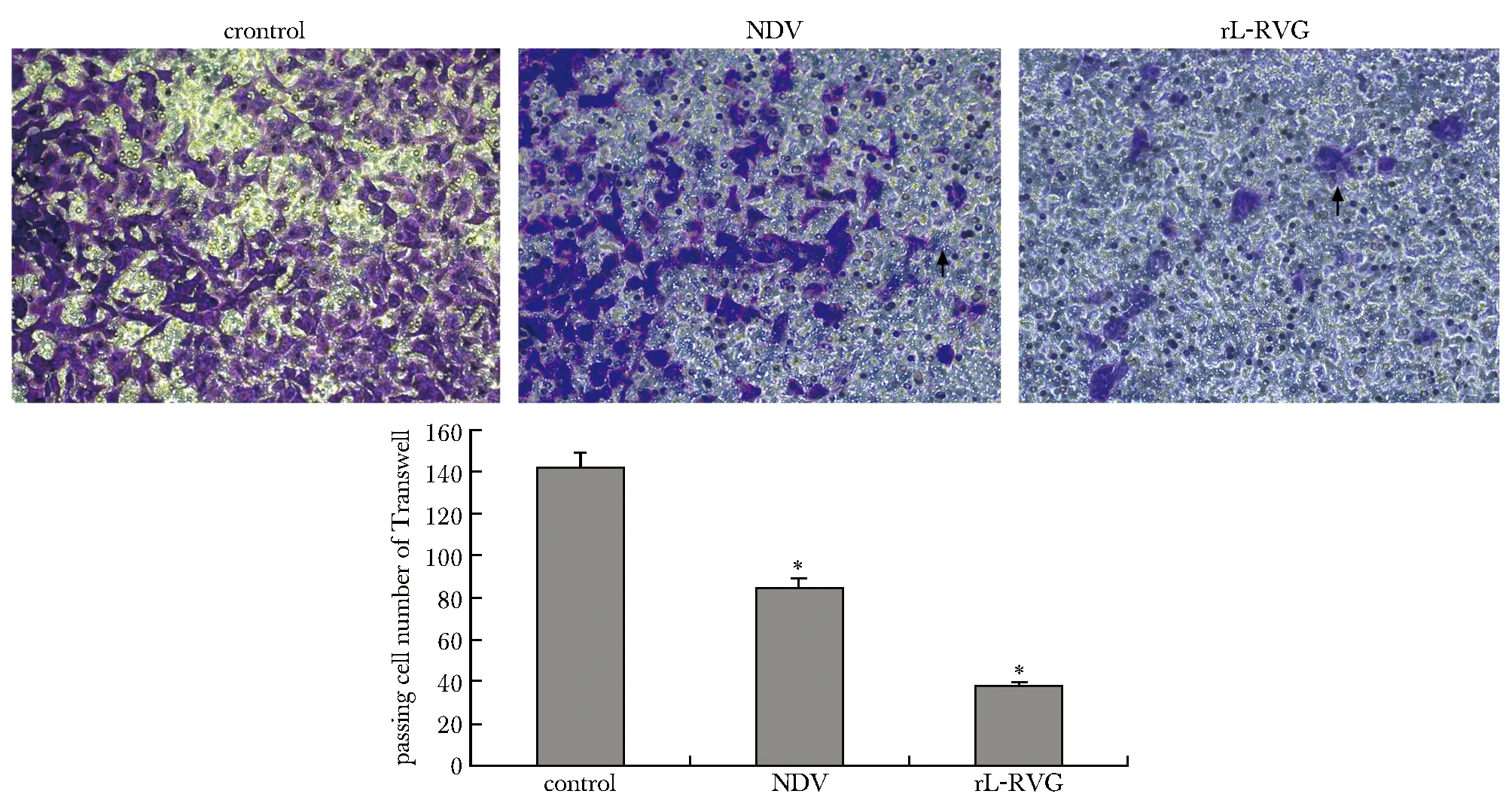
2 結果
2.1 RVG及NDV蛋白在細胞內的表達
在熒光顯微鏡下可見,RVG蛋白及NDV蛋白均可在細胞中穩定表達,NDV熒光蛋白表達量在rL-RVG組較NDV組多(圖1)。
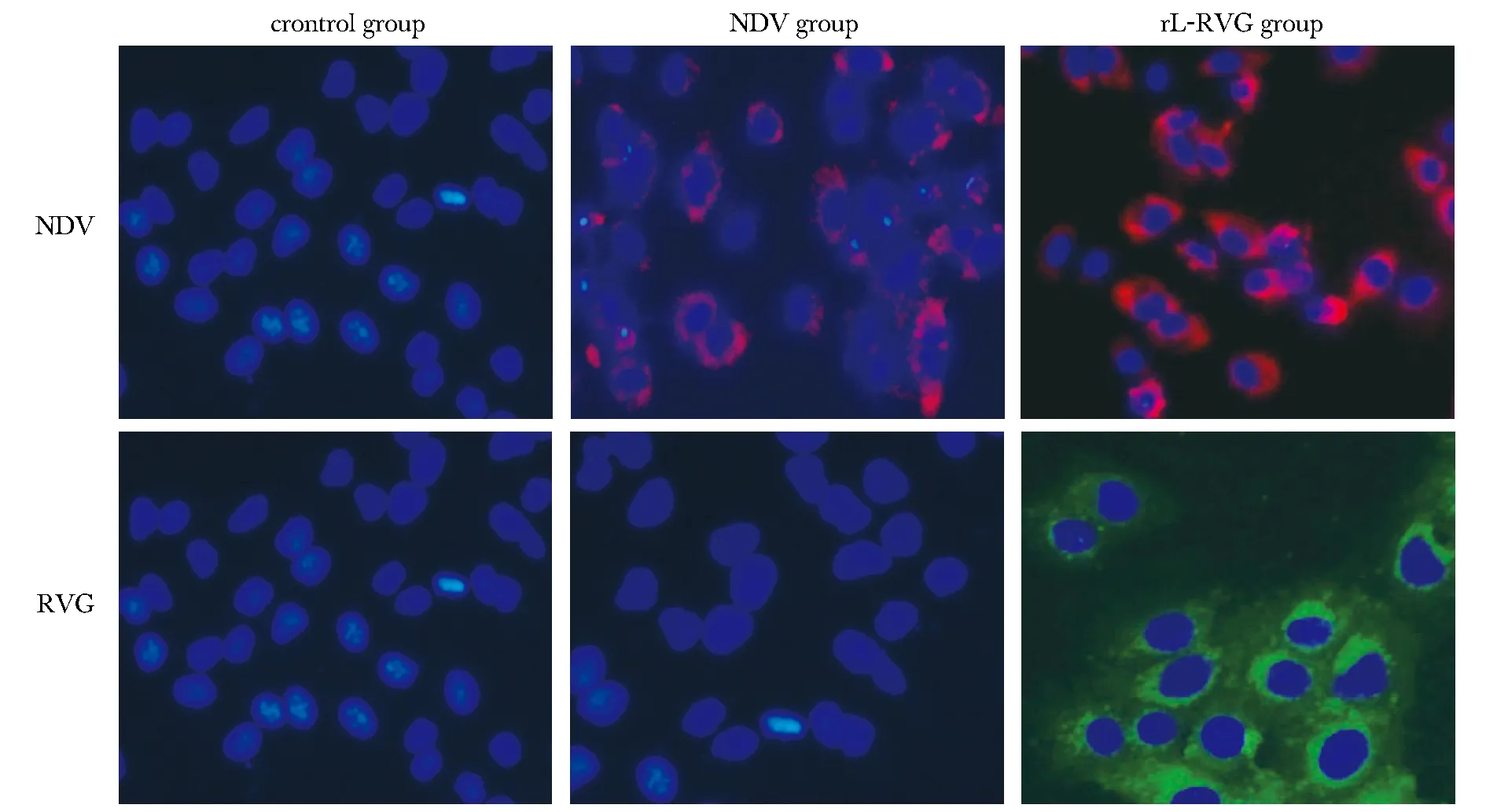
圖1 rL-RVG和NDV感染NCI-H446細胞24 h后RVG蛋白及NDV蛋白的表達
2.2 rL-RVG對細胞增殖的影響
rL-RVG病毒液及NDV病毒液被稀釋成不同濃度,rL-RVG和NDV均對細胞的增殖有一定的抑制作用;病毒濃度越高,對癌細胞的抑制作用越強;rL-RVG對小細胞肺癌細胞的抑制效果強于NDV(P<0.05)(圖2)。
*P< 0.05 compared with NDV group圖2 不同濃度的rL-RVG和NDV對NCI-H446細胞增殖的影響Fig 2 Effect of rL-RVG and NDV at different solubilities on cell proliferation of NCI-H446
2.3 rL-RVG對細胞遷移能力的影響
rL-RVG、NDV及PBS感染細胞劃痕后24 h,細胞的遷移距離分別為(465±40)μm、(739±7)μm及(1 505±13)μm,rL-RVG組細胞遷移距離顯著小于NDV組及對照組(P<0.05)(圖3)。
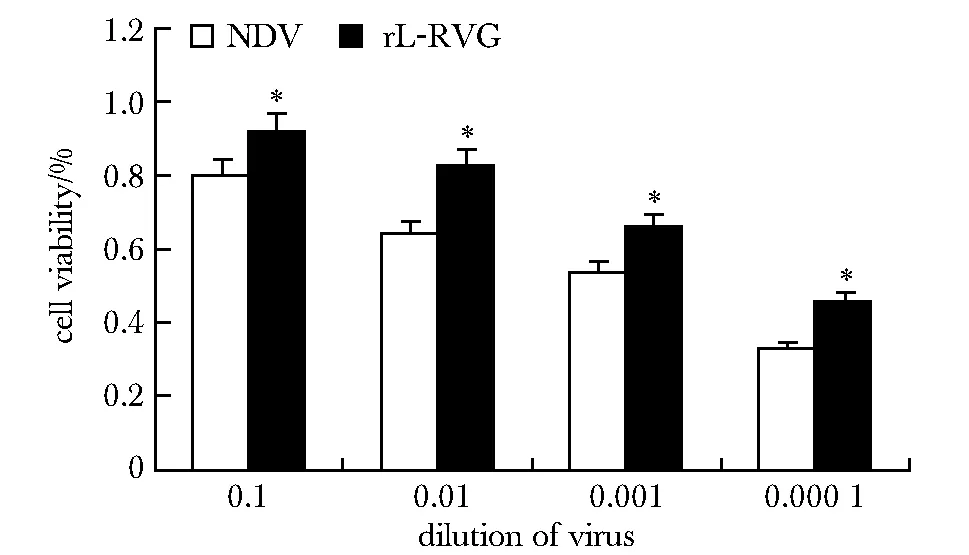
rL-RVG組及NDV組穿過小室的細胞數明顯少于對照組(P<0.05)(圖4)。
相較于對照組及NDV組,MMP2的熒光強度在rL-RVG組中減弱(P<0.05),而E-cadherin 熒光強度升高(P<0.05)(圖5)。
3 討論
小細胞肺癌的侵襲與轉移是其治療失敗的原因之一,嚴重影響患者的治療效果。新城疫病毒(NDV)隸屬禽副黏病毒屬,是一種主要感染禽類的雞瘟病毒[1]。根據NDV在禽類中的致病性,可以被分為3個主要致病型:低毒株、中毒株和強毒株, 其中NDV LoSata系是低毒株, 亦是本實驗選其的原因之一。有臨床試驗表明NDV野生株在各種實體腫瘤治療中未見明顯的不良反應[6],rL-RVG具有安全、高免疫活性、穩定表達的特點[3]。本實驗結果顯示,rL-RVG能在NCI-H446細胞中穩定表達,抑制細胞增殖,并且NDV熒光蛋白表達量在rL-RVG組中較NDV LaSota組多。在劃痕實驗及Transwell小室法中,rL-RVG明顯抑制NCI-H446細胞的遷移,較NDV作用強。細胞遷移是惡性腫瘤侵襲和遷移的關鍵步驟之一[5,7],上皮細胞間質轉化與癌細胞的侵襲和轉移關系密切[5,8]。參與上皮細胞間質轉化的重要調控因子有MMP2和E-cadherin。MMP2在細胞外基質的合成、降解過程中發揮重要作用,其降解細胞外基質的功能是腫瘤細胞侵襲和轉移的基礎,與腫瘤上皮細胞間質轉化的發生密切相關[9-10]。MMP2在SCLC中表達較高[11]。E-cadherin是一種鈣依賴性的跨膜蛋白,參與細胞與細胞間黏附,可以激活鈣黏蛋白,促進橋粒連接形成,能夠參與維持細胞的極性和完整性[5,8]。上皮細胞間質轉化的產生與E-cadherin的異常表達直接相關,在癌侵襲中起著重要作用[5]。本研究發現,rL-RVG感染NCI-H446后影響MMP2及E-cadherin的表達,從而抑制小細胞肺癌細胞的遷移。

圖3 劃痕實驗檢測rL-RVG和NDV對NCI-H446細胞遷移的影響Fig 3 Effect of rL-RVG and NDV on migration of NCI-H446 cells detected by scratch test(×40)
arrow pointed to NCI-H446 cells; *P< 0.05 compared with control group
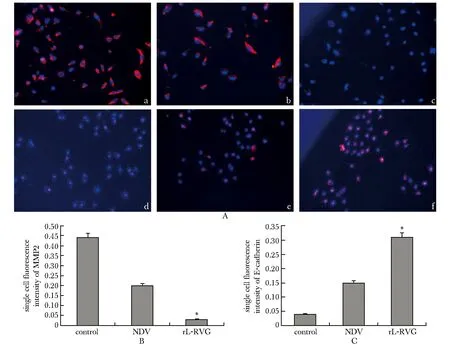
A:immunofluorescence analysis of MMP2 and E-cadherin protein expression: a-c.MMP2 of PBS,NDV and rL-RVG group,respectively, d-f.E-cadherin of PBS,NDV and rL-RVG group,respectively; B:single cell fluorsence intensity of MMP2, *P<0. 05 compared with control and NDV group; C:single cell fluorsence intensity of E-cadherin,*P<0. 05 compared with control and NDV group

