衛星藥房建設提升臨床試驗質量
董 晶 王雅瓊 朱 娜 周學鋒
衛星藥房是由臨床試驗專業科室直接對試驗用藥品進行管理的藥房。它是對符合藥物臨床試驗管理規范(Good Clinical Practice,GCP)藥房的補充。試驗用藥品的類型主要包括申辦方發起的藥物臨床試驗用藥品(GCP藥品),以及研究者發起的臨床研究試驗(Investigator Initiated Trial,IIT)藥品。GCP藥品是指用于臨床試驗的試驗藥物、對照藥品[1]。IIT藥品為已上市的藥品,其研究目的是擴展和優化現有療法,與企業發起的臨床試驗互為補充,以拓展藥物研究的深度和廣度,獲得更多研究數據,為循證醫學提供依據。因此,管理好試驗用藥品關乎醫院的科研水平和科研質量。近年來,青島市中心醫院以GCP藥房和衛星藥房相結合管理,在一定程度上解決了臨床研究用藥問題,為臨床用藥安全提供了保障。
1 為什么要設立衛星藥房
隨著《藥物臨床試驗機構管理規定》[2]的實施,GCP藥房成為藥物臨床試驗機構的必要組織單元,對臨床試驗用藥品進行統一、規范管理。但隨著臨床試驗的發展,IIT項目增多,試驗方案運行及用藥特點不同,使GCP藥房管理壓力逐漸增大,不能滿足臨床試驗科室7 d+24 h的用藥需求。例如,麻醉科、急診科等開展的臨床試驗項目,夜間、節假日取藥頻繁且用藥緊急,用藥時間不規律,由于GCP藥房轉運時間緊,藥品調配困難,影響了臨床研究用藥及試驗的開展。為方便研究臨床科室用藥,衛星藥房管理試驗用藥品的模式應運而生。衛星藥房與GCP藥房管理模式比較見表1。

表1 衛星藥房與GCP藥房管理模式比較
2 衛星藥房的建設
2.1 硬件設施
衛星藥房位于開展臨床試驗項目的臨床科室內部,有獨立的空間儲存試驗用藥品。根據試驗用藥品儲存條件,配備2℃~8℃冰箱、陰涼柜以及加濕器、除濕機、空調等溫濕度控制設備,以保證試驗用藥品儲存環境穩定[3-4]。衛星藥房配有溫濕度采集器,能夠監測環境溫濕度并導出數據記錄,以便在藥品出現超溫時,判斷超溫時限,評估藥品質量。衛星藥房還配有獨立的防火、防盜設備,用電為雙電路電源或配UPS不間斷電源,以保持電源的穩定性。藥房的相關設施設備每年至少檢定或校準一次,在設備設施等硬件方面滿足試驗用藥品的儲存要求。
2.2 人員配備及資質
衛星藥房由臨床科室自行管理,主要由護士/醫師管理藥品,相對于GCP藥房,缺少藥學專業管理人員。衛星藥房管理人員資質要求:首先,科室內部遴選藥品管理員,要求必須具備GCP培訓證書,并定期參加國家或省級的藥物臨床試驗規范化管理培訓,考核合格后方可介入試驗用藥品管理,培訓內容涵蓋試驗用藥品的接收、儲存、發放、回收、退回等管理環節[5]。其次,臨床監查員(Clinical Research Associate,CRA)對所有授權的藥房管理人員單獨進行培訓,培訓方式可采用線上或線下,培訓內容包括但不限于試驗方案、試驗用藥品及其輔助用藥的管理及使用、回收、藥物隨機系統的使用等,并由主要研究者(Principal Investigator,PI)授權。
2.3 文件管理
藥物臨床試驗過程中會產生大量文件資料,這些文件資料是研究過程的源文件,是主管部門核查的依據。衛星藥房劃分資料區,并配備帶鎖文件柜,文件管理包括試驗用藥物管理制度、標準操作規程(Standard Operating Procedure,SOP)及相關表格。本著“誰使用誰制定”原則,由科室藥品管理員制定管理制度,醫院藥品管理員審核,科室PI批準執行。文件內容包括人員職責,藥房管理制度,試驗用藥品的接收、儲存、發放、回收、退回或銷毀,藥品超溫的處理等標準操作規程與記錄,以及應急預案[5-8]。文件資料應由藥品管理員妥善保管,并在試驗完成后統一整理、歸檔至醫院檔案室以備核查。此外,衛星藥房還應保存日常相關文件,如藥品管理員資質、藥房訪問登記、溫濕度記錄表及相關設備設施校準證書等,所有文件保存均要符合防火、防盜、防潮、防蟲的條件,并定期檢查。
3 衛星藥房的質量控制
3.1 衛星藥房問題分析
衛星藥房相對于GCP藥房仍存在缺陷,如部分研究者對試驗用藥品/器械管理不重視、監管缺失、對GCP認識不足、試驗用藥品亂用于非項目內患者等。本研究調查2018年1月—2019年12月所有項目的質控報告、監查報告、稽查報告共50份,統計質控問題238條,其中有關試驗用藥品管理及記錄問題105條,占44.12%。試驗用藥品管理問題及原因見表2。

表2 衛星藥房管理存在的主要問題及原因分析
3.2 質量改進
3.2.1 系統培訓,嚴格考核 通過培訓、講評等方式強化衛星藥房管理人員全過程質控意識,提高各環節管理水平[6]。第一,醫院藥品管理員擔負衛星藥房監管責任,積極組織藥學基本知識及《中華人民共和國藥品管理法》相關內容培訓及考核,彌補衛星藥房藥品管理員的知識短板,強化藥學專業知識。第二,督促衛星藥房藥品管理員定期參加院內及院外GCP培訓,并考核GCP法律法規和臨床試驗標準操作規程等[9],強化科學管理思維。第三,建立衛星藥房管理微信群,醫院藥品管理員將工作中遇到的問題及注意事項同步分享給衛星藥房藥品管理員,以達到實時培訓和強化藥學知識的目的。
3.2.2 制定藥品檢查對照表 試驗用藥品管理是衛星藥房的主要工作。醫院藥品管理員與衛星藥房管理員結合日常工作中遇到的問題及管理經驗開展頭腦風暴,并基于風險質量管理,共同梳理了55項《藥品檢查細則》,涵蓋人員資質管理、藥品環境管理、試驗用藥品的接收/供應管理、儲存管理、使用管理、回收管理等6個方面[6,10-12],并作為日后衛星藥房的質量管理標準。此外,化繁為簡,將SOP轉化為流程圖,以卡片形式制定“衛星藥房管理小貼士”,供臨床試驗協調員(Clinical Research Coordinator,CRC)隨時查閱。
3.2.3 信息化監管 該院于2020年3月正式將試驗用藥品納入醫院信息管理系統(Hospital Information System,HIS),將試驗用藥品賦予“GCP”標識,與醫院常規用藥相區別,并通過權限管理限制試驗用藥品的開立。臨床研究醫生通過HIS開立試驗用藥品,藥房自動打印處方。藥品管理員與項目質控員可第一時間接收試驗項目的入組情況或進程[13]信息,有效把握質控節點,及時跟進項目質量情況,提高了質控效率。根據《藥物臨床試驗質量管理規范》,信息化管理實現了臨床試驗用藥醫囑載入門診/住院電子病歷系統,通過系統權限管理,規范試驗用藥品使用和研究病例記錄,切實實現了試驗用藥品的閉環管理。
3.2.4 以藥品為核心的臨床試驗全過程質控 臨床試驗項目實施過程的記錄是數據產生與獲取的重要環節,其質量控制有利于及時發現問題,針對性提高藥物臨床試驗質量。以藥品為核心,構建臨床試驗項目的質控模式,將有利于臨床試驗的全過程質控[9]。試驗用藥品貫穿整個臨床試驗的倫理審查、項目啟動、藥品管理、試驗實施、試驗結束全過程[13]。具體質控內容有:倫理審查涉及藥品包裝標簽設計的合規性、備案批號藥檢報告的完整性;項目啟動包括試驗方案、藥品管理流程及特殊注意事項、獲得授權、收集研究者簽名樣張以備日后核對處方信息;藥品管理涉及試驗用藥品的接收、分發、回收、退還,以及藥品管理文件記錄的及時性、完整性;試驗實施中的質控包括藥品首次發放前審核受試者知情同意書是否簽署、版本是否正確、入排標準核對、既往病史及合并用藥記錄、化驗單判定、是否由授權醫生開立處方、核對藥品隨機單信息等;試驗結束涉及藥品退還申辦方的結題質控和數據清理。
3.3 管理成效
上述措施實施后,該院選取2020年10月—2021年10月啟動并運行的臨床試驗28項,抽取其質控報告50份,共計94條質控問題,試驗用藥品管理相關記錄24條,占比25.53%,管理效果較前明顯改善。衛星藥房試驗用藥品質控問題頻次均有所下降:藥品接收為4條;藥品儲存為11條;藥品分發、使用、回收為7條。分析研究病例相關質控問題(知情同意、病程記錄規范、不良事件/嚴重不良事件相關、方案違背、電子數據采集系統錄入、檢查檢驗判定等),頻次由133條降低至70條,試驗質量有所提升,見圖1。
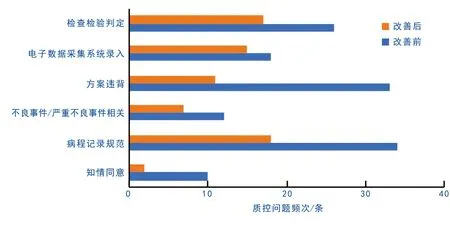
圖1 實施前后試驗病例質控問題比較
4 結語
臨床試驗是對試驗用藥品療效、安全性的探索,保證試驗用藥品規范使用,一定程度上可避免試驗結果偏倚。試驗用藥品管理是藥物臨床試驗的關鍵環節,衛星藥房的建設確保了臨床研究的用藥安全,提高了研究效率。該院以衛星藥房自主管理為主,GCP藥房監督為輔,充分發揮了藥師優勢,使試驗用藥品管理更加規范、高效。藥師可根據自身專業方向在藥物臨床試驗領域找準定位,充分發揮其專業優勢[14-15],評估藥物試驗進程中的質控點,基于風險進行質量管理,確保藥物臨床試驗規范化發展。目前,該院衛星藥房質控模式對于不良事件/嚴重不良事件的判定、疾病進展等醫學判斷仍有局限性,還需協同臨床科室項目專業質控員共同提高臨床試驗質量。

