檸檬皮多酚對胰島素抵抗的HepG2細胞葡萄糖消耗量的影響
王瑞雪,房一明,郭娜,姚晶,張筠,初眾
1. 黑龍江東方學院食品工程學院(哈爾濱市 150066);2. 中國熱帶農業科學院香料飲料研究所(萬寧市 571533)
糖尿病是由于胰島素分泌不足而引發的代謝紊亂疾病,主要分為Ⅰ型和Ⅱ型,其中Ⅱ型糖尿病患者占多數[1-2]。胰島β細胞功能缺陷和胰島素抵抗是Ⅱ型糖尿病的主要成因,胰島素抵抗主要表現為肝臟及其外周組織對葡萄糖的攝取和利用能力下降[3-5]。建立細胞模型是一種在體外探究物質功能性的試驗手段,HepG2細胞與正常肝細胞功能相近,在高濃度胰島素作用下,其表面的胰島素受體減少,較易產生胰島素抵抗,故此,用高濃度的胰島素誘導建立的IRHepG2模型是篩選改善胰島素抵抗成分的理想細胞模型[6-11]。
檸檬(Citrus limon)屬蕓香科柑橘屬,檸檬果皮占整個檸檬的20%左右,是檸檬加工的主要副產物[12]。其果皮富含精油、果膠、酚酸、類黃酮等活性物質,具有抗氧化、抗癌、抗菌和降血糖等作用[13-16]。試驗首先探究IR-HepG2細胞模型的最佳建立方法,其次來研究檸檬皮多酚對IR-HepG2細胞葡萄糖消耗量的影響,以期為進一步研究檸檬皮多酚的降血糖功能奠定試驗基礎。
1 材料與方法
1.1 材料與試劑
HepG2細胞株、DMEM高糖培養基、PBS、0.25%EDTA-胰酶、青-鏈霉素(蘇州美侖生物科技有限公司);胎牛血清(哈爾濱市立峰生物工程有限公司);鹽酸二甲雙胍、MTT、DMSO(北京博奧拓達科技有限公司);胰島素(Beyotime公司);葡萄糖檢測試劑盒(上海榮盛生物藥業有限公司);純度68%檸檬皮多酚(實驗室自制)。
1.2 儀器與設備
150iCO2細胞培養箱(美國Thermo公司);TS2-FL倒置顯微鏡(日本Nikon公司);SW-CJ-2FD超凈工作臺(上海博迅生物儀器股份有限公司);80-2離心機(上海浦東物理光學儀器廠);RT-6000酶標分析儀(深圳雷社生命科學股份有限公司)。
1.3 試驗方法
1.3.1 細胞培養
結合Seyfizadeh等[17]和馬萍等[18]的方法,將凍存的HepG2細胞于37 ℃水浴中1 min內快速解凍,于89%DMEM∶10%胎牛血清∶1%青-鏈霉素的培養基和37℃、5% CO2濃度的培養箱中培養,2~4 d按1∶3傳代。
1.3.2 不同濃度胰島素對HepG2細胞存活率的影響
參考隋淼等[19]的方法稍作修改,設立空白組(不含細胞)、對照組(含細胞不加胰島素)和模型組(含細胞和不同濃度胰島素),將HepG2細胞消化后,吹打均勻,以每孔2×104個細胞鋪于96孔板,培養過夜,模型組分別加入胰島素濃度為1×10-5,1×10-6,1×10-7,1×10-8和1×10-9mol/L的DMEM培養液,100 μL/孔,于37 ℃培養24 h后,根據MTT法[20],加入5 mg/mL MTT溶液(10 μL/孔),4 h后移除培養液,加入DMSO(150 μL/孔),充分振蕩,酶標儀492 nm測定吸光度,根據式(1)計算細胞存活率。

1.3.3 胰島素抵抗模型的建立
1.3.3.1 胰島素最佳作用濃度和時間的確定
參考王夢等[21]的方法稍作修改,設立空白對照組(不含胰島素)和胰島素組(分別加入胰島素終濃度為1×10-5,1×10-6,1×10-7,1×10-8和1×10-9mol/L的培養基),HepG2細胞鋪板同1.3.2小節,培養過夜,棄去舊液,加入各濃度胰島素培養液,100 μL/孔,培養48 h,每12 h用葡萄糖檢測試劑盒測定一次葡萄糖消耗量(方法參照試劑盒說明書),按式(2)、(3)計算葡萄糖消耗量和消耗率。


式中:Δm為葡萄糖消耗量,mmol/L;M為葡萄糖消耗率,%;n為空白對照組葡萄糖消耗量,mmol/L;m為模型組葡萄糖消耗量,mmol/L。
1.3.3.2 IR-HepG2模型穩定性的測定
用1.3.3.1小節中的最佳建模方案建模后,棄去舊液,更換為正常培養液,繼續培養72 h,每隔24 h測定一次葡萄糖消耗量(方法同1.3.3.1小節)。
1.3.4 IR-HepG2細胞葡萄糖消耗量及存活率的測定
結合符群等[22]和齊佳等[23]的方法稍作修改,以1.3.3小節中最佳建模方案建模,設空白對照組和0.05mg/mL二甲雙胍陽性對照組以及LPP樣品組,LPP終質量濃度分別為2.5,2,1.5,1,0.5和0.1 mg/mL,分別培養24,48和72 h,測定LPP干預后IR-HepG2細胞存活率(方法同1.3.2小節)及其培養液中葡萄糖的含量(方法同1.3.3小節),探究不同濃度的檸檬皮多酚對IR-HepG2細胞存活率和葡萄糖消耗量的影響。
1.4 數據處理
數據采用Origin 2019b、SPSS 17.0進行繪圖及數據分析,以Duncans’法進行組間差異顯著性分析。
2 結果與分析
2.1 不同濃度胰島素對HepG2細胞存活率的影響
通過測定24 h時各組細胞在不同劑量胰島素作用后的細胞存活率來判斷用胰島素建模的安全用藥濃度。
由表1可知,除1×10-8mol/L的胰島素組外,其余濃度的胰島素組,隨胰島素濃度增加,吸光度減小,1×10-8mol/L的胰島素可能對細胞生長具有促進作用。胰島素濃度在1×10-5~1×10-9mol/L濃度范圍內時,細胞存活率均在80%以上,對細胞基本無毒副作用,因此后續建模安全給藥濃度可以設置在1×10-5~1×10-9mol/L范圍內[24]。
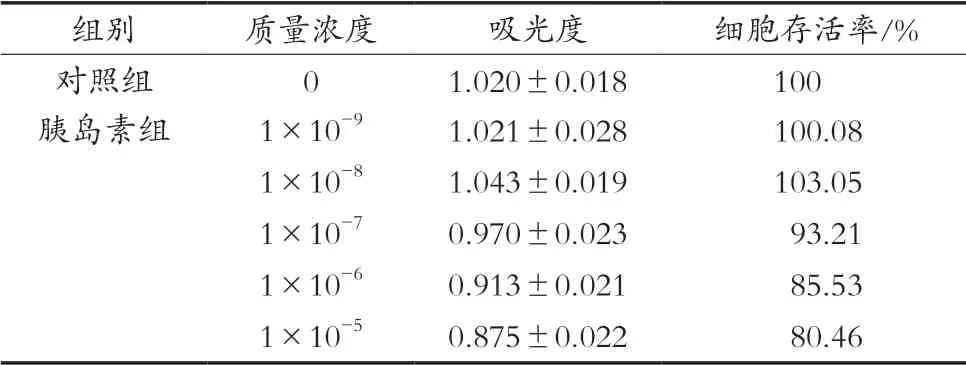
表1 不同濃度的胰島素對HepG2細胞存活率的影響(n=5)
2.2 建立胰島素抵抗模型
2.2.1 確定最佳濃度和作用時間
經過對比空白對照組和樣品組在各時間段的葡萄糖消耗量,來判斷IR-HepG2細胞模型的最佳建模方案。
由圖1可知,在0~12 h與對照組相比胰島素組的葡萄糖消耗量除了胰島素濃度為1×10-8mol/L組以外差異均不明顯,在細胞培養的前12 h內,HepG2細胞攝取葡萄糖的能力良好,未出現胰島素抵抗的現象。在細胞培養到24 h時,部分濃度下的HepG2細胞葡萄糖攝取和利用能力出現異常,當胰島素濃度為1×10-5mol/L和1×10-6mol/L時,葡萄糖消耗量相比前12 h有所下降,僅為1.81±0.05 mmol/L和1.84±0.11 mmol/L,與對照組相比葡萄糖消耗量分別減少了34.4%和33.3%,差異顯著(P<0.05),此時可以判斷HepG2細胞出現了糖代謝紊亂現象,且這兩組的葡萄糖消耗量在12~48 h內均顯著(P<0.05)低于對照組,在24 h時抵抗狀態最為明顯。結合1.3.4的細胞存活率,最終確定培養液中胰島素的濃度為1×10-6mol/L培養24 h為最佳建模方案。該結果與劉志霞等[25]建立IR-HepG2模型時所用的胰島素添加量和誘導時間相吻合。
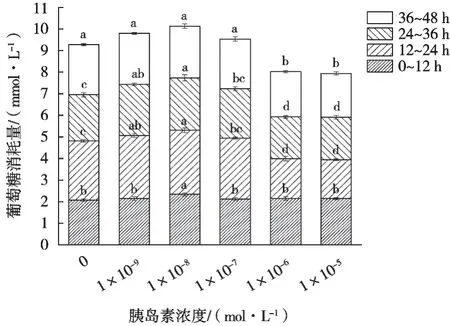
圖1 不同濃度胰島素對HepG2細胞葡萄糖消耗量的影響(n=5)
2.2.2 IR-HepG2模型穩定性評估
培養液胰島素濃度1×10-6mol/L作用24 h后IRHepG2細胞更換為正常培養基中每隔24 h測定葡萄糖消耗量,結果見表2。

表2 IR-HepG2細胞模型去負荷后不同時間點的葡萄糖消耗量(n=5) 單位:mmol/L
由表2可知,與對照組相比,胰島素組在24~72 h內HepG2細胞的葡萄糖消耗量更低,具有顯著性差異(P<0.05),因此本方法建立的IR-HepG2細胞模型可持續72 h。
2.3 檸檬皮多酚對IR-HepG2細胞葡萄糖消耗量及存活率的影響
用0.1~2.5 mg/mL的LPP分別作用于IR-HepG2細胞24,48和72 h,測定葡萄糖含量及細胞存活率。如圖2~圖3。
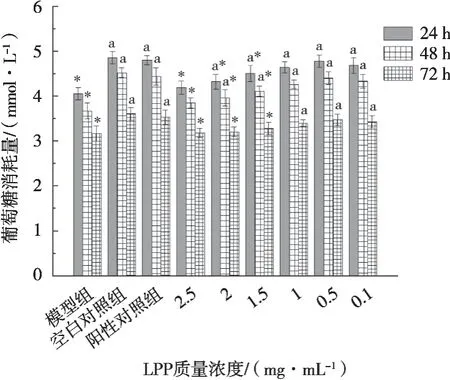
圖2 檸檬皮多酚對IR-HepG2細胞葡萄糖消耗量的影響(n=5)
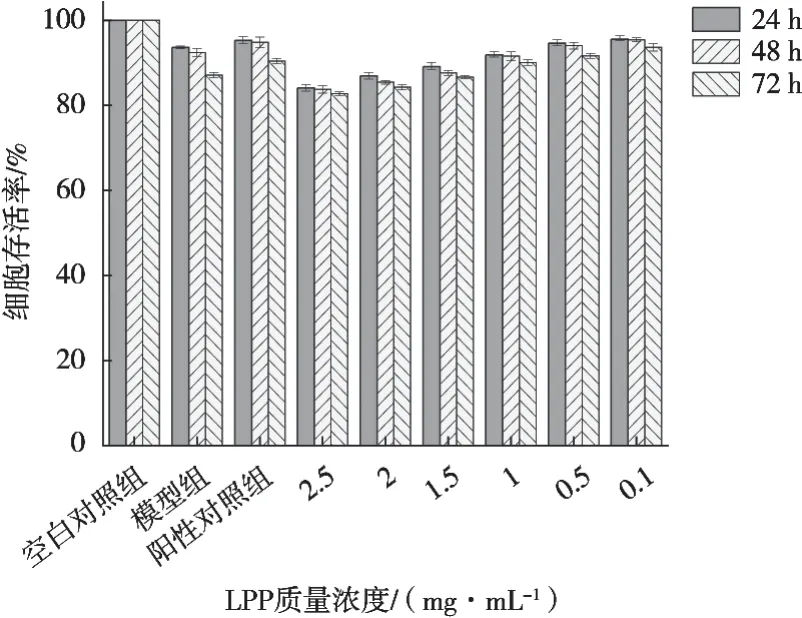
圖3 LPP對IR-HepG2細胞存活率的影響(n=5)
由圖2可知,各組葡萄糖消耗量隨時間的增加逐漸降低,出現這個趨勢的原因極可能是與細胞活性有關,隨著培養時間增加,細胞存活率逐漸下降,利用葡萄糖的能力有所下降[26]。模型組的葡萄糖消耗量在各時間段均顯著低于空白對照組,說明細胞出現了葡萄糖代謝異常[27]。與模型組相比,陽性對照組和LPP濃度為0.1~2 mg/mL時的葡萄糖消耗量在各時間段均顯著(P<0.05)高于模型組,且在LPP濃度為0.5 mg/mL時葡萄糖消耗量整體達到了峰值,在24 h時最高(4.78±0.13 mmol/L),比模型組的葡萄糖消耗率高了15.1%。與陽性對照組相比,在LPP質量濃度為0.1~1 mg/mL時各時段的葡萄糖消耗量與陽性對照組差異不顯著(P>0.05),說明LPP在這個濃度范圍內與0.05 mg/ml的二甲雙胍改善胰島素抵抗的能力相近。與王夢麗[28]研究的莢蒾果多酚相比,LPP在相同劑量(0.05 mg/mL)和培養時間(24 h)下對葡萄糖的消耗量比莢蒾果多酚多了1.29 mmol/L,相比之下LPP改善胰島素抵抗的效果更好。
評價LPP緩解胰島素抵抗時,對IR-HepG2細胞活性的影響,以確保對細胞的安全性。測定LPP在不同濃度和時間下,對IR-HepG2細胞存活率的影響,如圖3。
從圖3中可以看出,相較空白對照組,各組細胞存活率均在80%以上,且樣品組隨著LPP濃度的降低細胞存活率上升,呈現劑量依賴性,說明高濃度的LPP對IR-HepG2細胞存活率有一定的抑制作用[29]。整體趨勢表明24 h時細胞存活率高于其他時間組,72 h時細胞存活率最低。可判定24 h可作為LPP改善胰島素抵抗干預的最佳時間[30]。
3 結論
文章以 HepG2細胞為載體,通過建立最佳的IRHepG2細胞模型,探究檸檬皮多酚對IR-HepG2細胞葡萄糖消耗量的影響。研究發現當培養液中胰島素濃度為1×10-6mol/L培養24 h時可以建立效果最佳的IRHepG2細胞模型。當檸檬皮多酚質量濃度在0.1~2 mg/mL時可以明顯提高IR-HepG2細胞對葡萄糖的攝取和利用,但是對于其作用機制還不清楚,因此還需繼續深入探究其作用機制,為檸檬皮多酚在食品、生物醫藥等領域的運用提供理論依據。

