天然產(chǎn)物來源的β位淀粉樣蛋白前體蛋白切割酶1抑制劑的研究進展
趙澤豐,年 夢,姬曉彤,楊曉航,喬海法*
1.陜西中醫(yī)藥大學針灸推拿學院,咸陽 712046;2. 陜西省針藥結合重點實驗室,咸陽 712046;3.咸陽市神經(jīng)生物學(針灸)重點實驗室,咸陽 712046
在阿爾茨海默病(Alzheimer’s disease, AD)諸多的發(fā)病原因假說中,有學者提出β淀粉樣蛋白(Aβ)是AD發(fā)生的重要始動因素[1],并且在AD發(fā)展過程中發(fā)揮著至關重要的作用[2]。Aβ通過多種機制損傷神經(jīng)元,擾亂突觸功能,最終導致AD相關的認知功能障礙。Aβ是由36~43個氨基酸殘基組成的多肽,其主要成分為Aβ40和Aβ42,由β-淀粉樣前體蛋白(β-APP)先后經(jīng)β-分泌酶和γ-分泌酶水解生成,其中在細胞中Aβ40產(chǎn)生的量是Aβ42的9倍,較長的Aβ42更易發(fā)生聚集,具有較強的神經(jīng)細胞毒性[3]。β位淀粉樣蛋白前體蛋白切割酶1(BACE1,又稱β-分泌酶)是一種天冬氨酸蛋白酶,它在腔隙中精準切割APP的β位點,該步驟被認為是決定Aβ生成的限速步驟。BACE1抑制劑具有多種優(yōu)勢,能對APP的初步水解進行限制,在早期預防Aβ的生成。
目前,已有多種針對BACE1靶點的抑制劑進入上市前的臨床研究,包括處于臨床二期階段的阿斯利康的AZD3293、臨床三期的默克MK-8931、衛(wèi)材臨床三期的E2609等[4]。多種天然產(chǎn)物來源的BACE1抑制劑近年來也被各課題組廣泛報道,本文將根據(jù)抑制劑的結構類型對其進行分類,并對抑制劑的來源植物、有效劑量等方面進行總結,以期為該類天然產(chǎn)物的進一步開發(fā)提供理論依據(jù)。
1 BACE1的結構特征
隨著包括冷凍電鏡在內的結構生物學手段的進步,目前,BACE1蛋白的三維結構被解析并用于其抑制劑的篩選中[5-6],處于臨床研究或臨床前研究的抑制劑與BACE1的共晶結構均被報道[7]。結構上,BACE1與同源度較高蛋白B位淀粉樣蛋白前體蛋白切割酶2(BACE-2)等具有相似性,其催化活性位點空間較大,包含氨基酸殘基及10S loop區(qū)等,故設計與開發(fā)尺寸合適的小分子配體占據(jù)該活性位點具有一定挑戰(zhàn)性。BACE1屬于Ⅰ型跨膜天冬氨酸蛋白酶家族,由501個氨基酸組成(見圖1)。它有一個N端、一個C端和一個連接N端和C端結構域的間結構域。BACE1位于酸性細胞內室,包括反式高爾基體網(wǎng)絡和核內體裂解底物,促進Aβ蛋白片段的形成。目前研究表明,在酸性條件下,BACE1的酶活力處于最佳狀態(tài),BACE1抑制劑在結構上一般需要具有堿性基團裸露,酸度系數(shù)pKa在6.0以上往往表現(xiàn)出更好的親和力。位于配體結合位點的催化二聯(lián)體Asp32和Asp228(見圖1)對酶的蛋白水解活性至關重要。配體與2種氨基酸結合會增強結合親和力。

注:A.BACE1的蛋白結構;B.BACE1與配體的結合口袋。
根據(jù)BACE1的結構,目前已有多種抑制劑設計的研究被報道。早期設計的BACE1抑制劑以其底物類似物為主,主要是肽類和擬肽類抑制劑。肽類抑制劑針對BACE1在APP切割位置周圍的氨基酸序列而設計,此類抑制劑的化學結構上都有羥基的存在,可以與天冬氨酸蛋白酶的活性殘基以氫鍵結合從而達到抑制BACE1活性的目的[8]。但由于多肽抑制劑的口服生物利用度低、體內易水解、相對分子質量大、氫鍵供體及氫鍵受體數(shù)量較多等特征使得它們難以滲透,特別是難以通過血腦屏障,嚴重限制了其進一步在臨床應用。此后,在肽類抑制劑的研究基礎上,通過生物電子排體等藥物設計手段,研究者又設計了具有較小相對分子質量的擬肽類抑制劑及非肽類抑制劑等小分子抑制劑[9],為BACE1的小分子抑制劑探索與開發(fā)奠定了堅實的基礎。
2 天然產(chǎn)物來源的BACE1抑制劑
在我國,已有多種基于包括中藥在內的天然產(chǎn)物結構開發(fā)的成藥上市,其中包括抗AD藥物石杉堿甲[10]、抗卒中藥物丁苯酞[11-12]等。與合成藥物相比,天然化合物具有較高的安全性及多樣的分子骨架。目前,包括黃酮、三萜及甾體、香豆素、蒽醌、鞣質多酚及生物堿在內的多種成分已被報道具有BACE1抑制活性,本文將根據(jù)結構類型進行分類,對天然產(chǎn)物來源的BACE1抑制劑進行總結,并通過表格直觀總結各抑制劑的化學結構、來源植物及有效劑量,見表1。

表1 天然產(chǎn)物來源的BACE1抑制劑

表1(續(xù)) 天然產(chǎn)物來源的BACE1抑制劑
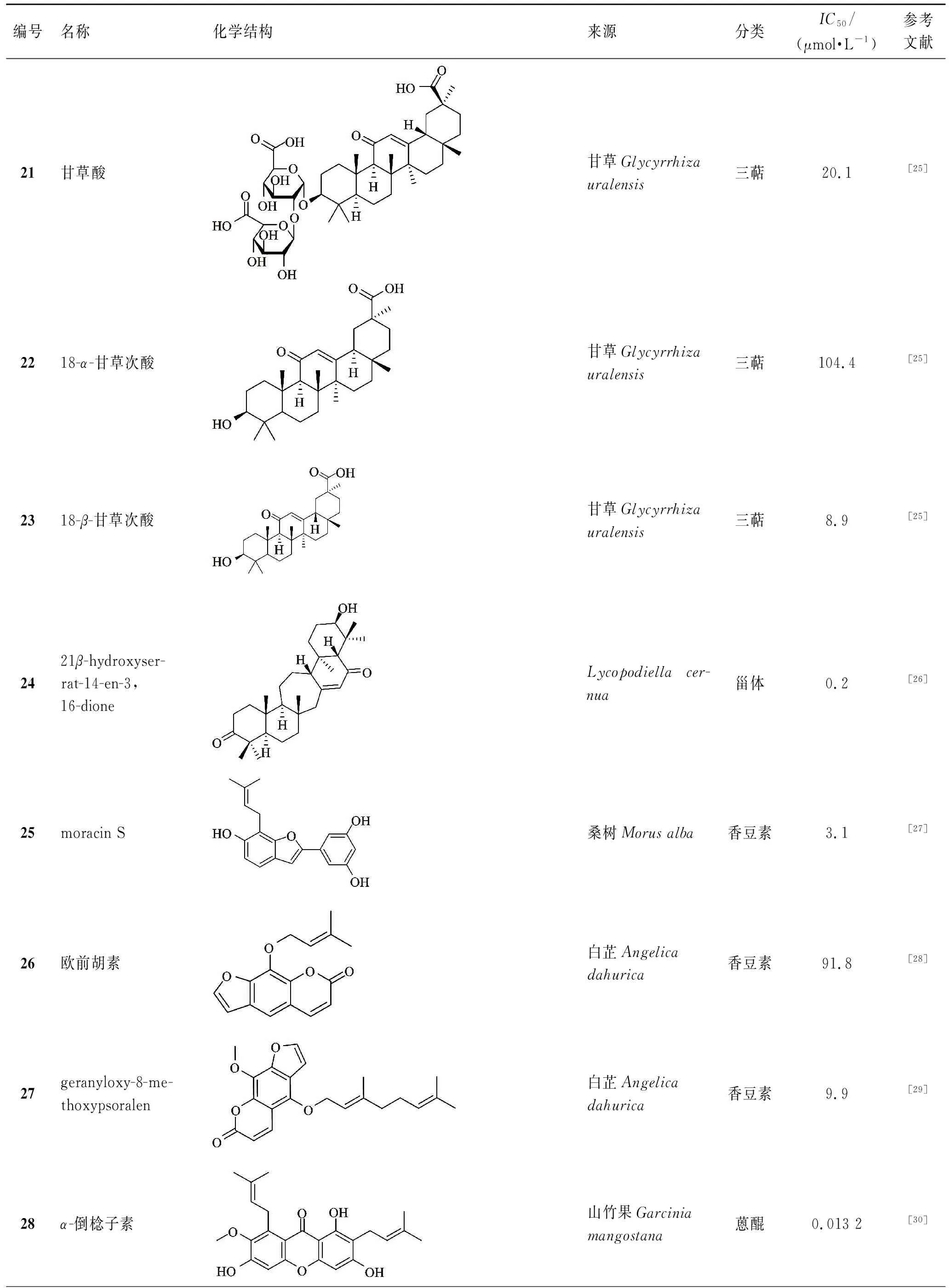
表1(續(xù)) 天然產(chǎn)物來源的BACE1抑制劑
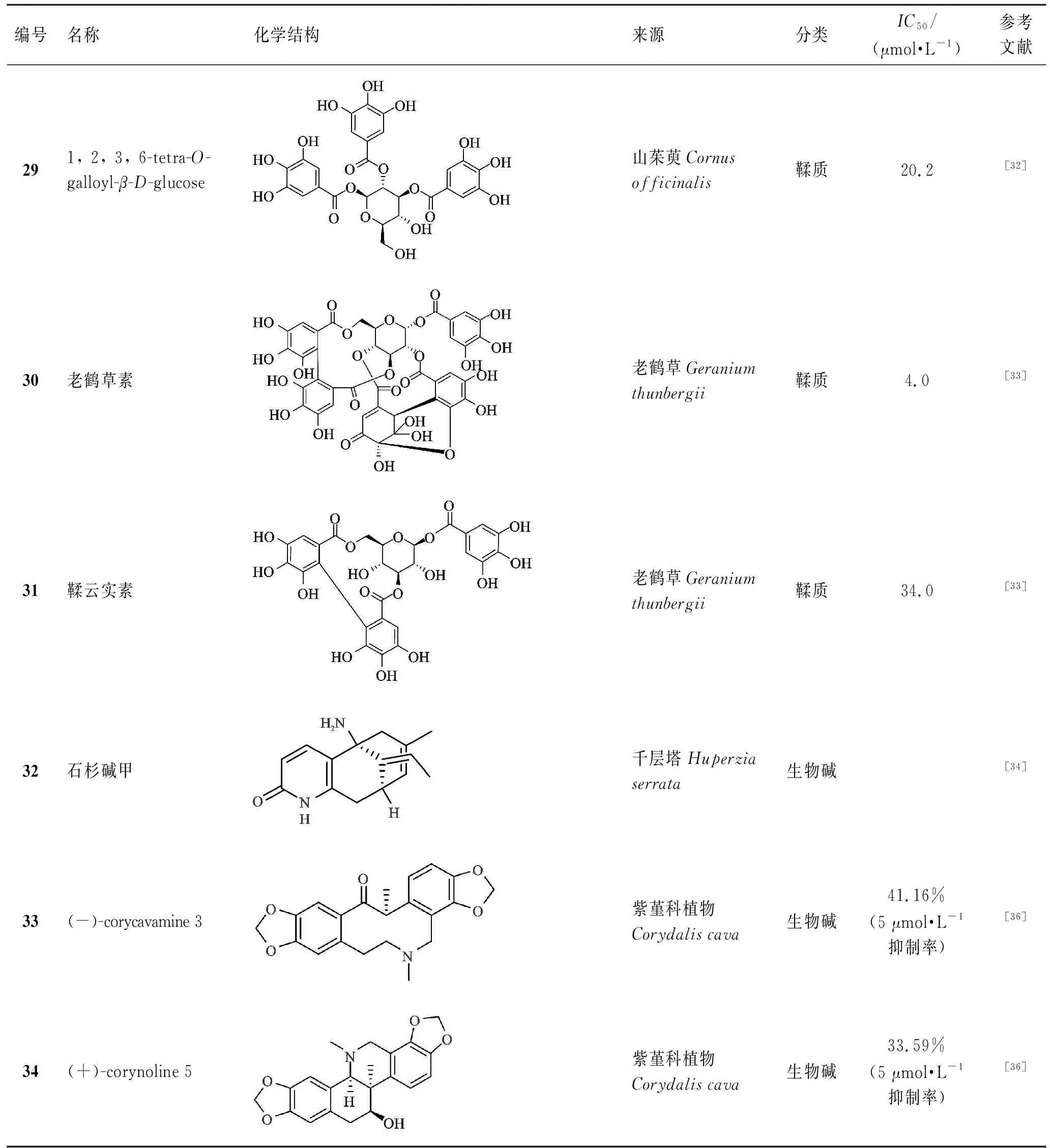
表1(續(xù)) 天然產(chǎn)物來源的BACE1抑制劑
2.1 黃酮類BACE1抑制劑
在開發(fā)天然產(chǎn)物BACE1抑制劑的過程中,許多研究者將目光投向了藥用植物中富含的黃酮類化合物。黑姜(Kaempferiaparviflora)中提取的多甲氧基黃酮主要由3種成分組成:5,7-二甲氧基黃酮(DMF),5,7,4′-三甲氧基黃酮(TMF)和3,5,7,3′,4′-五甲氧基黃酮(PMF),以上3個多甲氧基黃酮類化合物均被報道具有較強的BACE1抑制活性,而對α-分泌酶和其他絲氨酸蛋白酶的影響不顯著,具有較強的選擇性。KUMJU YOUN等[13]針對BACE1靶點抑制的多甲氧基黃酮開展了深入研究,結果表明,黑姜多甲氧基黃酮具有較強的BACE1抑制活性,其中TMF(化合物1,見表1)對BACE1的抑制效果最強,半數(shù)抑制濃度(IC50)為36.9 μmol·L-1,其次分別為DMF(化合物2,IC50為49.5 μmol·L-1)和PMF(化合物3,IC50為59.8 μmol·L-1)。構效關系研究表明,黃酮A環(huán)上C-5和C-7處的甲氧基及B環(huán)C-4′處的甲氧基提升了BACE1抑制活性(TMF>DMF>PMF),C-3處和C-3′位置上的甲氧基降低了BACE1的抑制活性。酶動力學實驗證明這些化合物是通過結合異構位點與酶相互作用,因此是非競爭性BACE1抑制劑,其抑制機制與直接和活性部位結合的人工合成的多肽類化合物作為競爭性抑制劑不同[14]。
此外,KUMJU YOUN等[15]對鷹嘴豆素(4)的BACE1抑制活性進行了探究。鷹嘴豆素為廣泛存在于中藥與功能食品中的一種異黃酮,研究表明,該化合物對BACE1的IC50為20 μmol·L-1,其抑制特征為非競爭性抑制。2017年KUMJU YOUN等[16]還從橘皮中提取得到了多種BACE1抑制活性成分,其結構均為多甲氧基黃酮類似物,典型化合物包括川陳皮素(5)、桔皮素(6)及5,6,7,3′,4′-五甲氧基黃酮(7),其抑制BACE1的IC50分別為59、49、63 μmol·L-1。
ZHENXING ZOU等[17]從深綠卷柏(Selaginelladoederleinii)中分離得到的黃酮三聚體化合物,被證實對BACE1有較好的抑制作用。在分離出的多種黃酮三聚體類化合物中,化合物8表現(xiàn)出較強的BACE1抑制潛力,體外熒光共振能量轉移法檢測結果表明,其抑制BACE1的IC50為0.75 μmol·L-1,其結構單元為柚皮素。
MD YOUSOF ALI等[18]報道了3種黃酮苷類化合物香風草苷(9)、枸橘苷(10)和柚皮素-7-O-葡萄糖苷(11)具有BACE1抑制活性(IC50分別為 2.3、4.0、13.4 μmol·L-1)。酶動力學研究發(fā)現(xiàn),這3種化合物均為BACE1混合型抑制劑,并且能夠減少Aβ在淀粉樣蛋白生成途徑中的聚集。進一步研究表明,這些黃酮苷類化合物對BACE1的抑制活性優(yōu)于黃酮苷元槲皮素(IC50為21.7 μmol·L-1)。
QING-XIA XU等[19]從補骨脂(Cullencorylifolium)中分離得到4種異戊烯基黃酮類化合物,并測定了其多靶點抗AD活性,結果發(fā)現(xiàn),4種化合物均具有一定的BACE1抑制活性,其中補骨脂查爾酮(12)表現(xiàn)出較顯著的BACE1抑制活性,其100 μmol·L-1抑制率為63%,進一步研究表明,該化合物也具有較強的抗Aβ42聚集活性,適宜作為先導物進行進一步開發(fā)。
JIAYI TAO等[20]從筒鞘蛇菰(Balanophorainvolucrata)中分離得到了多種二氫查爾酮及二氫黃酮類化合物并測定了其BACE1抑制活性,結果表明,化合物3,4,2′,6′-tetrahydroxydihydroflavone-4′-O-β-D-glucopyranose(13)具有較顯著的BACE1抑制活性,其100 μmol·L-1抑制率為21.4%,其他分離得到的化合物同劑量抑制率在5.3%~18%之間。
JINGQIU DAI等[21]從垂葉榕(Ficusbenjamina)的黃色果實中分離得到了多種單體,其中異黃酮類化合物5,7,2′,4′-tetrahydroxy-8-(3,7-dimethyl-2,6-octadienyl) isoflavone(14)與lupiwighteone(15)表現(xiàn)出明顯的BACE1抑制活性,其IC50分別為45、27 μmol·L-1,較其他類型化合物表現(xiàn)出了更強的開發(fā)潛力。
JUNG KEUN CHO等[22]從桑樹(Moruslhou)莖皮提取物中發(fā)現(xiàn)甲醇提取部位具有BACE1抑制作用,其IC50值為78.4 μg·mL-1,進一步采用活性導向分離的方法得到多種具有BACE1抑制作用的黃酮類化合物,其中優(yōu)效化合物為kuwanon C(16,IC50為3.4 μmol·L-1),初步構效關系研究表明,異戊烯基取代黃酮的BACE1抑制活性優(yōu)于閉環(huán)的吡喃類黃酮。
2.2 三萜及甾體類BACE1抑制劑
三萜及甾體類成分同樣被報道具有BACE1抑制活性。S M ZAHID HOSEN等[23]對印度民間抗痙攣止瀉藥物火筒樹(Leeaindica)中抑制BACE1活性成分進行了深入研究,通過植物化學方法從該植物中先后分離出40種單體,隨后結合分子模擬對接技術,鑒定出熊果酸(17)和羽扇豆醇(18)這2個具有較高BACE1親和力的三萜類化合物,后續(xù)研究表明,羽扇豆醇抑制BACE1的IC50值為5.12 μmol·L-1。構效關系研究表明,這些三萜結合與BACE1結合的活性位點是由熊果酸與Asn233和Thr232殘基之間形成氫鍵驅動的,而羽扇豆醇則通過氫鍵與Gly11殘基相互作用,并與活性位點形成更強的疏水作用。雖然這2種化合物都能與瓣區(qū)Tyr71殘基形成疏水性相互作用,但卻不能與天冬氨酸殘基(Asp32和Asp228)相互作用。藥代動力學參數(shù)計算結果表明,羽扇豆醇比熊果酸能更有效地穿過血腦屏障。
CLAUDIA SCHINKE等[24]從單環(huán)刺螠中分離出2種具有抗AD作用的甾體化合物。利用熒光共振能量傳遞法對這些化合物進行BACE1的半有效濃度(EC50)值測試,鑒定出海柯吉寧(19)的EC50值為116.3 μmol·L-1,而4-膽甾烯-3-酮(20)的IC50值為390.6 μmol·L-1。與人工合成BACE1抑制劑相比,天然產(chǎn)物來源的海柯吉寧與4-膽甾烯-3-酮的相對分子質量更低,可有效穿透血腦屏障。
ADITI WAGLE等[25]報道了甘草酸(21)及其代謝產(chǎn)物甘草次酸的BACE1抑制活性,結果顯示,甘草酸的BACE1抑制IC50值為20.1 μmol·L-1,而甘草次酸的抑制活性則受到C-18位構型的明顯影響,18-α型甘草次酸(22)IC50值為104.4 μmol·L-1,而18-β型甘草次酸(23)的IC50值僅為8.9 μmol·L-1,進一步酶動力學研究表明,甘草酸為非競爭性BACE1抑制劑,而甘草次酸則為競爭性BACE1抑制劑。
VAN THU NGUYEN等[26]從Lycopodiellacernua中分離純化了4種單體并測定了其BACE1抑制活性,結果表明,化合物21β-hydroxyserrat-14-en-3,16-dione(24)表現(xiàn)出了強于其他化合物的BACE1抑制活性(IC50值為0.2 μmol·L-1),初步構效關系分析可知,這類化合物的母核結構為甾體時,活性強于皂苷類衍生物。
2.3 香豆素類BACE1抑制劑
目前,從天然產(chǎn)物中提取分離的多種香豆素類成分也被報道具有BACE1抑制活性。SU HUI SEONG等[27]從桑樹的根皮中分離了多種單體并考察了桑辛素類似物的BACE1抑制活性,研究結果表明,化合物moracin S(25)表現(xiàn)出了較顯著的BACE1抑制活性,其IC50值為3.1 μmol·L-1,且呈競爭性抑制特點。
SHINSUKE MARUMOTO等[28]從白芷提取物中發(fā)現(xiàn)氯仿提取部位表現(xiàn)出了較強的BACE1抑制活性,其IC50值為3.1 μg·mL-1,進一步根據(jù)活性導向分離得到多種單體,其中活性最強的化合物是歐前胡素(26),其IC50值為91.8 μmol·L-1。此外,該課題組還揭示了其他香豆素抑制BACE1的構效關系[29],篩選得到活性最強的單體5-geranyloxy-8-methoxypsoralen(27,IC50值為9.9 μmol·L-1),其活性遠強于其他化合物,動力學研究表明,該化合物呈混合型抑制特征。
2.4 蒽醌類BACE1抑制劑
SHENG-NAN WANG等[30]從山竹果(Garciniamangostana)中提取得到了7種蒽醌類單體成分,對其進行BACE1抑制活性測定發(fā)現(xiàn),α-倒棯子素(28)的抑制活性較明顯,100 μmol·L-1抑制率為62.7%,進一步研究發(fā)現(xiàn),該化合物還具有抗Aβ42蛋白自發(fā)聚集活性。對于該化合物,LAN-XUE ZHAO等[31]做了進一步探索,發(fā)現(xiàn)其抑制BACE1的IC50值僅為13.2 nmol·L-1,且能減少Aβ42及Aβ42蛋白在小鼠皮層神經(jīng)元中的沉積,且不影響非淀粉樣和淀粉樣途徑或淀粉樣前體蛋白成熟相關酶的表達。
2.5 鞣質多酚類BACE1抑制劑
鞣質多酚類成分一般在天然產(chǎn)物開發(fā)過程中作為副產(chǎn)物存在,而目前部分研究揭示了其作為潛在BACE1抑制劑進行開發(fā)的可能。HIMANSHU KUMAR BHAKTA等[32]從山茱萸(Cornusofficinalis)中得到了與山茱萸新苷結構類似的多種鞣質類成分,其中化合物1,2,3,6-tetra-O-galloyl-β-D-glucose(29)表現(xiàn)出了明顯的BACE1抑制活性,其抑制BACE1的IC50值為20.2 μmol·L-1,且呈非競爭性抑制特征。其活性優(yōu)于同時測定的特里馬素Ⅱ等化合物。
KUMJU YOUN等[33]報道老鶴草(Geraniumthunbergii)的乙酸乙酯提取部位具有較強的BACE1抑制活性,其50 μg·mL-1抑制率為69.39%,多酚化合物老鶴草素(30)及鞣云實素(31)被鑒定為主要活性成分,其中老鶴草素的活性較強,其抑制BACE1的IC50值為4.0 μmol·L-1,約為鞣云實素的9倍。
2.6 生物堿類BACE1抑制劑
生物堿類成分同樣被認為具有BACE1抑制活性,根據(jù)BACE1結構特征,含有裸露堿性基團的抑制劑更有可能與BACE1發(fā)生親和作用,因此,生物堿類成分作為BACE1抑制劑進行進一步開發(fā)有其自身的合理性。作為從中藥千層塔(Huperziaserrata)中分離的主要成分石杉堿甲(32)的抗AD活性已被廣泛證實,而其BACE1抑制活性近年來亦被報道[34]。石杉堿甲被認為能夠通過激活腦內Wnt信號,以減少AD動物腦內淀粉樣病變,石杉堿甲處理的小鼠大腦中BACE1和APP695蛋白水平降低,隨后Aβ水平和Aβ負荷降低,這表明石杉堿甲增強了非淀粉樣變性APP分裂途徑。進一步研究結果表明,石杉堿甲抑制GSK3α/β活性、提高腦內β-catenin水平、激活腦內Wnt信號以發(fā)揮抗AD作用。后續(xù)有研究表明[35],石杉堿甲還可能通過調節(jié)BACE1的過度跨膜轉運以改善Aβ蛋白沉積。
JAKUB CHLEBEK等[36]從紫堇科植物Corydaliscava中分離得到了多種生物堿類成分,對其進行活性評價發(fā)現(xiàn),化合物(-)-corycavamine(33)與(+)-corynoline(34)呈現(xiàn)出明顯的BACE1抑制活性,其5 μmol·L-1抑制率分別為41.16%、33.59%,進一步研究表明,這2種化合物具有一定的血腦屏障透過能力,在抗AD多靶點研究層面,化合物33具有潛在的AChE/BChE抑制能力,而化合物34則具有一定的脯氨酰寡肽酶抑制能力。
3 總結與展望
BACE1抑制劑在治療AD方面的作用目前已在諸多研究中得到證實,目前已有多種天然產(chǎn)物活性成分被報道具有BACE1抑制活性。總體而言,該類天然產(chǎn)物的進一步開發(fā)仍面臨以下問題:(1)相較于基于BACE1靶標結構設計合成的抑制劑,天然產(chǎn)物對于BACE1的抑制活性總體較弱;(2)目前研究對天然產(chǎn)物來源的BACE1抑制劑仍以體外研究為主,藥代動力學等方面特征考察較少,成藥性尚不明確;(3)BACE1抑制劑目前尚無成藥上市,臨床研究多以失敗告終,對天然產(chǎn)物來源的BACE1抑制劑的進一步開發(fā)更是任務艱巨。盡管困難重重,從業(yè)者對于BACE1抑制劑的開發(fā)卻從未停下腳步,相信在未來,隨著免疫神經(jīng)學、表觀遺傳學、微生物組學、計算機輔助藥物設計[37-38]等新興技術的發(fā)展,基于天然產(chǎn)物的BACE1抑制劑的開發(fā)研究終將為AD患者帶來福音。

