GDY/HMX復合含能材料的熱分解動力學和機理
趙寧寧,曾見有,姚二崗,安 亭,馬海霞,趙鳳起
(1.西安理工大學 理學院,陜西 西安 710054;2.西北大學 化工學院,陜西 西安 710069;3.西安近代化學研究所 燃燒與爆炸技術重點實驗室,陜西 西安 710065)
引 言
在含能材料制造工藝技術及性能優化途徑中,添加燃燒催化劑可有效調節含能材料的能量輸出特性。HMX具有高爆熱(5249kJ/kg),分解后產生大量低分子量氣態產物(902L/kg),常用于固體推進劑、炸藥和煙火劑[1]。然而,HMX熱分解活化能較高,HMX基推進劑燃燒速率控制困難,壓強指數高[2]。研究發現,摻雜催化劑能夠改變HMX的熱分解及燃燒性能。Elbasuney等[3]通過共沉淀技術制備Fe2O3/Al/HMX納米復合材料,發現Fe2O3(5nm)/Al(100nm)能夠使HMX熱分解放熱量提高53%,分解溫度降低13℃,活化能降低24%~30%。Fe2O3(8nm)/Al(80nm)[4]可使HMX放熱量提高82%,活化能降低25%。Song等[5]采用超聲噴霧干燥技術成功制備Ph-Fe/HMX復合微球。與HMX相比,Ph-Fe/HMX復合微球的分解峰溫度和活化能分別降低15.6℃和7.0kJ/mol。Zhang等[6]構建的3D核/殼LaFeO3@MNO2異質結構使HMX熱分解峰溫降低9.6℃,其催化性能優于LaFeO3。Wang等[7]通過溶劑熱輔助原位合成法獲得MgWO4-GO納米復合材料,可使HMX熱分解峰溫降低15.06℃。He等[8]利用3D打印技術成功設計和制備了梯度結構HMX/Al,并發現通過控制Al和HMX的梯度質量比可調控HMX/Al的燃燒反應及能量輸出。
應用于含能材料領域的催化劑繁多復雜,輕質碳材料如石墨、富勒烯、碳納米管、石墨烯等對HMX熱分解影響已有較多報道[9-11]。不同于上述sp2、sp2/sp3雜化碳基材料,石墨二炔(GDY)是一種具有sp和sp2兩種雜化態的新型二維全碳同素異形體[12-15],由于其獨特的分子結構,使GDY與離子、原子、分子、納米粒子等多種物質間產生特異性相互作用,表現出卓越的電荷傳輸能力、獨特的傳質和能量轉換優勢[16]。目前,GDY和GDY基復合材料已在催化、太陽能電池、儲能、水凈化、探測器、傳感器、氣體分離以及生物醫學和治療等諸多領域顯示出其優異性能[17-18]。在含能材料領域,GDY可加快C—N鍵斷裂,從而促進RDX的熱分解[19]。GDY在NC熱解過程中能夠驅動O—NO2鍵斷裂,降低NC熱分解能壘,并增加熱量釋放[20]。以上研究表明,GDY在催化含能材料熱分解方面具有潛在應用價值。
為進一步拓展GDY在含能材料領域的應用范圍,探討其對HMX熱分解特性的影響,本實驗首次運用差示掃描量熱法(DSC)和熱紅質聯用技術(TG/DTG-FTIR-MS)研究了GDY/HMX復合含能材料的熱行為及催化熱分解機制,以期為GDY在含能材料領域的實際應用提供參考。
1 實 驗
1.1 原料
石墨二炔(GDY),自制;HMX,西安近代化學研究所。
1.2 GDY/HMX復合物的制備
將GDY與HMX按質量比1∶4研磨混合,得到GDY/HMX復合物。
1.3 樣品表征
采用ZEISS Gemini 300型掃描電子顯微鏡(SEM)對GDY/HMX形貌進行表征,加速電壓3kV;采用Thermo Scientific K-Alpha型X射線光電子能譜儀(XPS)對材料表面元素及其化學狀態進行分析,X射線源采用Al Kα(hv=1486.6eV),工作電壓12kV,燈絲電流6mA,分析室真空度優于5.0×10-7mBar。
1.4 熱分解特性測試
采用美國TA公司Q2000型差示掃描量熱儀(DSC)進行實驗,在動態高純氮氣氣氛保護下,測試分析GDY對HMX熱分解特性的影響,動態氣氛流速為50mL/min,溫度范圍50~350℃,升溫速率15、20、25、30℃/min,參比物為α-Al2O3,試樣質量0.20~0.50mg,盛放試樣的樣品池為鋁質坩堝。采用美國賽默飛世爾科技公司TGA-DSC3/IS0/GSD320型同步熱重/紅外光譜/質譜聯用儀(TG/DTG-FTIR-MS)在高純氬氣氣氛下(流速為20mL/min)分析GDY/HMX復合物熱解氣體產物。
2 結果與討論
2.1 表征分析
采用掃描電子顯微鏡對GDY/HMX樣品進行結構分析,結果如圖1所示。圖2為GDY、HMX和GDY/HMX的XPS全譜掃描圖和 C1s的XPS譜圖。

圖1 GDY/HMX的SEM圖Fig.1 SEM image of GDY/HMX
由圖1可知,GDY納米墻呈三維納米片陣列結構,其上負載HMX顆粒。GDY網絡中苯環間鏈接雙炔鍵,使其網絡框架具有孔隙結構,有助于空氣的吸附。由圖2(a)可知,在284.5、400.1及532.1eV處出現C1s、N1s及O1s軌道的特征峰,其中,N1s及O1s峰是由于GDY樣品暴露在空氣中時,空氣吸附在其網絡結構的孔隙中所致。HMX和GDY/HMX的XPS全譜圖均顯示存在C1s、N1s及O1s軌道的特征峰。圖2(b)GDY的C1s軌道的高分辨圖譜表明,284.5、285.3、286.9和288.5eV的4個子峰依次歸屬于C—C(sp2)、C—C(sp)、C—O和C═O鍵。sp2和sp雜化碳的計算比例約為2,與GDY的理論組成一致[12]。HMX的C1s圖譜顯示在284.4eV和287.5eV處出現HMX的C—C和N—C—N的典型特征峰[21]。在GDY/HMX的C1s圖譜中出現C—C(284.5eV)、C—C(sp,285.2eV)、C—O(286.1eV)、N—C—N(287.1eV)和C═O(288.5eV)的特征峰,證實GDY與HMX復合。
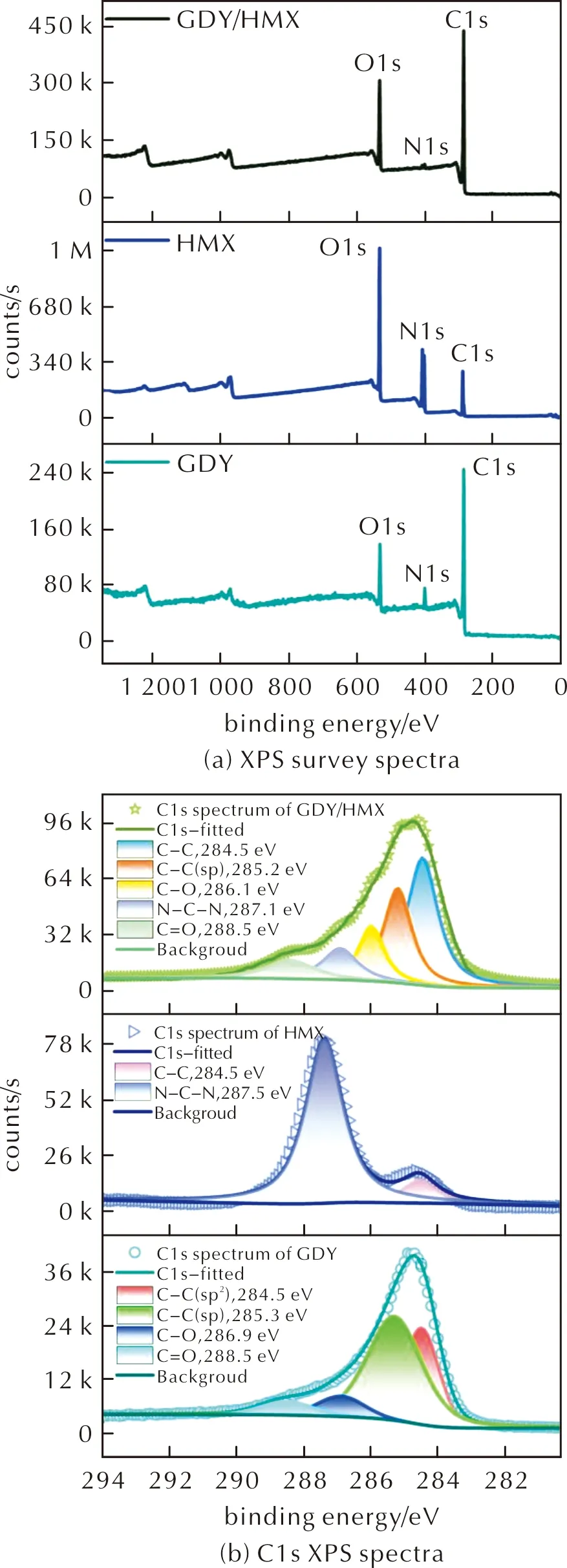
圖2 GDY、HMX和GDY/HMX的XPS全譜掃描圖和C1s的XPS譜圖Fig.2 XPS survey and C1s XPS spectra of GDY, HMX and GDY/HMX
2.2 GDY/HMX熱分解行為分析
圖3為HMX及GDY/HMX在升溫速率15、20、25及30℃/min下的熱分解曲線。由圖3可知,HMX的熔點在281℃左右,加入GDY后,未使HMX熔化峰溫度產生明顯偏移,說明GDY對HMX熔化過程影響不大。在升溫速率15、20、25及30℃/min下,GDY/HMX熱分解峰溫度比HMX熱分解峰溫度依次降低0.8、1.7、2.3、0.1℃,說明GDY可促進HMX的熱分解過程。
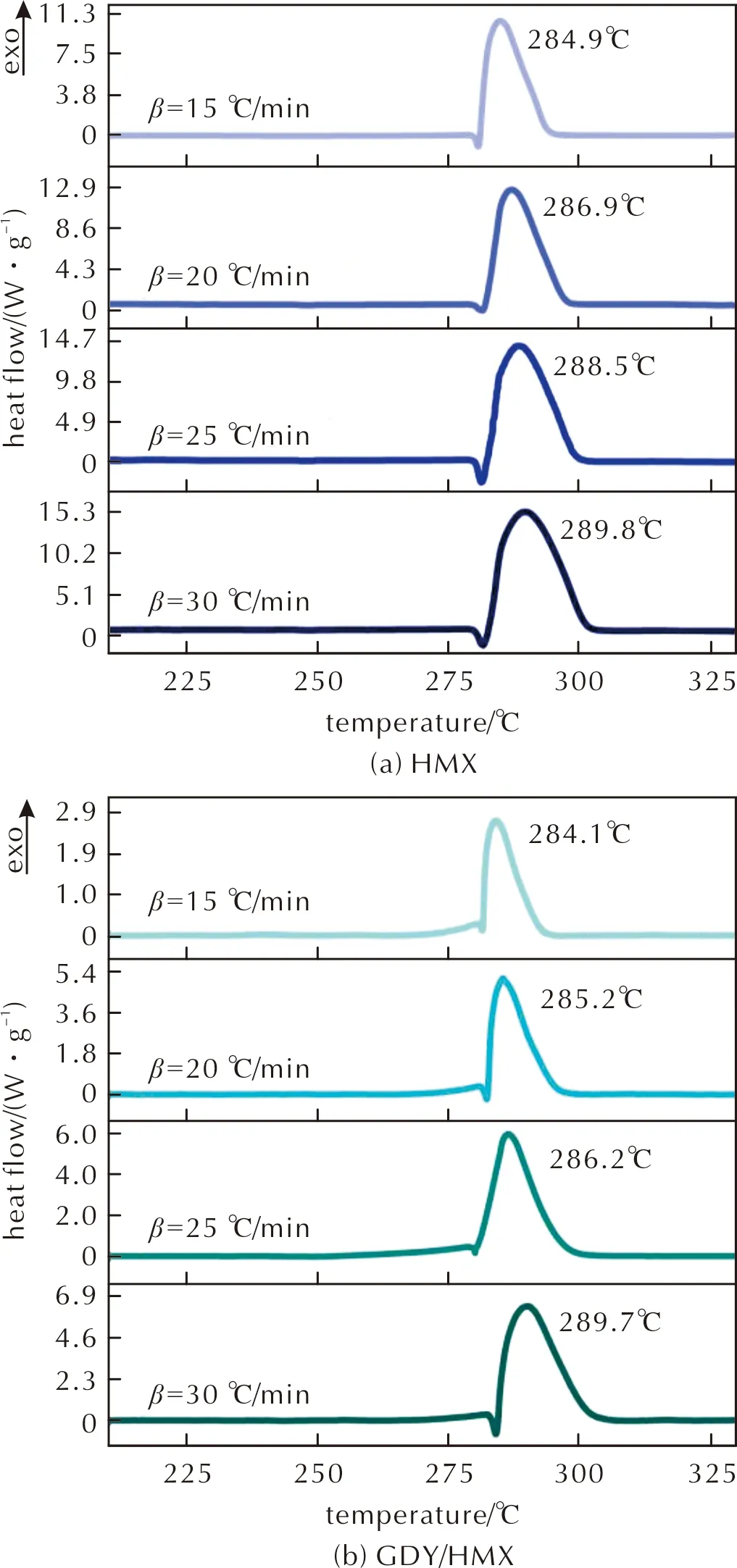
圖3 HMX及GDY/HMX在不同加熱速率的DSC曲線Fig.3 DSC curves of HMX and GDY/HMX obtained at different heating rates
2.3 GDY/HMX熱分解動力學
基于上述HMX和GDY/HMX的熱分解峰溫及升溫速率,通過Kissinger法[式(1)][22]、Flynn-Wall-Ozawa (FWO)法[式(2)][20]、Kissinger-Akahira-Sunose (KAS)法[式(3)][23]、Starink法[式(4)][24]、Kissinger-迭代法[式(5)~式(7)][25]及Ozawa-迭代法[式(6)~式(9)][26]對HMX和GDY/HMX的表觀活化能進行計算。
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
式中:β為升溫速率,℃/min或K/min;T為熱分解峰溫度,℃或K;const為常數項;A為指前因子;R為摩爾氣體常數,kJ/(mol·K);E為表觀活化能,kJ/mol;G(α)為積分機理函數;H(u)或Q4(u)為u(u=E/RT)的變量。
Kissinger法、FWO法、KAS法、Starink法、Kissinger-迭代法及Ozawa-迭代法計算所得GDY/HMX的表觀活化能分別為285.6、280.5、285.6、284.6、285.7和285.7kJ/mol,均低于HMX的表觀活化能(359.9、351.1、359.8、358.3、359.9和359.9kJ/mol)。且6種方法計算值相差不大,取平均值可得HMX的表觀活化能為358.2kJ/mol,接近文獻報道值[27-28]。GDY/HMX的表觀活化能為284.6kJ/mol,與HMX相比,GDY/HMX的表觀活化能降低了73.6kJ/mol。
為探討HMX和GDY/HMX熱分解動力學機理函數,將常見固相反應遵循的理想動力學反應模型與HMX、GDY/HMX熱分解實驗物理模型曲線進行對比研究,結果如圖4所示,其中,D2、D3為二維、三維擴散模型,F1為單分子衰變定律(瞬時成核和一維生長)模型(Avrami-Erofeev方程,n=1),R2、R3為相界控制反應(收縮面積、收縮體積)模型,L2、L8為隨機鏈斷裂模型(L=2、L=8),A2、A3和A4為成核-核生長模型(Avrami-Erofeev方程,n=2、3、4)。
由圖4可知,原始 HMX 和GDY/HMX的熱分解過程接近于隨機鏈斷裂(L2)模型,但與理想L2模型主曲線比較,由實驗數據所得HMX和GDY/HMX的反應模型主曲線并不與之完全符合,尤其在轉化率小于0.5的范圍內,其相關性較差。為獲得相關性理想的物理模型,引入修正后的esták-Berggren經驗方程[29]對其反應動力學模型進行重建,結果如圖4所示,HMX和GDY/HMX熱分解機理最終可描述為n級動力學模型,其表達式分別為f(α)=2.97α0.38(1-α)1.15和f(α)=3.04α0.39(1-α)1.17。
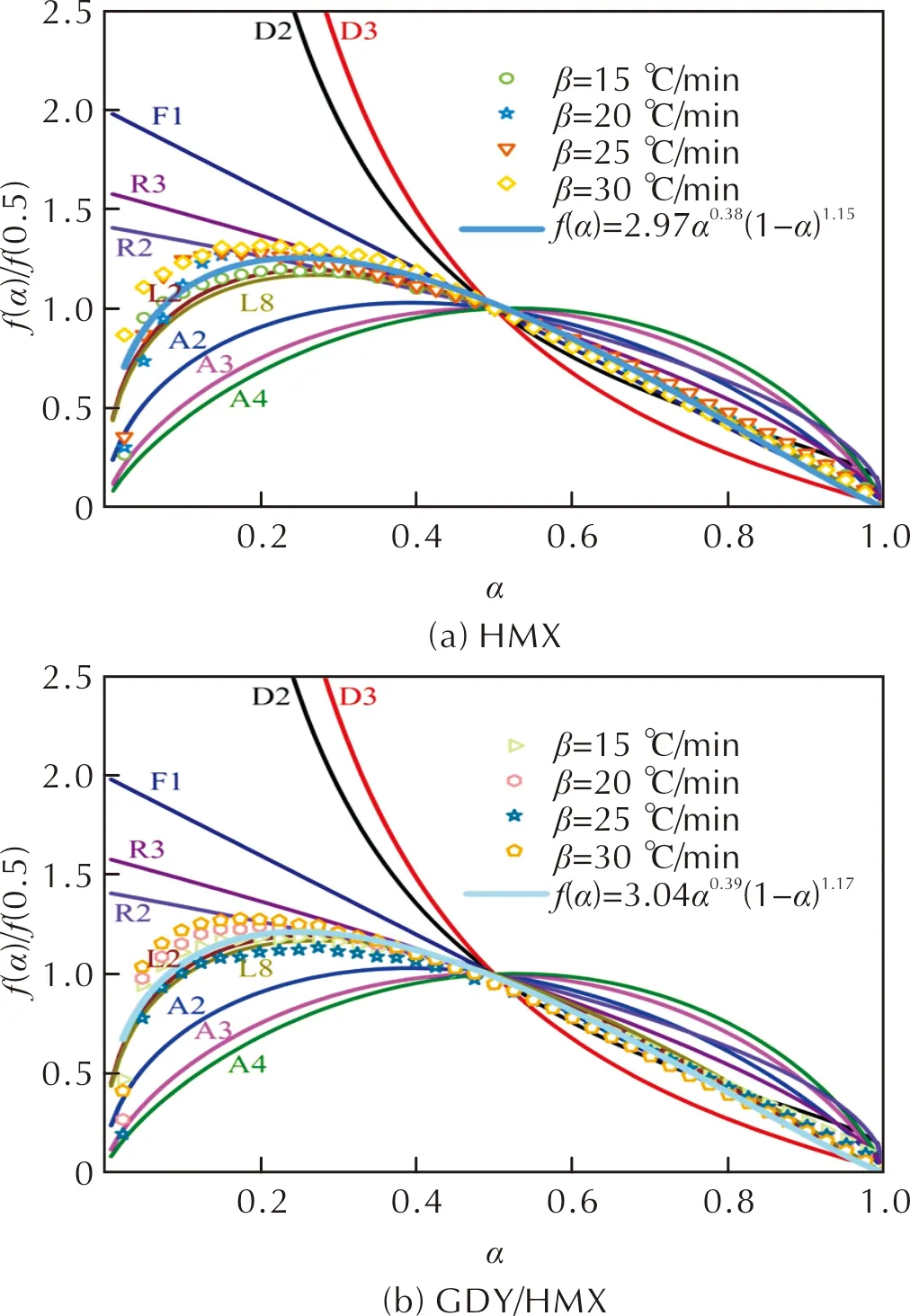
圖4 HMX和GDY/HMX反應模型曲線與理想反應模型建立的理論主曲線之間的比較Fig.4 Comparison between normalized curves of the reaction models for HMX and GDY/HMX and theoretical master curves established from the ideal reaction models
2.4 TG/DTG-FTIR-MS分析
采用TG/DTG-FTIR-MS熱紅質聯用技術對比研究HMX和GDY/HMX的熱分解過程。圖5為升溫速率10℃/min時HMX和GDY/HMX的TG/DTG曲線,圖6為升溫速率10℃/min時GDY的TG曲線。由圖5可知,HMX、GDY/HMX熱分解峰溫分別為284.5℃和281.3℃。將GDY與HMX復合后,GDY/HMX熱分解峰溫較純HMX熱分解峰溫低3.2℃,說明GDY的加入可促進HMX分解。HMX、GDY/HMX熱分解過程的最大質量損失分別為97.4%和91.4%,而GDY在284.5℃和281.3℃ 時的質量損失分別為7.8%和7.5%(圖6),說明GDY/HMX混合體系的質量損失由HMX和GDY分解兩部分所引起。且GDY/HMX混合體系中GDY與HMX質量比為1∶4,若組分HMX完全分解,則其最大質量損失應為80%,而GDY/HMX質量損失為91.4%,故其中至少11.4%由GDY分解所致,又比較圖5實驗結果可知,在281.3℃ 時GDY的熱分解質量損失至少增加3.9%,說明HMX在一定程度上也能促進GDY的分解。
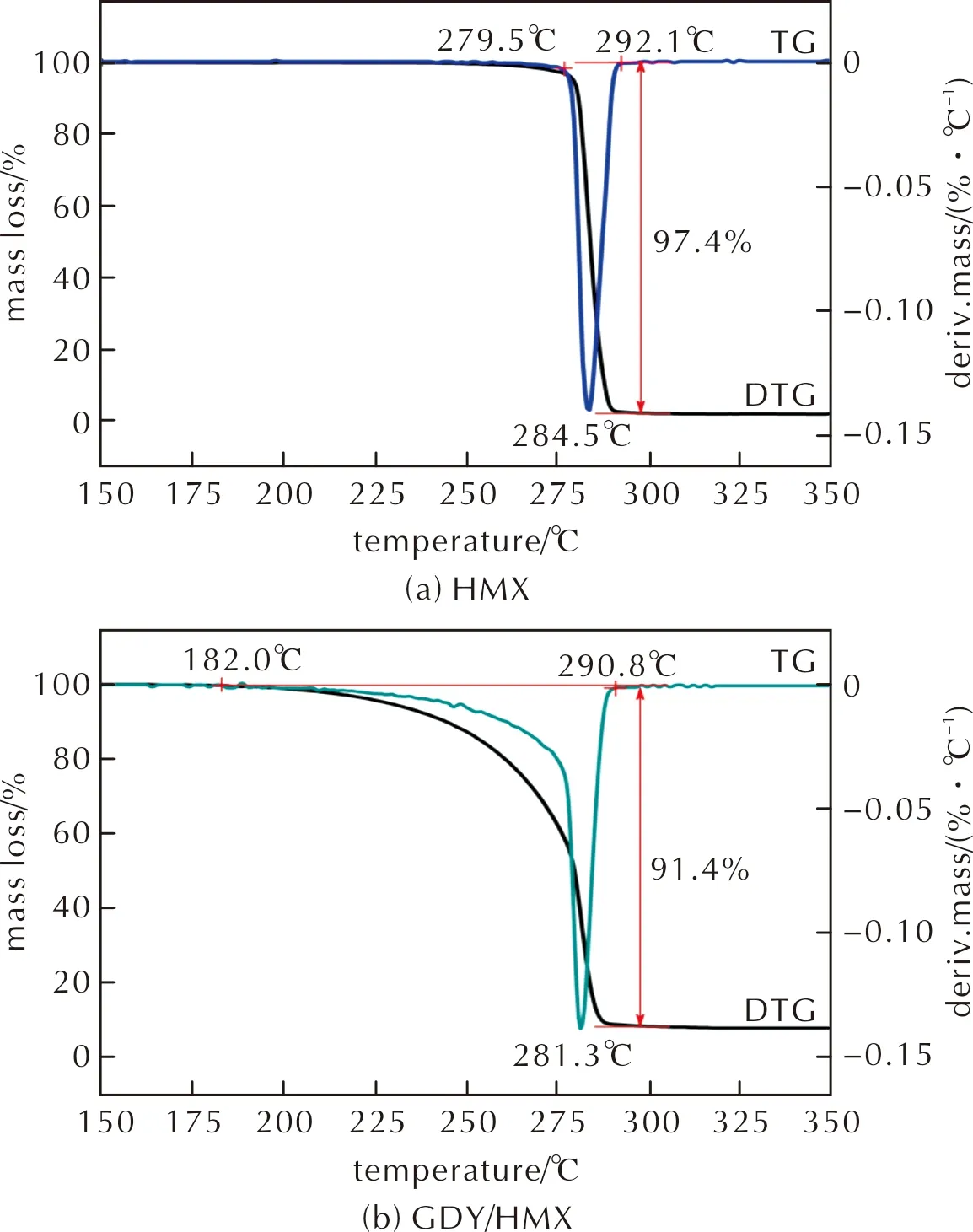
圖5 HMX和GDY/HMX的TG/DTG曲線Fig.5 TG/DTG curves of HMX and GDY/HMX
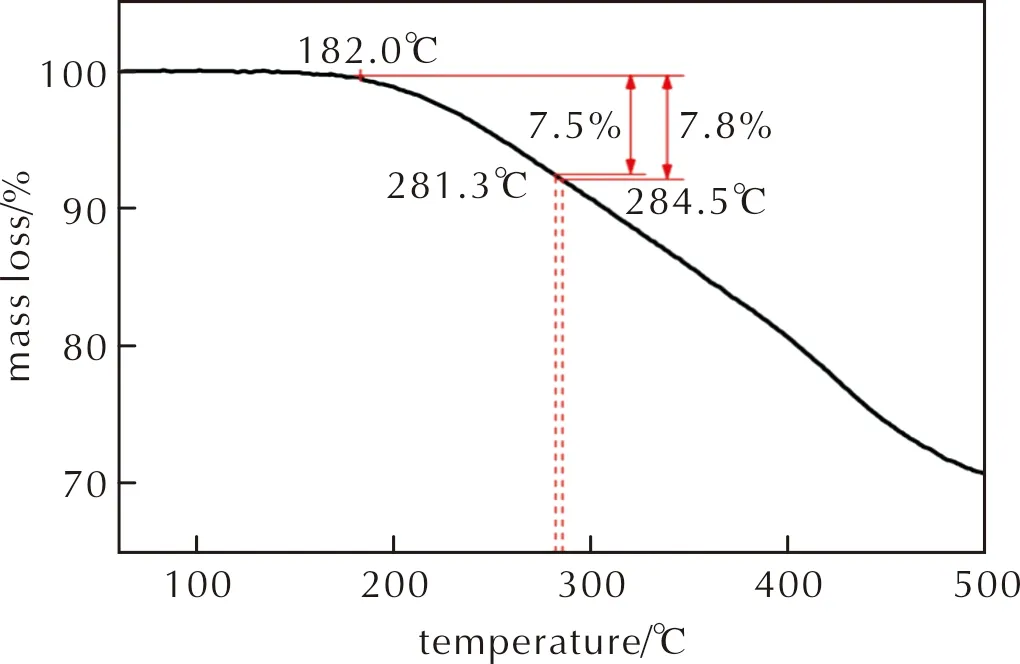
圖6 升溫速率為10℃/min時GDY的TG曲線Fig.6 TG curve of GDY at a heating rate of 10℃/min
研究表明[30],影響HMX熱分解過程的因素眾多,如溫度、壓力、晶型、結構缺陷、粒徑、雜質等。總體而言,HMX的初始熱分解普遍認為是環C—N鍵斷裂和N—NO2鍵斷裂的競爭過程,兩者分別以產物(CH2O+N2O)和[HCN+HONO(H2CN+NO2或H·+NO2+HCN)]為標志[31]。通過實驗及理論研究,HMX熱分解過程的氣體產物為N2O、NO、NO2、CH2O、HCN、CO、N2、CO2和H2O[32-33]。加入納米金屬離子、金屬氧化物、鹽類等添加劑后,HMX的熱解機制會發生變化,分解產物也有所不同。
圖7為在170~310℃范圍內選取的9個不同溫度對應的紅外光譜。圖8為HMX和GDY/HMX熱解產物的3D-FTIR圖譜。
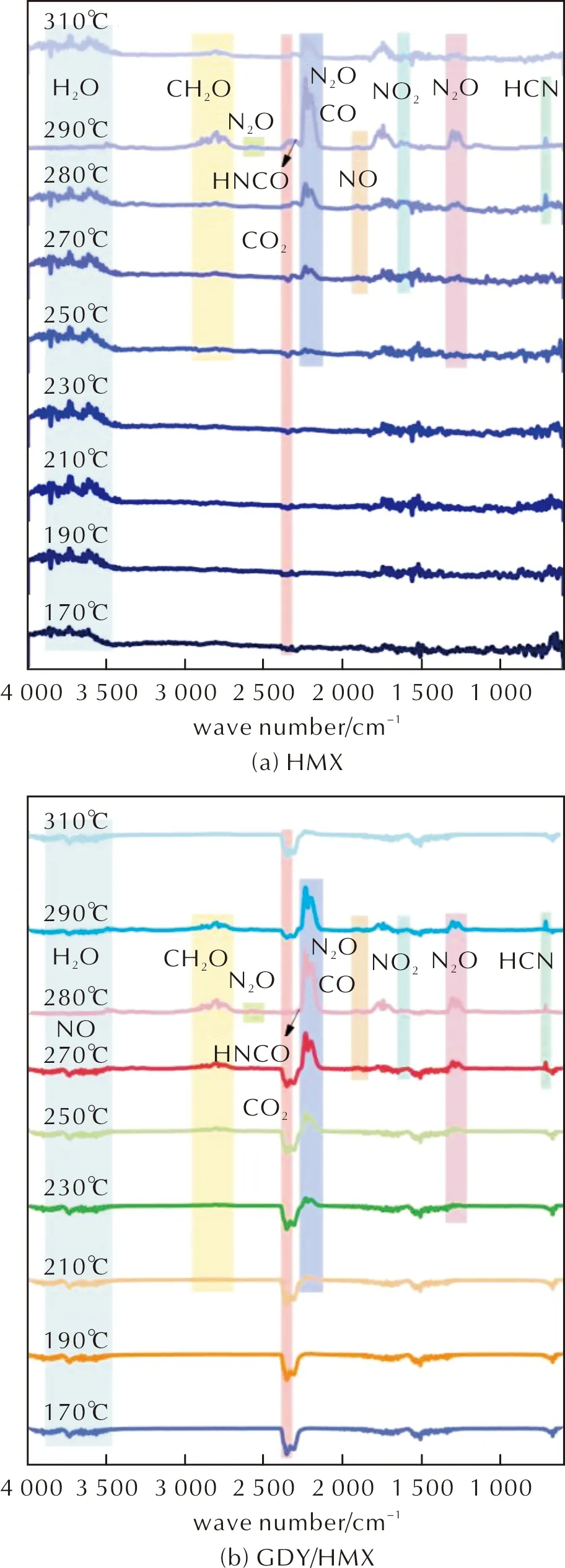
圖7 HMX和GDY/HMX熱解產物的FTIR圖譜Fig.7 FTIR spectra of decomposition products detected during the degradation of HMX and GDY/HMX
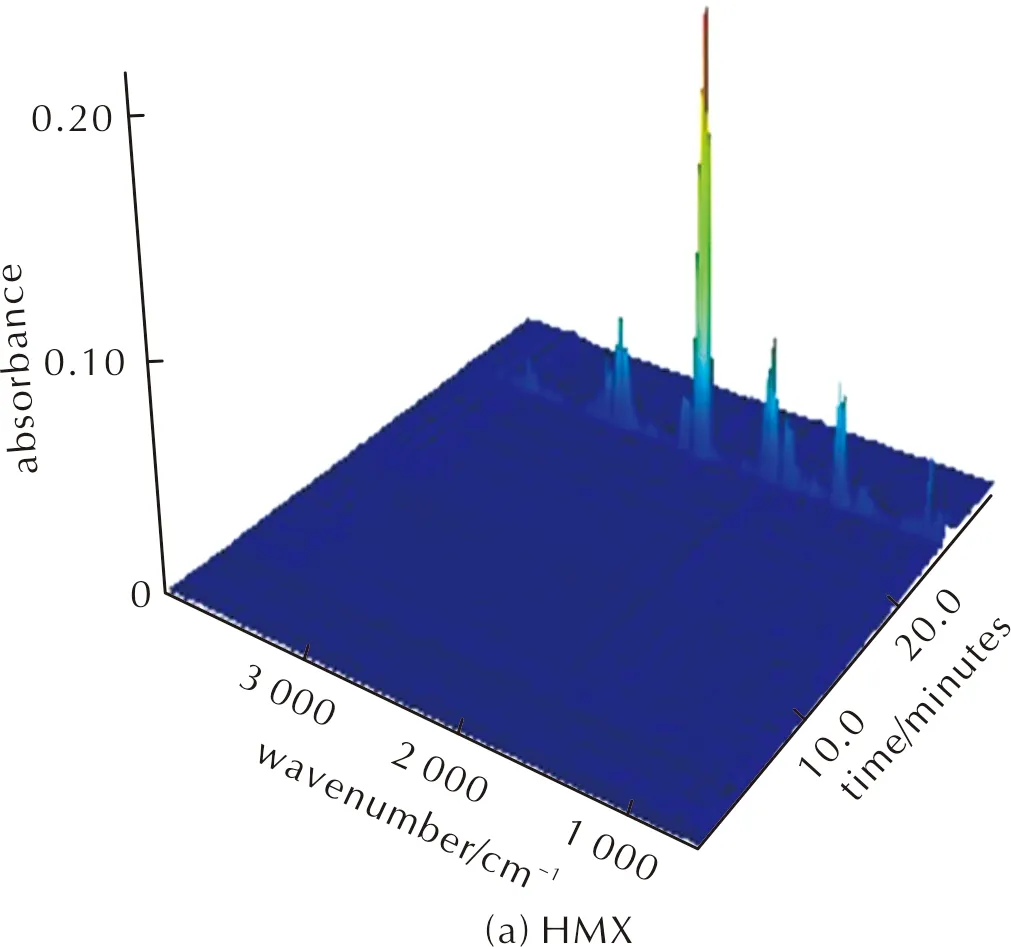
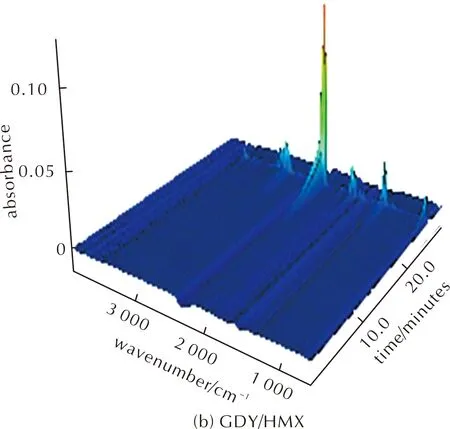
圖8 HMX和GDY/HMX熱解產物的3D-FTIR圖譜Fig.8 3D-FTIR spectra of decomposition products detected during the degradation of HMX and GDY/HMX
在HMX、GDY/HMX熱分解開始前,兩者170℃對應的FTIR圖譜顯示在3590~3759cm-1處出現H2O的特征吸收峰;在2360和670cm-1處出現CO2特征吸收峰。且發現在210℃和190℃時H2O吸收峰、CO2吸收峰強度無明顯變化,由此可確定在HMX、GDY/HMX熱分解開始時檢測到的H2O、CO2來源于環境,為雜質峰。同時發現,210℃時在2239cm-1處檢測到N2O的紅外吸收峰。在2813cm-1處檢測到CH2O的紅外吸收峰,但吸收強度較弱。230℃時,CH2O的紅外吸收峰越來越明顯,在2239cm-1處的N2O吸收峰強度也逐漸增大,同時在1260~1309cm-1處出現微弱的N2O吸收峰[34]。250℃時,CH2O、N2O吸收峰強度不斷增大。至此,H2O、CO2吸收峰強度仍無明顯變化,說明GDY/HMX熱分解過程在低于250℃時不生成H2O、CO2。對比HMX在190~250℃的紅外吸收峰,250℃時檢測到N2O的紅外吸收峰,而此時CH2O的紅外吸收強度非常弱。以上結果說明,HMX和GDY/HMX均首先發生公式(10)所示分解途徑且由于GDY的加入,使環C—N鍵提前斷裂。
C4H8N8O8→N2O+CH2O
(10)
為進一步確定HMX的初期熱分解為C—N鍵斷裂或是N—NO2鍵斷裂,基于質譜檢測結果,繪制HMX和GDY/HMX熱分解產物N2O和HCN的離子流強度比隨溫度的變化關系曲線,如圖9所示。圖10為HMX和GDY/HMX熱解產物的質譜圖。由圖9可知,分別在HMX起始熱分解溫度279~290℃、GDY/HMX起始熱分解溫度182~287℃時,N2O和HCN的離子流強度比大于1,說明HMX或在GDY作用下的HMX分解初期過程是C—N鍵斷裂占優。據文獻報道[35],當HMX中添加納米氧化物TiO2、Fe2O3、Al2O3、SiO2時得到相同結論。
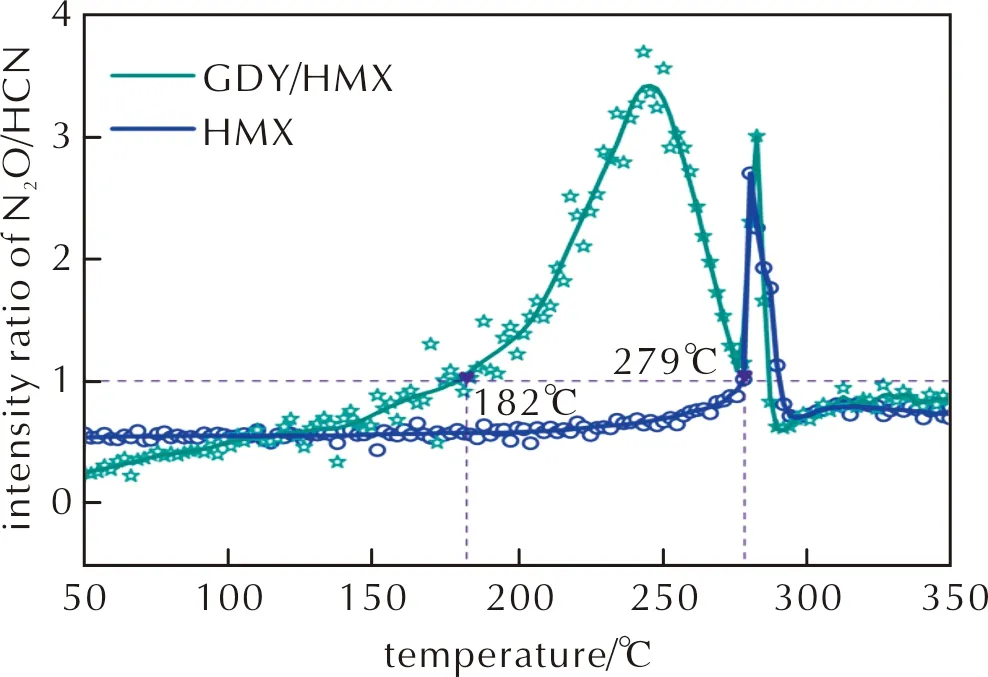
圖9 HMX和GDY/HMX熱解產物N2O/HCN離子流強度比—溫度曲線Fig.9 Ion current intensity radio of decomposition products N2O/HCN vs. temperature curves detected during the degradation of HMX and GDY/HMX
由圖7(b)可知,270℃時,除CH2O、N2O外,在717cm-1處檢測到明顯的HCN吸收峰,在1693~1806cm-1范圍內出現微弱的NO吸收峰,還可檢測到熱解產物NO2(1578~1655cm-1)、CO(2195cm-1)、CO2和H2O。圖7(a)顯示HMX熱解產物HCN出現在280℃,在270℃時檢測到CH2O、N2O、NO、NO2、CO、CO2和H2O。其中,CH2O、NO2吸收峰較弱,可能涉及復雜的次級反應[36]:
5CH2O+7NO2→3CO+7NO+5H2O+2CO2
(11)
NO2NO+1/2O2
(12)
根據圖7及圖8紅外檢測結果,在577、656、776cm-1未出現HNCO的特征吸收峰,可能出現在1338cm-1和3529cm-1HNCO的吸收峰與N2O、H2O吸收帶疊加。對于HMX,圖7(a)所示290℃時檢測到HNCO的微弱吸收峰,且由圖10(a)可知,m/z=43處出現HNCO質子峰。圖7(b)顯示在280℃時2285cm-1處檢測到HNCO的微弱吸收峰,但由圖10(b)質譜圖所示,m/z=43處并未出現HNCO質子峰。綜合FTIR-MS結果,在HMX分解過程中可產生HCNO,而HNCO不是穩定的GDY/HMX熱解產物。對于NO2氣體,出現類似情況,在圖7及圖8所示紅外譜圖中可檢測到其吸收峰,在圖10(a)中279~290℃范圍內m/z=46處出現NO2的特征峰,而圖10(b)中m/z=46處無明顯NO2特征峰,且檢測到CO或N2(m/z=28)、CO2或N2O(m/z=44)、H2O(m/z=18)信號峰。由此推斷,HNCO與NO2在GDY催化下可迅速發生以下選擇性催化反應[37]:
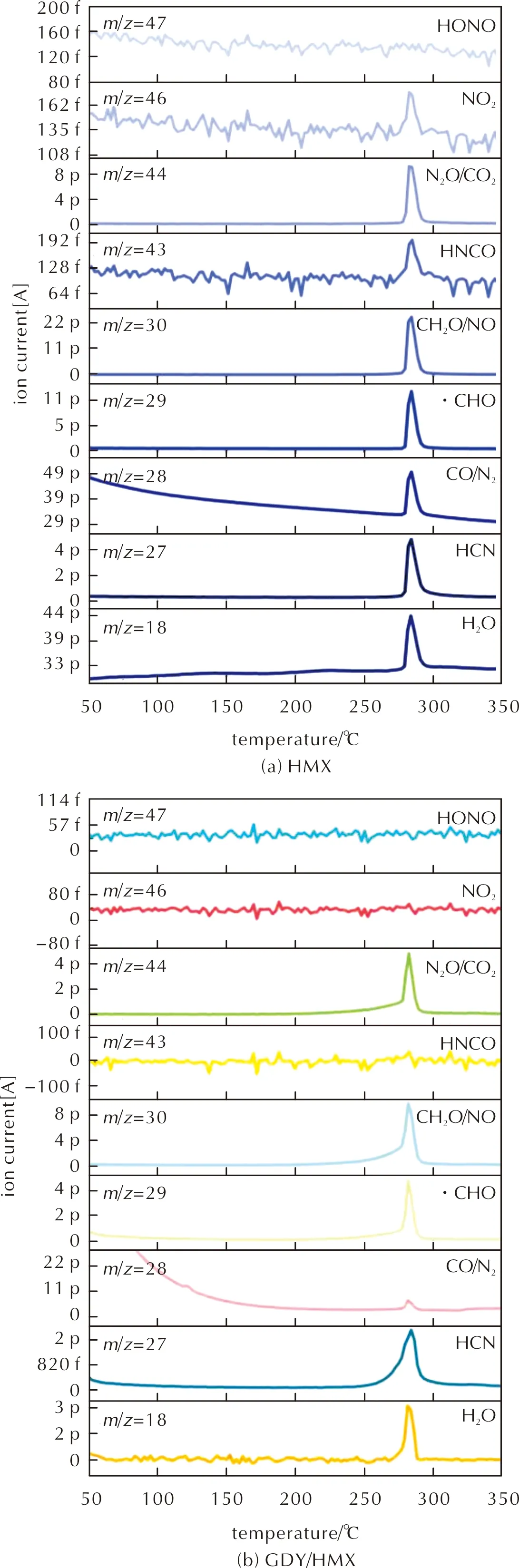
圖10 HMX和GDY/HMX熱解產物的質譜圖Fig.10 Mass spectra of decomposition products detected during the degradation of HMX and GDY/HMX
(13)
CO與N2O紅外吸收峰部分重疊,結合圖10在m/z=28處的特征信號峰,推測CO是可能的次級分解產物,對比圖10(a)和圖10(b)m/z=28處的特征信號峰,發現圖10(b)中m/z=28處信號峰明顯減弱,說明CO份量減少,推測在O2及GDY存在時CO會被氧化:

(14)
可能的反應機理為:GDY上吸附的O2通過Eley-Rideal機制氧化CO,經歷O—O鍵的斷裂、亞穩類碳酸鹽中間態的形成,最終產生CO2分子[38]。充分體現了具有高比表面積的GDY對CO氧化反應的高催化效率和活性。
另外,HONO也是可能存在的活性物種,其1696cm-1處紅外吸收峰可能與NO紅外吸收峰重疊。在圖10中未出現m/z=47信號峰,其原因為HONO在高升溫速率下僅存在幾秒鐘,此后迅速分解為NO、NO2和H2O[39]:

(15)
290℃時,GDY/HMX熱分解過程幾近結束,所有氣體產物吸收強度均較大程度減小,而NO2吸收峰幾乎消失。大于300℃時,分解產物為少量N2O、CH2O和HCN,此時CO2和H2O吸收峰強度與GDY/HMX熱分解前游離CO2和H2O吸收峰強度基本一致。結合圖5TG/DTG結果,GDY/HMX含能復合物在290.8℃時已結束分解,故上述氣體可能由于被GDY薄膜吸附后在高溫下脫附所致。
由圖10所示GDY/HMX熱分解產物的質譜圖可知,主要氣體產物及自由基包括:H2O(m/z=18)、HCN(m/z=27)、N2或CO(m/z=28)、NO或CH2O(m/z=30)、CO2或N2O(m/z=44)、·C(m/z=12)、·N(m/z=14)、·O(m/z=16)、·OH(m/z=17)、·CN(m/z=26)、·CHO(m/z=29)、·CH2C≡CH(m/z=39)。其中,HMX分子內的·O自由基從—NNO2基轉移到—CH2-上,導致C—H 鍵斷裂,并生成CH2O和N2O[40]。由·CH2C≡CH(m/z=39)自由基的產生可能來源于GDY苯環的分解,據本課題組前期研究,在182~300℃范圍內,GDY質量損失率約為8.5%[19]。
綜上所述,GDY催化作用下,C—N鍵斷裂是HMX的主要熱分解途徑,伴隨著氧轉移過程,首先釋放出CH2O和N2O氣體。并發生復雜的次級反應,進而檢測到N2O、NO、NO2、CH2O、HCN、CO、HCNO、N2、CO2和H2O氣體(見圖11)。
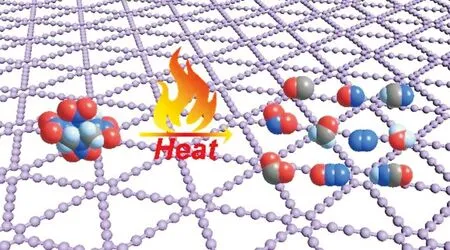
圖11 GDY/HMX熱解過程示意圖Fig.11 Proposed thermal decomposition process of GDY/HMX
3 結 論
(1)基于DSC數據研究了GDY/HMX復合含能材料的熱分解過程。與單組分HMX相比,GDY/HMX熱分解表觀活化能降低73.6kJ/mol,熱分解過程接近于隨機鏈斷裂模型,其動力學機理函數遵循f(α)=3.04α0.39(1-α)1.17。
(2)TG/DTG-FTIR-MS分析結果表明,GDY/HMX熱分解過程首先斷裂C—N鍵,生成CH2O和N2O氣體。在GDY催化作用下,伴隨發生復雜的次級反應,生成N2O、NO、NO2、CH2O、HCN、CO、N2、HCNO、CO2和H2O氣體。

