二代測序用于藥品微生物檢測潔凈區環境菌庫的建立
孫榮嶸,徐晨,劉洋,任曉偉
濟南市食品藥品檢驗檢測中心,濟南 250102
藥品的質量安全與控制關乎著人們的生命安全。近年來,藥品微生物污染如“欣弗事件” “刺五加事件”等都對社會造成了重大的危害與損失。2015~2017年,美國食品藥品監督管理局(FDA)公布的藥品召回事件中,因微生物污染風險導致的召回占總召回事件的50%[1]。各種事件和案例都提示我們對藥品微生物污染的風險控制不能大意。由于微生物的分布特點是分散的、不均一的,現行《中國藥典》(2020年版)[2]規定:“供試品檢出控制菌或其他致病菌時,按一次檢出結果為準,不再復試。”但出于謹慎的考慮,藥品微生物檢驗過程中的陽性結果除了樣品本身的原因外,有必要排除實驗室人員、環境等因素引入的污染。如果能對藥品微生物檢測潔凈區(以下簡稱“潔凈區”)環境微生物的群落分布及組成進行充分了解,建立潔凈區的環境菌庫,并對出現的污染菌進行溯源分析,可以在一定程度上有效地避免“假陽性”報告的出現,并可以制定有效的清潔消毒程序、規范檢驗人員在潔凈區的行為等[3],以期提高檢驗結果的準確性,同時還可以為生產企業的潔凈環境控制提供重要的參考。
目前,利用分子生物學手段進行的微生物檢測較傳統的形態學及生化水平上的手工鑒定在時效性和準確性上有著較大的優勢,當前實驗室中采用16S rRNA測序方法已成為微生物檢測的重要手段[4]。國內已有很多報道采用16S rRNA測序建立了環境菌庫[3,5]。但是16S rRNA測序的缺點是其雖然在種屬級別具有較高的準確度,但到了菌株級別,其區分能力會大大下降。因此,有部分研究提示該種方法在同種不同分離株內的分辨能力有限[6],并且一些芽孢桿菌屬的微生物,如枯草芽孢桿菌、短小芽孢桿菌等存在16S rRNA序列的高度相似性,也限制了16S rRNA測序在基因分型中的應用[7]。而2020年版《中國藥典》四部通則“9204 微生物鑒定指導原則”在微生物溯源分析中指出,菌株水平的鑒定在污染調查過程中非常重要[8],并給出了全基因組測序在藥品污染溯源分析中的重要指導意義。因此,本研究嘗試在4個月內,周期性地從潔凈區收集環境微生物并采用BBL CRYSTAL細菌鑒定儀進行生化鑒定,而后采用Miseq二代測序儀進行全基因組測序,以期獲得更精確的潔凈區環境微生物群落組成信息,并初步建立本實驗室的環境菌庫。
藥品生產質量管理規范(good manufacturing practice,GMP)中要求有關藥品質量控制的微生物檢驗必須要有驗證程序[9]。因此,本研究采用實驗室保存的標準菌株作為質控菌株。而本實驗建立標準菌株菌庫的另一原因還在于藥品微生物檢驗的方法學驗證中標準菌株的使用不可避免,因此即使不同實驗室交叉污染的可能性很低,在陽性菌的溯源分析中也最好排除實驗室標準菌株傳入污染的可能性。因此,本研究旨在建立潔凈區環境菌庫的同時,建立了本實驗室標準菌株菌庫,為今后污染菌的溯源分析提供更全面可靠的技術支撐。
1 材料與方法
1.1 儀器與試劑
PBS 100浮游菌采樣器(蘇州諾達凈化科技有限公司);BX51光學顯微鏡(日本奧林巴斯公司);SHP-350生化培養箱(上海精宏實驗設備有限公司);BBL CRYSTAL AutoReader細菌鑒定儀(美國BD公司);C1000 Touch PCR儀(美國Bio-Rad公司);QIAxcel Advanced毛細管電泳儀(德國Qiagen公司);Qbuit 3.0核酸蛋白測定儀(美國Invitrogen公司);Miseq二代測序儀(美國Illumina公司)。
胰酪大豆胨瓊脂培養基、沙氏葡萄糖瓊脂培養基、胰酪大豆胨液體培養基(北京奧博星生物科技有限公司)。試劑盒:革蘭氏染色試劑盒(青島海博生物科技有限公司);High Pure PCR Template Preparation Kit(美國 Roche 公司);Plant/Fungi DNA Isolation Kit(美國Sigma公司);QIAxcel DNA Screening Kit(德國Qiagen公司);Nextera XT Library Prep Kit、Miseq v2 Reagent Kit(美國Illumina公司)。本實驗室保存的標準菌株:大腸埃希菌[CMCC(B)44102]、沙門菌[CMCC(B)50094]、銅綠假單胞菌[CMCC(B)10104]、枯草芽孢桿菌[CMCC(B)63501]、金黃色葡萄球菌[CMCC(B)26003]、白念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]購自中國食品藥品檢定研究院;生孢梭菌[CMCC(B)64941]購自廣東環凱微生物科技有限公司。
1.2 標準菌株的生化鑒定
取實驗室的標準菌株大腸埃希菌、沙門菌、銅綠假單胞菌、枯草芽孢桿菌、金黃色葡萄球菌和生孢梭菌,劃線接種到胰酪大豆胨瓊脂培養基平板,于33℃培養18h后,選取相應的鑒定試劑盒,通過BBL CRYSTAL細菌鑒定儀進行種屬鑒定,采用甘油冷凍法,將鑒定后的細菌連同白念珠菌、黑曲霉置于冰箱冷凍保存。
1.3 環境微生物的采集
連續4個月采用浮游菌采樣器、表面接觸皿、沉降菌平皿從潔凈區不同區域(空氣、設備、生物安全柜、墻面、地面等)采集取樣。共收集細菌19株和霉菌1株。
1.4 環境微生物的生化鑒定
將采集的潔凈區環境微生物進行培養、分離純化和染色鏡檢后,對其進行初步分類。將純化的細菌劃線接種到胰酪大豆胨瓊脂培養基平板,于33℃培養18h后,選取相應的鑒定試劑盒,通過BBL CRYSTAL細菌鑒定儀進行種屬鑒定,采用甘油冷凍法,將鑒定后的細菌連同收集的環境中的霉菌置于-80℃冰箱中保存。
1.5 Miseq二代測序
1.5.1 細菌DNA提取
依據細菌基因組提取試劑盒產品說明書對6種標準菌株及收集到的環境中的19株細菌進行全基因組DNA抽提,利用Qbuit核酸蛋白測定儀檢測細菌基因組DNA濃度后保存待用。
1.5.2 真菌DNA提取
依據真菌提取試劑盒產品說明書對標準菌株白念珠菌、黑曲霉及所收集的環境中的1株霉菌進行全基因組DNA提取,利用Qbuit核酸蛋白測定儀檢測真菌基因組DNA濃度后保存待用。
1.5.3 建庫及上機
利用DNA文庫制備試劑盒進行標記基因組DNA、擴增標記后的DNA、純化擴增后的DNA等步驟后,利用Qbuit核酸蛋白測定儀和毛細管電泳儀分別檢測制備文庫的濃度和片段大小分布,建庫成功后進行標準化文庫及混合文庫。制備完成后利用Miseq二代測序儀對標準菌株及所收集的潔凈區環境微生物菌株進行全基因組測序。
1.6 數據分析
利用CLC軟件對測序數據進行分析,完成各菌株堿基序列的拼接,提交到美國國立生物技術信息中心(NCBI,www.ncbi.nlm.nih.gov /genbank),選取DNA序列相似度最高的菌株結果作為比對結果。
2 結果
2.1 潔凈區環境微生物和標準菌株生化鑒定結果
對收集的潔凈區環境微生物菌株進行初步染色鏡檢,利用BBL CRYSTAL細菌鑒定儀對收集到的環境中的細菌和標準菌株(細菌)進行生化鑒定。見表1和表2。
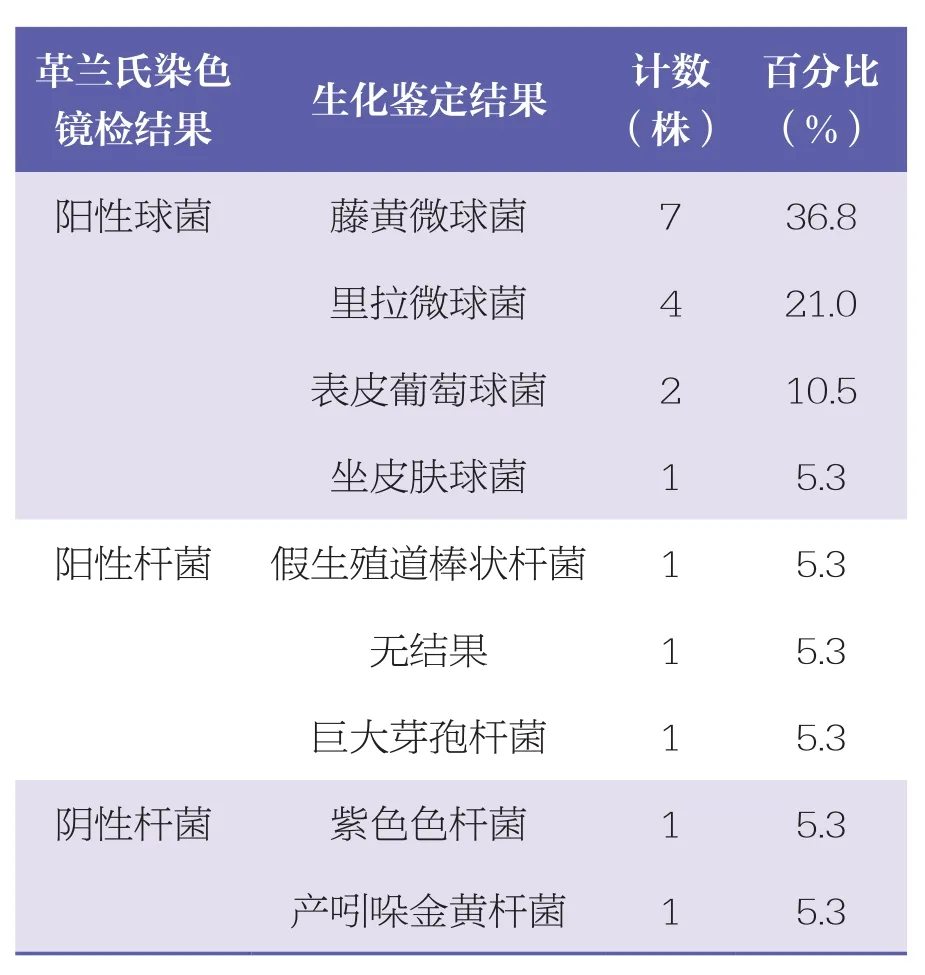
表1 環境微生物生化鑒定結果
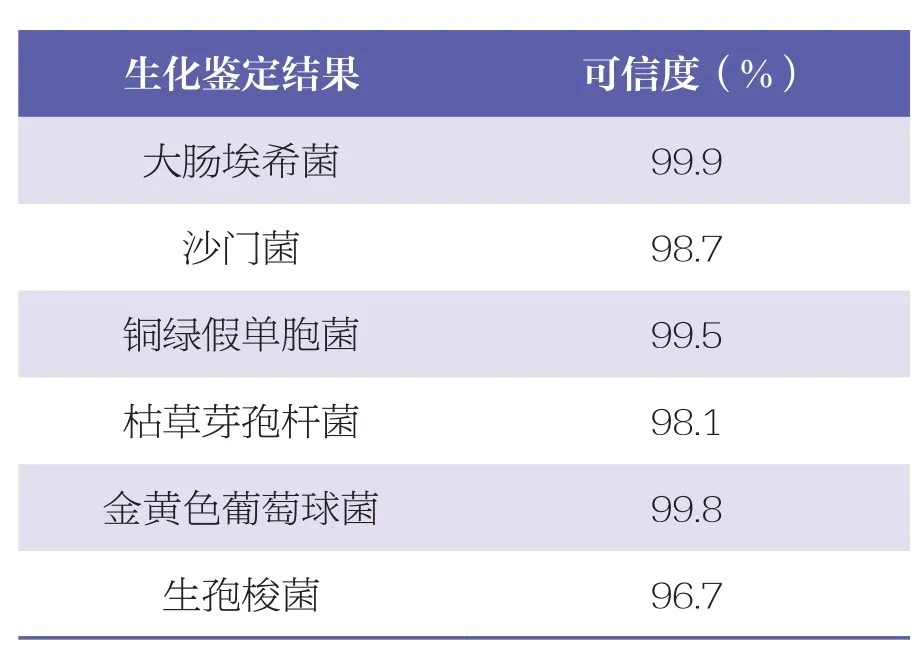
表2 標準菌株(細菌)生化鑒定結果
2.2 潔凈區環境微生物和標準菌株的全基因組分析
采用生物信息學方法對菌株的測序結果進行數據拼接,生化鑒定結果同二代測序的結果。見表3。
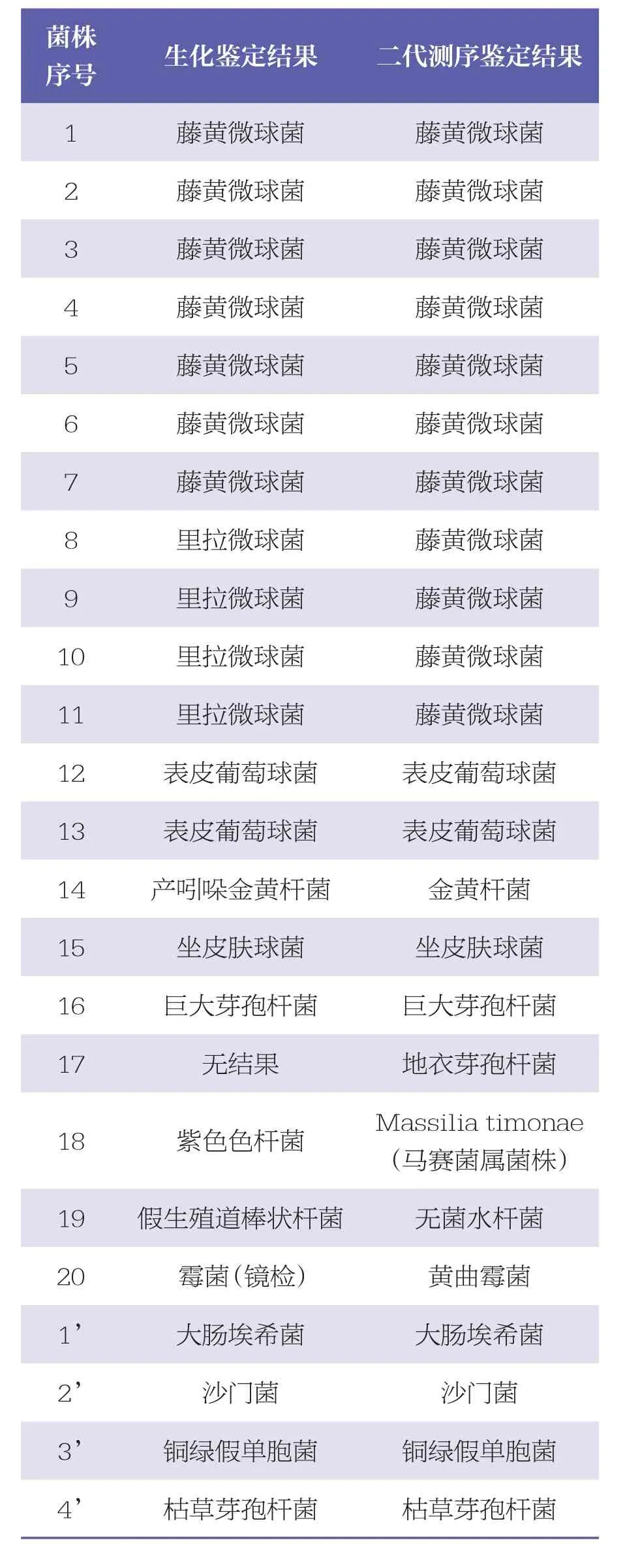
表3 2種鑒定方法分析結果對比
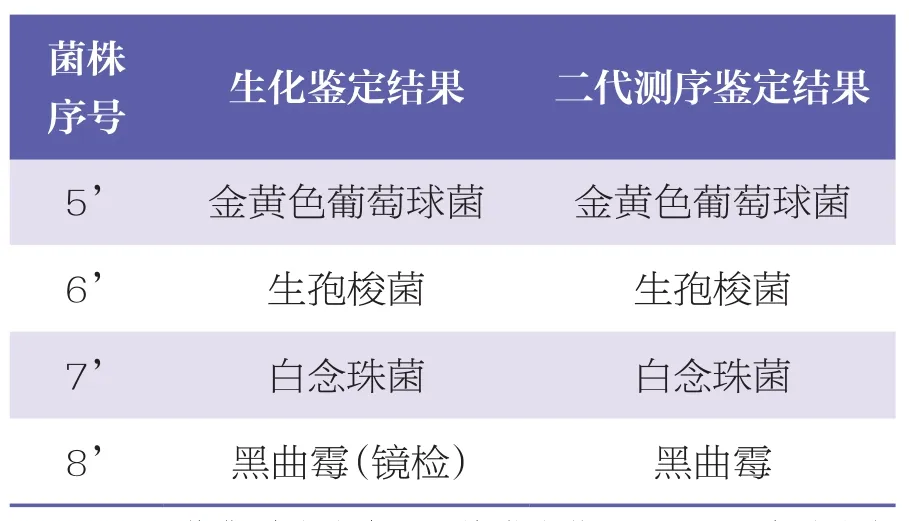
續表
2.3 潔凈區環境微生物的統計分析
對潔凈區收集的環境微生物進行統計分析,革蘭陽性球菌占70.0%;革蘭陽性桿菌占15.0%;革蘭陰性桿菌占10.0%;霉菌占5.0%。見圖1。
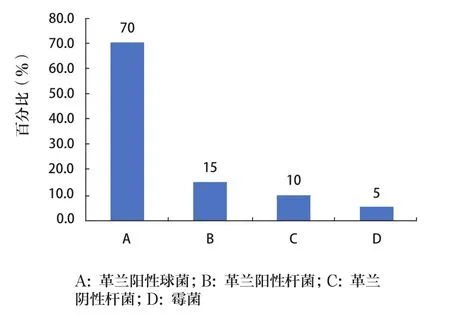
圖1 潔凈區環境菌的統計分析
3 討論
本研究從潔凈區分離出的環境微生物只有20株,菌株數量不多,分析原因可能與新建實驗樓潔凈區啟用時間不長有關。本研究潔凈區分布的細菌中革蘭陽性菌占絕大多數,其中又以微球菌屬和葡萄球菌屬為主,二者均是人體易攜帶污染的微生物;其次是芽孢桿菌屬,為消毒劑較難消殺的一類細菌,這與大多數實驗室潔凈區環境微生物的類型相似[7]。這也提示我們,在日常制定潔凈區的消毒規范時,應注意控制潔凈區人員數量、消毒的頻次和消毒劑類型的使用,以確保潔凈區的環境微生物在可控范圍內,不能影響藥品的微生物檢驗工作。
從表3可以看出,藤黃微球菌和里拉微球菌用BBL CRYSTAL生代鑒定為2種菌,而二代測序鑒定結果分析均顯示為藤黃微球菌。在前期對2種細菌進行革蘭染氏色鏡檢下的形態也有一些區別,藤黃微球菌鏡檢下細菌的著色較深,成四連體分布,而里拉微球菌的形態較小,不成明顯的四連體,提示在分類學上二者雖然同屬微球菌屬,卻分屬不同種[10]。測序通量與準確度密切相關,全基因組測序分析后的結果不一致的原因可能是二代測序的通量不夠,導致準確度下降。類似的情況是生化鑒定為假生殖道棒狀桿菌的菌株,二代測序為無菌水桿菌。因此,現階段認為有必要聯合運用多種手段對潔凈區環境微生物進行鑒別和溯源[11],可以大大地提高鑒定準確度,對后續相關性研究也能起到積極作用。
藥品微生物檢驗尤其是無菌檢驗中,環境微生物的種類和數量是影響檢驗結果的重大風險因素,直接關系著檢驗結果的準確性和可靠性[12]。因此,建立藥品檢驗潔凈區環境微生物數據庫、完善陽性檢出菌溯源體系,對判斷污染菌來源、實施有效的潔凈環境控制非常必要[13]。全基因組測序由于有著較高的準確度和分辨率,其在藥品微生物檢驗陽性菌的溯源分析中有著較大的應用價值和發展潛力。本研究在4個月的時間對潔凈區收集的環境微生物進行收集、生化鑒定及二代測序,初步建立了近期潔凈區環境菌株菌庫和標準菌庫,后續會不斷更新和完善潔凈區的環境菌庫數據,動態地反映近期潔凈區的環境微生物的分布情況,更好地進行環境微生物的動態監測,為藥品微生物檢驗尤其是無菌檢驗的污染調查及溯源分析提供技術支持。

