EGCG對高血壓的調節功能及其作用機理研究進展
張一帆,葉江成,龔明秀,李定國,趙 進,3*
1. 中國計量大學 生命科學學院,浙江 杭州 310018;2. 浙江三農茶業有限公司,浙江 永嘉 325101;3. 中國計量大學 食品加工與質量控制研究所,浙江 杭州 310018
高血壓是一種主要由機體內皮功能障礙和血管張力改變引發的疾病,并且伴有很高的致死率[1]。目前,對于高血壓的治療主要以服用抗高血壓藥物為主,但事實上藥物治療的效果不明顯,只有約十分之一的高血壓患者通過藥物完全實現對血壓的控制[2];同時,抗高血壓的藥物可能對患者產生較強的副作用,如長期服用抗高血壓藥物可能會增加患者患癌和意外摔倒的風險[3-4]。
茶是我們日常生活中最常見的功能性飲料之一,富含茶多酚等多種生物活性物質。茶多酚主要為兒茶素,其中表沒食子兒茶素沒食子酸酯(Epigallocatechin gallate,EGCG)是兒茶素中最具生物活性的化合物。EGCG主要具有抗氧化[5]、抗癌[6]、抗糖尿病[7]、抗應激[8]和抗炎癥[9]等多種有益功能。目前,盡管不斷有研究顯示EGCG有助于預防高血壓和減輕與其相關的慢性心血管疾病[10]。然而,EGCG對高血壓的作用機制仍不清晰,有待進一步闡明其調控機理。
1 EGCG的結構
EGCG是一種多酚類的結構(如圖1),包括兩個芳香結構和三個碳橋結構。EGCG可以利用氫鍵調節與其它物質的相互作用,還能依賴特有的鄰苯二酚結構進行自氧化作用,這使EGCG具有較強的抗氧化活性和清除自由基的能力[11]。并且,EGCG的自氧化作用還能產生大量活性氧(ROS),ROS主要由單態氧、羥基自由基、超氧化物和過氧化物等物質組成[12]。
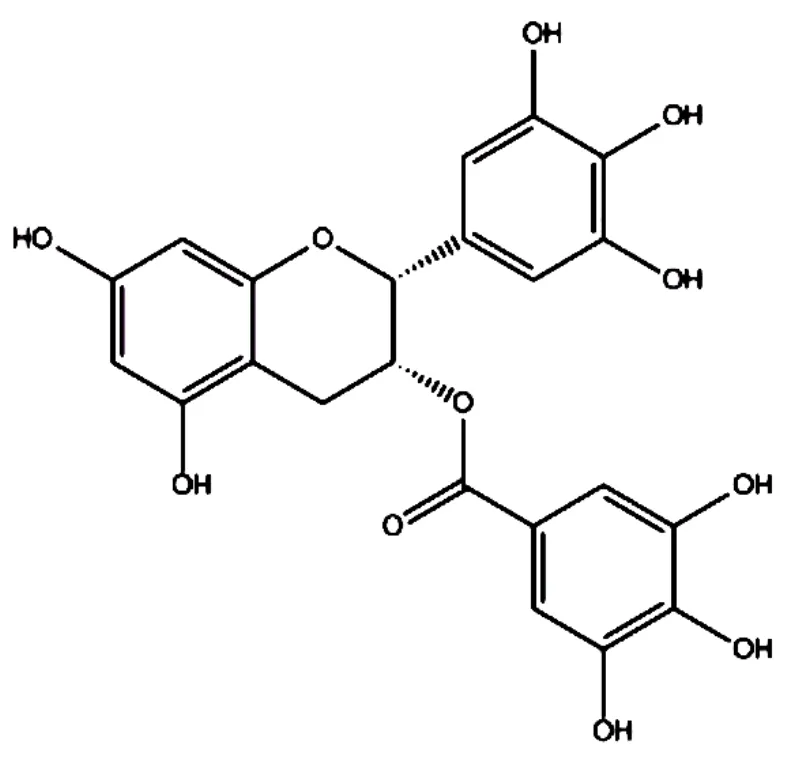
圖1 EGCG的結構式Figure 1 The structural formula of EGCG
EGCG是茶葉中主要的生物活性成分,對人體健康有許多益處[13]。但研究發現EGCG在水溶液中不穩定,在油脂中也不容易溶解[14],這種較差的穩定性和溶解度直接導致其生物利用度很低[15]。此外,EGCG還易受多種生物轉化的影響,如甲基化主要發生在肝臟和小腸中,由特定的酶介導EGCG在腸道上皮細胞中的吸收率也不高[16],并且還易在堿性pH環境中降解[17]。
2 EGCG對高血壓的調控作用
2.1 體外細胞干預試驗
肥胖是高血壓最重要的誘因之一,約70%的高血壓患者屬于超重或肥胖[18-19]。小鼠前脂肪細胞(3T3-L1)是研究肥胖及其相關疾病常用的細胞,Kim等[20]研究發現EGCG對3T3-L1有明顯的抗氧化和抗成脂作用,能顯著抑制3T3-L1脂質積累和成脂特異性蛋白的表達,并且降低3T3-L1內ROS的生成,表明EGCG通過提高3T3-L1抗氧化酶的活性和表達抑制脂質的積累。此外,該研究還發現EGCG能抑制3T3-L1自由基的產生,這可能與EGCG通過抗氧化作用抑制脂肪細胞分化有關。Lu等[21]研究表明EGCG對脂肪細胞分化和成熟的抑制效果與影響3T3-L1脂肪酸合成酶活性有關。Wu等[22]試驗發現EGCG通過調節脂肪細胞中有絲分裂的進程,顯著降低3T3-L1中脂肪的生成。Guan等[23]試驗發現,EGCG對3T3-L1脂滴積累和脂質代謝的抑制作用是通過激活腺苷酸活化蛋白激酶(AMPK)進而抑制PPAR-γ(過氧化物酶體增殖物激活受體的一種亞型)表達實現的。Oruganti等[24]以3T3-L1為研究對象,發現胡椒堿(PIP)和EGCG的協同作用對3T3-L1的細胞分化、脂滴沉積和甘油釋放效果明顯更好,該作用是通過調節參與脂肪形成和脂質代謝的關鍵脂肪因子實現的。Ahmed等[25]發現大豆中染料木素(G)、綠茶中EGCG(E)和葡萄中白藜蘆醇(R)組合使用能明顯抑制3T3-L1的分化,該研究認為G、E和R對3T3-L1的作用與PPAR-γ有關。上述研究表明EGCG對高血壓的預防和治療作用是通過抑制機體內脂肪生成實現的。
內皮細胞主要分布于血管周圍,是氧氣和營養物質輸送的重要通道,能有效調控血壓的變化以及維持血管正常舒張與收縮。Meng等[26]用不同濃度的EGCG預處理人血管內皮細胞,結果發現經EGCG預處理后過氧化氫誘導的人血管內皮細胞存活率明顯改善。Zhong等[27]以缺氧條件下培養的人臍靜脈內皮細胞為研究對象,發現EGCG通過抑制高遷移率族蛋白B1(HMGB1)表達,保障內皮功能正常。C反應蛋白(CRP)與高血壓等心血管疾病的發生密切相關,Li等[28]發現,EGCG可以抑制由血管緊張素 II(Ang II)和白細胞介素 6(IL-6)誘導的U937巨噬細胞中CRP的表達。
2.2 體內動物干預實驗
因與人類基因組具有高度的同源性,小鼠和大鼠作為模式動物被廣泛應用于高血壓等心血管疾病的研究中。Nomura等[29]發現EGCG通過影響大鼠體內NO信號轉導,顯著降低了高鹽飲食喂養的自發性高血壓大鼠的血壓。通過肝臟轉錄組和蛋白質組聯合研究[30],發現EGCG通過抑制機體內氧化應激、脂肪酸轉運和膽固醇代謝的激活,顯著改善了高脂飲食誘導的肥胖大鼠血壓水平和血脂含量,降低了總游離脂肪酸含量。Lee等[31]研究表明,EGCG可減輕高脂高糖飲食大鼠體內的氧化應激,降低線粒體和內皮細胞中凋亡信號的過度高表達。Hsieh等[32]以自發性高血壓大鼠為研究對象,發現EGCG治療的自發性高血壓大鼠收縮壓、舒張壓和平均血壓顯著降低。Luo等[33]研究表明,EGCG通過保護大鼠腎臟免受損害,緩解大鼠體內收縮壓的升高。Sabri等[34]試驗表明,EGCG對注入血管緊張素II的高血壓小鼠有降壓作用。Yi等[35]試驗發現EGCG能降低自發性高血壓大鼠體內的血壓,并且緩解機體內的氧化應激反應。Lamothe等[36]發現,向懷孕母鼠體內注射地塞米松(一種人工合成的皮質類固醇)后會增加后代子鼠患高血壓的風險,但懷孕母鼠經EGCG治療干預后能夠降低這種患高血壓疾病風險。
2.3 EGCG與其它物質的協同調控功效
許多研究證實EGCG對高血壓的治療有顯著作用,為提高EGCG在體內的生物利用率,研究人員開始將其他物質與EGCG協同使用,以增強EGCG在體內的活性和作用效果。Xie等[37]研究顯示,EGCG與維生素C(Vc)及甘油聯合使用可提升EGCG在高溫、堿性環境和人體胃腸液中的穩定性和生物活性。Kim等[38]發現EGCG和咖啡因具有與去甲腎上腺素發生協同作用,能夠調節與脂質合成和分解代謝有關的各種酶活性(如脂肪酸合成酶、胰脂肪酶和胃脂肪酶),刺激棕色脂肪組織的產熱。Liu等[39]用15種不同濃度的EGCG和咖啡因同時飼喂小鼠8周,結果發現EGCG和咖啡因的聯合治療能強烈抑制小鼠體重增加和脂肪積累,其中 0.1% EGCG + 0.1%咖啡因處理組對體重和脂肪積累的抑制效果最為明顯。Xin等[40]試驗發現,咖啡因和EGCG聯合使用可顯著改善高碳水化合物飲食誘導的小鼠體重增加、肝臟脂質沉積和糖代謝水平。Pathak等[41]研究發現EGCG與胰高糖素樣肽-1激動劑(exendin-4)聯合使用可降低高脂糖尿病小鼠的體重和脂肪含量,改善總膽固醇水平和甘油三酯含量。Most等[42]發現EGCG和白藜蘆醇協同使用可促進肥胖人群的脂肪氧化和分解水平。Sharma等[43]研究顯示,EGCG與益生菌的聯合作用可顯著改善小鼠體內的氧化應激。Shi等[44]發現硝苯地平(NIF)+EGCG組控制血壓所需時間顯著縮短,并且有效控制血壓所需的治療劑量也較低。Zhu等[45]發現低劑量的EGCG和咖啡因聯合使用可以產生協同抗肥胖效果,該機制可能是通過改善生物體內腸道微生物群落多樣性來實現的,如增加β多樣性。Yang等[46]研究表明,EGCG和檸檬酸聯合可顯著增加細胞內ROS和過氧化氫生成。Yoo等[47]發現,富含EGCG的綠茶提取物與綠茶加工過程中獲得的黃酮醇和多糖等副產物的聯合使用可降低脂肪細胞中脂質在腸道的吸收率,減少脂質積累。
3 EGCG對高血壓的調控作用機理
3.1 EGCG調節生物體內NO信號轉導
血管內皮細胞是一層扁平的鱗狀細胞,能連續覆蓋在血管腔表面。它不僅是血液和血管壁之間的重要屏障,還能分泌多種血管活性物質,在調節血管張力和維持血管功能方面發揮重要作用[48]。在內皮細胞中,一氧化氮(NO)是維持血管穩態的關鍵分子,當機體中NO濃度因某些異常生理條件而失衡時就可能誘發內皮功能障礙[49]。血管內皮功能障礙與高血壓的發生密切相關,血管內皮功能障礙引起的NO失衡在高血壓的發生發展中起著重要作用,而高血壓本身又能加重血管內皮功能障礙,進而導致惡性循環[50]。
健康的血管內皮細胞能調節血管張力和通透性,保證血管正常的舒張和收縮,并且產生血管活性物質如NO[51],而血管損傷后血管內皮NO合酶(eNOS)產生的NO會顯著減少[52]。NO由一氧化氮合酶(NOS)以L-精氨酸為底物產生,NOS有3種不同類型的亞型,包括誘導型NOS(iNOS)、神經元型NOS(nNOS)以及內皮型NOS(eNOS)。研究發現,作為血管舒張物質,NO在心血管系統中能發揮巨大作用[53-55]。血管內皮中NO含量的穩定主要靠eNOS維系,但當機體因外界環境改變而發生應激后會激發iNOS活性,導致NO過量產生,從而導致內皮功能障礙,并在后期誘發高血壓等心血管疾病[56]。Jamwal等[57]發現高血壓會導致血管內皮中L-精氨酸和eNOS的失調,從而降低NO的生物利用度,誘發血管內皮功能障礙。
通常而言,與健康人群相比高血壓患者體內NO水平明顯失衡[58]。研究發現,EGCG能改善機體內NO的失調[59]。作為一種抗氧化劑,EGCG能在內皮細胞中誘導NO釋放并減少內皮素的生成,并且EGCG通過降低內源性NO抑制劑的水平來提高正常NO的生物利用度[60]。Palai等[61]發現,EGCG可能通過調控eNOS的表達,促進血管平滑肌舒張。Huei 等[62]發現EGCG在骨骼肌中的血管舒張作用依賴于NOS,并且這種作用不會劇烈影響健康大鼠體內其他正常代謝活動,這表明EGCG可以作為血管舒張劑。Nomura等[63]發現,EGCG可通過抑制高鹽飲食喂養的自發性高血壓大鼠體內尿NO代謝物(NOx)的水平影響大鼠體內NO的含量。Xie等[64]研究表明,EGCG能緩解尿酸誘導的內皮細胞功能障礙并且抑制iNOS的表達。Potenza等[65]認為,EGCG對自發性高血壓大鼠內皮功能障礙的調節是通過激活磷脂酰肌醇-3-激酶(PI3-K)通路刺激內皮細胞產生NO實現的。Chen等[66]發現EGCG可以顯著抑制由利血平(RES)引起的大鼠NO水平的升高,但加入NO前體(L-精氨酸)后EGCG對大鼠體內NO的調控作用明顯減弱,再加入NOS抑制劑(硝基精氨酸甲酯)后ECCG又恢復對NO的調控作用,該結果表明ECCG對NO通路的調節作用可能與NO前體和NOS抑制劑有關。
3.2 抑制血管緊張素 II活性
研究表明腎素-血管緊張素系統(RAS)通過調節血壓和電解質平衡,在高血壓等心血管疾病發生中起著重要作用[67-68]。一般認為,RAS誘發的高血壓與血管緊張素II的血管收縮作用有關[69]。血管緊張素II是一種腎血管收縮劑,血管緊張素II在RAS中由血管緊張素I產生,是導致高血壓等心血管疾病的重要誘因[70]。Mondaca 等[71]和 Klatt等[72]發現 Ang II可促進機體內血管平滑肌細胞肥大,誘導高血壓的發生。Cai等[73]和Yang[74]試驗結果表明,EGCG能干擾Ang II在小鼠體內的表達,當注入血管緊張素II的小鼠經EGCG處理后小鼠體內血壓迅速下降。
Ma等[75]研究表明,EGCG通過調節Hippo信號通路抑制血管緊張素II的表達。Zhan[76]和Zhao[77]等研究發現,EGCG對血管緊張素II的抑制作用可能是通過可以抑制AT-1受體(血管緊張素II1型受體)的表達來實現的。Masi等[78]研究顯示,Ang II對機體的調控作用主要與Ang II 1型(AT1)和2型(AT2)受體有關,AT1受體能在心血管系統中普遍表達,而AT2受體在成人體內的活性很低。Liu[79]發現EGCG對血管緊張素II的抑制作用可能與血管緊張素轉換酶(ACE)有關,ACE能促進血管緊張素I(Ang I)轉化為Ang II[80],EGCG可能通過自身氧化轉化為親電的醌后再與ACE結合從而對ACE活性產生變構抑制作用。Korystova等[81]證實EGCG可以抑制ACE活性,并且EGCG的濃度越高,對ACE的抑制效果更顯著[82]。Yang等[83]證實EGCG可以改善由Ang II引起的人臍靜脈內皮細胞功能障礙,發現EGCG能抑制p38蛋白通路的表達,而p38蛋白通路可能是治療高血壓等心血管疾病的重要靶點。
3.3 調控脂質代謝通路
肥胖是由于機體攝入和消耗的熱量不平衡,導致脂肪細胞的過度生長和沉積[84]。肥胖與遺傳、日常習慣等諸多因素有關,是高血壓的重要誘因之一[85-86]。研究發現,肥胖兒童患高血壓的概率與體內脂質的堆積程度呈線性關系[87]。Kapoor等[88]實驗顯示EGCG可加速機體內能量消耗,加快代謝率,從而促進脂肪氧化。Santamarina等[89]發現,EGCG通過刺激線粒體呼吸鏈增加能量消耗,特別是加快脂肪氧化,從而抑制高脂飲食喂養的小鼠肥胖。Zhou[90]發現EGCG通過促進小鼠體內棕色脂肪組織產熱從而抑制高脂飲食誘導的小鼠肥胖。Bae[91]和Suzuki[92]研究發現,EGCG能有效緩解由高脂飲食誘導的機體內脂肪堆積作用。表明EGCG對高血壓的治療作用可能與調控脂質代謝通路有關。
Ushiroda[93]和Ning[94]研究發現,EGCG對小鼠體內脂質的抑制作用可能與改善小鼠體內腸道微生物群落失調有關,這與Adnan等[95]發現自發性高血壓大鼠血壓變化與體內腸道菌群的調節作用有關的結論一致。Tecce等[96]和Yuan等[30]的試驗發現,EGCG通過降低乙酰輔酶A羧化酶的活性抑制脂質在體內的分化以及膽固醇的積累。Javaid[97]、Zhang[98]和Yamashita等[99]研究發現EGCG對脂肪的抑制作用可能與PPAR-γ蛋白有關,EGCG可以與PPAR-γ蛋白在活性位點特異性結合并阻斷其活性,EGCG可以作為PPAR-γ蛋白在人體中潛在的靶點抑制人體內脂肪積累和脂肪細胞分化進而抑制肥胖。Liu[100]、Muhammed[101]、Park[102]和 Huang[103]試驗均發現,EGCG能夠顯著降低小鼠體重和脂肪重量,并且還改善了小鼠體內的血清脂質代謝,降低甘油三酯、總膽固醇和高密度脂蛋白膽固醇的表達,減少肝臟和脂肪細胞中脂肪的積累。Liu[104]發現EGCG通過抑制線蟲體內ATGL-1(編碼脂肪甘油三酯脂肪酶的同源物)和ACS-2(編碼酰基輔酶A合成酶的同源物)基因的表達,有效緩解線蟲體內脂肪的堆積。Li[105]實驗發現,EGCG可通過調控SREBP-2蛋白(調節膽固醇合成的重要因子)的表達,抑制體內肝臟膽固醇的合成。Yen等[106]發現EGCG能抑制高脂飲食誘導的肥胖大鼠體內脂質積累,減輕腹部脂肪的堆積,該機制可能與EGCG增加前脂肪細胞因子1(Pref-1)活性有關。Li[107]研究表明,EGCG能通過激活AMPK活性來降低小鼠肥胖和體內白色脂肪組織的增加。
3.4 調控 ROS 表達
活性氧是細胞正常代謝的中間產物,在細胞信號轉導中起著至關重要的作用[108],可以調節內皮細胞和平滑肌細胞的生長,維持血管張力以及促進新血管的形成[109]。ROS是一種含有氧的化學反應分子,是氧氣正常代謝的一種自然副產品。氧化應激是指機體內ROS和抗氧化防御之間的平衡失調。在健康機體中,ROS作為第二信使參與細胞生長、炎癥、凋亡和細胞分化等各種轉錄因子和激酶的激活和調控[110]。但在病理狀態下,機體內的ROS的含量往往不受調控,過量的ROS會引發機體產生嚴重的氧化應激[111],對細胞大分子如DNA、脂質和蛋白質造成嚴重損傷[112]并且引發脂質過氧化[113]以及導致機體新陳代謝障礙[114],最終誘發高血壓等多種慢性心血管疾病[115-117]。Rodríguez[118]和Senoner[119]等實驗表明,高血壓患者體內的氧化應激水平往往較高,減少機體內的氧化應激可以顯著降低高血壓等心血管疾病的死亡率。
研究者發現,ROS是高血壓的重要誘因之一[120],而NADPH氧化酶是ROS的重要來源[121],在血管平滑肌和內皮細胞中NADPH氧化酶通過促進ROS的生成,調控機體內血壓的變化[122]。天然酚類化合物(如EGCG)能通過擾亂NADPH氧化酶亞基的組裝來阻止ROS的產生[120],EGCG通過調控機體內ROS的含量在預防和治療高血壓等心血管疾病方面發揮重要作用[123]。EGCG具有強抗氧化活性,能在體外進行超氧催化自氧化,產生可誘導細胞死亡的ROS。但是在正常的生理條件下,EGCG這種自氧化并不會廣泛發生[124]。Yi[125]研究顯示,EGCG可以減緩腎血管性高血壓引發的氧化應激的反應從而減少ROS的生成。Liang[126]發現,EGCG可顯著減輕由吸煙誘發心肌細胞中的氧化應激反應,減少細胞內和線粒體ROS的產生。Rasheed等[127]發現,EGCG顯著降低了小鼠體內的NADPH氧化酶的含量,增強了小鼠體內總抗氧化能力,從而抑制了小鼠體內ROS生成。Sarkar等[128]研究表明,EGCG通過降低細胞膜上p47phox和p67phox(NADPH氧化酶復合體的組成成分)的表達,抑制NADPH氧化酶的活性。Ma等[129]發現高糖顯著刺激細胞中ROS的產生,而EGCG能降低ROS的表達。Casanova[130]研究發現,EGCG通過調節線粒體參與的自噬、增加抗氧化酶的表達和改善過度的肌肉自噬,逆轉肥胖骨骼肌中ROS生成、內質網應激和蛋白質降解的增加。Yi等[131]發現,EGCG對ROS的作用與抗氧化酶、超氧化物歧化酶(SOD)活性的增加有關。Yi等[35]試驗發現,添加EGCG后可以緩解神經遞質之間的失衡,從而緩解ROS的生成。核因子2(Nuclear factor 2, Nrf 2)是一種轉錄因子,可以通過調節某些基因的表達,緩解機體內的氧化應激反應[132-133],調控血管血壓的異常變化[134]。Wada等[135]試驗發現,EGCG通過Nrf 2通路抑制胰島細胞中抗氧化酶的表達和ROS的產生。Xie等[136]研究發現,EGCG通過激活Nrf 2信號通路降低小鼠體內ROS的水平。Singh等[137]試驗認為,EGCG對砷中毒小鼠體內氧化應激的緩解作用與Nrf 2信號通路的改變有關。
EGCG在高血壓中的作用機制見圖2。
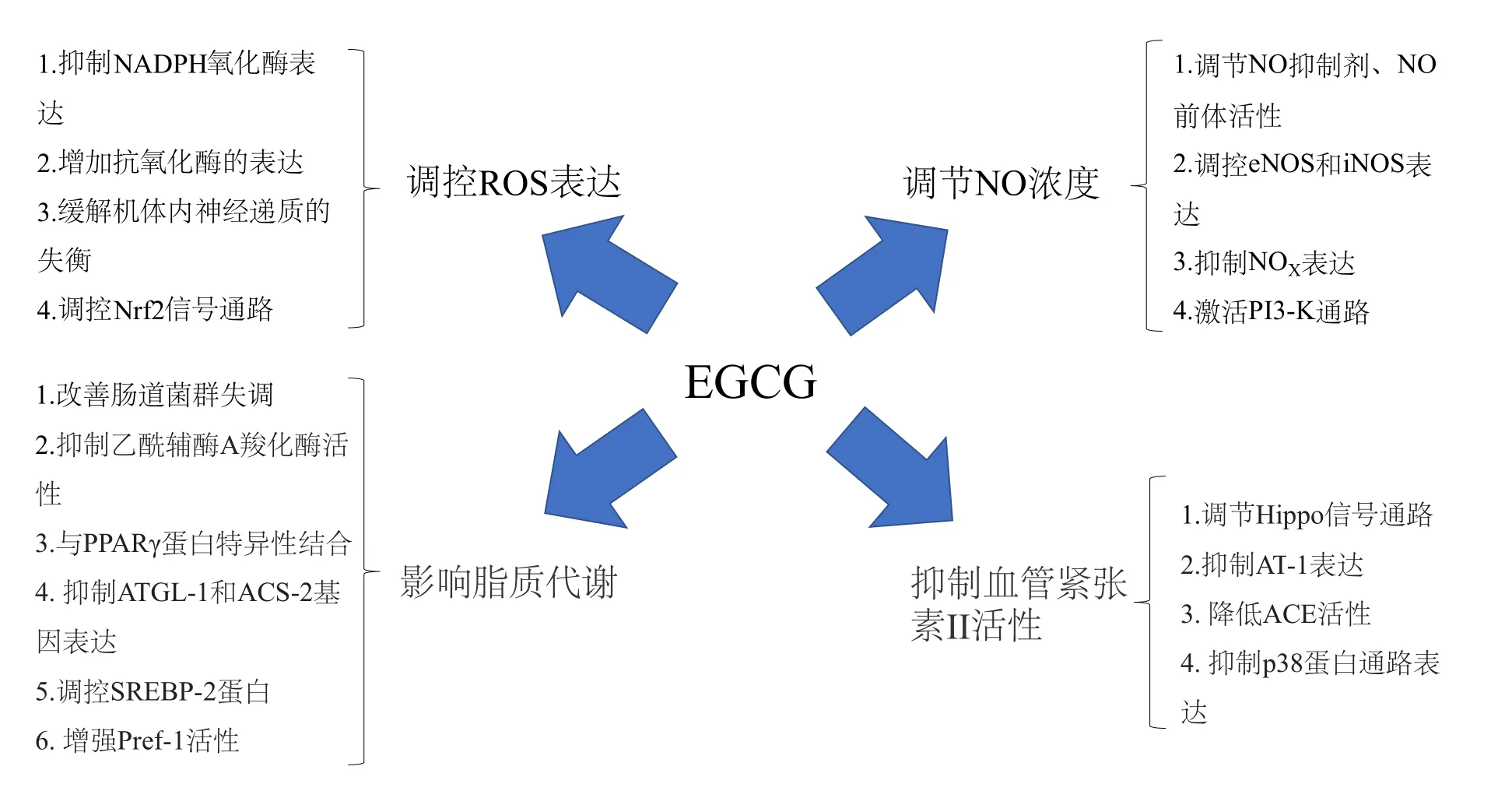
圖2 EGCG在高血壓中的作用機制Figure 2 The regulation mechanism of EGCG on hypertension
4 研究展望
EGCG可以有效調控高血壓,其作用機理主要包括調節NO濃度、抑制血管緊張素II活性、影響脂質代謝通路和調控體內ROS表達。EGCG顯示出了良好的治療高血壓的特性,但目前對EGCG的臨床藥物研發仍存在一些問題。
一是EGCG的安全性。作為茶葉中的主要功效成分之一,Yates等[138]和Zhang等[139]研究發現,攝入過高劑量的EGCG可能會對人體產生一定危害,這與Peng等[140]發現高劑量EGCG會導致秀麗隱桿線蟲壽命縮短的結論相類似。研究發現[141-143]成人每日攝入EGCG的安全劑量約為 300 ~ 700 mg,需要對 EGCG 在人體內的安全性進行更為深入系統的研究。
二是EGCG的生物利用度。EGCG在機體內的生物利用度不高,易受濃度、環境等因素的影響[144]。EGCG的生物利用度在很大程度上取決于它們在腸道中的轉化率,研究發現大多數被攝入的EGCG會被腸道微生物代謝成各種衍生物[145]。因此,如何將EGCG有效地在機體內降解和吸收,是應用EGCG進行高血壓治療領域亟待解決的問題。

