半導體/聚合物納米復合材料光催化降解污水的研究
趙 麗,蘇碧桃
(1.西北師范大學,甘肅 蘭州 730070;2.酒泉職業技術學院,甘肅 酒泉 735000)
1 引言
隨著人類社會的發展,能源短缺、環境污染已成世界未來發展中的重大難題而日益受到關注[1]。其中工業生產過程中排放的大量有機染料引起的水污染問題是環境污染的主要難題之一,除去有機染料的主要技術包括化學氧化[2]、膜分離[3]、吸附[4]、光催化[5]和生物修復[6]等。其中,利用半導體材料在太陽光下對污水中有機染料進行降解,利用取之不盡、用之不竭太陽能的大規模使用或將成為解決困境的絕佳措施[7,8]。
自1972年Fujishima等[9]報道了TiO2作為光催化劑用于水裂解產生O2,大量的半導體光催化材料如ZnO[10]、SnO2[11]、Bi2O3[12]、CuO[13]等應用于有機污染物的光降解。理想的光催化劑應具有高效的敏化能力、充分利用太陽光的輻照能量、價格低廉、毒性小、可持續性強等優點[14]。光催化領域,開發新型、高效、無污染的光催化劑是一個研究熱點,同時也面臨著諸多挑戰。
相對于結構難以調控的無機半導體材料,共軛高分子聚合物因具有π-共軛結構,在光催化水分解和有機污染物的光降解等領域得到了廣泛應用[15~18]。本課題針對α-Fe2O3/聚糠醇(PF)納米復合催化材料制備問題進行了系統的探究。通過兩步法(即:原位酸催化聚合、熱活化處理),使得復合材料中的強化學鍵能夠有效結合并保證其穩定性。同時,利用XPS、FTIR等對所制備材料的相關性能進行了表征,通過描述其對于MB的脫色功能了解了其催化活性情況。
研究結果證實:課題采用兩步法制備的納米復合材料,能夠有效地對可見光區以及紫外光區的全程光波進行吸收。在室溫自然光環境下,可以使MB脫色,80 min的脫色率便可以達到100%,而同等條件下純的α-Fe2O3納米粒子對MB的脫色降解還達不到10 %。該納米復合催化劑穩定性高、無二次污染,預計在光能的利用、有機污染物的處理等方面有應用前景。
2 實驗部分
2.1 試劑與儀器
本課題相關實驗涉及的主要試劑如下:糠醇F(分析純),上海同方精細化工有限公司(上海);乙二醇(C2H6O2)(分析純),萊陽市雙雙化工有限公司(山東煙臺);亞甲基藍(MB)(分析純),北京化工廠(北京);Fe(NO3)3·9H2O(分析純),天津市巴斯夫化工有限公司(天津);無水乙醇(分析純),北京中聯化工試劑廠(北京)。
本課題相關實驗涉及的主要儀器如下:熱重分析儀,Diamond TG/DTA/SPAECTRUN ONE型,美國PE公司(美國);粉末X射線衍射儀,D/Max-2400型,日本理學公司(日本);紫外-可見光譜儀,UV-2550型,日本Shimadzu公司(日本);多功能電子能譜儀,PHI5702型,美國物理電子公司(美國);電子透射顯微鏡,JEM-1200EX型,日本光學公司(日本);傅立葉變換紅外光譜儀,FTS3000FX型,美國DIGILAB公司(美國)。
2.2 α-Fe2O3/PF的制備
2.2.1 納米粒子α-Fe2O3的制備:
α-Fe2O3納米微粒的制備,主要步驟如下:第一,在磁力攪拌環境下,在60 mL的乙二醇當中,加入 Fe(NO3)3·9H2O15.15 g 使其混合均勻。在70 ℃的環境下進行回流,時間為12 h,回流獲得的溶膠放置于烘箱當中;第二,選擇70 ℃進行烘干,得到顆粒物,將其碾磨成粉,放置到干鍋當中,進行煅燒,溫度為600 ℃,時間為2 h,經過高溫煅燒,即可以獲得α-Fe2O3納米顆粒。
2.2.2 原位聚合
將3.000 gα-Fe2O3納米顆粒在攪拌的環境下,分散到10 mL的EtOH當中,在形成的懸浮體系當中,加入10 mL F,然后繼續進行攪拌,持續時間為12 h,一直到F單體分子能夠充分地吸附到α-Fe2O3納米顆粒表面。隨后,繼續對其進行攪拌,緩慢地滴入H2SO4溶液,逐漸完成原位聚合。經過一段的時間后,即可以獲得棕黑色固體,將其在室溫環境下進行干燥,便可以獲得復合材料的前驅體,也就是α-Fe2O3/PF。
2.2.3 熱轉化
在獲得前驅體后,需要進一步進行熱轉化處理。具體的處理步驟為:第一,將前驅體放置到空氣氣氛當中,進行熱處理,時間為30 min,從180 ℃(標記為s-1)開始間隔60 ℃至540 ℃(標記至s-7);然后,將前驅體于空氣氣氛、360 ℃,從10 min(標記為t-1)開始間隔10 min 進行熱處理至50 min(標記至t-5);最后,將不同α-Fe2O3含量的前驅體于360 ℃下熱處理30 min,α-Fe2O3及對應標記分別為:13.91%(p-1)、24.23%(p-2)、34.82%(p-3)、45.26%(p-4)、56.42%(p-5)、71.49%(p-6)、100 %(p-7)。本研究選擇最佳性能的樣品產物,即:p-4。
2.3 光催化實驗
在室溫和自然光條件下,進行催化實驗,通過MB溶液的顏色變化,了解所獲得的納米復合材料所具有的催化性能。具體的步驟為:第一,選擇50 mL的燒杯,將10 mg/L的MB溶液40 mL放置其中,然后進行攪拌,在攪拌環境下,加入催化劑樣品,質量為40 mg,每間隔固定的時間,取4 mL的生成物,進行離心處理,使用722s型分光光度計,對MB中離心液的最大吸收波長(λmax=662 nm)進行測定,獲得具體的吸光度(At)情況。通過脫色率Dt(%)評價所制備材料的催化性能。其中,公式為:Dt(%)=(Ao-At)/Ao×100%。在公式當中,Ao和At分別表示染料溶液初始階段以及反應時間為t時的具體的吸光度數值情況。
3 結構表征與討論
3.1 IR分析
通過基于前驅體α-Fe2O3/PF(a)描述的相關IR譜圖可以看出,3421 cm-1附近存在可以對O-H進行振動吸收的寬吸收帶,在2926 cm-1附近存在可以對高分子鏈上=C-H及-C-H振動吸收的微弱吸收帶,在1629 cm-1附近存在可以對呋喃環中C=C振動吸收的吸收峰,在1711 cm-1附近存在可以與C=O特征峰的產生對應的吸收峰,在1145 cm-1附近出現與C-O-C和C-O-Fe具有一定關系的對稱和反對稱振動吸收峰(圖1)。

圖1 前驅體與樣品s-1(b)、s-4(c)、s-6(d)IR譜
結合樣品OR譜圖與前驅體的譜圖進行對比,可以看出:第一,在經過適當處理的情況下,在,1700 cm-1附近出現了特征吸收峰的紅移,在與C=C共軛雙鍵吸收峰對應的吸收峰當中,1616 cm-1附近出現了寬化并且在強度方面有所增加。其主要是因為在活化處理后,由于獲得較大的能力,各個分子鏈之間會出現相互攻擊[19]。在攻擊過程中,發生取代基團減除以及交聯反應,從而使復合材料當中的聚合物不飽和度增加[20],與此同時,C=C共軛鏈長度也在不斷增加,最終導致C-H吸收峰逐漸消瘦;第二,隨著溫度的不斷升高,與C-O-C、C-O-Fe存在對應關系的對稱吸收峰和反對稱振動吸收峰,在1136 cm-1附近出現寬化成帶的情況,其主要原因在于經過熱處理后,α-Fe2O3與PF共軛鏈上原本的極性基團出現了較強的鍵和現象。強極性基團C=O、C-O-Fe使得π電子容易出現離域流動的情況,對于光電荷的分離具有十分重要的作用,因此能夠有效的提升光催化活性;第三,在700~400 cm-1附近出現有α-Fe2O3的特征吸收,隨著熱處理溫度的不斷增加,對應于C=C、C-O-Fe、C=O以及C-O-C的吸收峰在吸收強度方面出現了明顯的弱化,有的甚至直接消失。
相關的結果表明:在經過適當的熱處理后,能夠有效地保證有機與無機相之間的聚合,提升高分子材料PF的共軛程度,使其逐漸變化為大共軛鏈高分子。
3.2 XPS分析
通過圖2可以看出,在樣品P-4當中,含有鐵、氧、碳、硫等元素,其中,硫元素主要是由催化劑H2SO4產生,主要出現在170和235 eV處。從譜峰看,714譜峰與Fe2p3/2能譜對應,730與Fe2p1/2對應,288與C1s對應,535 eV與O1s對應。
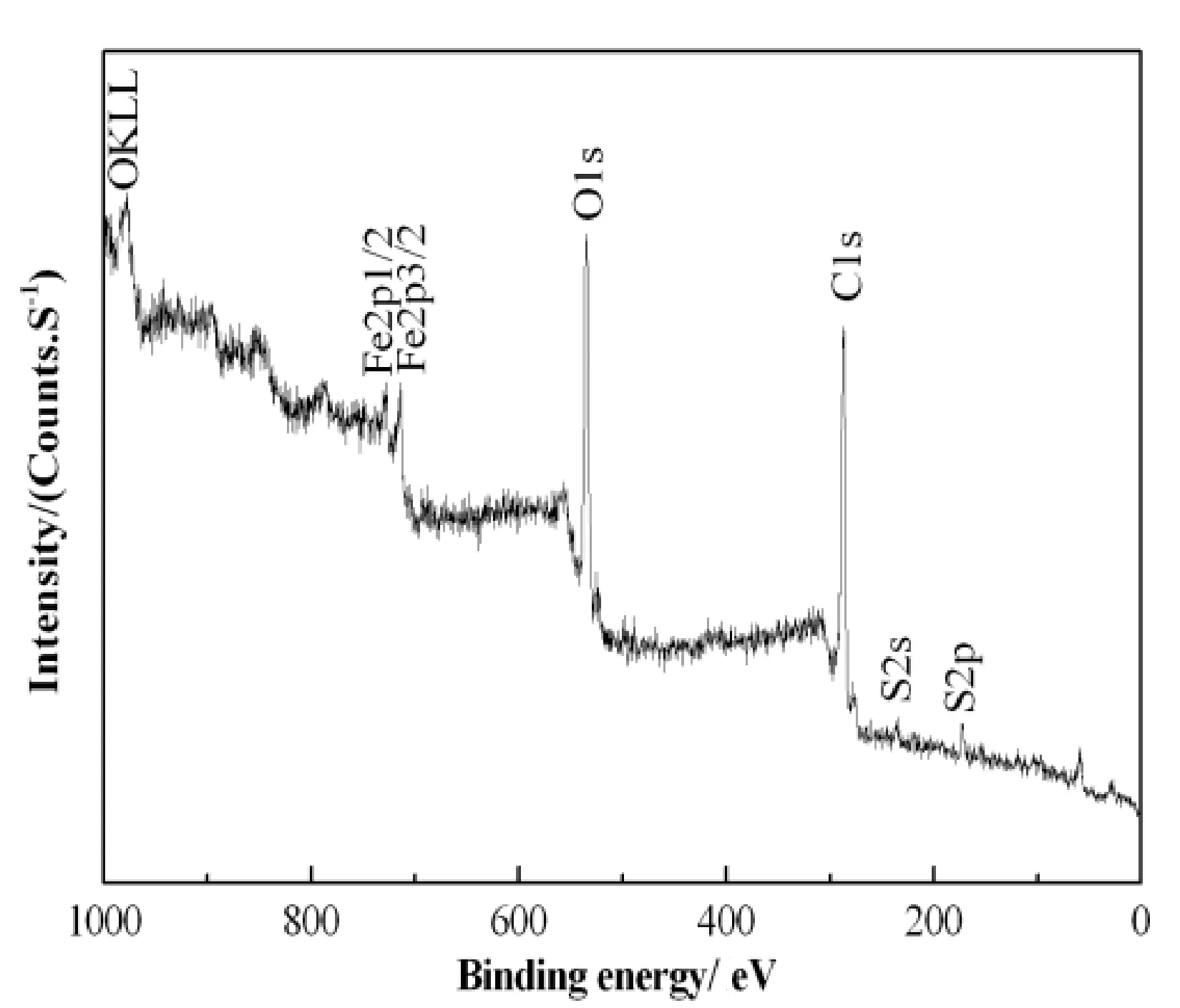
圖2 樣品p-4的XPS總譜
通過圖3即可以看出,C1s在經過一定程度的擬合后,會得到3個峰,分別位于284(對應高分子鏈中的C=C)、286(對應高分子鏈中的C-O)、287eV(對應高分子鏈中的C=O)處。通過圖4可以看出,C1s在經過一定程度的擬合后,會得到5個峰,分別位于283(對應高分子鏈中的C-Fe)、284(對飲高分子鏈中的C=C)、286(對應高分子鏈中的C-O)、287(對應高分鏈中的C=O)、289eV(對應高分鏈中的O-C=O)處。其中,結合C=C的強度可以判斷高分子PF的不飽和度較強,而且樣品p-4中PF含有O-C=O和C=O、C-O。由于這些不對稱電子結構的存在,使得催化劑的極性得到顯著的增強,從而能夠保證電子與空穴分離,提升活性。
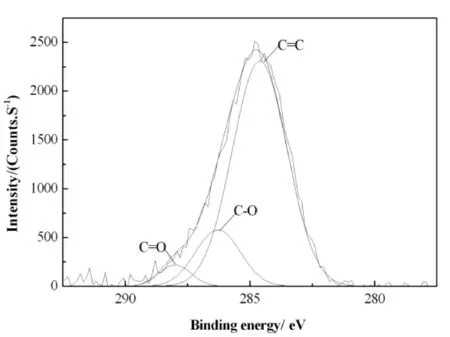
圖3 前驅物的XPS譜圖C1s擬合曲線

圖4 樣品p-4XPS譜圖C1s擬合曲線
4 光催化實驗
通過前期的研究,本課題組發現隨著熱處理溫度的不斷升高,復合材料的相關催化活性出現了先增加后降低的情況。在經過360 ℃、30 min的熱處理后,樣品活性最高。圖5主要描述的是在上述最佳條件下制備的具有不同α-Fe2O3含量的復合催化材料與純α-Fe2O3催化活性的時間變化曲線。通過圖5可以看出:與純α-Fe2O3相比,復合催化材料的催化性能得到顯著提升,樣品p-4穩定性和活性最好,當α-Fe2O3含量為45.26 %時,對應α-Fe2O3/PF復合催化劑的催化性能、穩定性能最好,在自然光和室溫條件下,80 min就可使MB的脫色率達到100%,反復3次實驗對于MB的脫色率仍然可以達到75%以上。而純的α-Fe2O3納米粒子在同等條件下,對MB的脫色降解僅達不到10 %。說明α-Fe2O3、PF之間量的關系能夠對復合催化劑的催化活性帶來一定的影響。其主要原因在于:α-Fe2O3含量較低的情況下,會導致催化劑的活性中心減少,此時,大量的PF會在α-Fe2O3表面形成包裹,影響MB與催化劑的接觸。α-Fe2O3含量較高的情況下,PF與α-Fe2O3無法充分鍵和,α-Fe2O3表面的PF較少,單位時間內無法大量注入給α-Fe2O3粒子電子,最終使得生成的電子-空穴減少,影響催化活性。自然光照射下MB溶液在催化反應前、后的UV-Vis譜圖證實[21]:反應后譜線與去離子水譜線一致,紫外光以及可見光區的吸收峰出現消失的情況,并且無新吸收峰出現,說明在反應液當中并不存在任何有機分子,這一催化過程,使得MB的整個分子結構和共軛發色體系受到破壞。
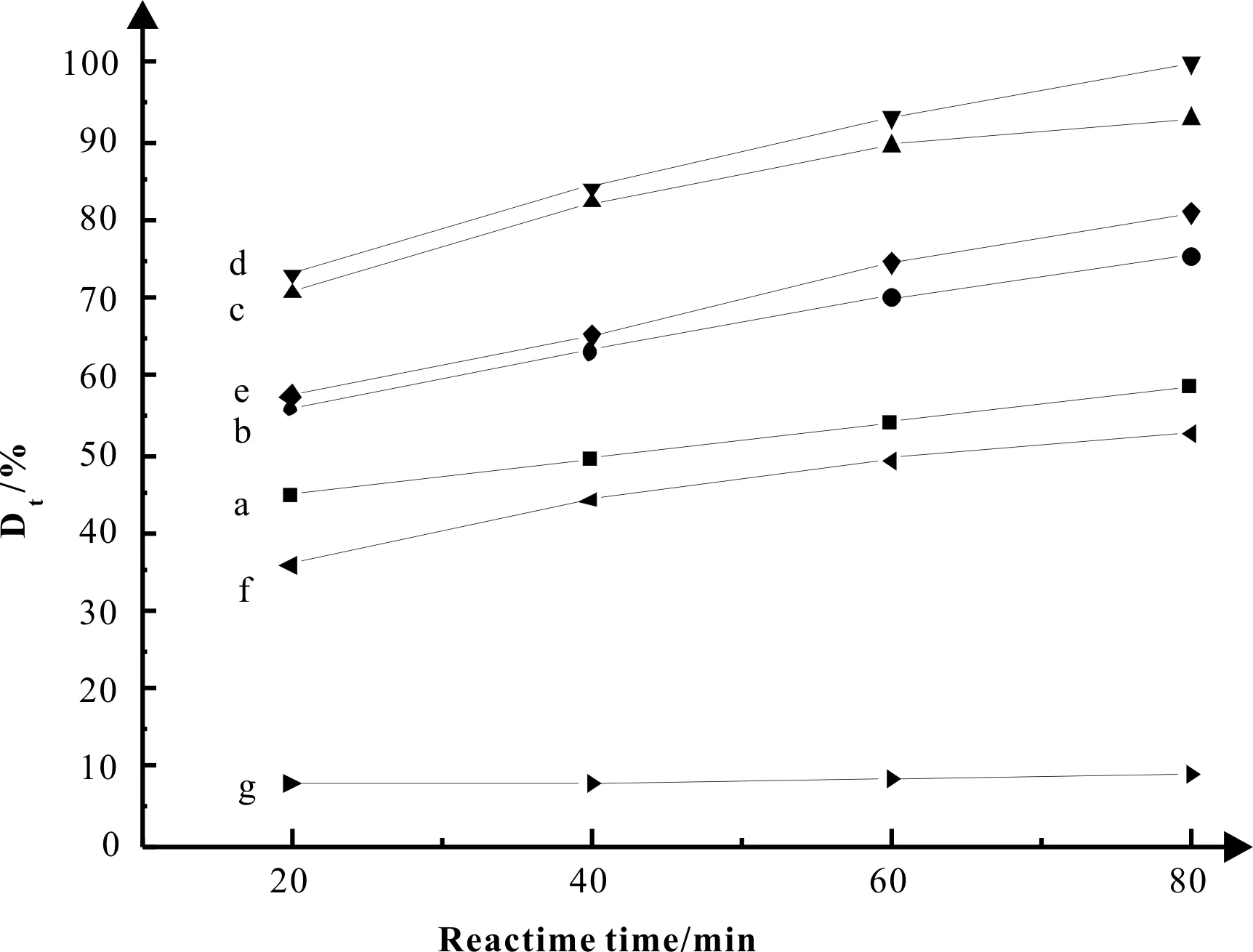
圖5 純α-Fe2O3與α-Fe2O3/PF催化活性對比
5 結論
采用兩步法,利用Fe(NO3)3.9H2O和糠醇(F)制備復合催化材料,可以獲得納米級的具有較強相互作用的α-Fe2O3/PF。本課題的相關研究顯示,PF可以有效地拓寬α-Fe2O3的光譜響應范圍,同時降低光生電子-空穴對的復合,對于光能利用率的提升具有重要意義。同時,也保證了這一復合材料可以在自然光的作用下,發揮其催化性能。和純α-Fe2O3相比,性能好,容易分離且效率高,無污染,在未來的發展中,具有廣闊的前景。

