東北林蛙皮糖胺聚糖分析及其體外免疫活性
于 奇鄭冉張怡李波劉達 李宜平 焦麗麗
(1.長春中醫藥大學藥學院, 吉林 長春130117; 2.長春中醫藥大學吉林省人參科學研究院, 吉林 長春130117)
東北林蛙Rana dybowskiiGuenther 為蛙科林蛙屬兩棲動物,俗稱“哈士蟆”[1],廣泛分布于黑龍江、吉林、遼寧、內蒙古等地區,主產于長白山區域,是我國著名的藥食兩用藥材[2]。東北蛙皮中具有一定量的糖胺聚糖,在抗氧化[3]、抗凝血[4]、抗腫瘤[5]及免疫調節[6]方面呈現出較強的生物活性。近年來,許多國內外學者對林蛙皮多糖的研究主要集中在提取、分離純化及抗氧化[7?9]活性等方面,但對其結構特征仍不清楚。基于此,本研究以東北林蛙皮為原料,采用水提醇沉法分離純化得到林蛙皮多糖DGP 和DGPA,初步分析兩者基礎結構,并對其體外免疫活性進行研究,以期為進一步研究該成分結構及構效關系奠定基礎。
1 材料
1.1 試劑、藥物與動物 東北林蛙皮采自吉林省舒蘭市上營森林經營局桃園林場(東經127°25′36.18",北緯44°09′41.7",海拔338 m),經長春中醫藥大學李宜平教授鑒定為東北林蛙Rana dybowskiiGuenther 的干燥皮膚。8~10周齡ICR 雄性小鼠,體質量(20.0±2.0)g,購自長春市億斯實驗動物技術有限責任公司,實驗動物生產許可證號SCXK(遼)2020?0001,在相對濕度40%~60%,溫度22~25 ℃的無菌動物房中適應性喂養1 周。研究獲長春中醫藥大學倫理委員會批準,實驗操作嚴格執行國際動物實驗方針。SepharoseTMCL?6B 凝膠柱購自美國GE Healthcare 公司。標準分子量葡聚糖、單糖對照品購自上海源葉生物科技有限公司;考馬斯亮藍試劑盒購自南京建成生物工程研究所;1640 培養基購自美國Gibco 公司;新生牛血清購自浙江天杭生物科技股份有限公司;脂多糖(LPS)、半刀豆蛋白(ConA)、青霉素、鏈霉素、二甲基亞砜、MTT 均購自美國Sigma 公司。無水乙醇、氫氧化鈉、三氟乙酸、三氯甲烷、正丁醇、氨基磺酸、鹽酸、苯酚、硫酸等試劑均購自國藥集團化學試劑有限公司。
1.2 儀器 Model 680 型酶標儀購自美國Bio?Rad 公司;真空干燥箱購自上海精宏實驗設備有限公司;恒溫磁力攪拌器購自杭州儀表電機有限公司;離心機購自美國Sigma 公司;循環水式真空泵購自鄭州長城科工貿有限公司;二氧化碳培養箱購自日本Sanyo 公司;UV?8000 型紫外分光光度計購自上海元析儀器有限公司;傅里葉紅外光譜儀購自美國Thermo Fisher Scientific 公司。
2 方法
2.1 多糖制備 林蛙皮經水提[10]、醇沉后得粗多糖DGP,采用Sevage 法[7]脫蛋白后進一步用Sepharose CL?6B 瓊脂糖凝膠柱層析,得純化后多糖DGPA。
2.2 多糖理化性質分析 采用考馬斯亮藍法、間羥基聯苯法對DGP、DGPA 總蛋白及糖醛酸水平進行檢測。
2.3 多糖分子量測定 參考文獻[6] 報道,色譜條件為TSKgel G3000 PWXL 色譜柱(7.8 mm×30.0 cm,5 μm);流動相超純水;體積流量0.5 mL/min;柱溫40 ℃;進樣量20 μL。采用視差折射檢測器,用流動相配制不同分子量對照品溶液,多糖配制為10 mg/mL 溶液,0.22 μm 微孔濾膜過濾。
2.4 多糖傅里葉變換紅外光譜分析 2~3 mg 多糖與適量KBr 混合研細后壓片,在4 000~500 cm-1波數范圍內進行紅外光譜掃描。
2.5 單糖組成分析 多糖經三氟乙酸(TFA)水解后進行PMP 衍生。參考文獻[11] 報道,色譜條件為C18Thermo hyperil ODS?2 色譜柱(4.6 mm×25 cm,5 μm);流動相17%乙腈?83% PBS;體積流量1 mL/min;柱溫25 ℃;進樣量20 μL;檢測波長245 nm。
2.6 體外免疫活性檢測
2.6.1 多糖對小鼠淋巴細胞增殖轉化的影響 小鼠脫頸處死,無菌條件下解剖并取出脾臟,研磨制成脾細胞懸液,1 500 r/min離心5 min,棄上清,Tris?NH4Cl 低滲液裂解紅細胞,離心,D?Hanks 緩沖液洗滌,培養液將細胞密度稀釋至1×106/mL,制成單細胞懸液[12],加入細胞培養板中,每孔100 μL,隨機分為空白 組、ConA 組(5 μg/mL ConA)、LPS 組(10 μg/mL LPS)、DGP 組(50、100、200、400 μg/mL 多糖溶 液)、DGPA 組(50、100、200、400 μg/mL 糖胺聚糖溶液)、陽性對照組(5 μg/mL ConA或10 μg/mL LPS),培養液補至200 μL,混勻,重復3孔,在5% CO2、37 ℃條件下培養44 h后,每孔加入20 μL MTT(5 mg/mL),繼續培養4 h,棄上清,加入150 μL 二甲基亞砜,于570 nm 波長處測定吸光度。
2.6.2 多糖對腹腔巨噬細胞的影響 小鼠腹腔注射6%可溶性淀粉2 mL,3 d 后處死,10 mL D?Hanks 緩沖液清洗腹腔,收集液體,4 ℃離心后棄上清,1640 完全培養基重懸細胞,調整細胞密度為2×106/mL,取100 μL 接種至96 孔板,在5% CO2、37 ℃下預孵3 h,PBS 清洗2~3次,除去貼壁細胞,制得純化巨噬細胞。
2.6.2.1 多糖對腹腔巨噬細胞吞噬功能的影響 將純化后的巨噬細胞加到待測糖樣(200 μL/孔)中,繼續培養24 h后吸棄上清,每孔加入100 μL 0.075%中性紅溶液繼續培養1 h,pH 7.4 PBS 洗去剩余中性紅后,加入100 μL 細胞裂解液,24 h 后采用酶標儀于550 nm 波長處檢測吸光度。
2.6.2.2 多糖對腹腔巨噬細胞NO 水平的影響 配制6 個不同濃度的NaNO2溶液,分別加到96 孔板中,加入等體積Griess 試劑,10 min 后于540 nm 波長處檢測吸光度,繪制標準曲線。細胞以2×106/mL 密度接種至24 孔板,加入多糖培養24 h,吸取細胞培養液上清100 μL 加到另一培養板中,加入等體積Griess 試劑,10 min 后在540 nm 波長處測定吸光度,根據標準曲線計算NO 水平。
2.6.2.3 TNF?α 水平檢測 腹腔巨噬細胞與多糖一起培養,取上清液,采用ELISA 試劑盒檢測細胞上清TNF?α水平。
2.7 統計學分析 通過SPSS 23.0 軟件進行處理,結果以()表示,組間比較采用單因素方差分析,兩兩比較采用t檢驗。P<0.05 表示差異具有統計學意義。
3 結果
3.1 糖胺聚糖柱層析純化 圖1 顯示,DGP 過SepharoseTMCL?6B 柱后得到單一、對稱的洗脫峰,收集相應多糖洗脫液,即為糖胺聚糖DGPA。
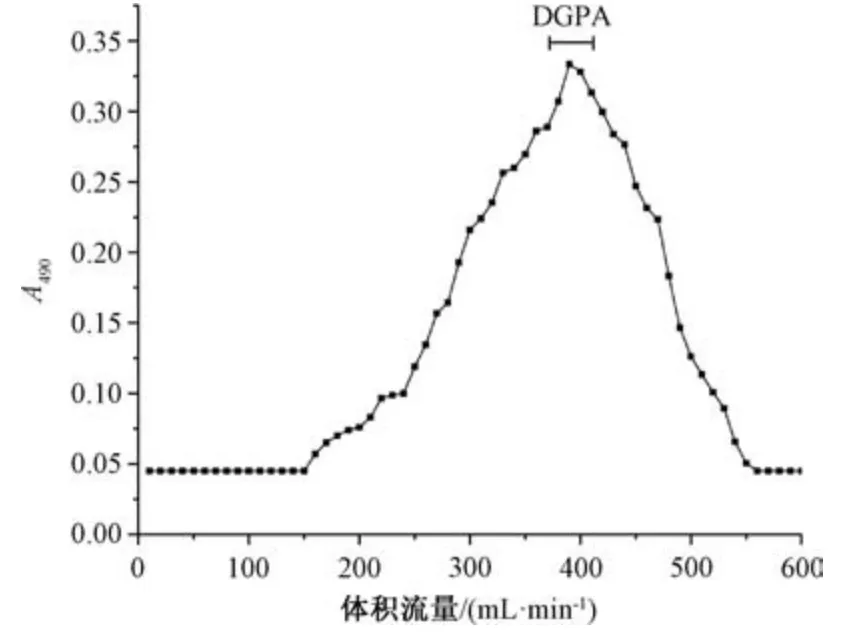
圖1 糖胺聚糖DGPA SepharoseTMCL?6B 柱層析
3.2 多糖理化性質 DGP、DGPA 總蛋白質量分數分別為19.93%、6.24%。采用間羥基聯苯法,以D?半乳糖醛酸含量為橫坐標(X),吸光度為縱坐標(A)進行回歸,得方程為A=0.010 7X+0.059 2(R2=0.998 3),DGP、DGPA糖醛酸質量分數分別為14.5%、18.6%。DGPA 經高效凝膠滲透色譜法分析,以保留時間為橫坐標(X),標準分子量為縱坐標(Y)進行回歸,得方程為Y=-0.354 1X+9.392 7(R2=0.996 7),測得DGPA 分子量為141 kDa。
3.3 單糖組成 圖2~3 顯示,DGP、DGPA 單糖組成相同,均由甘露糖、葡萄糖醛酸、葡萄糖、氨基半乳糖、半乳糖組成,前者摩爾比為0.30∶2.05∶0.17∶1∶0.23,以葡萄糖醛酸、氨基半乳糖為主,表達為81.3%;后者摩爾比為0.41∶2.67∶0.16∶1∶0.25,以糖醛酸為主,表達為59.4%。
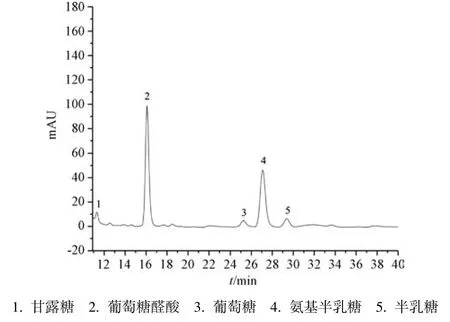
圖2 DGP 單糖HPLC 色譜圖
3.4 多糖紅外光譜分析 圖4 顯示,3 370.38 cm-1左右的吸收峰為糖類?OH 的特征吸收峰,2 936.27 cm-1處的吸收峰為C?H 鍵強伸縮振動,1 653.10、1 544.57 cm-1左右的吸收峰說明有乙酰氨基(?NH2COCH3)存在,1 408.12 cm-1處的吸收峰為?COO-的特征吸收峰。綜上所述,?OH、?C?H鏈、?NH2COCH3、?COO 是糖的特征基團,故DGPA 為糖胺聚糖。

圖3 DGPA 單糖HPLC 色譜圖
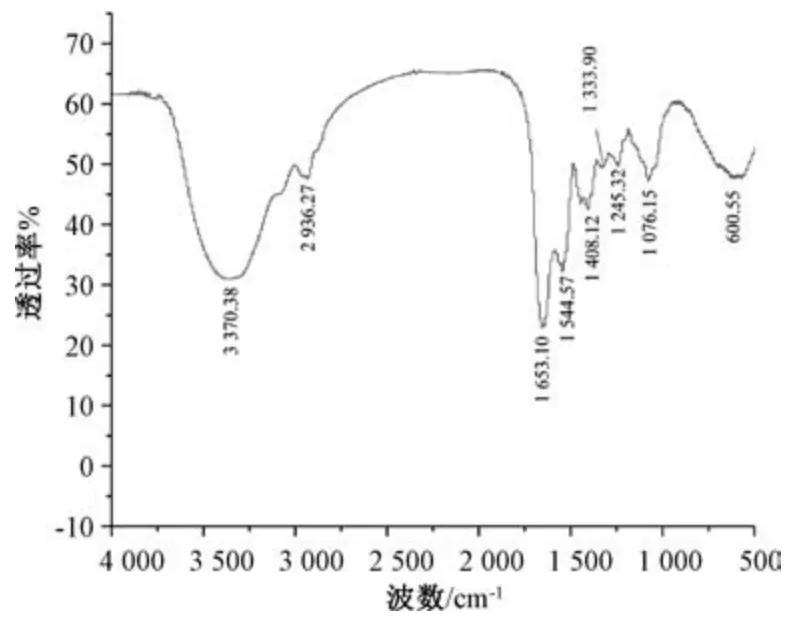
圖4 DGPA 紅外光譜圖
3.5 多糖對小鼠脾淋巴細胞增殖的影響 圖5 顯示,與空白組比較,DGP 組、DGPA 組小鼠淋巴細胞增殖能力增強(P<0.05,P<0.01),并均呈劑量依賴性;與DGP 組比較,DGPA 組小鼠淋巴細胞增殖能力增強(P<0.05,P<0.01)。圖6~7 顯示,在50~400 μg/mL 質量濃度范圍內,DGP組、DGPA 組協同ConA 作用小鼠脾淋巴細胞時,細胞增殖能力高于ConA 組(P<0.01),表明兩者均能促進誘導ConA 誘導的T 淋巴細胞增殖,并呈劑量依賴性,在400 μg/mL時作用最強,為空白組的3~4 倍;在50~100 μg/mL質量濃度范圍內,DGP 組、DGPA 組協同LPS作用于小鼠脾淋巴細胞時,細胞增殖能力低于LPS 組(P<0.05),表明兩者均能抑制LPS 誘導B 淋巴細胞增殖;在200~400 μg/mL 質量濃度范圍內,細胞增殖能力高于LPS組(P<0.01),表明兩者促進LPS 誘導B 淋巴細胞增殖,并且在相同質量濃度下DGPA 組作用更優。

圖5 多糖對小鼠脾淋巴細胞增殖的影響(,n=10)

圖6 多糖對ConA 誘導小鼠脾淋巴細胞增殖的影響(,n=10)
3.6 多糖對小鼠腹腔巨噬細胞吞噬功能的影響 巨噬細胞的主要功能是吞噬病原體等異物[13]。圖8 顯示,與空白組比較,DGPA 組小鼠巨噬細胞吞噬功能增強(P<0.05,P<0.01),并呈劑量依賴性;當質量濃度為400 μg/mL時,DGP 組、DGPA 組均能增強小鼠巨噬細胞吞噬功能,效果分別為空白組的1.25、2 倍。
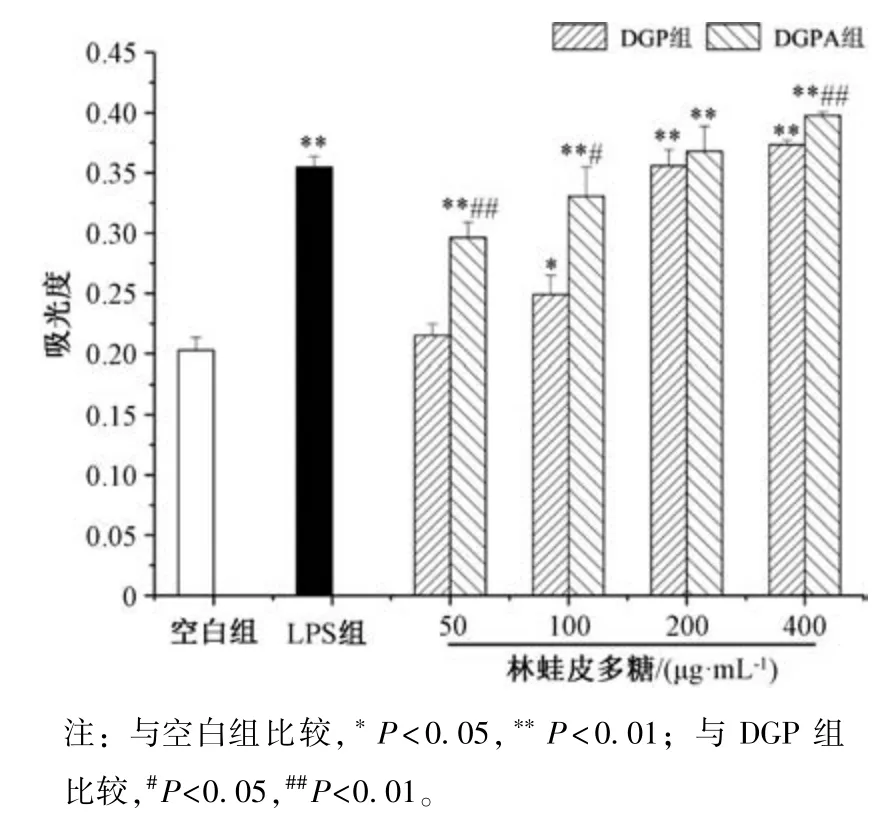
圖7 多糖對LPS 誘導小鼠脾淋巴細胞增殖的影響(,n=10)
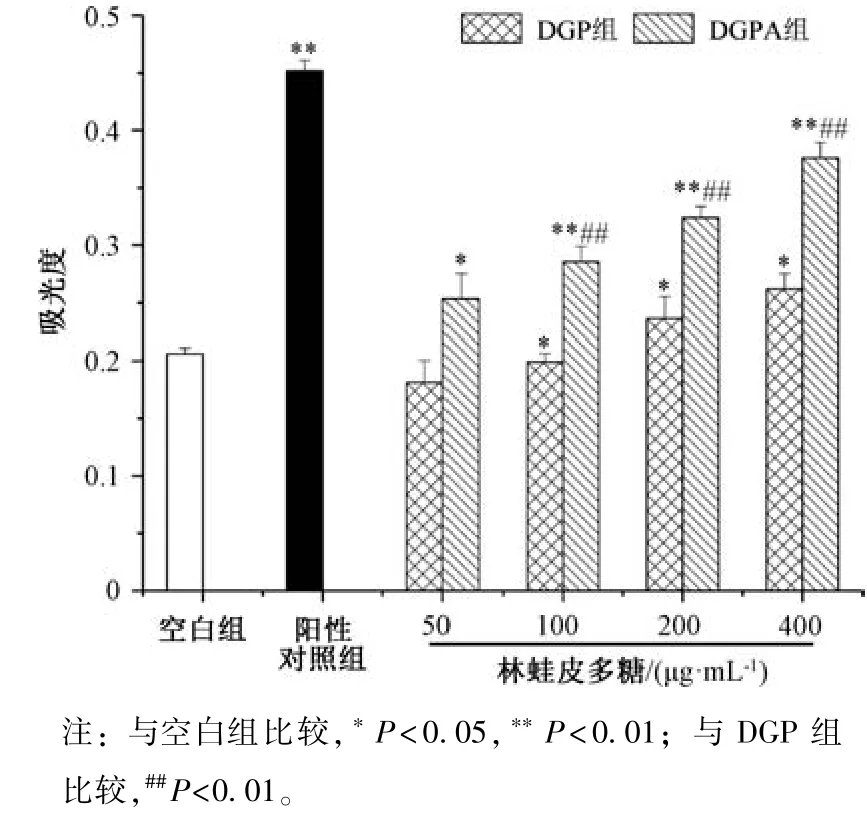
圖8 多糖對小鼠腹腔巨噬細胞吞噬功能的影響(,n=10)
3.7 多糖對小鼠腹腔巨噬細胞NO 水平的影響 圖9 顯示,與空白組比較,DGPA 組小鼠巨噬細胞NO 水平升高(P<0.05,P<0.01),并呈劑量依賴性;當質量濃度為400 μg/mL時,DGP 組、DGPA 組均能增強小鼠巨噬細胞產生NO 的能力,效果分別為空白組的3、5 倍。

圖9 多糖對小鼠腹腔巨噬細胞NO 水平的影響(,n=10)
3.8 多糖對小鼠巨噬細胞TNF?α 水平的影響 圖10 顯示,在100~400 μg/mL 質量濃度范圍內,DGPA 組能增強小鼠巨噬細胞分泌細胞因子TNF?α 能力(P<0.05,P<0.01),并呈劑量依賴性;當質量濃度大于100 μg/mL時,DGPA組增強小鼠巨噬細胞分泌TNF?α 的能力大于DGP 組(P<0.05)。

圖10 多糖對小鼠腹腔巨噬細胞TNF?α 水平的影響(,n=10)
4 討論
通過對分子量、單糖組成、特殊基團的研究,確定了DGPA 為糖胺聚糖類化合物。已有研究表明,糖胺聚糖類化合物等具有顯著的免疫調節作用,其功能與結構密切相關[14],楊潔[15]發現仿刺參糖胺聚糖能促進DC 細胞的增殖和細胞因子IL?12、TNF?α 的分泌。多種糖胺聚糖,例如仿刺參糖胺聚糖[12]、菲律賓蛤仔糖胺聚糖[16]、珠貝母糖胺聚糖[17]、近江牡蠣糖胺聚糖[14]等均被證明具有顯著的有免疫活性。本研究發現,林蛙皮糖胺聚糖具有顯著的免疫調節作用,且純化后的林蛙皮多糖DGPA 對淋巴細胞和巨噬細胞的激活作用明顯優于粗多糖DGP,而這2 種多糖的單糖組成存在一定差異,尤其是純化后多糖DGPA 的氨基半乳糖和葡萄糖醛酸的相對水平高于粗多糖DGP,而單糖組成是影響多糖活性的重要因素。因此,林蛙皮多糖DGPA 組與DGP 組的免疫活性差異可能與其單糖組成的差異有關,具體影響機制有待進一步研究。

