繼發于腦橋梗死的雙側橋臂華勒變性的臨床分析
橋臂又稱小腦中腳位于第四腦室兩側,由腦橋小腦纖維束組成,連接小腦和腦橋基底部[1]。雙側橋臂對稱性病變臨床并不常見,隨著磁共振成像(magnetic resonance imaging,MRI)技術的廣泛應用,后顱窩病變檢出率大幅提高,逐漸可見雙側橋臂梗死、多系統萎縮、多發性硬化以及海洛因相關腦病等報道[2-3]。部分腦橋梗死患者發病數周或數月后顱腦MRI可出現與神經功能缺損癥狀或體征不相符的雙側橋臂異常信號,查閱文獻可見國外散發的個案報道,描述該現象為華勒變性(Wallerian degeneration,WD)[4-5]。WD是指近端神經細胞胞體或軸突損傷后營養支持中斷,遠端軸突順性解體、進行性脫髓鞘的過程,是典型事件損傷神經纖維后繼發的一系列反應,而非原發、獨立的病變[6]。目前,國內對WD的臨床特點、病因及機制等認識略有不足,臨床與放射線科醫師容易將其誤診為急性腦梗死,給予過度的干預和治療[7]。因此,本研究回顧性分析我院收治的8例急性腦橋梗死后出現雙側橋臂異常信號患者的臨床資料,總結此類患者的臨床表現和影像學特點,進一步分析出現該影像學表現的原因與可能機制。
1 材料與方法
1.1 臨床資料
回顧性連續納入2017年6月至2019年4月中國醫科大學附屬第一醫院神經內科收治的8例急性腦橋梗死后雙側橋臂出現異常信號患者的臨床資料。其中,男6例,女2例;發病年齡49~69歲,平均發病年齡(58±7)歲。納入標準:(1)初始急性腦橋梗死診斷符合《中國急性缺血性腦卒中診治指南 2018》[8];(2)年齡>18歲;(3)急性發病,主要表現為局灶性神經功能缺損癥狀與體征(偏癱、眩暈、言語障礙、單側肢體麻木或無力等)或全面性神經功能缺損,且癥狀與體征持續>24 h;(4)初始影像學可見與癥狀或體征一致的孤立的腦橋責任病灶,隨后影像學可見雙側橋臂異常信號。排除標準:(1)缺乏彌散加權成像(diffusion-weighted images,DWI)資料;(2)短暫性腦缺血發作(transient ischemic attack,TIA)或腦出血;(3)伴有其他的原發性或繼發性顱腦病變。本研究獲得醫院倫理委員會批準。
1.2 研究方法
1.2.1 資料收集:詳細記錄患者的發病年齡、性別,血管病危險因素 [吸煙、高血壓、糖尿病、高脂血癥、心房顫動、冠狀動脈粥樣硬化性心臟病(coronary atherosclerotic heart disease,CAHD)、既往TIA或卒中病史、酗酒)],前后兩次病變的臨床癥狀與體征、MRI特點及時間間隔。
吸煙定義為目前正在吸煙的患者。高血壓定義為未使用降血壓藥的情況下,非同日3次測量血壓,收縮壓≥140 mmHg和(或)舒張壓≥90 mmHg或目前正在服用降壓藥物。糖尿病定義為典型糖尿病癥狀(煩渴、多飲、多尿、多食伴不明原因的體質量下降)加上隨機血糖≥11.1 mmol/L或空腹血糖≥7.0 mmol/L或葡萄糖負荷后2 h血糖≥11.1 mmol/L且經復查確認或目前正在服用降糖藥物者。高脂血癥定義為血清總膽固醇≥5.20 mmol/L或甘油三酯≥1.70 mmol/L或低密度脂蛋白膽固醇≥3.40 mmol/L或目前正在應用降脂藥物。心房顫動定義為心電圖顯示P波消失,f 波代之,頻率350~600次/min,QRS 波節律絕對不規則或既往確診心房顫動。CAHD定義存在心絞痛、心肌梗死或冠狀動脈重建史。酗酒定義為男性每日飲酒的酒精含量超過25 g,女性超過12.5 g。
1.2.2 MRI:采用德國西門子Trio 3.0 T MR掃描儀對所有患者進行矢狀位和軸位顱腦掃描。掃描序列包括T1加權成像(T1 weighted images,T1WI)、T2加權成像(T2 weighted images,T2WI)、液體衰減反轉恢復(fluid-attenuated inversion recovery,FLAIR)序列、DWI和表觀擴散系數(apparent diffusion coefficient,ADC)。
2 結果
2.1 一般資料
患者均存在血管病危險因素。其中,高血壓7例,吸煙3例,糖尿病2例,高脂血癥2例,CAHD 1例。首次發病,急性起病的臨床癥狀與體征包括偏癱7例、吞咽/構音障礙6例、眩暈4例、步態共濟失調2例。第2次發病時(時間間隔:3~25周),1例患者自覺偏癱較前加重,余7例患者初始癥狀減輕或消失,且未出現新發癥狀與體征,偏癱2例、構音障礙2例、步態共濟失調1例。2次病變時間間隔為3~25周,平均時間間隔(16±7)周,其中6例超過16周。見表1。

表1 8例腦橋梗死后雙側橋臂異常信號患者的臨床資料
2.2 影像學表現
患者初始病變部位均為腦橋基底部,MRI表現為長T1、長T2、高FLAIR信號影及DWI彌散受限信號。其中,左側病變3例,右側病變3例,雙側受累2例,而雙側橋臂未見異常信號(表2)。8例患者后期MRI均表現為雙側橋臂對稱性長T1、長T2、高FLAIR信號影(表2);其中5例患者出現DWI高信號,4例相應ADC為等、稍高或高信號影,1例未完善ADC圖,見圖1。
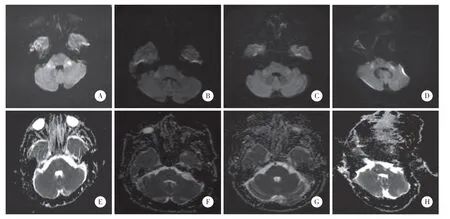
圖1 4例第2次顱腦DWI有雙側橋臂異常信號的患者影像

表2 8例患者前后兩次病變MRI成像特點
3 討論
本研究結果顯示,腦橋基底部梗死數周或數月后顱腦MRI可見雙側橋臂長T1、長T2、FLAIR高信號影,部分患者可出現DWI高信號;雖然出現雙側橋臂病變,但患者初始癥狀或體征多減輕或消失,且無新發癥狀與體征。這種臨床與影像學變化不相符,腦橋基底部梗死后出現雙側橋臂異常信號的現象是腦橋小腦束WD所致,與SHEN等[9]研究結果一致。目前,WD尚無明確的臨床診斷標準,研究[5,10]表明不同時期的組織和代謝特點與MRI各階段特征性變
化一致,有助于診斷。損傷后4周內該階段軸突和髓鞘分離,傳統MRI常無異常信號,DWI可出現一過性錐體束異常高信號[11];損傷后4~16周髓鞘蛋白快速降解、脂質成分保留,組織的疏水性增加,T2WI為低信號,但近14周T2WI亦可呈高信號;損傷16周后髓鞘幾乎完全消失,膠質細胞增生填充變性的軸突和髓鞘區,組織含水量增加,表現為T2WI、FLAIR和DWI高信號,ADC為低/等或高信號;損傷后數年腦干萎縮,異常信號可持續存在。本組患者2次就診時間間隔為3~25周,平均時間間隔為(16±7)周,其中6例超過16周。這可能與該時間段常出現運動障礙促使患者就診且MRI平掃即可發現明顯的雙側橋臂異常信號有關。
既往研究[12]表明,中樞神經系統WD最常累及存在大量軸突和重要神經功能的皮質脊髓束,而累及橋臂臨床十分罕見。橋臂主要是由連接腦橋基底部與小腦的腦橋小腦束組成,是腦橋小腦纖維束中最大、最主要的通路。腦橋小腦束起自對側腦橋核、接受對側皮質腦橋束,在腦橋上部交叉通過橋臂到達小腦皮質;故一側腦橋基底部梗死,既損害同側腦橋核及其發出的將要交叉到對側的軸突,又損害對側已交叉的腦橋小腦束[13]。這就是腦橋小腦束WD引起雙側橋臂異常信號的原因。
綜上所述,腦橋基底部梗死后出現雙側橋臂對稱性異常信號,臨床應考慮腦橋小腦束華勒變性的可能。MRI隨WD不同時期各序列信號變化多樣,最常出現雙側橋臂長T1、長T2和FLAIR高信號,部分患者可出現DWI高信號,需要結合病史、臨床癥狀和體征與腦梗死仔細鑒別,避免誤診。未來期待進一步大樣本、多中心研究以探索確切機制和特異性表現。

