利托君致肺水腫病例分析*
張姣,黃雅群,白嘎力,曹明雪,于芝穎,文睿婷,封宇飛
(1.北京大學人民醫院藥劑科,北京 100044;2.北京大學醫學部藥學院藥事管理與臨床藥學系,北京 100191)
早產指妊娠滿28周至不足37周間分娩,是圍生兒死亡和各種疾病高發的主要原因之一,延長妊娠對降低圍生兒的傷殘率和死亡率具有重要意義[1]。利托君作為高選擇性β2受體激動劑,是目前美國食品藥品管理局(FDA)唯一批準用于抗早產治療的宮縮抑制劑,但在抑制宮縮的同時,可導致母體心血管副作用,其中以肺水腫最為嚴重,不僅影響母體呼吸,還可引起胎兒宮內窒息[2]。本文通過報道北京大學人民醫院(以下簡稱“我院”)1例利托君致急性肺水腫病例,并結合國內外已報道的文獻進行綜合分析,為利托君的安全使用提供參考。
1 資料與方法
1.1病例資料與轉歸 患者,女,35歲,因“孕29+1周,發現血糖升高4周,陰道流液2 h”于2020年12月17日入院。既往多囊卵巢病史12年,無食物藥物過敏史。入院診斷:孕29+1周(G1P0,頭位)、胎膜早破、妊娠期糖尿病,給予地塞米松磷酸鈉注射液(國藥集團容生制藥有限公司,批號:2005203)5 mg,q12h,肌內注射促進胎兒肺成熟,硫酸鎂注射液(上海旭東海普藥業有限公司,批號:FB200407)靜脈滴注(負荷劑量4 g后,1 g·h-1維持劑量持續給藥)進行胎兒腦保護,克林霉素(宜昌人福藥業有限責任公司,批號:03N04031C2)0.9 g,q8h+氨曲南(山西仟源制藥有限公司,批號:20190102)1 g,q12h,靜脈滴注控制感染。12月18日20:00患者宮縮3~5 min一次,每次十余秒,有痛感,心率(heart rate,HR)72次·min-1,胎心146次·min-1。為延長保胎時間,在無明顯禁忌情況下,給予利托君注射液(信東生技股份有限公司,批號:2PR1620)持續靜脈滴注(100 mg溶于0.9%氯化鈉注射液500 mL)抑制宮縮,起始量15 mL·h-1,逐漸加量至45 mL·h-1,同時停用硫酸鎂。用藥后,患者腹部發緊感較前緩解。22:00患者自覺心慌,HR 115~120次·min-1,血氧飽和度(SpO2)97%~98%,逐漸下調利托君給藥速度至15 mL·h-1維持。2020年12月19日1:00患者訴咳嗽,無咳痰,偶有腹部發緊感,HR約110次·min-1,與患者溝通訴心悸可耐受。6:50患者心悸、咳嗽加重,HR 110次·min-1,停用利托君,予硫酸鎂注射液1 g·h-1繼續胎兒腦保護。8:00患者自訴咳嗽明顯,間斷有羊水流出。體檢:HR 93次·min-1,血壓(BP)99/60 mmHg(1 mmHg=0.133 kPa),呼吸頻率(RR)28次·min-1,SpO2(未吸氧)90%,(吸氧后,氧流量6 L·min-1)91%~94%;心肺聽診:雙肺呼吸音粗,雙肺底散在濕啰音;內診:宮頸消平,宮口開全,胎先露頭,S+2,羊水清。胎心監護基線160次·min-1,變異好。考慮肺水腫可能,予以呋塞米注射液20 mg靜脈注射,決定盡快陰道分娩終止妊娠。8:45患者煩躁,呼吸困難,胸悶憋氣,出現端坐呼吸,HR 100~120次·min-1,BP 110~130/80~90 mmHg,RR 30~40次·min-1,SpO2(氧流量6 L·min-1)90%~94%。宮縮強度較弱,胎心162次·min-1,微小變異。動脈血氣回報:pH值7.42,氧分壓10.52 kPa,二氧化碳分壓3.09 kPa,乳酸3.7 mmol·L-1,氧合指數262.7 mmHg。考慮患者出現急性肺水腫、心功能不全,立即提高氧流量至10 L·min-1,先后給予呋塞米注射液20,40 mg,去乙酰毛花苷0.2 mg靜脈注射,嗎啡5 mg皮下注射。9:04以會陰側切+產鉗助產娩出一早產女活嬰,重1460 g,Apgar評分:1 min評分3分(呼吸、心率、膚色各1分),5 min評分8分(肌張力、呼吸各-1分)、10 min評分10分,臍動脈血氣pH值7.27,診斷為新生兒窒息(重度)、新生兒呼吸窘迫綜合征,轉新生兒重癥監護室(neonatal intensive care unit,NICU)進一步治療。胎兒娩出后予產婦氣管插管正壓通氣,轉至ICU予呼吸機輔助通氣、鎮痛鎮靜、維持循環及水電解質平衡等對癥支持治療,此后患者情況逐漸好轉,HR和RR逐漸降低,血壓趨于穩定,血管活性藥物逐漸減停。2020年12月22日患者一般情況可,HR 64次·min-1,BP 149/78 mmHg,RR 12次·min-1,SpO299%,動脈血氣分析:pH值7.46,氧分壓16.81 kPa,二氧化碳分壓4.68 kPa,乳酸0.8 mmol·L-1,氧合指數42.0 kPa,給予脫機拔管,鼻導管吸氧;2020年12月23日轉回產科病房繼續治療,于2020年12月31日出院。新生兒于NICU經予無創呼吸機輔助通氣、抗感染、靜脈營養支持等治療后恢復良好,體質量穩步增長,2021年1月13日轉為鼻導管吸氧,2021年1月24日撤離呼吸支持,2021年1月28日出院。
1.2藥物不良反應因果關系 根據我國藥品不良反應關聯性評價方法,該患者肺水腫的發生與利托君關聯性評價如下:①時間關聯性:患者使用利托君2 h后出現心率加快,12.5 h后出現肺水腫體征,用藥與不良反應出現存在密切時間關系;②是否符合該藥已知不良反應類型:肺水腫符合該藥說明書中已知的嚴重不良反應類型,且國內外文獻均有類似報道;③停藥或減量后不良反應是否消失或減輕:患者停藥經緊急分娩和對癥治療后肺水腫癥狀明顯好轉;④再次使用可疑藥品是否再次出現同樣反應:患者癥狀緩解后未再次使用該藥;⑤反應是否可用合并用藥、病情進展或其他治療措施解釋:患者既往無心肺疾病史,不能以原發疾病解釋。因此,判定該病例利托君致肺水腫關聯性等級為“很可能”,同時采用諾氏評估量表進行評分為5分,結果為“很可能”。
1.3文獻檢索 以“ritodrine”或“β adrenergic agonist”“pulmonary edema”“adverse drug reaction”為英文檢索詞,以“利托君”或“安寶”“肺水腫”“不良反應”為中文檢索詞,檢索PubMed、中國知網、萬方、維普等數據庫自建庫至2021年12月發表的利托君致肺水腫相關文獻。文獻納入標準:①病例報告;②數據資料完整;③不良反應關聯性評價為“可能”相關以上。排除標準:①學位論文等非公開發表文獻;②綜述、重復發表的文獻;③無法明確肺水腫與利托君相關性。采用回顧性研究方法,詳細閱讀病例資料,提取相關信息進行統計分析。
2 結果
2.1文獻收集及患者一般資料 共得到符合納入條件的文獻19篇,其中英文文獻13篇,中文文獻6篇;涉及病例24例,加上本院報告的1例合計25例。年齡18~46歲[3-4];入院時孕周23~35周;單胎妊娠16例,多胎妊娠6例(雙胎4例,三胎1例[5],五胎1例[6]),其余3例胎數不詳。患者具體資料見表1。

表1 患者一般資料 Tab.1 Clinical characteristics of patients
2.2既往史 25例患者中,除1例有急性重度哮喘和發作性血管性水腫病史,并于孕期規律使用抗哮喘藥物治療[7],1例有漏斗胸、蛋白尿外,其余孕前均無心肺基礎疾病、高血壓、糖尿病等。
2.3給藥方案與合并用藥 利托君給藥方式包括持續靜脈滴注(18例),口服(2例)及持續靜脈滴注聯合口服(4例),1例給藥方式不詳。靜脈給藥的22例患者中,利托君劑量多從0.05 mg·min-1開始,逐步調整直至宮縮被有效抑制,維持劑量多為0.2 mg·min-1[8-10],最大為0.333 mg·min-1[7],未超出說明書規定范圍(0.15~0.35 mg·min-1)。利托君輸注溶媒包括0.9%氯化鈉注射液(4例),5%葡萄糖注射液(1例)及葡萄糖氯化鈉注射液(1例),其余不詳。單純口服給藥的2例患者中,1例為10 mg,q2h,規律給藥[11];另1例按5 mg,tid,服用5個月后,因宮縮加劇加量至10 mg,q6h、10 mg,q3h,但均在說明書推薦的日劑量范圍(80~120 mg·d-1)[5]。具體給藥方式和劑量見表2。

表2 利托君給藥方式及劑量分布 Tab.2 Route of administration and dosing reginen of ritodrine
共9例(36.00%)患者使用利托君單藥抗早產治療;9例聯用硫酸鎂抗宮縮或胎兒腦保護,其中6例為兩藥同時靜脈滴注,3例為非同時使用;13例聯用糖皮質激素促進胎兒肺成熟(倍他米松7例,地塞米松6例)。
2.4肺水腫發生時間 20例患者肺水腫發生在產前,5例發生在產后(4例剖宮產術后、1例陰道分娩后),具體時間因利托君給藥方式和劑量不同而有所差異:22例靜脈給藥者(含靜脈+口服聯合給藥)肺水腫均發生在開始給藥后96 h內,最早為給藥后2 h;單純口服給藥者,1例于服藥后約3 h出現肺水腫癥狀[11],另1例長期服藥者,在利托君末次調量后約36 h出現呼吸窘迫等癥狀[5]。肺水腫發生的時間見表3。
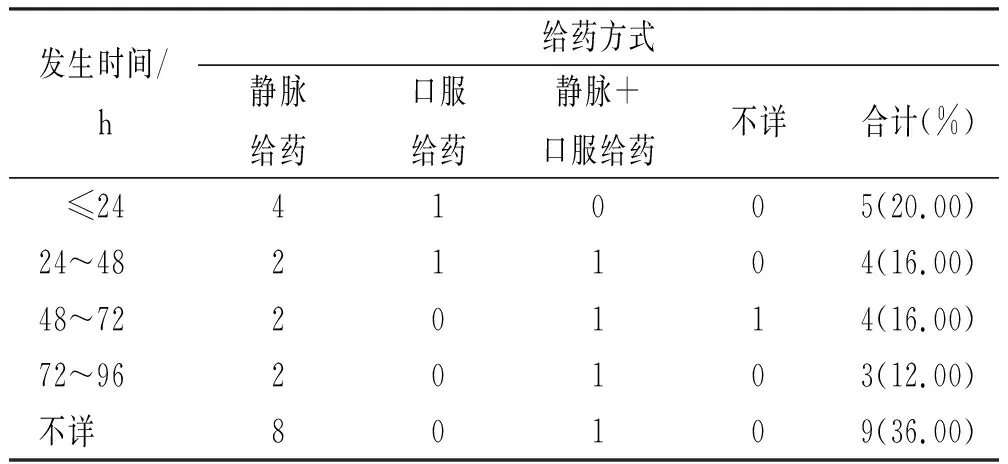
表3 利托君所致肺水腫的發生時間 Tab.3 Occurrence time of ritodrine-induced pulmonary edema例
2.5治療措施及轉歸情況 發生肺水腫后,所有患者均立即減量或停用利托君,并視情況進行呼吸支持、抗心力衰竭等搶救治療。1例孕婦經積極治療后因心臟驟停死亡[12],其余24例均癥狀緩解。肺水腫發生在產前的20例患者中,除上述1例死亡,12例行剖宮產術,4例緊急陰道分娩,3例經治療成功后,繼續保胎;肺水腫發生在產后的5例患者,經治療后均順利出院。
治療與轉歸明確的29例圍生兒中,3例死亡,其中1例因母親心臟驟停而胎死宮內[12],1例因暴露胎糞污染羊水宮內死亡[7],1例為雙胞胎之一,出生后1周死亡[9]。存活的26例新生兒中,5例出生時存在不同程度的窒息,其中4例1 min Apgar評分<5分,1例為7分,經呼吸支持及對癥治療后順利出院。
3 討論
3.1利托君致肺水腫的臨床特點 本研究統計顯示,利托君所致肺水腫在18~46歲不同年齡段、單胎和多胎妊娠的孕產婦中均可出現,多數患者既往無心肺基礎疾病。肺水腫的發生多見于利托君靜脈給藥,在常規劑量時即可發生,癥狀多出現在給藥后96 h內。利托君所致肺水腫進展迅速,危險程度高,對母體和胎兒均構成生命威脅,亟需警惕。
3.2利托君致肺水腫的發生機制 利托君通過選擇性激動子宮平滑肌細胞膜上的β2受體,激活腺苷酸環化酶,使細胞內環磷酸腺苷(cAMP)水平升高,抑制鈣離子釋放,從而抑制子宮收縮。研究顯示,利托君治療早產的病例中有3%~9%可出現肺水腫[13],其機制尚未完全明確,可能是多因素綜合作用的結果,其中液體負荷過量最為重要[9]。在利托君使用前2 h內,尿液和電解質排泄減少,尿滲透壓升高,同時抗利尿激素和腎素水平升高,腎小球濾過率下降,導致水鈉潴留。這些變化在2 d后達到高峰,表現為血紅蛋白和紅細胞比容的降低及體質量增加,恢復到基線值至少需要5 d[14-15]。因此,大多數病例肺水腫發生在抗宮縮治療早期。靜脈滴注較口服給藥更易加重液體負荷,且利托君片劑口服生物利用度低,靜脈給藥血藥濃度升高更快,故本文調研病例以靜脈給藥居多(88.00%)。另由于利托君對心臟β1受體有輕微激動作用[16],孕婦心率長時間加快,舒張期充盈時間減少,也可能造成心功能不全,誘發心源性肺水腫[15]。此外,利托君致肺水腫存在多方面協同因素,如多胎妊娠,靜脈輸注溶媒的選擇、聯合藥物治療等。
妊娠時循環血量增加35%~40%,多胎妊娠更為顯著[3]。同時,多胎妊娠者早產更為常見,故使用利托君等宮縮抑制劑的概率更高[6]。另一方面,多胎妊娠時膈肌壓迫較單胎妊娠嚴重,更易發生呼吸窘迫。本文病例統計中多胎妊娠者占24.00%,顯著高于我國總人群中多胎妊娠比例(為1.9%[17])。因此,多胎妊娠很可能是導致利托君相關肺水腫的重要危險因素。
國外研究顯示,當利托君分別與0.9%氯化鈉注射液和5%葡萄糖注射液配伍時,孕婦肺水腫癥狀只在氯化鈉注射液組出現[18]。其原因可能是,妊娠晚期0.9%氯化鈉注射液相對體內仍然高滲,導致血漿容量進一步增大,且由于利托君阻礙作用,無法通過水鈉排泄代償,液體平衡進一步被破壞,肺水腫風險增加。而葡萄糖進入機體后,部分參與有氧代謝,部分以糖元形式貯存在肝臟及肌肉中,對血漿滲透壓影響較小。本文調研病例中,輸注溶媒以0.9%氯化鈉注射液居多,但由于大部分病例溶媒信息缺失,故輸注溶媒在利托君相關肺水腫中的作用仍需進一步研究闡明。
此外,硫酸鎂和糖皮質激素的聯合使用可能是利托君所致肺水腫的另一重要因素。本文調研顯示,聯合用藥誘發肺水腫的病例占64.00%,且硫酸鎂與利托君同時給藥較序貫給藥致肺水腫占比更高。目前國內外指南已不再推薦硫酸鎂用于抗宮縮治療,而多用于胎兒腦保護和子癇的防治[19]。但硫酸鎂與利托君作用機制相似,均可導致肺水腫[20],應避免同時輸注。另一方面,由于國內外指南推薦,早產風險增加者需給予糖皮質激素促胎肺成熟[21-22]。糖皮質激素可加重水鈉潴留,與利托君合用使肺水腫發生風險升高。
3.3治療措施及轉歸 利托君致肺水腫不良反應兇險,嚴重者可危及生命,早期預防、識別尤為重要。用藥前應行心臟疾病篩查,既往有確診或疑似心肺疾病史的孕婦禁用[16]。靜脈給藥時,建議選擇5%葡萄糖注射液作為溶媒,從小劑量0.05 mg·min-1開始給藥,最大維持劑量為0.15~0.35 mg·min-1[2]。給藥期間嚴密監測孕婦心率、血壓及胎心率,尤其針對多胎妊娠、聯合用藥等肺水腫發生風險較高的患者:當孕婦心率>130次·min-1時,應減慢滴速;當孕婦心率>140次·min-1,收縮壓<90 mmHg或胎心≥180次·min-1時,應進一步評價孕婦心肺功能并停藥[10]。同時應每日測量孕婦體質量同時嚴格記錄出入量,最大限制入量為2000 mL·d-1[23]。若發生肺水腫,應立即停藥并給予呼吸支持、利尿等措施;病情嚴重時,可使用高選擇性β1受體阻斷藥(如美托洛爾)[15]。
綜上所述,利托君致急性肺水腫不良反應危險程度高,可危及母兒生命。目前尚無有效措施預防肺水腫的發生,因此使用利托君時應嚴格掌握用藥指征與禁忌證,做到密切監護、早期識別肺水腫征象并提前準備搶救措施。同時,應加強醫護人員對該不良反應的認識,保證利托君的合理使用。

