補腎促卵方治療腎虛肝郁型卵巢功能低下所致不孕癥臨床研究*
趙楠,蔣蓮麗,張海峰,朱娜
靖江市中醫院,江蘇 靖江 214500
卵巢儲備功能是指卵巢皮質區卵泡生長發育狀態的能力,即形成優質卵母細胞的能力,主要指卵巢內卵泡的數量和質量[1]。卵巢功能低下(decreased ovarian reserve,DOR)是指卵巢產生優質卵母細胞能力下降,致使女性生殖能力下降,同時伴隨有激素水平異常等病理狀態[2]。近年來,DOR臨床發病率逐年上升,臨床表現為月經量少、閉經、不孕等,直接影響了育齡婦女的身體健康和生活質量。因此,關注生殖能力、改善孕育狀態已成為現代社會亟待解決的問題[3]。
DOR的發病機制尚不明確,據文獻報道[4-6],其發病可能與卵巢儲備功能降低或卵巢早衰等因素有關,即腦-心(腎)-子宮軸平衡紊亂,致使激素調節能力降低,無法動態調整機體激素水平[7]。臨床治療主要以激素輔助治療為主(如脫氫表雄酮、睪酮凝膠等),該治療方法是采用藥物調控機體激素周期變化,進而發揮調節激素分泌的作用,但長期使用可降低對激素水平的自我調整能力,且遠期效果不佳[8]。中醫治療DOR以辨證施治為特點,結合患者體征及經期特點針對性用藥,臨床效果明顯。筆者采用補腎促卵方治療DOR所致不孕癥,取得滿意療效,現報道如下。
1 資料與方法
1.1 一般資料選擇靖江市中醫院 2019年10月至2022年1月收治的100例DOR所致不孕癥患者為研究對象,按照隨機數字表法分為觀察組和對照組,每組各50例。觀察組年齡(31.5±8.5)歲;病程(2.1±1.3)年;原發性不孕癥30例,繼發不孕癥20例。對照組年齡(33.7±9.1)歲;病程(3.2±1.1)年;原發性不孕癥26例,繼發性不孕癥24例。兩組患者一般資料比較,差異無統計學意義(P>0.05),具有可比性。本研究經醫院倫理委員會批準通過。
1.2 診斷標準
1.2.1 西醫診斷標準符合《婦產科學》[9]中卵巢儲備功能低下的診斷標準,即月經稀發或閉經超過4個月;稀發排卵或無排卵;間隔4周以上檢測兩次早卵泡期血清卵泡刺激素(follicle-stimulating hormone,FSH)>25 IU·L-1,或FSH/黃體生成素(luteinizing Hormone,LH)>3,或雌二醇(estradiol,E2)>80 ng·L-1,或基礎竇卵泡個數≤4個。
1.2.2 中醫診斷標準符合《中藥新藥臨床指導原則》[10]中不孕癥及腎虛肝郁證診斷標準。主癥:月經不定期,量少甚至閉經,經色暗紅有血塊,久婚不孕;次癥:腰骶酸困,頭暈耳鳴,性欲減退,少腹脹痛或脅痛、乳房脹痛,情志不暢,煩躁易怒,善嘆息,舌紅苔薄白、脈沉細或沉弦。符合至少2項主癥,次癥2項或以上者;舌診和脈診作為參考。
1.3 病例納入標準年齡≤40歲;符合上述診斷標準;患者或家屬均知情并同意簽署知情同意書。
1.4 病例排除標準卵巢功能衰竭或早衰者;由卵巢器質性病變、先天因素等引起的卵巢功能低下者;合并有嚴重心腦血管疾病、惡性腫瘤患者;近3個月內有服用過其他激素,對該研究用藥有干擾者;對研究用藥過敏或其他不適宜采用本治療方案者。
1.5 治療方法對兩組患者進行心理疏導,詳細講解疾病的成因、發展及治療方案,盡可能消除夫妻雙方心理干擾,減輕其心理壓力,增強患者及其家屬治療信心,保持良好的心理狀態,并保持適當運動,調整生活習慣,積極配合治療。
對照組給予雌二醇/雌二醇地屈孕酮復合片(荷蘭Abbott Biologicals B.V.,批號:注冊證號H20150346)治療,每日1次,每次1片,飯后30 min口服,連續服用 28 d,停藥后觀察月經情況,如月經來潮,可在月經第5天開始服用,如月經未來,在停藥后7 d繼續服用。連續服用3個月經周期。
觀察組在對照組治療的基礎上給予補腎促卵方治療,具體藥物組成:黃芪20 g,熟地黃20 g,菟絲子15 g,淫羊藿15 g,女貞子15 g,墨旱蓮15 g,白芍 12 g,柴胡15 g,制香附15 g,當歸9 g,川芎6 g,炙甘草6 g。經前期加巴戟天15 g,肉蓯蓉12 g,紫石英 6 g;行經期加赤芍15 g,丹參20 g;經后期加枸杞子 15 g,女貞子30 g;排卵期加澤蘭15 g。每日1劑,水煎500 mL,分早晚2次服用,連續3個月經周期。
1.6 觀察指標
1.6.1 激素水平檢測兩組患者治療前后激素水平變化情況,抽取患者清晨空腹靜脈血,采用電化學發光法測定FSH、LH和E2水平。
1.6.2 卵泡發育情況及子宮內膜厚度采用多普勒彩超診斷儀測定兩組患者治療前后月經周期的第5天、第10天至第14天卵泡發育情況及子宮內膜厚度(根據患者卵泡發育情況可適時調整檢測時間)[11]。初級卵泡為月經周期的第5天檢測的卵泡數量,直徑約7 mm;優勢卵泡是指直徑>16 mm的卵泡。
1.6.3 卵巢血流指標采用多普勒彩超檢查患者卵巢血流指標,包括子宮動脈收縮期峰值流速(peak systolic velocity,PSV)、竇卵泡計數(antral follicle count,AFC)、搏動指數(pulsation index,PI)、血管阻力指數(resistance index,RI)。
1.6.4 妊娠率比較兩組患者在治療后1年內妊娠情況,并對妊娠結果進行比較。
1.7 療效判定標準參照《中藥新藥臨床研究指導原則》[10]制定。顯效:患者臨床癥狀基本消失,血清FSH、E2、LH恢復正常;有效:患者臨床癥狀有所改善,血清FSH、E2、LH水平基本恢復正常,但仍有部分異常;無效:患者臨床癥狀及血清FSH、E2、LH水平無明顯變化。
有效率=(顯效+有效)/n×100%
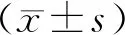
2 結果
2.1 兩組DOR所致不孕癥患者臨床療效比較觀察組有效率為96.00%,對照組有效率為80.00%,兩組患者有效率比較,差異具有統計學意義(P<0.05),見表1。

表1 兩組DOR所致不孕癥患者臨床療效比較例(%)
2.2 兩組DOR所致不孕癥患者治療前后激素水平比較兩組患者治療后血清激素FSH、LH、E2、FSH/LH水平均低于本組治療前,且治療后觀察組低于對照組,差異具有統計學意義(P<0.05),見表2。
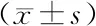
表2 兩組DOR所致不孕癥患者治療前后激素水平比較
2.3 兩組DOR所致不孕癥患者治療前后卵泡發育情況及子宮內膜厚度比較兩組患者治療后初級卵泡數、優勢卵泡、排卵數、子宮內膜厚度高于本組治療前,且治療后觀察組高于對照組,差異具有統計學意義(P<0.05),見表3。
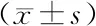
表3 兩組DOR所致不孕癥患者治療前后卵泡發育情況及子宮內膜厚度比較
2.4 兩組DOR所致不孕癥患者治療前后卵巢血流情況比較兩組患者治療后PSV、RI、AFC高于本組治療前,PI低于本組治療前,組間比較,差異均有統計學意義(P<0.05),見表4。
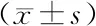
表4 兩組DOR所致不孕癥患者治療前后卵巢血流情況比較
2.5 兩組DOR所致不孕癥患者妊娠率的比較觀察組妊娠32例,妊娠率為64.00%;對照組妊娠21例,妊娠率為42.00%,觀察組妊娠率高于對照組,差異具有統計學意義(P<0.05)。
3 討論
DOR的主要病機為腎虛,同時伴隨其他臟腑功能不足,臨床以經期紊亂為主,伴繼發性不孕、潮熱汗出等,屬中醫學“月經后期”“閉經”“不孕”等范疇[12-13]。沖任調、肝氣疏,則孕自成。孕育之要在于卵子生長發育成熟與腎精充盈健壯[14-15]。《醫學正傳·婦人科》曰:“腎水既乏,則經血日益干涸。”即指腎虛是導致DOR發病的核心病機。補腎促卵方為臨床經驗方,主要功效為補益肝腎、養血調經、疏肝柔木[16]。方中黃芪補益腎氣;熟地黃、菟絲子、淫羊藿、女貞子、墨旱蓮等5味藥溫補陰陽、滋陰又助陽,以適應機體在此階段重陰必陽的動態變化及陽長的需要;白芍、柴胡、制香附發揮柔肝、疏肝、緩急之作用;當歸、川芎補血、和血、調經,以適應促排卵、促轉化之需要,促使卵泡順利排出;炙甘草調和諸藥。諸藥合用,共奏補益肝腎、疏肝柔木、養血調經的功效,使精血充足而天癸至[17-18]。
DOR患者由于其卵母細胞產生能力降低,致使卵巢內留存的卵泡數量減少,如未能及時治療,可進一步發展成卵巢早衰,嚴重影響女性生理、心理健康。雖然現代輔助生殖技術在臨床已廣泛開展,但該技術尚不能完全被患者接受[19],再加之卵母細胞質量的降低,對藥物的應激性反應亦降低。因此,尋求安全、有效的治療手段是近些年的研究熱點。DOR的發生可由多種因素導致,如多次流產、感染、放療、化療、免疫因素、不良生活習慣、心理應激等[20-21]。下丘腦-垂體-性腺軸是調控月經周期的主要通路[22],垂體在下丘腦促性腺激素的刺激下,釋放FSH,同時受E2、血清抑制素的雙向反饋性調節,FSH的升高可導致機體對卵泡生成提前,致使月經周期縮短。因此,FSH表達水平的高低可間接評價卵巢儲備功能,反映DOR發展程度,但其變異性較大,個體差異明顯,臨床應用時只能作為粗略參考,并沒有明顯的范圍閾值,臨床上常以FSH≥10 IU·L-1作為提示卵巢功能異常的預測標準[23]。有研究顯示[24],FSH/LH可作為衡量卵巢儲備功能的指標,即FSH/LH>3.6提示卵巢儲備功能下降,FSH/LH>2.0提示存在卵巢功能減退[25-26]。
綜上所述,補腎促卵方治療DOR所致不孕癥療效確切,其作用機制可能是通過多成分、多靶點的刺激作用,發揮改善患者卵巢功能,調節性激素水平等作用,進而提高妊娠率。

