曲札茋苷與鹽酸法舒地爾聯用對腦梗的保護作用研究
付傳美 楊旭娟 劉一丹 孟 珂 黃 茜 陳建勛 劉軍鋒 楊兆祥* 劉國光
1. 昆明醫科大學,云南 昆明 650500;2.昆藥集團股份有限公司,云南 昆明 650100
腦卒中是全球第二大、中國第一大致死性疾病,具有高發病率、高致殘率、高死亡率、高復發率、高經濟負擔等五大特點, 嚴重影響了患者的身體健康和生活質量[1-2],給社會和家庭帶來了沉重負擔。腦卒中包括缺血性腦卒中和出血性腦卒中,缺血性腦卒中亦稱“腦梗”,是腦血管閉塞或阻塞引起的腦供血不足而導致神經組織損傷,表現為能量代謝衰竭,細胞膜內外離子平衡紊亂,進而使興奮性氨基酸釋放,Ca2+超載,自由基、炎癥因子大量釋放,引發一系列級聯反應。針對以上特點,目前臨床上治療腦梗的策略主要是恢復供血、改善循環以及神經保護[3]。考慮到其復雜的病理生理過程,針對任何單一環節的治療都難以完全有效地阻止缺血損傷,聯合用藥有可能達到協同作用[4]。注射用曲札茋苷為昆藥集團自主研制的擬用于急性腦梗患者的神經保護劑,可通過清除自由基、抗氧化、抗炎、抗凋亡作用等途徑發揮神經保護作用[5-8]。鹽酸法舒地爾是一種新型的異喹啉磺胺衍生物,主要通過抑制Rho激酶達到擴張血管、改善腦循環,也具有阻斷炎癥反應、抗氧化等作用[9-12]。 二者聯用治療缺血性腦卒中的研究鮮有報道,且有無聯用的價值還需進一步探究。故本實驗在動物水平上,通過觀察全腦缺血后小鼠的存活時間,局灶性腦缺血再灌注24h時的神經行為學評分、腦梗死體積,血清中SOD活力、MDA、TNF-α、IL-1β、IL-6等含量變化,探討二者聯用對腦梗的保護作用及其能否產生協同增效作用,為臨床的應用進行探索并提供理論依據。
1 材料
1.1 動物 雄性ICR小鼠,體重24~28 g,由昆藥集團股份有限公司實驗動物中心提供,生產許可證:SCXK(滇)K2019-0001,發證機關:昆明市科學技術局。小鼠采用透明塑料盒群養,每箱≤6只;溫度20~25 ℃(日溫差≤3 ℃);濕度40%~70%;照明12 h∶12 h明暗交替,照度150~300 lx;噪音≤60 dB。實驗動物使用許可證號:SYXK(滇)K2019-0001,發證機關:昆明市科學技術局。每日喂飼鼠用配合飼料,自由飲水,視情況更換籠具和墊料。
1.2 藥品與主要試劑 注射用曲札茋苷(20 mg/支,含量98.7%,批號:20200530),室溫、避光、密閉保存。鹽酸法舒地爾注射液(昆藥集團股份有限公司,批號:20GE03-211,規格為2 mL∶30 mg,6支/盒);依達拉奉右莰醇注射用濃溶液(先聲藥業,國藥準字H20200007,批號:181-201017,規格為5 mL:依達拉奉10 mg與右莰醇2.5 mg,6支/盒);丁苯酞氯化鈉注射液(石藥集團恩必普藥業有限公司, 批號: 6182103107,規格為100 mL:丁苯酞25 mg與氯化鈉0.9 g),甘露醇注射液;(青島明月海藻集團有限公司,批號:36150506);2,3,5-氯化三苯基四氮唑(TTC,Sigma,CAS:298-96-4),水合氯醛(山東西亞化學工業有限公司,批號:119957,Cas 號:302-17-0)。小鼠TNF-α、IL-1β、IL-6試劑盒均購于武漢貝茵萊生物制劑有限公司;SOD、MDA試劑盒均購于南京建成生物工程研究所。
1.2 儀器 AR224型電子分析天平(奧豪斯儀器(上海)有限公司);JX5001/5000g電子天平(上海浦春儀器計量有限公司);PowerWave XS2型連續波長酶標儀(美國Bio Tek);Biofuge Stratos型臺式高速冷凍離心機(德國Thermo Scientific Heraeus公司);各種規格移液器,德國Eppendorf公司;Millipore純水處理系統(美國Millipore公司);1622A3腦缺血再灌注模型線栓(線栓直徑0.16±0.01,北京西濃科技有限公司)。
2 方法
2.1 雙側頸總動脈結扎小鼠全腦缺血模型 雄性小鼠84只,按體重隨機分為7組:模型對照、丁苯酞(8.3 mg/kg)、曲札茋苷(3.35 mg/kg、6.7 mg/kg)、法舒地爾(7.5 mg/kg、15 mg/kg)、曲札茋苷聯合鹽酸法舒地爾(3.35 mg/kg +7.5 mg/kg)組,每組12只。各組動物每日按10 mL/kg體重尾靜脈注射給藥1次(聯合給藥間隔1 h),連續5 d;末次給藥15 min,用400 mg/kg水合氯醛腹腔注射麻醉動物,仰位固定,頸部正中切口,分離、結扎雙側頸總動脈后縫合傷口。觀察并記錄每只小鼠自結扎至2 h內的死亡時間為耐缺血缺氧時間,對存活時間超過2 h者計為2 h。
2.2 線栓致局灶性腦缺血小鼠再灌注模型 參照文獻[13-14],取24~28 g雄性小鼠,腹腔注射水合氯醛麻醉小鼠,仰位固定、備皮、消毒后頸部正中切口,分離、結扎右側頸總動脈脈(common carotid artery,CCA)近心端及頸外動脈(externalcarotid arter,ECA);在CCA分叉處的近心端 2 ~ 3 mm 處切口, 插入線栓 8~10 mm, 使線栓進入頸內動脈( internal carotid artery,ICA),穿過大腦中動脈( middle cerebralartery, MCA) 起始端至大腦前動脈近端, 阻斷 MCA的所有血流來源,固定線栓,縫合切口回籠飼養;假手術組僅分離CCA、ECA。將造模動物分為6組:模型對照、陽性對照右莰醇(10 mg/kg )、曲札茋苷(3.35 mg/kg、6.7 mg/kg)、法舒地爾(7.5 mg/kg、15 mg/kg)及聯合用藥(3.35 mg/kg +7.5 mg/kg)組,每組12 只。造模后2 h,各組動物分別按10 mL/kg體重靜脈注射給藥(聯合給藥間隔1 h),同時拔出線栓實現再灌。再灌后24 h,參照改良的 Longa 評分標準[15]對各組動物進行神經行為學評分后,眼球取血用于測定SOD、MDA、TNF-α、IL-1β、IL-6。處死小鼠,取腦切成厚度均為2 mm的腦片于1% TTC 溶液中,37 ℃、孵育20 min顯色后, 4%多聚甲醛中固定 24 h 后,數碼相機拍照, 以 Image J 軟件統計全腦片與梗死區面積(紅色區域為正常腦組織,蒼白色區域為梗死區),計算腦梗死體積百分率,腦梗死體積百分率=[(非缺血側半球面積-缺血側半球未梗死區面積)×厚度(2 mm)/全腦體積]×100%。
神經行為學評分(改良的 Longa 評分)。0分: 無明顯神經功能缺損;1 分: 提尾時,對側前肢不能前伸;2 分: 向缺血對側轉圈;3 分: 不能承受對側自身重量;4 分: 無自主運動或意識障礙。分值越高,說明動物行為障礙越嚴重。
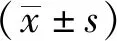
3 結果
3.1 對全腦缺血小鼠存活時間的影響 表1結果顯示,與模型組比較,曲札茋苷低劑量(3.35 mg/kg)組、法舒地爾低劑量(7.5 mg/kg)組在2 h內死亡率與存活時間上均沒有體現出差異;曲札茋苷高劑量(6.7 mg/kg)組、法舒地爾高劑量(15 mg/kg)組及低劑量聯合用藥(3.35 mg/kg +7.5 mg/kg)組均能明顯延長全腦缺血小鼠的存活時間,降低2 h內的死亡率;其中,兩藥低劑量單用組與各自高劑量單用組比沒有差異(P>0.05),與低劑量聯用組比,聯用能明顯延長存活時間、降低2 h內死亡率(P<0.01);以上表明曲札茋苷聯合法舒地爾對提高全腦缺血小鼠的耐缺血缺氧能力有協同作用。
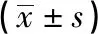
表1 對全腦缺血小鼠存活時間的影響
3.2 對局灶性腦缺血再灌注小鼠腦梗死體積的影響 與假手術組比,模型小鼠表現出明顯的行為學缺陷(P<0.01)和腦梗死(P<0.01),表明造模成功(表2、圖1) 。與模型組比,曲札茋苷低劑量(3.35 mg/kg)組、法舒地爾低劑量(7.5 mg/kg)組單用在神經行為學評及腦梗死體積上降低趨勢不明顯,均沒有體現出差異;曲札茋苷高劑量(6.7 mg/kg)組、法舒地爾高劑量(15 mg/kg)組及低劑量聯合用藥(3.35 mg/kg +7.5 mg/kg)組對小鼠的神經行為學評分有降低的趨勢,對腦梗死體積有明顯的降低作用(P<0.05或P<0.01) ;其中,兩藥低劑量單用與各自高劑量單用比無差異(P>0.05);與低劑量聯用比,聯用能明顯降低腦梗死體積(P<0.01)。陽性對照右莰醇(10 mg/kg )亦可降低小鼠的行為學評分及腦梗死體積(P< 0.05,P<0.01) 。
3.3 對局灶性腦缺血再灌注小鼠血清中SOD、MDA、TNF-α、IL-1β、IL-6的影響 如表3 所示,與假手術組相比,模型組小鼠血清中 SOD 活性明顯降低、MDA含量明顯升高(P<0.01),表明氧化應激失衡。與模型組比,曲札茋苷及聯合用藥組均能升高血清中SOD活性,均能減少MDA的生成(P<0.05),且聯合給藥較兩藥單用組有不錯的趨勢。提示曲札茋苷聯合法舒地爾提高了缺血再灌注模型小鼠的抗氧化能力。
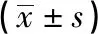
表2 對缺血再灌注小鼠腦梗死體積的影響統計表

A:假手術;B:模型對照;C:陽性對照右坎醇(10 mg/kg );D:曲札茋苷(6.7 mg/kg);E:鹽酸法舒地爾注射液(15 mg/kg);F:曲札茋苷+鹽酸法舒地爾注射液(3.35 mg/kg +7.5 mg/kg)
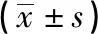
表3 對小鼠血清SOD、MDA含量的影響統計表
如表4所示,與假手術組相比,模型組血清中TNF-α、IL-1β、IL-6明顯增加(P<0.01),表明炎癥反應增強。與模型組比,曲札茋苷、鹽酸法舒地爾注射液、聯合用藥組均能減少缺血再灌注小鼠血清中 TNF-α、IL-1β、IL-6 生成(P<0.05或P<0.01) ;且聯合用藥的效果較單用藥組有更好的趨勢。提示曲札茋苷聯合法舒地爾提高了腦缺血小鼠的抗炎能力。
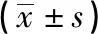
表4 對小鼠血清TNF-α、IL-1β、IL-6含量的影響統計表
4 討論
腦梗又稱缺血性腦卒中,是腦卒中最常見的類型,常產生一系列神經缺損癥狀,如神經系統缺血和缺氧性的壞死、腦水腫、炎癥反應等,重者意識喪失,是病人致殘和致死的主要原因[16]。腦缺血再灌注發生后腦組織中活性氧(reactive oxygen species,ROS)過量產生,炎癥細胞聚集,產生大量炎癥因子,谷氨酸興奮性毒性,鈣穩態失衡,細胞凋亡及血腦屏障(blood brain barrier,BBB)破壞等多種病理機制參與腦缺血再灌注損傷(cerebral ischemia-reperfusion injury,CIRI)[17-20]。氧化應激是缺血性腦損傷的主要病理機制,也是影響腦缺血嚴重程度的重要因素之一。CIRI激活炎癥因子是導致腦損傷的重要機制。在正常人體內,自由基的生成、清除處于動態平衡,但在缺血性腦卒中發生后,過量自由基生成,進而出現細胞膜損傷、神經元死亡和腦組織梗死等。MDA是膜脂過氧化的重要產物,其可加劇細胞膜的損傷,與體內自由基的多少有關。SOD的水平高低間接反映機體清除氧自由基的能力,其本身有助于保護腦細胞免受氧自由基的損傷。缺血后細胞因子IL-1β、TNF-α 和IL-6刺激趨化因子中性粒細胞趨化因子、單核細胞趨化因子-1和巨噬細胞炎性蛋白-1產生和釋放,促進單核細胞、中性粒細胞和淋巴細胞遷移[21]。TNF-α濃度在腦梗死癥狀出現后6~12 h在血清中升高,在梗死后24 h內腦脊液中顯著升高,與梗死面積呈正相關[22]。IL-6刺激淋巴T細胞增殖滲透加重炎癥反應,其抗炎作用主要體現在可以上調IL-1ra,實驗證明IL-6缺陷鼠梗死后結局不好[23]。目前對腦卒中發病機制的研究得到不斷地深入和發展,但其中各種機制相互關聯的樞紐點尚不明確,有待更深入地研究;且面對復雜發病機制的缺血性腦卒中,單一的藥物治療并不足以應對腦缺血缺氧及再灌注引發的病理生理改變。
研究采用雙側頸總結扎的全腦缺血模型與局灶性腦缺血再灌注模型,主要從存活時間、神經功能評分、腦梗死體積、抗氧化應激指標(SOD、MDA)、抗炎(TNF-α、IL-6、IL-1β)等方面對比曲札茋苷、鹽酸法舒地爾注射液單獨給藥及聯合用藥對腦梗的保護作用。全腦缺血模型選擇丁苯酞作為陽性對照,考慮到其可改善腦缺血區的微循環和能量代謝,增加缺血部位腦血流量,能有效延長模型小鼠的存活時間;局灶性腦缺血再灌注模型選擇依達拉奉右坎醇濃溶液作為陽性對照,其科學配伍了依達拉奉和右莰醇兩種活性成分,應用兩種成分清除自由基、抗炎等作用機制,可顯著降低急性缺血性腦卒中引發的腦神經損傷。一項納入1200名急性缺血性腦卒中患者的隨機、雙盲、頭對頭比較的III期研究[24]表明,對比單方依達拉奉注射液,依達拉奉右莰醇顯示出明確的療效優勢、臨床安全性相似,對國內卒中治療來說意義重大。
法舒地爾作為一種腦血管及周圍血管擴張藥物,主要藥理作用是擴張血管,抵抗血管痙攣,改善腦組織的微循環;減少炎癥介質產生,減輕炎癥反應[25-26]。曲札茋苷屬二苯乙烯類化合物,結構中含有多個酚羥基,文獻報道該類化合物具有多種藥理活性,對心腦血管具有明顯的保護作用,其機制包括抗氧化活性[27]、抗炎[28]、抗細胞凋亡[29]等。本實驗結果顯示,曲札茋苷低劑量(3.35 mg/kg)組、法舒地爾低劑量(7.5 mg/kg)組對雙側頸總結扎小鼠的存活時間,缺血再灌注小鼠的神經行為學評分、腦梗死體積無改善作用(P>0.05)。曲札茋苷高劑量(6.7 mg/kg)組、法舒地爾高劑量(15 mg/kg)組均能改善小鼠存活時間及腦梗體積(P<0.05或P<0.01),也說明改善循環或是神經保護都發揮了腦保護作用。兩藥低劑量聯用(3.35 mg/kg +7.5 mg/kg)能顯著延長存活時間、降低腦梗死體積與神經行為學評分,降低TNF-α、IL-1β、IL-6與MDA含量,升高SOD活力(P<0.05或P<0.01)。與兩藥低劑量單用組比較,高劑量單用組對存活時間、腦梗死體積的保護作用沒有顯示出差異(P>0.05),而低劑量聯用組表現出差異(P<0.05或P<0.01)。表明通過改善循環或神經保護對腦梗的保護作用有限,聯合用藥可使曲札茋苷與法舒地爾在改善循環及神經保護方面發揮協同作用,從而進一步改善腦梗,這一結果也為臨床應用提供理論依據。

