Cu-Mg-Ce復合氧化物活化過硫酸鈉降解羅丹明B
郭 濤,陳彥新,賈青竹
(1.天津科技大學海洋與環境學院,天津 300457;2.山東省臨沂市生態環境局臨沭縣分局,臨沂 276700)
我國是世界染料第一大國.隨著染料行業的發展,染料廢水排放量也隨之增大,我國工業廢水排放總量大約為 2.28×1010t/a,其中紡織廢水排放量約為2.0×109t/a,而紡織廢水中約 80%為染料廢水[1].染料廢水具有成分復雜、有機物含量高、可生化性差、色度高、毒性大等特點[2–4],常規方法很難將其處理達標,因此,染料廢水成為近年來典型的難降解有機廢水之一[5].羅丹明 B(RhB)結構式如圖1所示,分子式為 C28H31ClN2O3,相對分子質量為 479.01.羅丹明 B穩定性好、質優價廉,被廣泛應用于染料激光材料和印刷造紙業等.然而,已有研究證明羅丹明B能夠對血液系統以及肝、脾、腎等內臟器官造成一定損害,甚至可以致癌、致畸、致死[6].
圖1 羅丹明B的結構式Fig.1 Structural formula of rhodamine B
化學法可以利用強氧化劑將污染物降解,常用的化學法有臭氧氧化法、芬頓法(Fenton法)和光催化法等[7–9],這些方法在反應中產生的羥自由基(·OH)可與大多數有機物發生氧化還原反應.硫酸根自由基氧化技術是目前有機廢水處理的熱點,相比羥自由基,硫酸根自由基()具有更高的氧化還原電位,其官能團選擇性好,對底物的氧化更具選擇性[10–11].孫威等[12]使用 5種過渡金屬離子(Mn2+、Fe2+、Cu2+、Co2+、Ag+)活化的過硫酸鹽對甲基橙進行降解,研究發現在金屬離子用量相同的條件下,Fe2+活化效果最好,但對甲基橙的降解率只有 90%,且要求溶液 pH必須控制在 5~6.Yang等[13]利用浸漬法制備的催化劑 Co/TiO2(物質的量比為 1∶10)活化過一硫酸鹽(PMS),其活化能力遠高于 Co3O4.蘇冰琴等[14]使用Fe3O4活化過二硫酸鹽同步去除污染物諾氟沙星和鉛,在最優條件下諾氟沙星的去除率可達 90.2%,鉛的去除率可達 99.5%,但是其穩定性較差,非常容易氧化導致其催化活性降低,4次循環使用后去除率只有40%.
研究表明 Fenton法[15]、光催化法[16]以及電化學法[17]等對羅丹明 B印染廢水都有較好的處理效果.但是,Fenton 法會產生大量鐵泥,光催化法的催化劑循環使用過后會出現性能衰減,電化學法能耗過高.最近研究發現過硫酸鹽活化法對羅丹明 B有較好的降解效果.張凱等[18]用合成出的 Fe3O4/水熱炭活化過硫酸鹽降解羅丹明 B,降解率可達 94.6%.李靜等[19]采用 Ce-Fe復合催化劑活化過硫酸鹽用于羅丹明 B的降解,羅丹明 B在 45min后降解率達到88.9%.
本文利用共沉淀法制備的 Cu-Mg-Ce復合氧化物活化過硫酸鈉(PS)用于降解羅丹明B,對比了不同體系對羅丹明 B的去除效果,考察不同催化劑投加量、底物初始質量濃度、氧化劑 PS濃度、溶液初始pH對羅丹明B降解的影響,并且考察催化劑的穩定性,推斷出催化劑活化 PS降解羅丹明 B的機理.本研究工作為處理其他難降解的有機廢水提供了參考.
1 材料與方法
1.1 原料與儀器
硝酸銅水合物,分析純,上海麥克林生物科技有限公司;硝酸鈰水合物,分析純,天津市光復精細化工研究所;硫酸鎂水合物、無水碳酸鈉,分析純,天津市博歐特化工貿易有限公司;PS、乙醇,分析純,天津市大茂化學試劑廠;氫氧化鈉,分析純,上海市阿拉丁生化科技有限公司;硝酸,分析純,天津市化學試劑五廠.
TU–1810型紫外可見–分光光度計,北京普析通用儀器有限責任公司;Milli–Q system型凈水系統(用于制備配制溶液所使用的超純水),德國 Merck KGaA公司.
1.2 催化劑制備
利用共沉淀法制備Cu-Mg-Ce復合氧化物.具體制備過程如下:配制 50mL Cu(NO3)2·3H2O、MgSO4·7H2O、Ce(NO3)3·5H2O 物質的量比為 1∶1∶1的混合溶液 A;配制50mL NaOH與Na2CO3物質的量比為2∶1的混合堿性溶液B;將混合溶液A滴加到 50mL超純水中,恒定滴加混合堿性溶液 B以保持 pH=9.0,得到混合體系 C;將混合體系 C在50℃下陳化 24h,使用真空泵抽濾得到沉淀物,沉淀洗滌至表面溶液 pH=9.0;洗滌后在 80℃下干燥12h,再置于馬弗爐中,在空氣氛圍中 600℃煅燒5h,得到Cu-Mg-Ce復合氧化物.
1.3 催化降解反應
將Cu-Mg-Ce復合氧化物、羅丹明B溶液、氧化劑PS一起投入250mL溶液中,羅丹明B溶液初始質量濃度為 5~20mg/L,Cu-Mg-Ce復合氧化物投加量為 0.1~1.5g/L,氧化劑 PS濃度為 0.1~1.5mmol/L.取樣間隔 15min,取樣量 5mL(兩組平行樣),取樣后迅速添加無水乙醇,并充分混合.
1.4 羅丹明B去除率的測定
用外標法測定 554nm 波長下羅丹明 B的吸光度.根據羅丹明 B的標準曲線計算樣品中羅丹明 B的質量濃度,進而計算去除率(R).
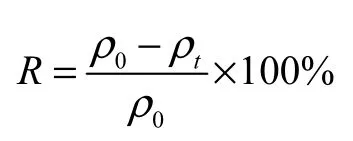
式中:ρ0為羅丹明 B 的初始質量濃度,mg/L;ρt為反應至t時刻時羅丹明B的質量濃度,mg/L.
2 結果與討論
2.1 RhB降解效果的影響因素
2.1.1 不同體系
在催化劑投加量為 1.0g/L、底物的初始質量濃度為 10mg/L、氧化劑 PS濃度為 1mmol/L的情況下,通過實驗對比了 8種不同體系(僅加 PS、僅加Cu-Mg-Ce、CuO/PS、CeO2/PS、CuMg/PS、MgCe/PS、CuCe/PS和Cu-Mg-Ce/PS)對RhB的降解效果,結果如圖2、表1所示.
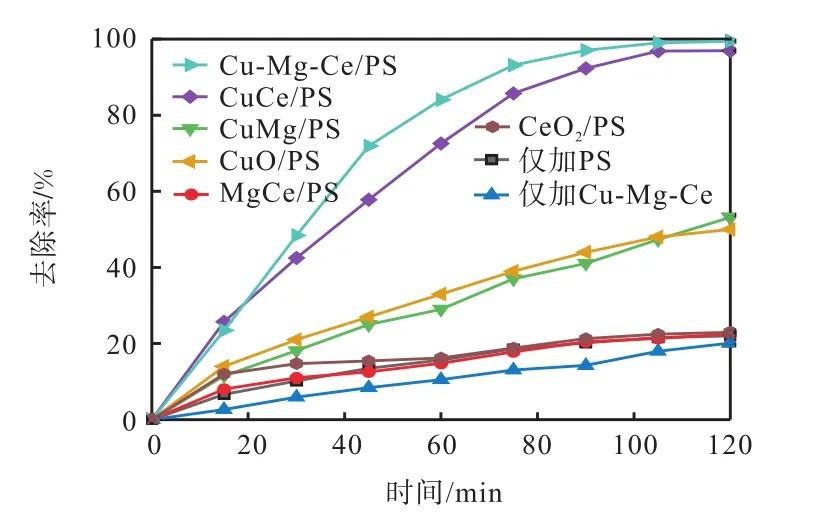
圖2 不同體系對羅丹明B的降解效果Fig.2 Degradation effects of different systems on rhodamine B
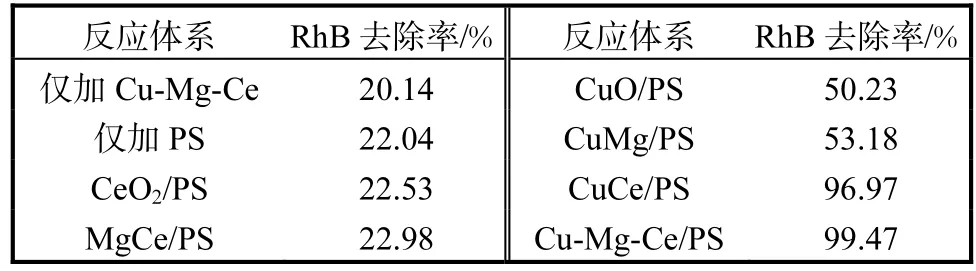
表1 反應至120 min時不同體系對羅丹明B的去除率Tab.1 Removal rates of Rhodamine B in different systems at 120 min
由圖2和表1可知,反應至120min時,RhB的去除率變化規律是:Cu-Mg-Ce/PS>CuCe/PS>CuMg/PS>CuO/PS>MgCe/PS>CeO2/PS>僅加PS>僅加 Cu-Mg-Ce.不加 PS時和僅有 PS時,RhB去除率很低;但是隨著引入 Cu離子或加入 PS,RhB去除率顯著提升,表明含 Cu離子的體系能很好地活化 PS.并且,在 CuO/PS體系中再引入 Ce離子后RhB去除率從50.23%升至96.97%,遠高于Mg離子體系.因此,Cu與 Ce同時存在時,能更好地活化PS,降解RhB.
2.1.2 Cu-Mg-Ce復合氧化物投加量
Cu-Mg-Ce復合氧化物的投加量對降解 RhB有直接影響.在 RhB溶液質量濃度為 10mg/L、氧化劑PS的濃度為1mmol/L的條件下,設置4個不同的催化劑投加量(0.1、0.5、1.0、1.5g/L)考察 Cu-Mg-Ce 復合氧化物投加量對去除 RhB的影響,結果如圖3所示.由圖3可知:隨著Cu-Mg-Ce復合氧化物投加量從 0.1g/L增加到 1.0g/L,在反應到 120min時 RhB的去除率也逐漸增加,RhB去除率最高達到99.47%.這可能是由于體系內 Cu-Mg-Ce復合氧化物越多,活性位點越多,更多的PS被活化產生,促進 RhB降解.當 Cu-Mg-Ce復合氧化物投加量到達 1.5g/L時,RhB的去除率達到 99.67%,去除率略有增加,90min前平均反應速率略有減慢,90~120min時平均反應速率與1.0g/L時相差不大.這可能是 Cu-Mg-Ce復合氧化物過多導致反應體系中的Cu離子過量,使產生的SO·4-被淬滅,反應速率放緩,且 Cu離子活化 PS產生的SO·4-的量受氧化劑 PS濃度的限制[20].因此,Cu-Mg-Ce復合氧化物催化劑的最佳投加量為1.0g/L.
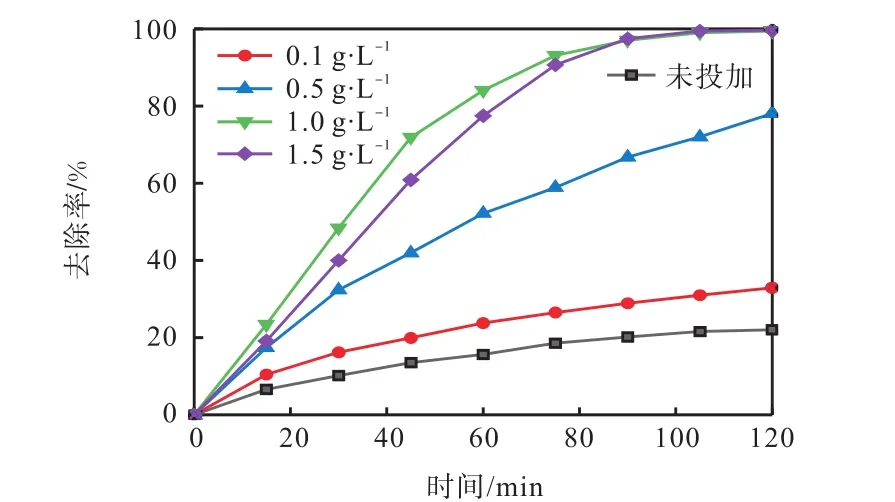
圖3 Cu-Mg-Ce復合氧化物投加量對羅丹明B降解的影響Fig.3 Effects of Cu-Mg-Ce composite oxide dosage on rhodamine B degradation
2.1.3 PS濃度
在 RhB溶液質量濃度為 10mg/L、Cu-Mg-Ce復合氧化物投加量為 1.0g/L條件下,設置 4個不同的PS 濃度(0.1、0.5、1.0、1.5mmol/L),探究 PS 濃度對Cu-Mg-Ce/PS體系降解 RhB效果的影響,實驗結果如圖4所示.由圖4可知:PS濃度從0.1mmol/L增加到 1mmol/L,反應 120min時,RhB的去除率也隨之增加,最大去除率為 99.47%.這可能是當催化劑投加量一定時,氧化劑越多,產生的越多,促進了 RhB的降解.當 PS濃度達到 1.5mmol/L時,PS投加過量,此時受RhB濃度的影響,導致沒有足夠的RhB 與產生的SO4·-及時反應,使自由基之間發生競爭和消耗,RhB的降解沒有明顯變化.因此,確定最佳PS濃度為1.0mmol/L.
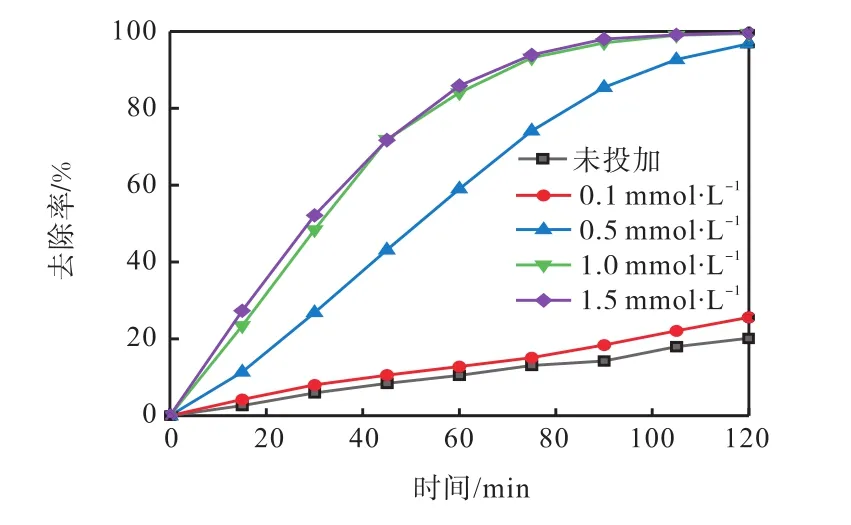
圖4 PS濃度對羅丹明B降解的影響Fig.4 Effects of PS concentration on rhodamine B degradation
2.1.4 羅丹明B的初始質量濃度
為考察RhB初始質量濃度對Cu-Mg-Ce/PS體系中RhB去除率的影響,選定催化劑投加量為1.0g/L,氧化劑 PS濃度為 1.0mmol/L,配制不同初始質量濃度(5、10、15、20mg/L)的 RhB 溶液,反應 120min,并對不同羅丹明 B初始質量濃度的反應體系進行動力學分析,實驗結果見表2.
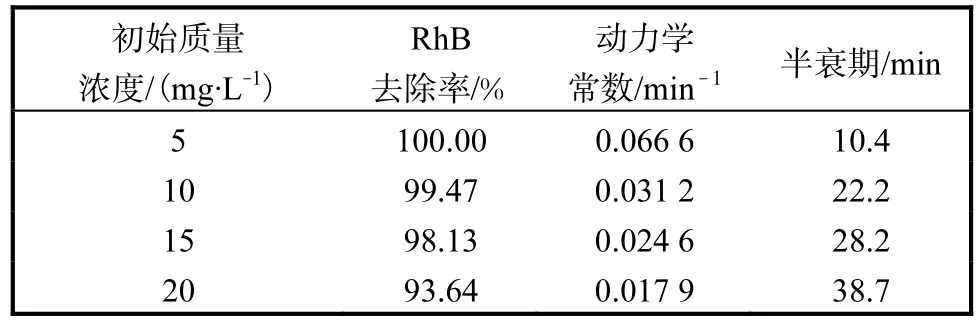
表2 不同羅丹明B初始質量濃度的降解動力學Tab.2 Degradation kinetics of different initial rhodamine B initial concentration
由表2可知:當 RhB初始質量濃度為 5、10、15mg/L時,RhB的去除率均在 98%以上;當初始質量濃度增加至 20mg/L時,RhB的去除率降至93.64%.RhB初始質量濃度從 5mg/L增加至20mg/L時,動力學常數從 0.0666min-1降低至0.0179min-1.產生這種現象的原因很可能是受到PS濃度的影響.RhB濃度過大時,RhB與活性物質產生競爭,阻礙催化劑和氧化劑之間的接觸,PS活化受阻,因此相同時間產生的SO4·-減少,從而導致反應速率減慢,去除率降低[21].
2.1.5 溶液初始pH
反應溶液 pH是影響RhB降解效果的關鍵因素之一.為研究反應溶液初始 pH對 RhB降解的影響.配制了 5份 pH 分別為 3、5、7、9、11的 RhB 溶液(10mg/L)進行降解實驗,結果如圖5所示.由圖5可知:在 pH 為 5、7、9的反應體系中,反應至120min時,RhB的去除率均可達到 100%;而此時,pH為3的反應體系RhB的去除率為57.29%,pH為11的反應體系 RhB的去除率為 68.94%.由此可以看出在弱酸、弱堿以及中性范圍內,Cu-Mg-Ce復合氧化物能夠很好地去除RhB.
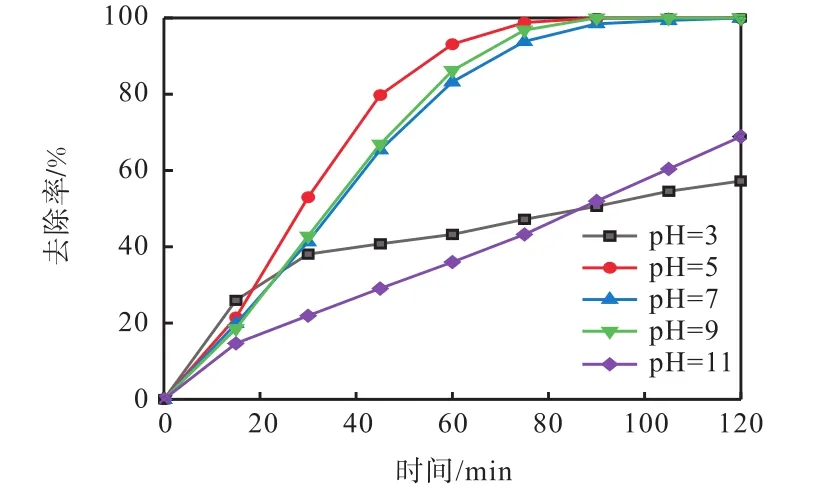
圖5 溶液初始pH對羅丹明B降解的影響Fig.5 Effects of initial pH on degradation of rhodamine B
在強酸性條件下,H+會與生成的以及·OH反應[22].會在強酸性條件下水解成 H2O2[23],發生式(1)所示的反應,進而生成氧化電位低于的·OH,并且還會催化產生大量的,導致相互淬滅,降低RhB的降解效果[24].
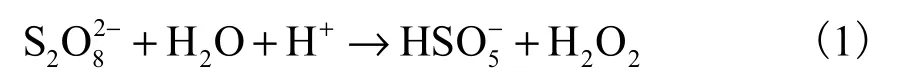
在弱酸性、弱堿性和中性條件下,當溶液 pH小于等電點時(CuO等電點為 9.5)顆粒質子化,帶正電,PS帶負電,因此催化劑與氧化劑產生靜電吸引,促進和·OH的生成,增強對RhB的降解效果[25].
在堿性條件下,Cu離子會生成氫氧化銅,導致其催化活性降低.在強堿性環境下,產生的易發生式(2)所示的反應,且堿性環境下·OH 的氧化還原電位比的氧化還原電位低,導致 RhB的降解能力下降.

2.2 催化劑的穩定性
為了考察催化劑的穩定性,在Cu-Mg-Ce復合氧化物投加量為 1.0g/L、PS濃度為 1.0mmol/L、RhB初始質量濃度為 10mg/L、溶液初始 pH為 5的條件下對催化劑進行5次循環實驗,結果如圖6所示.經過5次循環實驗后,RhB的去除率仍能大于97%.雖然 5次實驗后 Cu2+浸出質量濃度略有上升(最高為1.23mg/L),但仍低于國家排放標準(2.0mg/L).因此,Cu-Mg-Ce復合氧化物擁有很好的穩定性.
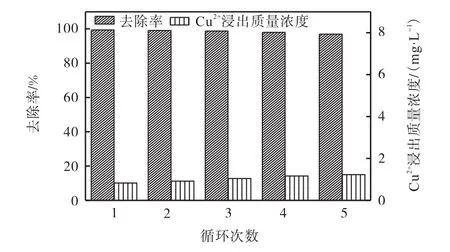
圖6 催化劑重復使用后羅丹明 B的去除率及 Cu2+浸出質量濃度Fig.6 Removal rates of rhodamine B and leaching concentration of Cu2+ with reused catalysts
2.3 Cu-Mg-Ce復合氧化物活化PS的機理
為了驗證 Cu-Mg-Ce復合氧化物活化 PS的機理,使用X射線光電子能譜(XPS)對反應前后的Cu-Mg-Ce復合氧化物進行表征.Cu的XPS譜圖如圖7所示.在使用前催化劑的譜圖中能看到 Cu在934.05eV和933.0eV處有峰值,使用后催化劑的Cu結合能產生了偏移,在934.4eV和933.05eV處出現峰值.大于933.l eV的Cu 2p3/2的峰是Cu2+的顯著特征峰.932.2~933.l eV處出現的Cu 2p3/2的峰是Cu+的特征峰.多金屬的混合導致 Cu2+產生 Cu+,Cu+活化氧化劑 PS 產生SO4·-,降解 RhB.
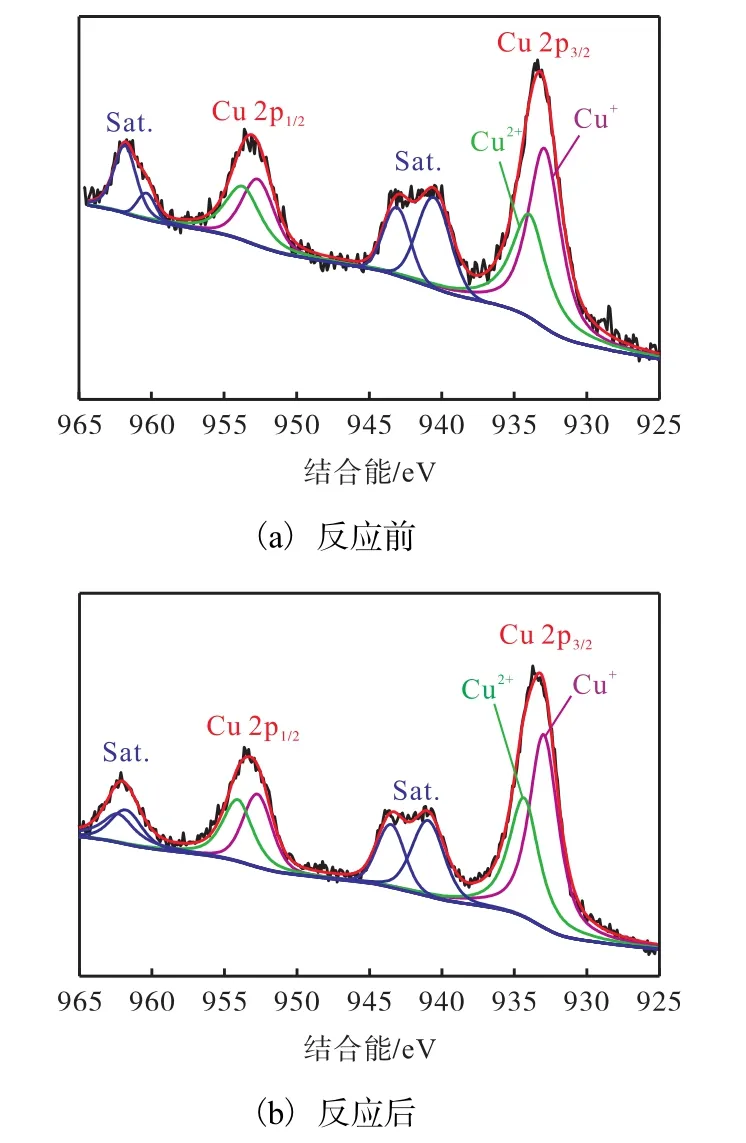
圖7 Cu-Mg-Ce復合氧化物的Cu 2p XPS譜圖Fig.7 Cu 2p XPS spectrum of Cu-Mg-Ce composite oxide
反應前后Ce的XPS譜圖如圖8所示.反應前后Ce3+和 Ce4+含量有明顯的變化,反應后催化劑中的Ce3+含量減少,Ce4+含量增大.這可能是由于在反應過程中Ce3+給出了電子,使得Cu2+變成了Cu+.
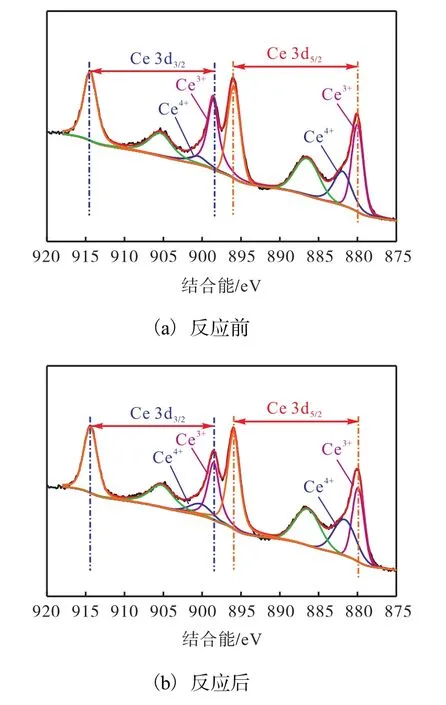
圖8 Cu-Mg-Ce復合氧化物的Ce 3d XPS譜圖Fig.8 Ce 3d XPS spectrum of Cu-Mg-Ce composite oxide
由以上分析可以看出,Cu與 Ce具有協同作用,Cu2+起主要催化作用,Ce3+是助催化劑起次要作用,Mg2+起分散 Cu2+的作用,減少其浸出[26].根據以上分析,推導出的 Cu-Mg-Ce復合氧化物活化 PS的機理如圖9所示.
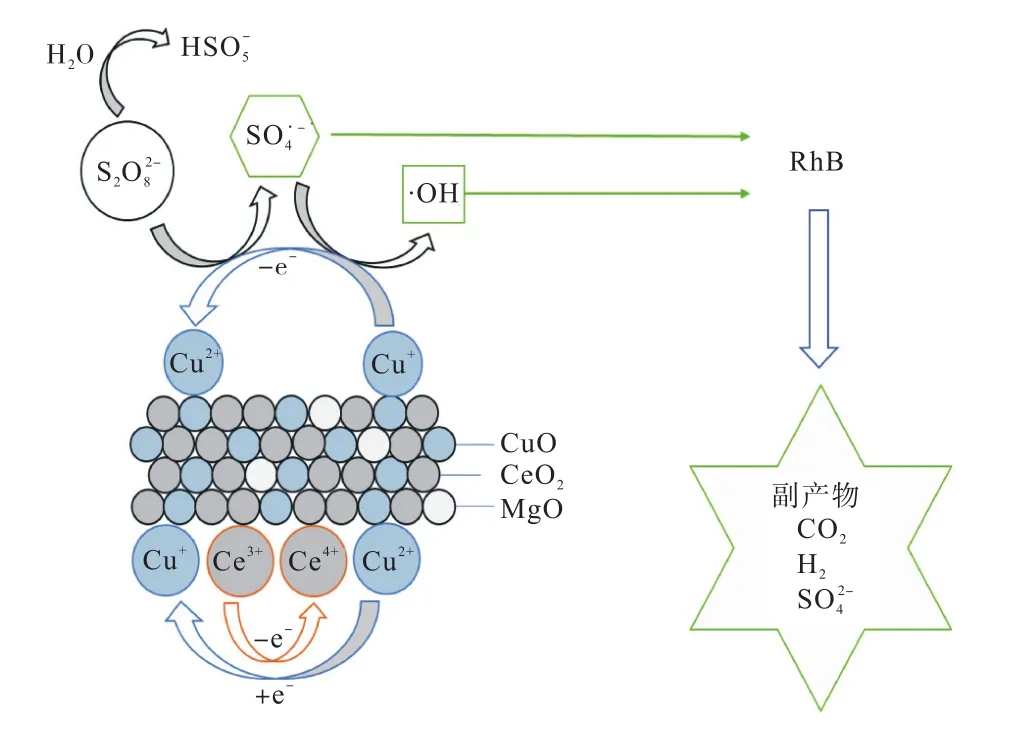
圖9 Cu-Mg-Ce復合氧化物活化 PS降解羅丹明 B機制概念圖Fig.9 Conceptual diagram of rhodamine B degradation mechanism by activated PS with Cu-Mg-Ce composite oxide
先前研究已經得出催化劑是層狀結構[27]的結論.Cu-Mg-Ce復合氧化物中Cu2+與Ce3+具有協同作用,Cu2+與 Ce3+發生電子轉移,產生的 Cu+活化 PS產生,實現RhB的降解.RhB降解過程主要是2個步驟,先是 RhB發色基團氧雜蒽和苯基之間的鍵被破壞脫色,之后苯環開環被降解成CO2[17,28].
3 結 語
Cu-Mg-Ce復合氧化物能夠協同活化過硫酸鈉高效降解羅丹明 B.催化劑投加量、底物初始質量濃度、過硫酸鈉濃度、溶液初始 pH對羅丹明 B降解有顯著影響;Cu-Mg-Ce復合氧化物投加量為 1.0g/L、氧化劑濃度為 1mmol/L、底物質量濃度為 10mg/L時,羅丹明 B去除率高達 99.47%;Cu-Mg-Ce/PS體系有效降解濃度范圍為5~20mg/L,最適宜pH范圍為5~7;催化劑能夠穩定使用5次以上,且具有很高的活性.Cu-Mg-Ce復合氧化物具有優異的催化活性、良好的穩定性,制備方法簡便且成本低廉,為今后消除其他染料污染水體提供了參考.

