miRNA的非經典作用機制研究進展
李瀟凡 耿丹丹 畢瑜林 江勇 王志秀 常國斌 陳國宏 白皓
(1.揚州大學農業科技發展研究院 教育部農業與農產品安全國際合作聯合實驗室,揚州 225009;2.揚州大學動物科學與技術學院,揚州 225009)
microRNA(miRNA)是一類在進化上較為保守的內源性非編碼單鏈RNA 分子,包含大約20-22個核苷酸,是基因表達的重要調控因子[1-2]。自發現以來,人們對其生物學功能進行了大量的研究,截至2021年12月,miRNA 數據庫(miRBase,http://mirbase.org/)的最新版本包含了近300 個物種中超過38 000 個潛在miRNA 的信息。隨著人們對miRNAs 的結構特征和成熟機制認識逐漸深入,它們在細胞中的主要功能和相關蛋白因子的范圍被確定。目前,科學界公認其功能是在細胞質中負調控基因表達[1],即編碼miRNA 的基因通過細胞核中的RNA 聚合酶Ⅱ或Ⅲ轉錄為包含5′帽子結構和3′端polyA 尾的miRNA 的前體(pri-miRNA)[3],隨后pri-miRNA 由RNAse III 酶Drosha 和輔助因子DGCR8 共同組成的復合體進一步加工以形成莖環或發夾結構前體miRNA(pre-miRNA)[4-5],并通過exportin-5[6]從細胞核運輸到細胞質,后通過Dicer酶和RNA 結合蛋白TRBP 進一步加工成miRNA 雙鏈。miRNA 雙鏈解開后,引導鏈與Argonaute(AGO)蛋白形成RNA 誘導沉默復合體(RNA-induced silencing complex,RISC),其中成熟的miRNA 通過靠近5′端的種子區與同源mRNA 3′端的堿基配對結合,進而抑制靶標mRNA 翻譯或者影響mRNA穩定性,對轉錄后基因表達水平進行負調控,該過程主要由AGO 的合作伙伴-功能蛋白GW182 介導完成[7],而雙鏈的另一條鏈則立即降解,這就是miRNA 在生物體內的經典作用機制。
如今越來越多的證據闡明了miRNA 在細胞核中的亞細胞定位[8],并研究了其在細胞穩態中的各種新功能是通過非經典作用機制進行調控[9],主要包括miRNA 前體可編碼多肽、miRNA 可與其他功能蛋白相結合、miRNA 可直接激活TLR 受體蛋白、miRNA 可提高蛋白表達水平、miRNA 靶向調控線粒體相關基因mRNA 以及miRNA 可直接調控基因轉錄過程等6 種非經典作用機制。本文針對近年來miRNA 的6 種非經典作用機制進行總結,旨在能夠更加深入和系統地理解miRNA 的非經典作用模式,為解析miRNA 在生物體內復雜的分子調控機制提供新的思路和方法。
1 miRNA 前體pri-miRNA 編碼調節肽miPEPs
成熟的miRNA 是由編碼基因(MR 基因)轉錄后經過一系列加工后所得。在轉錄過程中,primiRNA 易被剪切為pre-miRNA,且存在時間較短,因此有關于miRNA 的機制研究主要集中于miRNA成熟體方向。近期研究表明,miRNA 的前體primiRNA 可能具有潛在的編碼功能。pri-miRNA 序列的5′UTR 包含短的開放閱讀框架(small open reading frames,smORFs),能被翻譯成大小4-60 個氨基酸的功能短肽(microRNA-encoded peptides,miPEP),過表達或外用miPEP 可通過增強其相關MR 基因的轉錄,影響相應miRNA 的轉錄水平,對成熟miRNA 進行正向調控[10-11]。一般情況下miPEP 通過被動擴散和胞吞作用相關過程進入細胞進行調控,合成的miPEP(無額外的修飾和加工)也能產生相同的自動調節效果,這與通常作為配體被相關受體識別的前體衍生肽不同[12-14]。
2015年,Lauresergues 等[15]首次發現蒺藜苜蓿(Medicago truncatula)的pri-miR176 和擬南芥的primiR165a 能分別編碼短肽miPEP176 和miPEP165a,這兩個短肽增加了相應miRNA 的積累和靶基因的下調,導致側根發育遲緩并能刺激主根生長。目前通過人工合成miPEP,在大豆、葡萄等農業作物上miPEP 的調節功能都得到了驗證[11,16]。由于在人類、動物和植物中miRNA 序列都很保守,因此研究pri-miRNAs 在哺乳動物細胞中是否編碼miPEP具有重要的價值。目前已證明在人類細胞中可以編碼miPEP-200a 和miPEP-200b[17-18]。2020年,Niu等[19]研究報道人樹突狀細胞(dendritic cells,DCs)中miR-155 可以編碼多肽miPEP-155,其可以特異性地與DC 細胞的互作蛋白HSC70 的ATPase 功能域綁定,降低炎癥環境中DC 細胞MHC-Ⅱ的表達和轉運水平,調控其抗原提呈功能。
如今多項研究表明動植物細胞中的pri-miRNA具有潛在的編碼功能,能編碼出具有調控功能的短肽miPEP,miPEP 其能影響相應的miRNA 的轉錄水平,可通過增強其相關MR 基因的轉錄,對成熟miRNA 進行正向調控。
2 miRNA 可與多種功能蛋白相結合
幾十年來,RNA 互作結合蛋白(RBPs)在前體mRNA(pre-mRNA)剪接、mRNA 移動、mRNA分解和翻譯中的作用均被廣泛研究[20-22]。一般認為,成熟的miRNA 與AGO 蛋白復合體組成一個RISC 復合物,結合并調節含有相關順式調控元件的靶標mRNA 的表達[23]。在此過程中,AGO2 蛋白及其家族蛋白(AGO1、AGO3 和AGO4)被認為是專門處理和裝載具有獨特結構特征的miRNA 的RBP[24]。近期研究表明,有少數功能蛋白(miRBPs)與AGO2 蛋白功能相似,也可以與成熟的miRNA結合[25-26]。
2012年有研究報道,在HeLa 細胞中miRNA的表達量是AGO 家族蛋白的13 倍,而miRNA 與mRNA 的結合量是AGO 家族蛋白的7 倍[27],這種“過量”miRNA 分子在細胞中的作用仍不清楚,而維持miRNA 的濃度和穩定性已被證明涉及許多RNA結合蛋白,例如HuR 和AUF1[28]。這些研究結果表明除AGO 蛋白家族外,miRNA 還可與其他功能蛋白結合發揮非經典調控途徑。Mukherjee 等[29]研究發現,HuR 可以從AGO2 中競爭性結合mir-122,并在自身泛素化作用下從結合狀態中脫離,來調節mir-122 的胞外輸出。Eiring 等[30]研究發現,mir-328 除了發揮正常負調控功能,還可以競爭性結合hnRNP E2 蛋白來阻礙其與CEBPA 蛋白的mRNA 結合,導致了CEBPA 核轉錄因子表達量上升。除了競爭性結合,也有一些研究支持miRNA 與AGO 和miRBPs三者之間存在合作性結合:如UF1 與let-7 的直接結合有助于其在體外以單分子水平轉移至AGO2[31-32],HuR 可以增加let-7 與AGO2 的結合量[31]。Song等[33]研究發現mir-346 的中間序列基序(CCGCAU)可以與GRSF1 相結合,再與hTERT 3′UTR 結合時形成“鼓包環”,促進hTERT mRNA 向核糖體的聚集從而上調hTERT 的表達,以獨立于AGO2 調節的方式促進翻譯。另外,除了成熟的miRNA,premiRNA 也可以與功能蛋白相結合[34]。
可以看出,成熟miRNA 和pri-miRNA、premiRNA 能與多種功能蛋白相結合,并存在多種結合方式,如可逆性結合、競爭性結合和合作性結合等,發揮非經典調控途徑,展現出miRNA 調控細胞命運的雙重控制能力。
3 miRNA 可作為信號分子直接激活TLR 受體蛋白
如今普遍認為,miRNA 能夠感知Toll 樣受體(Toll-like receptor,TLR),特別是核內受體TLR7 可以被大腦中存在的miRNA 直接激活,miRNA 作為信號分子在不影響受體蛋白量的情況下發揮作用。早期研究報道,細胞外的let-7 能激活TLR7,并通過神經元TLR7 誘導神經變性[35]。游離的細胞外miRNA let-7b 可以激活小鼠巨噬細胞和小膠質細胞中的TLR7 信號,誘導腫瘤壞死因子-α(tumor necrosis factor,TNF-α)的產生導致神經元死亡,這種效應在TLR7 缺乏的細胞中并不存在[35]。
目前研究表明,游離miRNA 進入細胞并到達核內體誘導信號傳導主要受兩方面因素影響:一方面是miRNA 需要被包裹在某些類型的載體里以保護它們在到達核內體的過程中免受降解,有研究發現,猿猴免疫缺陷病毒誘導的腦炎模型腦中的細胞外囊泡(EVs)中miR-21 水平升高,并且miR-21可以通過TLR7 發出信號誘導神經毒性[35]。通過將miRNAs 與陽離子脂質體如1,2-二油酰-3-三甲基銨- 丙烷(DOTAP)、lipofectamine 或LyoVec 相絡合來模擬EVs 的作用,將細胞暴露于這些絡合物中,能發現miRNAs 位于TLR7/8 附近的核內體中。研究表明在巨噬細胞中,與DOTAP 復合的miR-21和miR-29a 通過小鼠TLR7 和人TLR8 發出信號,誘導TNF-α 和IL-6 的產生[28],而未與DOTAP 結合的游離miRNA 在體外不會誘導TNF-α 的產生。另一方面研究發現,miRNA 序列特定位置的某些核苷酸會影響TLR 的激活[28]。Wu 等[36]認為具有特定序列基序和長度的細胞外miRNA 是有效的TLR7 激活劑,可以觸發先天免疫反應。其中U 和C 對TLR7 活化起到關鍵作用,并鑒定出兩個由10 個核苷酸組成的miRNA 序列UGCUUAUAGU 和GUGCUUAUAG,可以刺激TNF-α 的產生,這是已知激活TLR7 的最短ssRNA 序列。
TLR7 是導致中樞神經系統損害擴散的途徑中的一個基本要素,miRNA 的這種作用機制與腫瘤—免疫系統的通訊有關,在腫瘤生長和擴散中起到關鍵作用,具有重要的研究意義。
4 miRNA 可上調蛋白表達水平
基因表達調控是一個復雜而有序的過程,包括有多種水平的調控,其中轉錄后水平的調控起著不可忽視的作用。在該過程中,miRNA 主要作為抑制劑來影響mRNA 穩定性及翻譯效率,下調蛋白表達水平。但最近的一些研究揭示了miRNA 在翻譯過程中對mRNA 穩定性及翻譯效率起到積極作用,達到上調蛋白表達水平的效果[37-38]。
研究發現,位于一些mRNA 3′UTR AU 富含元件(AU-rich element,ARE)是能在轉錄后水平調節mRNA 穩定性的元素之一,它兼具介導相關因子mRNA 衰變及增強某些mRNA 穩定性的作用。Vasudevan 等[39]首先發現在細胞周期停滯時,miRNAs 可以通過招募AGO 和FXR1 到靶標mRNAs的ARE 區域來激活翻譯。而let-7 可以和人工合成的mircxcr 4 在細胞周期阻滯中協同促進靶標mRNA的翻譯上調,但在細胞增殖過程中抑制翻譯,即其翻譯調控隨細胞周期的變化在抑制和激活之間波動。與此相似,AGO2-miR369-3p 復合物可以結合TNF-α ARE 招募FXR1,從而刺激TNF-α 的翻譯[39],而miR-125b 可以通過防止ARE 降解來增強κB-Ras2 mRNA 的穩定性和表達[40]。除了與3′UTR 的ARE的結合之外,miRNA 還可以通過與mRNA 的5′UTRs相互作用來促進mRNA 翻譯。如miR-10a 通過與核糖體蛋白mRNA 的5′UTRs 相互作用來增強mRNA的翻譯[41];miR-346 除了與3′UTR 結合激活翻譯之外[42],還可以通過靶向RIP140 mRNA 的5′UTR 來提高RIP140 蛋白水平[43];miR-483-5p 也被證明可以通過與IGF2mRNA 的5′UTR 結合來促進IGF2 轉錄[44]。此外,在實際生產中有研究結論表明miRNA可能在mRNA 轉錄后調節過程中起到作用,如ggamiR-222a 能上調兩個蛋氨酸合酶基因Odosp_3416 和BF9343_2953 的表達,增加蛋氨酸濃度[45],在植物中,干旱脅迫條件下miRNA-156能上調花青素基因表達,形成多酶復合物,該復合物將在粗面的內質網(RER)的胞質面合成更高水平的花青素,從而提高抗干旱脅迫能力[46]。
miRNA 在發揮抑制劑作用的同時,也能夠在翻譯過程中起到上調靶向mRNA 表達作用,其可以通過招募功能蛋白到靶標mRNAs 3′UTR 的ARE 區域或5′UTRs 來激活翻譯,上調蛋白表達水平。
5 miRNA 靶向調控線粒體相關基因mRNA
Mitochondrial microRNA(mitomiRs)指位于線粒體內部的miRNA,它們絕大部分由核基因組編碼并轉移至線粒體的miRNA,在線粒體內轉錄并調節線粒體基因表達。還存在少部分由線粒體基因組直接編碼合成的miRNA[47-48],這些mitomiRs 的功能與細胞質定位的miRNA 存在差異。
對于核來源mitomiRs,普遍認為核編碼的miRNA 成熟后進入線粒體抑制線粒體轉錄物的翻譯[47,49]。研究發現,miR-181c 作為核來源miRNA定位于新生大鼠心室肌細胞線粒體中,可以與來自線粒體基因組的細胞色素c 氧化酶亞基1(mt-COX1)mRNA 的3′UTR 相結合,過表達miR-181c 可以顯著降低mt-COX1 蛋白水平[50]。Fan 等[51]研究發現,核來源的miR-2392 可以穿梭到線粒體中并與mtDNA雜交,下調調控癌癥中氧化磷酸化、代謝重編程和化學抗性的基因。此外,有研究發現在肌肉分化過程中,miR-1 可以通過與特異性mRNA 堿基互補配對來促進線粒體基因組轉錄物的翻譯,在該過程中miR-1 只需要與AGO2 結合,功能蛋白GW182并沒有參與[52]。隨著研究進一步深入,發現這些mitomiRs 在缺乏線粒體DNA 的細胞中不表達,如在針對人正常前列腺上皮細胞(PNT1A)的野生型(WT)和mtDNA 缺失型(Rho0)細胞中mitomiRs 的表達水平研究發現,mitomiRs 在Rho0 型PNT1A 細胞中的表達水平顯著低于其在WT 型PNT1A 細胞中的表達水平[53]。對于線粒體來源的miRNA 研究相對較少,目前在人類和哺乳動物中已檢測到線粒體來源miRNA[53-54],在人類和小鼠的線粒體基因組也存在編碼類似miRNAs 的mitomiRs[55]。尚未檢測到線粒體內存在由miRNAs 介導的翻譯抑制過程中必須的功能蛋白GW182,這與前文中的研究結果相照應[52-53],miRNA 加工蛋白Drosha 和DGCR8 也未檢測出;Dicer 酶同樣被證實不存在于線粒體中[53],該結論在小鼠心肌細胞也被證實[56]。但Vargas等[57]研究報道pre-miR-338 和Dicer 酶可以在SCG神經元軸突線粒體中共定位。
多項研究表明線粒體功能障礙與心腦血管疾病及癌癥等有關,miRNA 在細胞特異性表達表明他們有可能參與線粒體相關疾病,這無疑為線粒體ncRNA 調控網絡的研究指明了方向,有助于更全面的理解線粒體生物學,未來對mitomiRs 分布和功能的具體機制的研究可以確定新的藥物遞送途徑和線粒體生物標志物,有助于更好地理解線粒體功能障礙相關疾病的診療和治療方法。
6 miRNA 可直接調控基因轉錄過程
在miRNA 經典調控途徑中,成熟的miRNA 通常在細胞質中形成RISC,與靶標mRNA 的3′UTR堿基配對,靶點選擇主要由miRNA 5′UTR 序列決定,對細胞質中的蛋白質合成進行抑制[58-59]。有不同研究表明,miRNA 包含的額外序列元素可以改變它們的亞細胞定位進而調控它們的轉錄后行為,即miRNA 也可以在細胞核中發揮作用,來自高通量測序的數據甚至預測了核miRNA 的基因組DNA 結合位點,這可能在miRNA 轉錄調控研究中發揮作用[60]。
在細胞核中已證實存在miRNA 作用機制所需的成分,比如AGO2 和Dicer 酶,但在細胞核和細胞質之間的機制不同。其中,核RISC 蛋白分子量158 kD,相較于核RISC 平均3 MD 的分子量要小很多,成分有所缺失,僅由AGO2 和一個短RNA 形成[61]。因此普遍認為AGO2/miRNA 復合物可以在細胞核外構成,形成的RISC 復合物可進入細胞核內[62]。核-細胞質運輸也由Exportin-1 介導[63],由miRNA 序列中特定核定位信號(AGUGUU基序、5′-UUGCAUGU-3′和5′-AGGUUGKSUG-3′基序等)指導富集[64-65],再由核孔蛋白泵入到細胞核內進行修飾[66],與靶基因啟動子區域相互作用直接激活轉錄過程,如在AGO2 和GW182 作為支架參與的情況下,miR-589可結合環氧化酶-2(COX-2)啟動子并激活基因轉錄[67];miR-744 和miR-1186 通過靶向cyclinB1 基因啟動子上調Ccnb1 基因的表達[68],這種小RNA 參與的通過結合啟動子區域在轉錄水平激活基因的現象被稱為RNA 激活(RNAa)。此外miRNA 也可以靶向負調控其他非編碼RNA 的前體RNA,如miR-709 可以與pri-miR-15a 和pri-miR-16-1 結合,阻止它們的進一步加工以調節小鼠細胞的凋亡[69]。miR-122 可以通過與核蛋白結合來阻止pri-miR-21 的成熟[70],近年來有研究發現,NamiRNAs(核激活miRNAs)能夠激活增強子,如miR-24 可以改變增強子位點的染色質狀態,使組蛋白修飾H3K27ac 富集在miR-24 靶向的增強子區域,該過程依賴增強子的完整性;miR-26a-1 在400 kb 的窗口中被蛋白質編碼基因ITGA9 和VILL 包圍,過表達的情況下能激活其轉錄[71]。綜上可以看出miRNA 與增強子相互作用能調節基因表達和細胞穩態,然而miRNA 增強子相互作用機理和功能的分子機制仍有待進一步挖掘。
除卻自細胞核轉移至細胞質發揮作用的經典調控途徑,部分miRNA 還可以依照自身額外的序列改變亞細胞定位從而調控自身的轉錄后行為,即在細胞核內調控基因轉錄過程,發揮非經典調控作用。
7 問題與展望
本文重點闡述了6 種miRNA 非經典作用機制及其研究進展,在實際研究中仍有其他的非經典調控途徑被科學家們所關注,如miRNA 可以與細胞核中的pri-miRNA 結合來阻止它們的進一步加工[69,72],但其作用機制仍需深入研究,是今后miRNA 研究的一個重要方向;還有研究發現在細胞內同一條信號轉導通路上,miRNA 可以同時通過其種子區序列和非種子區序列與靶基因/轉錄因子的3′端結合[73-74],這種功能機制可以達到更加有效且穩定的基因調控作用,對以miRNA 為靶點的多種疾病治療提供了新的思路和方法。另外,通過對miRNA 的亞細胞定位,在內質網[75]和無細胞質膜的小室(如SGs)[76]中都檢測到了miRNA,這些miRNA 可能是調節特定生物過程和腫瘤發生所必需的,對研究細胞適應性具有重要意義。然而,由于相關研究較少,位于不同亞細胞區室的miRNA 的組織、運輸和功能在很大程度上是未知的,在本文中并未詳細闡述。
近年來,miRNA 在許多重要生物過程中得到了研究者的廣泛關注。miRNA 的結構、基因組編碼、表達和成熟方式等方面的許多具體特征已被闡明,參與的事件范圍在經典調控途徑的基礎上逐步擴大,這為我們揭示了一片新的圖景(圖1)。可以看出多數非經典調控機制都涉及到miRNA 的亞細胞定位,其中miRNA 前體可編碼多肽、miRNA 可直接激活TLR 受體蛋白、miRNA 靶向調控線粒體相關基因mRNA 以及miRNA 可直接調控基因轉錄過程都與miRNA的亞細胞定位有關。自從發現miRNA以來,由于技術限制,它們的亞細胞定位在很大程度上被忽視。盡管在分離純亞細胞組分和基于免疫熒光的精確定位分析方面仍存在一些技術困難,但積累的研究為miRNA 的亞細胞定位和新的miRNA 調控機制提供了廣闊的視野,測序技術的進步已經確定大量miRNA 富集于細胞核和多種細胞器中,他們的高豐度表明了miRNA 在轉錄和轉錄后調節中存在重要功能作用。
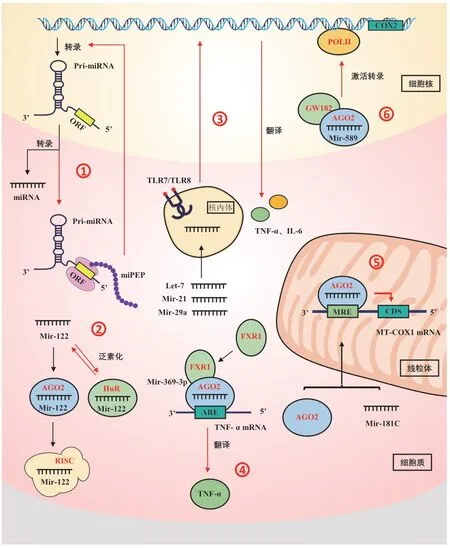
圖1 miRNA 非經典作用機制Fig.1 Unconventional miRNA functions
但受制于目前多數動植物基因組、轉錄組、蛋白質等信息的匱乏以及技術手段的限制,調控機制的某些關鍵節點和細節仍沒有得到答案,比如在primiRNA 編碼調節肽miPEPs 中,miPEP 如何執行他們的生物學功能,與其對應的pri-miRNAs 的上調是否有特異性;pri-miRNA 的細胞質翻譯和miRNA 的核成熟能否同時發生,pri-miRNA 如何協調其編碼和非編碼過程;在miRNA 作為信號分子進入細胞并到達內體誘導信號傳導的機制并不清楚,誘導miRNA激活TLR7 激活的基序尚未確定;mitomiRs 易位進入線粒體調控的具體機制還存在爭議,mtDNA 編碼的miRNAs 是否存在非典型的生物發生機制依然存疑,無法證明這些miRNA 是否來自mtDNA 編碼,還是污染副產物,或是線粒體中存在另一套RNA 干擾機制。另外,大多數調控機制僅停留在研發階段,植物研究多集中在擬蘭芥和苜蓿等模式植物上,其他植物上少見報道,而動物上使用人類和小鼠細胞系進行研究,未進行到臨床試驗階段(表1)。相信實驗技術的精進和研究的深入,miRNA 及其他小RNA 分子參與的表達調控機制的網絡會逐步明晰,這將有利于我們進一步了解生物體內部的運作機制,為研究miRNA 在調控基因表達和功能中的作用及其機制打開了新的窗口,釋放其在人類和動植物上重大的應用潛能。

