負壓封閉引流技術聯合系統性濕性療法治療Ⅳ期壓瘡效果分析
張冰
(廣東醫科大學附屬醫院,廣東 湛江 524023)
壓瘡好發于老年、水腫、長期臥床、營養不良、骨折等患者,是常見局限性損傷[1],雖然目前臨床致力于預防壓瘡,但是壓瘡發生率仍居高不下[2]。壓瘡是一項全球性健康問題,不僅會增加患者身心痛苦,也會延長住院時間,提升醫療成本,降低生活質量,甚至會誘發感染等多種并發癥,導致患者死亡,特別是Ⅳ期壓瘡深達皮膚全層,或是累及骨骼、肌腱等,造成傷口經久難愈,危害較大。以往常對Ⅳ期壓瘡患者采用干性療法,但對于滲液量巨大、存在壞死組織的患者效果有限。系統性濕性療法以濕性愈合環境理論為依據,強調以活性敷料營造微酸、無氧、濕潤的利于傷口愈合的微環境[3],從而加速傷口愈合。負壓封閉引流技術(VSD)首創于1993年,之后被用于處理各種急慢性傷口[4],亦取得理想療效。本文觀察了VSD聯合系統性濕性療法對Ⅳ期壓瘡患者的臨床效果,報告如下。
1 資料與方法
1.1 一般資料
選擇2020年1月—2022年2月Ⅳ期壓瘡患者40 例,按照隨機方式分為觀察組和對照組,每組20 例。對照組男 8 例,女12 例;年齡(68.8±4.5) 歲;髖部1 例,骶尾部8 例,臀部6 例,大轉子2 例,背部3 例。觀察組:男7 例,女13 例;年齡(69.3±4.4) 歲;髖部2 例,骶尾部7 例,臀部5 例,大轉子3 例,背部3 例。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2 納入和排除標準
納入標準:依據美國國家壓瘡咨詢委員會(NPUAP)的相關標準確診為Ⅳ期壓瘡;患者知曉研究,自愿參與。排除標準:治療期間因免疫性疾病、出血性疾病等中斷治療者;合并糖尿病者;依從性差,無法完成療程者;有通往器官、胸腔的瘺管患者;對所用敷料過敏者;因認知、精神障礙無法配合治療者。
1.3 方法
對照組采用系統性濕性療法。干燥壞死期:先行清創,之后外貼水膠體敷料;潰瘍滲出期:覆蓋黏性敷料+藻酸鹽敷料+凝膠填塞,并且每日換藥;肉芽組織期:覆蓋無菌紗布,填塞凡士林油紗+康倍,隔日換藥;上皮形成期:外貼薄型水膠體敷料。
觀察組采用VSD聯合系統性濕性療法。干燥壞死期以及上皮形成期:同對照組;潰瘍滲出期、肉芽組織期:行VSD治療,準備一次性負壓引流護創材料(山東創康生物科技有限公司;產品注冊號:國械注準20183661697),儀器為電動負壓吸引器。評估且記錄創口深度、腔道方向、創口面積、滲液量;清創、涂抹皮膚保護膜;參照傷口愈合世界聯盟指南建議,選用間歇模式,設定中心負壓-125 mmHg(1 mmHg≈0.133 kPa),待肉芽組織生長良好、每日引流量不足15 mL時拔除VSD管。
1.4 觀察指標
壓瘡愈合計分表(PUSH)評分:含有滲液量[無(0 分)、少量(1 分,<5 mL/24 h)、中量(2 分,5~10 mL/24 h)、大量(3 分,>10 mL/24 h)]、面積(由小到大為0~10 分)、組織類型(包括肉芽組織、壞死組織等,計0~4分)[5],評分高則提示傷口惡化。
視覺模擬評分法(VAS):借助刻有數字、長10 cm的游標卡尺評估疼痛程度,“0”表示“無痛”,“10”表示“劇痛”,在患者選擇出代表自身疼痛程度的數字后,醫生予以記錄[6]。
創面面積:更換敷料時,以鑷子、棉簽、數碼尺等工具測量創面寬度、長度,再計算創面面積。
血紅蛋白(Hb)、紅細胞計數(RBC)、白細胞計數(WBC):取3 mL靜脈血,測定Hb,RBC,WBC[7]。
血清炎性因子:采集血液檢測白細胞介素-6(IL-6)、腫瘤壞死因子-α(TNF-α)。
臨床治療參數:評價肉芽組織增生時間、住院時間、換藥次數、治療費用[8]。
創面恢復情況如下。差:肉芽組織生長情況差,創面有大量壞死細胞組織,顏色暗淡;中:肉芽組織生長情況一般,創面有少量壞死細胞組織,顏色為紅色略暗;良:肉芽組織生長良好,創面無壞死細胞組織,顏色為紅色;優:新生肉芽組織豐富,創面為亮紅色;創面恢復優良率=(優+良)例數/總例數×100%[9]。
并發癥發生率:記錄并發癥例數、類型。
1.5 統計學方法

2 結 果
2.1 兩組PUSH和VAS評分及創面面積比較
治療前,兩組PUSH評分、VAS評分和創面面積比較,差異無統計學意義(P>0.05)。治療后,兩組PUSH評分、VAS評分低于治療前,且觀察組低于對照組,差異有統計學意義(P<0.05);兩組創面面積小于治療前,且觀察組小于對照組,差異有統計學意義(P<0.05)(見表1)。
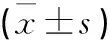
表1 兩組PUSH評分和VAS評分及創面面積比較
2.2 兩組Hb和RBC及WBC比較
治療前,兩組Hb,RBC,WBC比較,差異無統計學意義(P>0.05);治療后,兩組Hb和RBC高于治療前,且觀察組高于對照組;兩組WBC低于治療前,且觀察組低于對照組,差異均有統計學意義(P<0.05)(見表2)。
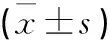
表2 兩組Hb和RBC及WBC比較
2.3 兩組血清炎性因子比較
治療前,兩組IL-6和TNF-α比較,差異無統計學意義(P>0.05);治療后,兩組IL-6和TNF-α低于治療前,且觀察組低于對照組,差異有統計學意義(P<0.05)(見表3)。

表3 兩組血清炎性因子比較
2.4 兩組臨床治療參數比較
觀察組肉芽組織增生時間、住院時間短于對照組,換藥次數、治療費用少于對照組,差異有統計學意義(P<0.05)(見表4)。

表4 兩組臨床治療參數比較
2.5 兩組創面恢復情況比較
觀察組創面恢復優良率為90%,高于對照組的60%,差異有統計學意義(P<0.05)(見表5)。

表5 兩組創面恢復情況比較 單位:例(%)
2.6 兩組并發癥發生率比較
觀察組并發癥發生率為5%,低于對照組的30%,差異有統計學意義(P<0.05)(見表6)。

表6 兩組并發癥發生率比較 單位:例(%)
3 討 論
壓瘡是摩擦力、剪切力、壓力合作的結果,臨床依據壓瘡所致軟組織損傷的解剖學深度進行系統分期[10],旨在指導診斷與治療。以往常對壓瘡患者采用干性療法,該法通過暴露感染的創口,使其脫水干燥結痂,之后借助植皮、手術切痂等清除失活組織,促進創口愈合,亦或是通過使用藥物、乙醇濕敷;或借助濕到干的方法,促進炎癥消退,加強引流滲液,縮短創口愈合時間。不過對于滲液量巨大、有竇道或潛行難以引流、存在壞死組織、肌腱/骨外露壞死等造成的Ⅲ期、Ⅳ期壓瘡而言,上述方法效果欠佳。研究發現[11],濕性療法、VSD能夠有效治療Ⅲ期、Ⅳ期壓瘡患者,其中濕性療法有循證依據支持,加之無痛、微創,患者接受度較高,而VSD能夠形成密閉環境、增加組織灌注、清除細菌、減輕創口及周圍水腫,最終促進創口愈合。
本研究表明,VSD聯合系統性濕性療法對Ⅳ期壓瘡患者有較好療效。第一,系統性濕性療法結合患者壓瘡及皮膚狀況、敷料特點、成本、治療目標選用恰當敷料,能夠取得理想的濕性治療效果,例如Ⅰ期、Ⅱ期壓瘡損傷程度較輕,通常選用泡沫敷料、水凝膠、水膠體等,能夠促進創口上皮化;Ⅲ期、Ⅳ期壓瘡,則需結合各階段治療目標選用敷料。初期以清創為主,可以選用水凝膠敷料,通過發揮自溶作用實現清創目的,有助于保護暴露的骨骼、肌腱,促進創口愈合,而選用含銀敷料重在控制創口感染,適用于嚴重定植、感染、高危感染類壓瘡,不過需避免持久使用。一旦創口滲液量巨大,需使用藻酸鹽敷料,該類敷料可吸收滲液,加之具有止血功能,能夠促進肉芽組織生長,但單用系統性濕性療法作用有限。近年來,VSD的優越性逐漸得到臨床認可。本研究結果顯示,觀察組PUSH,VAS評分和創面面積、臨床治療參數、創面恢復情況更佳(P<0.05)。分析原因為:一是VSD能夠改善創口血流,該法憑借在創口提供物理負壓,能夠在創口床及周圍組織產生壓力梯度[12],提高創口血流灌注,擴張微血管,促進血管內皮細胞功能、結構、形態改變,加速分泌血管活性因子,促使毛細血管口徑擴大,最終增加創口床血流量,而濕性療法僅能對創口床起到保持低氧、濕潤環境的作用,并不能改善創口血流;二是VSD借助對創口的機械牽拉力還能縮小創口,主要是創口承受物理負壓時,容易因機械牽拉力而向中心聚攏,從而減弱創口邊緣張力[13],縮小創口面積,同時該機械力也能對細胞增殖、復制產生刺激,加速肉芽組織生長,減少創口深度及面積;三是VSD能改善創口周圍組織水腫,因為當創口周圍組織承受物理負壓時,將會降低其組織壓力,減輕微血管后負荷,促進血液流動,清除創口局部堆積的緩激肽、5-羥色胺、組胺、前列腺素等炎性因子,降低血管通透性,減輕周圍組織水腫,并且VSD也能促進血管內皮細胞間連接,提高血管基底膜完整性,進而減少組織水腫,但是濕性療法重在通過吸收過多滲液、借助敷料所含活性成分等減輕組織水腫[14]。第二,清創壓瘡創面時能夠清除大部分感染壞死物質,不過仍存在感染情況,且創口內部還有混合肉芽組織(既有致病菌也有軟組織活力),若不徹底清創,容易加重出血,擴大創面,降低后期創面愈合難度,而加用VSD時可以吸走創面細菌與分泌物[15],使留存下的感染組織逐漸成為無菌新鮮肉芽組織,從而控制創面感染,促進肉芽組織生長,提升Hb和RBC,降低WBC。第三,IL-6是促炎癥介質,對炎癥反應、免疫應答反應有重要作用;TNF-α產生于T細胞、巨噬細胞,能夠參與炎癥反應,導致血管功能紊亂或損傷內皮細胞,加重炎癥損害,影響血液循環。本研究顯示觀察組IL-6和TNF-α低于對照組(P<0.05),可能是因為VSD聯合系統性濕性療法能夠清理分泌物及壞死組織,抑制細菌繁殖,故能降低炎癥介質表達水平。第四,本研究顯示觀察組并發癥發生率低于對照組(P<0.05),表明加用VSD還能減少并發癥發生,可能與VSD能夠盡快促進創口愈合有關。
本研究病例數相對偏少,尚需擴大樣本量進一步了解VSD聯合系統性濕性療法的臨床應用價值。

