基于網絡藥理學和分子對接探討腎衰寧治療糖尿病腎病的有效成分及作用機制
王 娜,梁建慶,馮 鑫,楊偉杰,張媛媛
(1.甘肅中醫藥大學基礎醫學院,甘肅 蘭州 730000;2.甘肅中醫藥大學附屬醫院內分泌科,甘肅 蘭州 730000)
糖尿病腎病(diabetic nephropathy,DN)是糖尿病最重要的全身微血管病性合并癥之一,初始表現為早期腎小球超濾過出現微量蛋白尿,隨病程進展出現持續大量蛋白尿、高血壓、水腫,腎小球濾過率降低進而腎功能不全。近年來,我國糖尿病患病率顯著增加,全國有20%~40%的糖尿病患者合并DN,且目前已成為慢性腎臟病(CKD)和終末期腎病的主要原因[1]。隨著中西醫結合治療在DN 的廣泛應用,中醫藥在減輕臨床癥狀、保護腎功能方面展現出越來越大的優勢,與此同時中醫藥在治療DN 的基礎研究成果不斷涌現,研究領域也逐漸細化[2-4]。既往研究證實[5-8],腎衰寧有抑制炎癥、改善腎功能及機體營養狀態、提高機體免疫功能的作用。但對于腎衰寧治療DN 的機制的研究局限于單個分子或單條途徑的實驗室研究,中藥復方治療疾病是多靶點、多途徑而實現,單個分子及途徑難以全面解釋。本研究通過構建“藥物-成分-靶點-疾病”網絡圖,探尋腎衰寧治療DN 的潛在靶點和活性成分,并結合分子對接技術驗證篩選出的活性成分與其靶點蛋白的親和關系,預測此復方治療DN 的作用機制,為腎衰寧治療DN 提供科學依據,現報道如下。
1 資料與方法
1.1 腎衰寧有效成分的篩選 利用中藥系統藥理學分析平臺數據庫(https://tcmspw.com/tcmsp.php),設置口服生物利用度(oral bioavailability,OB)≥30%、類藥性(drug-likeness,DL)≥0.18,對“丹參、大黃、太子參、黃連、牛膝、半夏、紅花、茯苓、陳皮、甘草”的有效成分及相關靶點進行篩選,并將靶點基因全稱轉換為簡稱。
1.2 腎衰寧作用靶點與DN 疾病靶點的預測 以“diabetic nephropathy”為關鍵詞在GeneCards(http://www.genecards.org/)數據庫進行檢索,得到DN 相關疾病靶點。將腎衰寧有效成分對應靶點與DN 相關疾病靶點導入Venny 2.1.0 取交集,交集靶點即腎衰寧治療DN 作用靶點。
1.3 構建“藥物-成分-靶點-疾病”網絡 將藥物和疾病的交集基因輸入Cytoscape 3.8.0 軟件中,構建“藥物-成分-靶點-疾病”可視化網絡圖,利用cytoNCA插件對網絡圖節點進行分析,標明的每個節點的屬性即為腎衰寧治療DN 的有效成分。
1.4 蛋白-蛋白相互作用網絡的構建與分析 將獲得的藥物-疾病交集靶基因文件數據導入STRING(http://string-db.org),并將物種限定為“homo sapiens”。選取置信度高于0.95 的數據,完整構建腎衰寧的蛋白相互作用PPI 網絡,根據網絡中基因與鄰接基因的數目,找出網絡的核心基因。
1.5 GO 和KEGG 富集分析 將上述藥物-疾病交集靶基因使用R 語言包bioconductor 包(http://www.bioconductor.org/)分別進行GO 分析通路KEGG 分析,設定富集分析統計學過濾值(P-value=0.05,Q-value=0.05),篩選結果以生成圖表進行可視化。
1.6 分子對接 選擇PPI 網絡中度值前3 的靶點及藥物活性成分,于Pubchem 數據庫找尋活性成分3D 構象,使用RCSB 數據庫比對活性成分相似配體,篩選出靶蛋白構象結構,導入PyMOL 軟件,去除水分子、分離原有配體及各項優化,將優化后的靶蛋白導入AutoDockTools-1.5.6,使對接位點選擇以原有配體為中心,設置網格箱(gird box)為默認值,使用AutoDock 模擬活性成分與靶蛋白分子對接,將結果輸出并進行分析。采用PyMoL 軟件對靶點蛋白和小分子進行可視化處理。
2 結果
2.1 腎衰寧活性成分的篩選 通過TCMSP 數據庫檢索,以“OB≥30%和DL≥0.18”為條件篩選后得到丹參54 個、大黃6 個、太子參3 個、黃連10 個、牛膝12 個、半夏11 個、紅花16 個、茯苓15 個、陳皮5個、甘草85 個,共得到腎衰寧有效成分217 個。
2.2 腎衰寧作用靶點與DN 疾病靶點信息 利用TCMSP 數據庫預測得到的腎衰寧成分靶點經Uniprot 數據庫基因注釋后得到的Symbol 文件共241 個注釋基因;通過GeneCards 數據庫檢索后得到3397 個與DN 相關的基因,取腎衰寧與疾病的交集靶點,共獲得161 個交集基因,見圖1。
圖1 藥物成分與疾病的交集基因
2.3 “藥物-成分-靶點-疾病”網絡 利用Cytoscape 3.7.2 繪制腎衰寧治療DN 的“藥物-成分-靶點-疾病”網絡圖,共含有355 個節點和2722 條邊,見圖2;通過CytoNCA 分析發現腎衰寧中前10 的活性成分為槲皮素(quercetin)、木犀草素(luteolin)、山奈酚(kaempferol)、黃芩素(baicalein)、β-谷甾醇(betasitosterol)、柚皮素(naringenin)、豆甾醇(stigmasterol)、漢黃芩素(wogonin)、丹參酮ⅡA(tanshinone iia)、川陳皮素(nobiletin)。

圖2 腎衰寧治療DN 的“藥物-成分-靶點-疾病”網絡圖
2.4 PPI 網絡 將共有靶點基因輸入STRING 網站,基因類型選擇人類(homo sapiens)并設置最小關系值≥0.95,刪除無連接節點,生成藥物-疾病共有靶點PPI 網絡,將結果導出,輸入cytoscape3.8.0 軟件,進行拓撲參數分析,得出PPI 網絡共17 個節點、84 條邊,其中度值排名前10 位的靶蛋白為JUN、MYC、FOS、STAT3、MAPK14、HIF1A、ESR1、AKT1、CCND1、MAPK3,見圖3。

圖3 藥物-疾病共有靶點PPI 網絡圖
2.5 靶蛋白的富集分析
2.5.1 GO 富集分析 將藥物-疾病共同靶點輸入R語言bioconductor 包中,分別進行分子功能、生物途徑功能、細胞成分3 方面的GO 富集分析,取排名前10 的條目制作條形圖(圖4),其中靶蛋白分子功能主要集中于RNA 聚合酶Ⅱ-特異性DNA-結合轉錄因子結合、核受體活性、配體-激活轉錄因子活性、細胞因子活性、細胞因子受體結合、轉錄共激活因子的結合、磷酸酶結合、血紅素結合及轉錄輔助因子結合等方面;細胞組成涉及膜筏、膜微域、膜區、等離子膜筏、囊泡腔、RNA 聚合酶Ⅱ轉錄調控復合物、轉錄調節因子復合物、細胞質囊泡腔及內質網腔得組成成分等方面;生物過程涉及對氧化應激反應、細胞對化學應激的反應、對活性氧的反應、細胞對氧化應激的反應、類固醇激素反應、脂多糖反應、對細菌來源的分子的反應、活性氧的代謝過、藥物反應等方面。

圖4 藥物-疾病共同靶點的GO 生物學過程富集分析
2.5.2 KEGG 通路分析 將藥物-疾病共同靶點輸入R 語言bioconductor 包中,選取P較小,count 數較大的前30 個通路利用氣泡圖進行可視化(圖5)。富集結果分析得知,腎衰寧治療DN 是通過多種途徑的,與脂質和動脈粥樣硬化、人巨細胞病毒感染、糖尿病并發癥中的AGE-RAGE 信號通路、PI3K-Akt 信號通路、MAPK 信號通路、化學致癌作用的-活性氧、TNF 信號通路、IL-17 信號通路、HIF-1 信號通路、內分泌抵抗等多種途徑相關。

圖5 藥物-疾病共同靶點的KEGG 富集分析氣泡圖
2.6 分子對接 篩選PPI 網絡中度值前3 的靶蛋白進行分子對接(表1),使用AutoDock 軟件進行分子模擬對接的結果。取degree 值前3 的蛋白質與化合物結合進行可視化處理(圖6),結果顯示各化合物與蛋白對接的結合能均<0 kcal/mol。

圖6 靶蛋白與化合物的結合模式圖
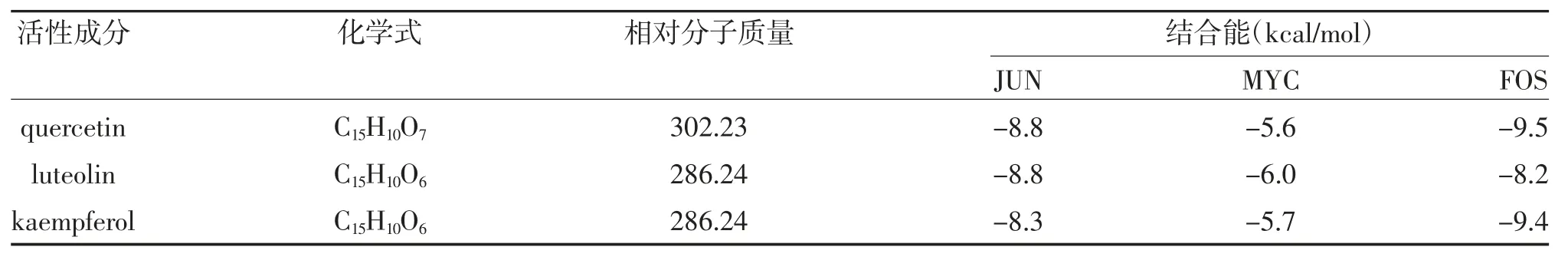
表1 活性成分與靶點蛋白結合能
3 討論
目前DN 發病機制尚未完全明確,有研究認為與血流動力學改變、代謝紊亂、炎癥反應、自噬、細胞因子、氧化應激以及遺傳因素等密切相關[9]。腎衰寧是由丹參、大黃、太子參、黃連、牛膝、半夏(制)、紅花、茯苓、陳皮、甘草10 味中藥組成的中成藥,具有益氣健脾、活血化瘀、通腑泄濁的功效。方中太子參、制半夏、茯苓、陳皮益氣健脾,利水滲濕;丹參、紅花活血祛瘀,涼血消癰;大黃、黃連重在瀉火解毒,燥濕利水;牛膝滋補肝腎,利尿通淋;甘草和中緩急,調和諸藥。現代藥理學研究發現,丹參注射液能通過抑制氧化應激、炎癥反應和纖維化進程來挽救DN[10];大黃不僅能夠抑制高代謝及腎臟代償性肥大,促進機體排泄,而且能抑制蛋白質分解,促進其大量合成,從而改善氮質血癥[11];黃連能夠通過lncRNA CLYBL-AS2-miR-204-5p-SNAI1 軸抑制DN 的上皮-間充質轉變和纖維形成,從而改善DN[12];紅花有效成分紅花黃色素能夠降低心率,提高血糖的比例,改善DN 相關的檢測指標[13];陳皮提取物(OPE)可改善腎功能,顯著防止肌酐、尿素和血尿素氮水平的升高,降低腎小管間質纖維化指數[14];甘草提取物降低血糖水平,恢復腎功能,減輕體重,恢復糖尿病腎臟的總抗氧化能力,對糖尿病有潛在的治療作用[15]。
本研究得到217 個活性成分,度值前3 的活性成分為槲皮素(quercetin)、木犀草素(luteolin)、山奈酚(kaempferol)。研究表明,槲皮素能夠抑制DN 腎小球系膜細胞增殖、降低DN 的足細胞凋亡水平從而治療DN[16-18];木犀草素通過抑制STAT3 通路,抑制炎癥反應和氧化應激,減輕DN 癥狀[19],同時抑制超氧化物歧化酶(SOD)活性、丙二醛(MDA)含量和血紅素加氧酶-1(HO-1)蛋白表達,從而達到對DN的保護作用[20];山柰酚能夠通過抑制炎癥、抗氧化、改善腎纖維化,減輕DN[21-23]。
通過PPI 分析得到17 個核心靶點,度值前3 的靶點為JUN、MYC、FOS。JUN 是具有轉錄活性的轉錄因子,高糖環境可使腎臟c-Jun 蛋白的表達顯著增加,活化JNK 信號通路,激活的JNK 途徑通過磷酸化轉錄因子和其他目的因子來調節基因轉錄,誘導Nephrin 表達下調,從而引起足細胞功能異常,導致DN 加重[24];MYC 作為一種生長轉化因子,表達與細胞增殖有密切的關系,可直接參與細胞生長周期的調控[25],有研究表明減輕C-myc 表達,能夠減輕腎臟肥大和纖維化[26];FOS 家族成員包括c-Fos 和Fos B,在高糖環境下腎小球系膜細胞c-FOS 表達增加,Jun 蛋白與激活蛋白-1(AP-1)形成二聚體,因而表明FOS 在DN 中起重要作用[27]。GO 分類和KEGG 富集分析結果顯示,腎衰寧治療DN 作用的生物學過程主要涉及序列特異性DNA 結合轉錄因子活性的調控、蛋白質磷酸化及對氧化應激、類固醇激素、脂多糖反應等,通過調控糖尿病并發癥中的AGE-RAGE 信號通路、PI3K-Akt 信號通路、MAPK信號通路、化學致癌作用的活性氧、TNF 信號通路、IL-17 信號通路、HIF-1 信號通路、內分泌抵抗等發揮治療DN 的作用。最后對篩選得到的活性成分及靶點進行分子對接驗證,結果顯示腎衰寧與相對應的作用靶點均展現出較好的親和力,且結合位點均有穩定的氫鍵,構象穩定,有強烈的結合能力,進一步驗證了本研究預測的準確性,也表明腎衰寧可能通過多成分作用于多靶點發揮治療DN 的作用。
綜上所述,本研究通過對腎衰寧治療DN 作用靶點的生物過程及信號通路進行富集分析,明確了腎衰寧治療DN 作用的分子機制具有多成分、多靶點、多途徑的特點,這為后續實驗提供了研究思路。

