乳腺多形性腺瘤臨床病理分析并文獻復習
周兵,黃京,劉浩茹,黃傳生
(1.九江市第一人民醫院病理科,九江 332000;2.南昌醫學院,南昌 330004;3.江西省腫瘤醫院病理科,南昌 330006)
多形性腺瘤(Pleomorphic Adenoma,PA)也稱為良性混合瘤,常發生于頭面部如涎腺、喉、鼻竇、腭和鼻中隔,也可發生在皮膚,臨床表現為慢性病程,漸進性生長[1]。自1978年由Sheth等首次發現1例原發于乳腺肌上皮的PA以來,后續國內外偶有個例報道[2]。本文現報道1例原發于乳腺的PA,并復習既往國內外文獻報道9例臨床及病理資料,并總結鏡下形態及免疫組化表型,以期提高對該罕見病的認識水平。
1 材料與方法
1.1 臨床資料 女性,53歲,因發現左乳腫物3 d入院。乳腺B超示:左乳實性低回聲團,考慮纖維腺瘤可能。術中外下象限近乳暈處可見2.5 cm×2 cm灰白結節性腫物,表面光滑,與周圍組織界線清,行腫物完整切除術。
1.2 方法 組織標本經中性福爾馬林固定、石蠟包埋、4 μm厚度切片后,HE染色,倒置顯微鏡下進行組織形態學觀察。免疫組化采用EnVision法,抗體SMA、P63、S-100、CK5/6、CD117、CK7、ER、PR、Cal-ponin、Her2、GCDFP-15和Ki67等均購自福州邁新公司,同時設立陰、陽對照,熟練技師按試劑說明標準化操作。
2 結果
2.1 眼觀 送檢灰白結節狀腫物1個,2.5 cm×2 cm×2 cm,表面光滑,似有包膜,切面灰白、灰紅,實性,質稍韌,局部質稍硬,灶性區域呈微囊性,流少許灰褐色液體。
2.2 鏡檢 乳腺腺體及導管旁見腫瘤由上皮細胞及肌上皮細胞構成,界限清楚,有纖維包膜,呈結節性生長,見圖1。其旁可見增生的乳腺腺體及纖維組織伴導管擠壓呈裂隙狀,見圖2。腫瘤結構復雜,形態多樣,見由圓形、卵圓形矮柱狀或立方狀內層腺上皮及外層肌上皮排列呈不規則的腺管狀、微囊狀結構,腔內富含嗜酸性分泌物,見圖3。部分區域以短梭形肌上皮細胞為主,呈雜亂、片狀排列,細胞形態一致,較為溫和,胞質淡染、核仁不可見,背景見少許炎性及玻變的纖維間質,其旁可見大囊腔形成,內含多量紅染液體,見圖4。部分區域可見黏液性或軟骨粘液性間質,間質內見多量的真性軟骨成分,軟骨結構呈多結節狀,軟骨細胞陷入其中,軟骨周圍分布腺管結構呈島狀、分葉狀排列,見圖5。本例未見明確的鱗狀上皮分化、骨樣分化和脂肪瘤樣分化等特殊分化成分。
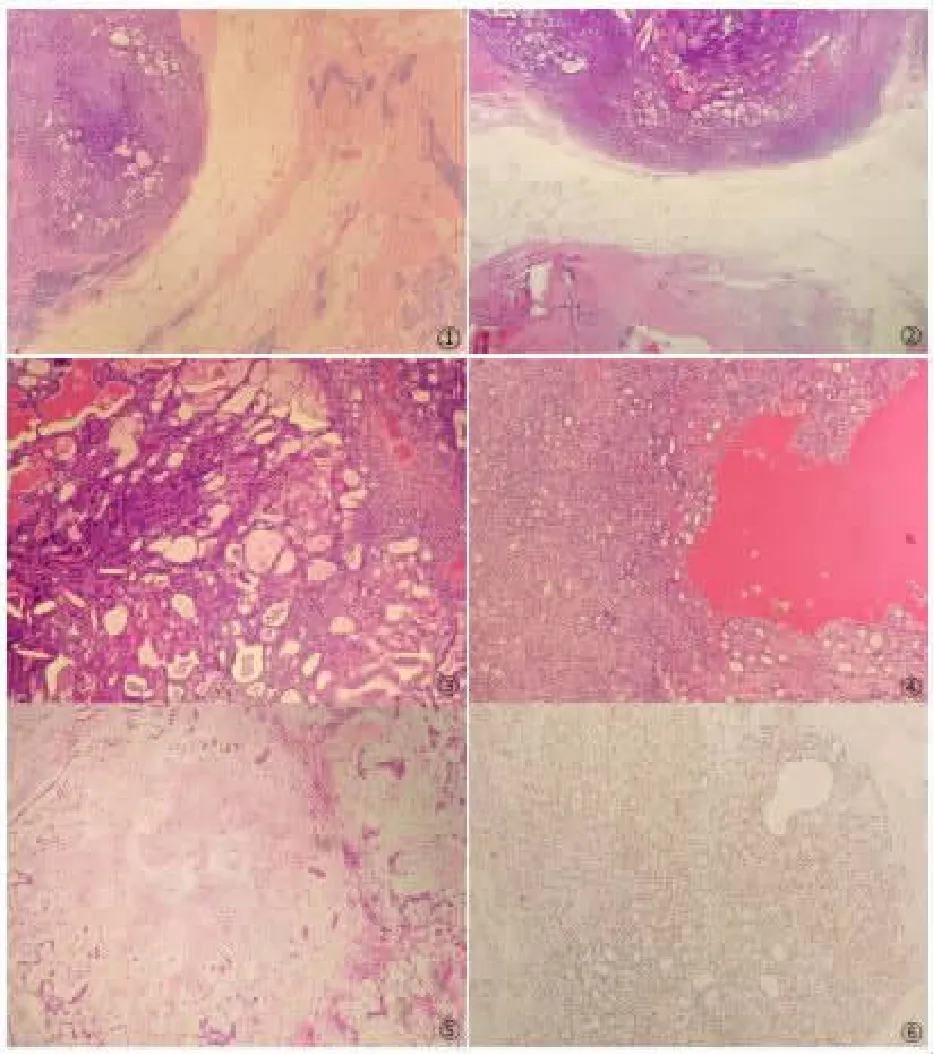
圖1 乳腺腺體及導管旁見腫瘤形成(40)圖2腫瘤旁合并纖維腺瘤(40)圖3腫瘤由內層腺上皮及外層肌上皮構成腺腔樣結構(100)圖4單一的梭形肌上皮細胞呈索狀、片狀排列(100)圖5間質呈黏液軟骨樣成分(100)圖6瘤細胞P63呈彌漫陽性,EnVision法(100)
2.3 免疫表型 腺上皮標記CD117、CK7和肌上皮標記SMA、P63,見圖6、S-100、CK5/6呈彌漫陽性,激素受體ER、PR呈灶性陽性;Her2、GCDFP-15為陰性表達,Ki67增殖指數約2%。
2.4 治療及隨訪 局麻下行左乳腫物完全切除術,隨訪27個月,患者健在,未見腫瘤復發及轉移。
3 討論
乳腺PA最常見于女性病例,但男性病例也有個別報道[9]。發病年齡跨度較大,患者年齡從19歲到85歲均有文獻報道[8],但本例和近年已報告的8例病例中以中老年為主,歐美人多見,亞洲人較少,這可能與不同地區的人種和哺乳習慣的差異有關。發病部位文獻報道多見于右乳,但本例和既往我國報道病例以左乳多見[10]。PA有發生在乳暈區的傾向,這可能表明它可能起源于乳腺大導管,本例發生于外下象限近乳暈處與此類似[12]。臨床多以患者可觸及性的實性結節性包塊就診,因其并不具有影像學的特征性改變,在B超和鉬靶上很難與其它乳腺腫瘤區別開來,本例乳腺B超初始診斷為纖維腺瘤,最后通過組織病理學檢查確診,見表1。
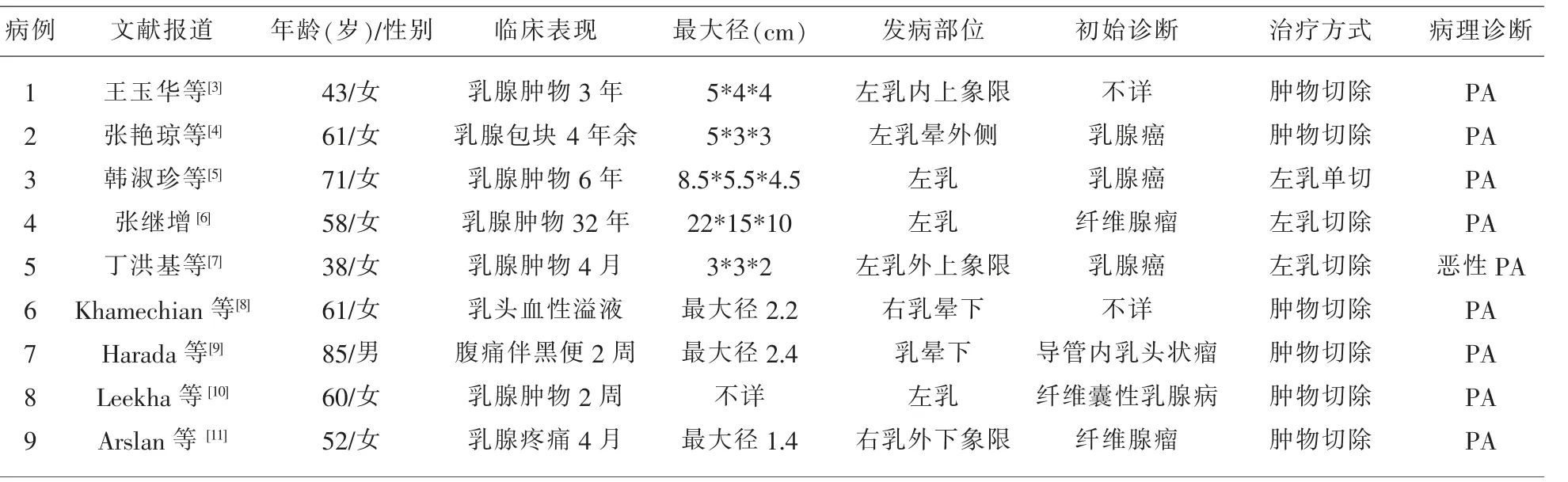
表1 文獻報道乳腺PA臨床病理特征
目前對于乳腺PA的起源存在著一定的爭議,部分學者認為乳腺和唾液腺的胚胎發育存在著相似性,均存在雙重的腺上皮和肌上皮細胞分化起源,而PA作為唾液腺最常見的良性腫瘤,同樣也可以在乳腺上發生[13]。也有學者認為PA可能起源于乳腺導管內乳頭狀腫瘤,當其內的肌上皮細胞受到某些刺激時,可以發生多向潛能分化,這也可以解釋PA間質內可以出現黏液軟骨樣化生和其它類型的化生,同時,部分乳腺PA病例中也可以存在導管內乳頭狀瘤的區域進一步證實了該觀點[14]。也有學者認為PA與導管腺瘤或結節性腺肌上皮瘤存在關聯性,因其上皮成分和組織結構與兩者存在一定的關聯性[15]。隨著分子生物學的發展,越來越多的基因調控和蛋白表達被證實與PA的發生有關。一項國外的體外細胞學研究發現,當HRAS基因Q61R位點發生突變后,可以使乳腺上皮細胞增殖活性增加和發生肌上皮細胞分化,而肌上皮的分化被認為是發生PA的重要因素[16]。同時,多形性腺瘤基因1(PLAG1)和高遷移率族蛋白A2(HMGA2)的高表達被認為與乳腺PA的發生關系密切,能誘導乳腺干細胞的雙相上皮分化模式[17]。
乳腺PA的診斷多不太復雜,形態學與其它部位發生的PA結構類似。鏡下腫瘤邊界清楚,呈結節狀生長,組織結構具有明顯的多形性特點。實質由大量圓形腺上皮細胞排列成腺管狀和短梭形肌上皮細胞排列成片狀共同構成,腺、肌上皮細胞形態溫和,不具有異型性。間質由大量黏液樣軟骨基質和骨化生區構成,實質與間質界限不清,混雜分布。免疫組化多表達腺上皮標記CD117、CK7、CK8/18和 肌 上 皮 標 記SMA、P63、S-100、CK5/6、Calponin、GFAP;免疫標記不表達Her2和GCDFP-15被認為在診斷乳腺PA具有特征性,但ER、PR的表達還存在一定的爭議,研究認為該部位表達于PA腺上皮細胞,本例免疫組化結果與此類似[18]。依據PA腫瘤細胞組織結構的不同,我們需要與乳腺其它腫瘤進行鑒別。(1)腺肌上皮瘤:腺上皮和肌上皮組成的小葉型、梭形細胞型結構伴間質的黏液樣變性時與PA形態類似,但前者大體邊界常不清,無纖維性被膜包饒,且間質不存在明顯的的軟骨和骨化性區域。(2)硬化性導管乳頭狀腫瘤:當導管內乳頭狀瘤間質發生黏液樣變性和軟骨樣化生時與PA形態類似,但前者不具有組織學的多形性,且整體以纖維血管為軸心的乳頭狀生長方式,同時外層腺上皮和內層肌上皮腺管結構與PA排列方式相反。(3)腺樣囊性癌:復雜多樣的組織學形態和腺腔樣的生長方式,同時腔內富含嗜酸性分泌物均與PA形態類似,但前者邊界不清、細胞異型性明顯,且腫瘤細胞伴有明顯的嗜神經現象。(4)化生性癌:明顯的黏液樣軟骨基質和骨化生區與PA的典型形態學一致,但前者邊界不清,細胞異型明顯,核分裂易見,可見明顯的壞死區,且黏液樣軟骨基質一般不混雜排列,常出現忽然的移行。
乳腺PA首選治療方法為手術切除,雖然腫瘤性質為良性,但因腫瘤富含的黏液成分的外溢和腫瘤細胞包膜外的延伸性,不充分的切除會導致腫瘤的復發,手術切除范圍建議大于腫瘤邊緣3mm,當不能確定達到完全性切除時,補充放療被認為可以有效防止復發[19]。PA惡變也有個別文獻報道[20],特別發生在反復復發的病例,但尚未見到發生轉移的文獻報道,本例隨訪27個月,未出現復發、惡變或轉移。

