圖像識別分析子宮內膜腺體密度在評價子宮內膜容受性中的應用
施政,朱閩波,陳麗萍,胡敏,童春芽
體外授精-胚胎移植(IVF-ET)目前已經成為治療不孕癥的重要手段。目前隨著臨床促排卵治療方案的個體化和精細化,胚胎的質量已經得到了顯著的優化[1]。但是,胚胎移植以后的妊娠率卻始終徘徊在35%左右[2]。其中子宮內膜容受性的不足是引起胚胎著床失敗的一個重要原因[3]。子宮內膜容受性是指子宮內膜處于一種允許胚泡定位、黏附,直至內膜間質發生改變,胚胎完成著床的特殊狀態[4]。目前超聲、生物化學等指標無法很好的改善患者妊娠結局,因此,尋找新的評價子宮內膜容受性的指標成為改善患者妊娠結局,減少胚胎浪費的關鍵。本研究在宮腔鏡檢查過程中采集宮腔鏡下內膜圖像,利用已報道的圖像識別算法所設計的計算機軟件進行子宮內膜腺體計數,計算子宮腺體密度,并以此來評價子宮內膜容受性以及對妊娠結局的預測價值。
1 資料與方法
1.1 一般資料 本研究收集2017年1月至2019年12月在寧波市婦女兒童醫院生殖醫學中心接受自然周期胚胎移植的不孕癥患者98例,年齡22~41歲,不孕年限1~17年,其中原發不孕52例,繼發不孕46例。納入標準:平時月經周期規律,無子宮及卵巢手術史,無內分泌相關疾病,無子宮腺肌病、子宮內膜異位癥等疾病。所有患者在宮腔鏡探查中無異常發現,并于宮腔鏡手術后3個月內進行胚胎移植。所有患者中確診臨床宮內妊娠46例(妊娠組),即早孕期B超檢查提示宮內妊娠,見孕囊發育(孕囊三徑線平均值>10 mm),妊娠結局包含足月分娩、早產、中期引產及早期人工流產、稽留流產。未宮內妊娠52例(未妊娠組),包括HCG陰性、生化妊娠(HCG陽性,B超未見妊娠,月經自然來潮)以及異位妊娠(非宮腔內妊娠,不包括宮角妊娠)。
1.2 方法
1.2.1 宮腔鏡手術及術后處理 宮腔鏡手術均由本院婦科日間宮腔鏡手術中心的醫療團隊完成,手術者均接受了培訓,以確保嚴格按照要求執行所有宮腔鏡手術。麻醉方式采用丙泊酚靜脈麻醉+喉罩輔助通氣。手術選擇經排卵監測證實排卵后第3~7天(種植窗口期前后2 d內)進行。手術儀器為德國Storze公司生產的檢查鏡,置入宮腔鏡探查整個宮腔,明確有無宮腔粘連、畸形、宮腔及宮頸管有無異常占位,如無異常情況,經宮腔鏡操作孔置入帶刻度的硬膜外導管,以宮腔底部居中處宮腔鏡屏幕中心,以帶有刻度的硬膜外導管垂直達到宮腔底部后實測距離鏡頭1 cm為基準,調整焦距后對子宮內膜予以截圖(封三彩圖6),術后使用計算機圖像識別軟件(Glands Detector)對子宮內膜腺體識別、標記(封三彩圖7)及計數,并計算子宮腺體密度。
圖6 獲得圖像
圖7 標記腺體
1.2.2 腺體密度計算方法 在軟件(Glands Detector)中使用鼠標依次點擊硬膜外導管的起始部和1 cm的刻度位置,畫出一條直線,其長度定義為圖像中1 cm長度;再使用鼠標框選一定的范圍,由軟件計算出框選范圍的面積,并計數其內的腺體個數,并由此計算出腺體的密度(以每cm2面積內包含腺體個數表示,封三彩圖8)。為減少誤差,每張圖片在不同位置選取3個不同的范圍,并求出3個值的平均數,作為腺體密度的最終值。
圖8 選取范圍并計數
1.2.3 圖像識別軟件 由合作的團隊成員編寫,其算法使用了楊森等[5]的基于形態學重構的宮腔鏡下子宮內膜腺體開口標記算法,并參考了Gaviao等[6]的研究。軟件通過將圖像RGB轉換為HIS模式的亮度分量,除噪后識別提取腺體開口區域,最后將腺體開口逐一標記(封三彩圖9)。根據楊森等[5]的報道,該算法的靈敏度為84.72%±8.00%,Dice相似系數達83.80%±4.56%。筆者也將30幅宮腔鏡圖像的軟件分析結果與人工識別計數的結果進行了比較,發現軟件分析的結果是人工識別數的(86.73±7.59)%。仿真和實驗結果表明,該算法可以有效地識別宮腔鏡下的子宮內膜腺體。

圖9 圖像處理步驟示意圖
1.3 統計方法采用SPSS 19.0統計軟件進行分析,計量資料以均數±標準差表示,采用獨立樣本t檢驗;計數資料采用2檢驗。P<0.05表示差異有統計學意義。
2 結果
妊娠組與未妊娠組年齡、不孕年限、體質量指數、抗苗勒管激素(AMH)和移植胚胎數差異均無統計學意義(均P>0.05),妊娠組子宮內膜腺體密度高于未妊娠組(P<0.05),見表1。妊娠組中原發不孕20例,繼發不孕26例,未妊娠組中原發不孕32例,繼發不孕20例;兩組原發與繼發不孕差異無統計學意義(2=3.196,P=0.074)。
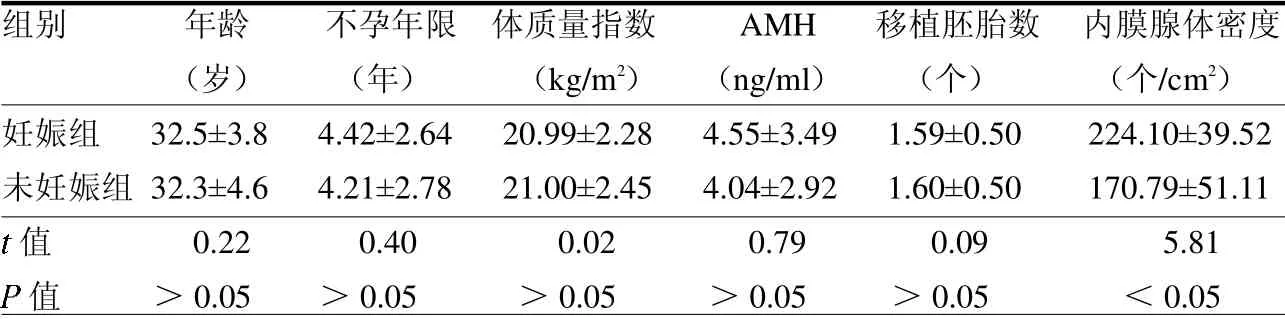
表1 兩組年齡、不孕年限、體質量指數、AMH、胚胎移植個數及內膜腺體密度比較
3 討論
目前,有研究報道反復胚胎種植失敗的患者中,大約有50%存在宮腔異常,而宮腔鏡相比B超而言,能夠更加直觀的觀察宮腔及子宮內膜情況,并能同時處理宮腔微小病變[7-8],成為處理宮腔病變的主要手段。但是仍有另外50%的胚胎移植失敗患者,其通過宮腔鏡檢查并未發現既往認知中的典型宮腔異常。因此需要尋找其他一些微觀指標,來解釋這些患者與正常妊娠者存在的子宮內膜容受性上的不同。
Sakumoto等[9]報道了分泌中期宮腔鏡下子宮內膜的形態學表現,其根據子宮內膜表面腺體開口大小及血管分布情況,將子宮內膜分為分為“good”和“poor”組,發現“good”組在IVF-ET時,妊娠率高于“poor”組。Masamoto等[10]則利用類似的分類標準進行分組后發現“poor”組的流產率高于“good”組。這些研究提示著床窗口期觀察子宮內膜腺體開口及血管分布情況可能對判斷子宮內膜容受性有一定意義。但是,受限于既往宮腔鏡設備所采集的圖像精度,以及人工智能技術發展的不成熟,對于子宮內膜腺體開口及血管分布情況的判斷依賴于手術醫生的經驗,缺少客觀數據。得益于高清攝像設備在宮腔鏡手術中的廣泛應用,在宮腔鏡手術中,可以觀察到0.1 mm級別的子宮內膜形態。而在著床窗口期佳型子宮內膜血管呈網狀分布,腺體開口大[11],在高清宮腔鏡下,可以清楚的加以辨識。而與此同時,隨著近幾年人工智能的逐漸成熟,圖像識別技術日新月異,并廣泛應用于醫療領域,使得利用計算機軟件,對高清宮腔鏡所采集的子宮內膜圖像中的腺體加以智能識別成為可能。
本研究組制作了一個針對性的子宮內膜腺體識別軟件,對高清宮腔鏡所采集的子宮內膜圖像進行識別,能有效識別宮腔鏡下的子宮內膜腺體,初步做到子宮內膜腺體數量的具體化。經與臨床妊娠數據相比較,證實了其在預測妊娠結局中的參考價值。但本研究中的局限性在于硬膜外導管在圖像中的位置是斜行放置到宮底,所以圖像中導管的起始部和1 cm的刻度之間的實際距離應該是小于1 cm的,而且宮腔的形態并不是一個平面,因此軟件計算的框選面積和實際面積并不完全一致。目前只能借助于帶刻度的硬膜外導管盡可能使圖像采集時各個攝像頭的位置盡可能一致,同時硬膜外導管在圖像中的位置、傾斜程度盡量接近,但是難以做到非常精準。而且針對Sakumoto等[9]所提出的子宮內膜形態學分組依據中,還包括腺體開口大小以及血管分布情況。自帶刻度的硬膜外導管其測量準確度有限,故無法對子宮內膜腺體開口大小做出準確計量,另因血管分布同樣受測量精度限制,尚無法做出自動識別及評價。所以,筆者計劃設計一款帶有刻度的宮腔鏡器械,可以精確測量宮腔的大小及定位攝像頭的位置。同時目前圖像中腺體的軟件識別率大概在85%左右,希望在日后的工作中可以改進算法,進一步提高腺體的識別率和準確度。更可以借助軟件的輔助,測量更多的形態學指標,如內膜腺體的開口大小及內膜血管分布情況。甚至可以依據這些多元化的指標設計一個評分表,使臨床對子宮內膜容受性的評估更加科學及準確。
綜上所述,利用高清宮腔鏡手術系統,結合人工智能發展而來的計算機圖像識別軟件,目前已經可以初步做到對子宮內膜容受性的數字化、客觀化評價,并對預測妊娠結局具有參考價值。當然,其各項指標仍有待進一步改進,軟件系統的算法、功能有待進一步拓展,以便于將子宮內膜容受性的評價進一步數字化,從而減少經驗性判斷而造成的誤差,改善患者妊娠結局,提高IVF-ET治療的經濟性,減少胚胎的浪費。

