白羊草BiMYB52基因的克隆及轉基因擬南芥抗旱性表達分析
李春艷,鐘 華,杜利霞,侯向陽*
(1.山西農業大學草業學院,山西 太谷 030801;2.農業農村部飼草高效生產模式創新重點實驗室,山西 太谷 030801)
轉錄因子因其具有調控基因表達的作用,在過去被廣泛應用于提高作物的農藝性能[1]。MYB蛋白是數量最多,功能多樣化的轉錄因子之一[2],它廣泛分布在真核生物中。MYB轉錄因子的結構特征是含有1-4個高度保守的DNA結合功能域“R”,根據R的數量將MYB轉錄因子家族分為四類1R-MYB,R2R3-MYB,3R-MYB和4R-MYB[3]。每個重復R約有51~52氨基酸,其中包含3個以17~19個氨基酸殘基為間隔的色氨酸殘基,形成3個α螺旋,其中第2和第3個形成一個螺旋-轉角-螺旋(HTH)的結構,第3個螺旋能直接結合DNA被稱為“識別螺旋”。R2R3-MYB在植物中數量最多,幾乎占MYB家族的50%以上,同時大量研究證明這類蛋白參與了植物的生長發育和抗逆等多種生物過程[4]。如擬南芥(Arabidopsisthaliana)中編碼R2R3-MYB類蛋白的GL1和WER基因,分別在其早期皮毛和根部特異性表達,突變體表現為皮毛和根毛缺失和減少,這說明這兩個基因參與了擬南芥皮毛和根毛的形成[5-6]。擬南芥在干旱條件下,AtMYB2蛋白在ABA誘導下,與脫水應答基因RD22作用,促其表達增強,這說明AtMYB2蛋白在干旱脅迫下通過ABA途徑誘導基因表達中發揮轉錄激活因子的作用[7]。將AtMYB44基因轉入大豆中發現,轉基因大豆對干旱和鹽脅迫的耐受性顯著增強[8]。
白羊草(Bothriochloaischaemum)為禾本科孔穎草屬多年生植物。具有固土保水、生命力強,耐旱、高產耐牧等優點,是一種優質的鄉土草資源[9]。但對其研究主要集中在生產性能[10]、營養價值[11]、生理生態[12]及遺傳多樣性上[13]等方面,尚缺乏對其抗逆優良性狀關鍵調控基因的挖掘與利用。因前期對干旱脅迫條件下白羊草轉錄組測序的研究表明,轉錄因子MYB在白羊草響應干旱脅迫的過程中具有重要的作用[14],因此,本研究從前期白羊草轉錄組測序中篩選出的一段對干旱脅迫響應表達量變化顯著的MYB序列為基礎[15],克隆得到其全長,并命名為BiMYB52,為了更好地研究BiMYB52基因在抗逆中的作用,采用染色體步移技術從白羊草中擴增出了BiMYB52啟動子序列,根據啟動子順式作用元件分析結果對白羊草進行了相應逆境脅迫,以期了解在不同逆境脅迫下的表達特性,為深入研究BiMYB52抗逆機制提供基礎。
1 材料與方法
1.1 材料的種植與處理
將采集于山西省太谷縣(采集地海拔978 m,經緯度分別為112°34′E,37°21′N)的白羊草種子,經過酒精浸泡30 s,0.1%升汞處理15 min消毒后,播種于蛭石和珍珠巖比例為3∶1的營養缽中,出苗后培養約30 d,選取長勢一致幼苗進行不同的處理:放入4℃培養箱進行低溫培養;將白羊草幼苗根部分別置于250 mmol·L-1的氯化鈉(NaCl)、20% 聚乙二醇(PEG)和100 μmol·L-1脫落酸(Abscisic acid,ABA)的1/2 MS營養液中培養;分別用200 μmol·L-1水楊酸(salicylic acid,SA)和100 μmol·L-1茉莉酸甲酯(Methyl jasmonate MeJA)噴幼苗葉片至飽和后套袋密封培養;每個處理5株,重復3次,分別取處理0,2,4,8,12和24 h的葉片,-80℃保存待用。
1.2 白羊草BiMYB52基因的克隆與生物信息學分析
用Trizol法提取白羊草幼葉總RNA后,采用RevertAidTM反轉錄試劑盒將RNA反轉錄合成cDNA第一鏈,根據轉錄組測序得到的類MYB序列,設計引物BiMYB52-F和BiMYB52-R(見表1),以cDNA為模板,根據TA/Blunt-Zero Cloning Kit基于拓撲異構酶的超快速克隆試劑盒說明書進行PCR擴增,反應體系為20 μL:cDNA模板 1 μL(<200 ng),2×Pfu Master Mix 10 μL,引物BiMYB52-F和BiMYB52-R各0.5 μL,ddH2O補充至20 μL。反應程序:95℃ 5 min;94℃ 30 s,58℃ 30 s,72℃ 30 s·kb-1,30 cycles;72℃ 10 min。反應結束后,將PCR產物置于1% 瓊脂糖凝膠中進行電泳,按照百泰克凝膠回收試劑盒的說明書,進行目的片段的回收,然后將目的片段與T載體連接,緊接著將反應液轉化到DH5α感受態細胞中,用含卡納抗生素進行篩選,挑選陽性克隆進行鑒定。
用DNAstar 7.0分析BiMYB52基因的核酸及氨基酸序列,用ScanProsite對氨基酸序列的保守結構域進行分析。從NCBI上下載同源性較高的其他植物R2R3-MYB蛋白序列,用DNAMAN6.0對同源物種的氨基酸序列進行比對;利用MEGA5.0 軟件鄰位歸并發法構建系統進化樹。
1.3 BiMYB52啟動子克隆與分析
根據已經克隆到的白羊草BiMYB52基因序列,分別設計SP1,SP2,SP3引物(見表1),以白羊草DNA為模板,采用染色步移法進行BiMYB52 基因啟動子序列的擴增。根據Genome Walking Kit的說明進行3步擴增,產物進行電泳檢測后與T載體鏈接,然后轉化大腸桿菌,挑選陽性克隆送上海英俊公司測序。
利用PlantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html)對克隆得到的BiMYB52基因啟動子序列進行分析。
1.4 不同逆境脅迫下白羊草BiMYB52基因的表達特異性
用Trizol提取上述(1.1)各處理的RNA,根據反轉錄Thermo Fisher公司cDNA Synthesis Kit說明書將RNA反轉成cDNA,以白羊草BiMYB52的序列設計定量引物P1和P2(見表1),以cDNA為模板,參照Thermo Fisher公司的SYBRTMGreen PCR試劑盒說明書,進行實時熒光定量PCR擴增,擴增體系為20 μL:2 μL cDNA模板,0.8 μL引物P1和0.8 μL P2,10 μL SYBR Green Realtime PCR Master Mix,0.4 μL ROX Reference Dye Ⅱ(50×),ddH2O補足至20 μL。反應程序為:95℃ 3 min;95℃ 5 s、60℃ 20 s,35~40個循環。每個樣品3個重復,以18S rRNA為內參基因[16],利用2-ΔΔCt法[17]計算BiMYB52基因在不同處理下的表達量。
1.5 植物表達載體構建及擬南芥轉化
設計含有Nco I和Xba I酶切位點的引物P5和P6(表1),擴增BiMYB52的啟動子序列,得到帶有酶切位點的目的基因片段;用Nco I和Xba I雙酶切該基因片段和pCAMBIA1301質粒載體,經T4 DNA連接酶連接,得到插入目的基因的pCAMBIA1301-BiMYB52植物表達載體。將構建pCAMBIA1301-BiMYB52表達載體轉化大腸桿菌DH5α,經PCR驗證,挑選陽性克隆送生物公司測序,將測序正確的pCAMBIA1301重組質粒轉化農桿菌感受態GV3101。用花序侵染法轉化野生型擬南芥,在含有潮霉素的培養基篩選轉基因抗性植株,采用引物HPT-F和HPT-R通過RT-PCR法鑒定轉基因植株陽性苗。再經過自交和篩選后得到T3代轉基因擬南芥,用于后續試驗。

表1 實驗中的引物序列
1.6 轉基因擬南芥的抗旱性分析
將野生型擬南芥種子和已鑒定出的BiMYB52-1,BiMYB52-2和BiMYB52-3轉基因擬南芥種子,用75%的酒精消毒1 min,再用9%的次氯酸鈉消毒10 min,最后用滅菌的雙蒸水清洗,然后置于1/2MS固體培養基上。4℃冰箱中放置48 h進行春化,之后放置于光照培養箱中,溫度22℃,光強10 000 Lx,相對濕度50%~60%,光照16 h和黑暗8 h交替進行培養,培養7 d幼苗,選擇長勢一致的幼苗轉至裝有蛭石的花盆中培養。將生長至30 d的幼苗進行干旱處理。干旱處理采用不澆水處理14 d,恢復處理采用與對照相同的培養方式進行復水,復水5 d后計算存活率。每個處理設置3個生物學重復。生理指標的檢測采用南京建成公司的試劑盒測定,丙二醛MDA含量的測定采用試劑盒A003-1,脯氨酸Pro含量的測定采用試劑盒A107。
1.7 數據梳理
采用SPSS25.0軟件進行雙因素方差分析,Duncan’s法對平均值進行比較和Excel軟件進行分析和作圖。
2 結果與分析
2.1 白羊草BiMYB52基因的克隆
根據轉錄組測序得到的435 bp MYB轉錄因子片段,利用TA/Blunt-Zero Cloning Kit技術,擴增得到1個長度為1 149 bp的序列(圖2A),其陽性克隆菌落鑒定圖為2B。Blast比對結果顯示該序列與高粱(Sorghumbicolor)、玉米(Zeamays)、糜子(Panicumhallii)等物種的MYB基因高度同源,初步認為獲得的序列是一個MYB類蛋白序列。
2.2 白羊草BiMYB52基因的生物信息學分析
BiMYB52基因含有一長度為714 bp的ORF(開放閱讀框),編碼237個氨基酸,其蛋白分子量為26.98 kDa,理論等電點為7.09。該蛋白的N端含有兩個保守的結構域R2和R3(圖2),R2和R3 N端保守基序分別為[W]-x(19)-[W]-x(19)-[W]和[W]-x(18)-[W],說明這次克隆的蛋白屬于MYB家族的R2R3亞族。利用GenBank上的BlastP搜索到不同物種的9個R2R3-MYB蛋白序列,并進行了比對分析,由圖3可見,該基因N端存在兩個保守的結構域,與其他R2R3-MYB轉錄因子的同源區都集中在這一區域,C端同源性極低。
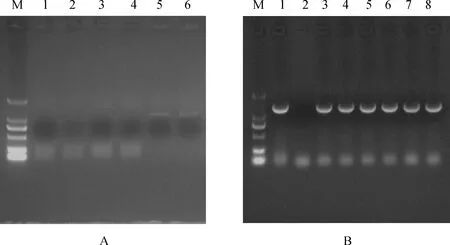
圖1 白羊草BiMYB52基因的克隆及陽性菌落鑒定結果
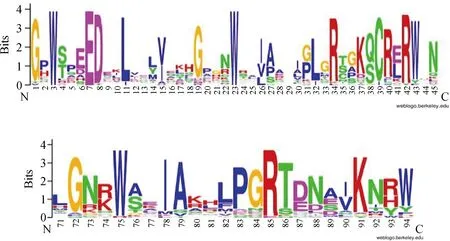
圖2 R2R3-MYB蛋白N-端DNA-binding結構域

圖3 BiMYB52氨基酸序列與其他植物R2R3-MYB蛋白的多序列比對
該基因編碼蛋白與其他物種的R2R3-MYB蛋白的同源性相對較高,與高粱同源性達到94.56%,與芒草(Miscanthuslutarioriparius)同源性達到93.7%、與谷子(Setariaitalica)、糜子、玉米、柳枝稷(Panicumvirgatum)等同源性達88.33%~92.86%。
系統進化樹分析表明,BiMYB52與高粱SbMYB52聚為一類,與玉米ZmMYB52,芒草MlMYB52的親緣關系較近,與野生型二粒小麥(Triticumdicoccoides)TdMYB52、二穗短柄草(Brachypodiumdistachyon)BdMYB52、水稻(Oryzasativa)OsMYB52、谷子SiMYB52等也聚為一類,但親緣關系較遠(圖4)。由于該系統樹上,功能相關的MYB大都聚到一起,故將其命名為BiMYB52。
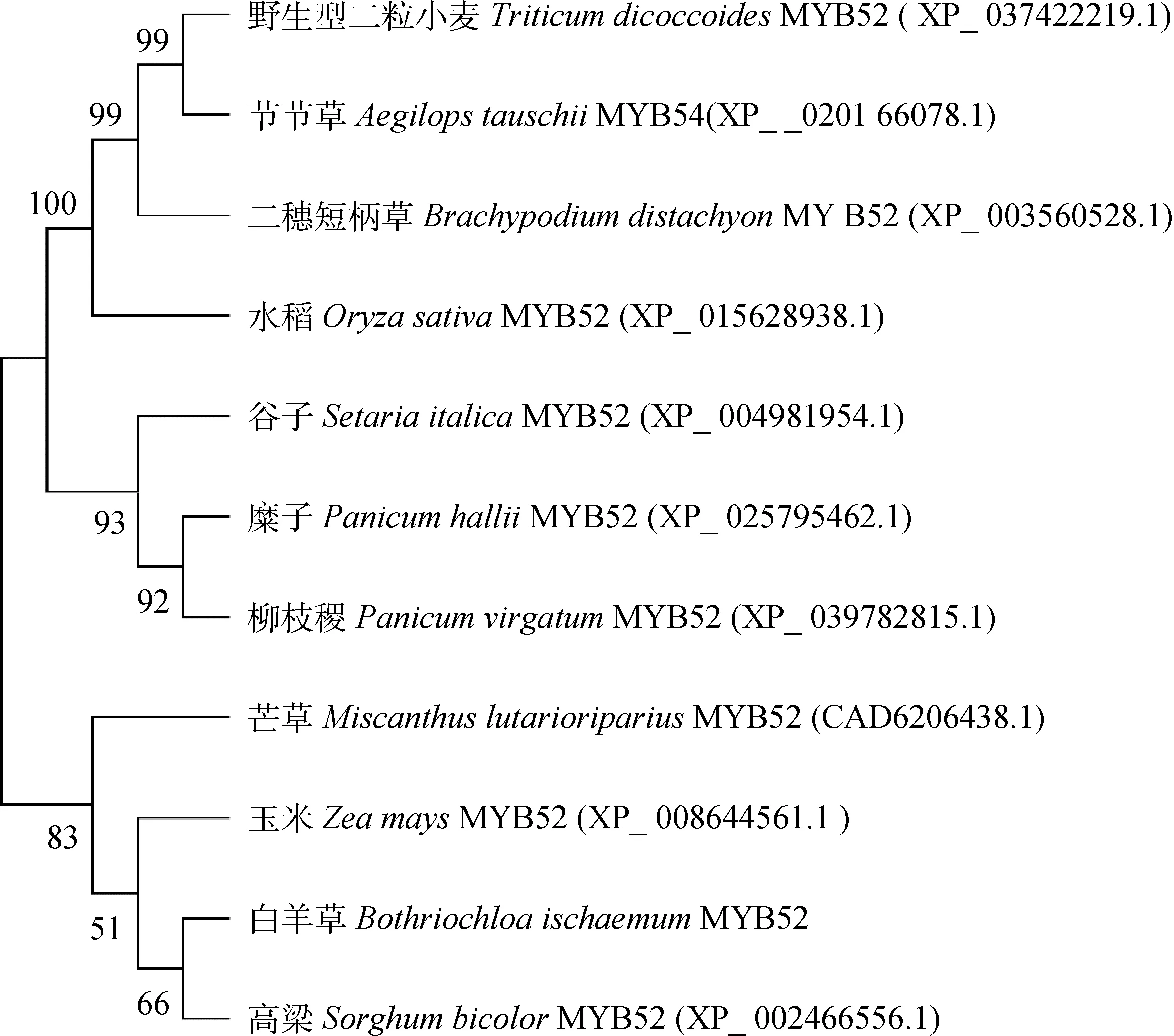
圖4 基于氨基酸序列構建的BiMYB52系統進化樹
2.3 BiMYB52啟動子的克隆與序列分析
以白羊草DNA為模板,根據白羊草中克隆到的BiMYB52基因開放閱讀框序列,設計特異性引物SP1,SP2,SP3(表1),采用步移法得到2 127 bp啟動子序列(圖5)。利用Plant-CARE對克隆得到的BiMYB52基因啟子序列進行分析。結果顯示,序列中除含有TATA-box(17個)和CAAT-box(7個)一般啟動子所具有的特征元件[18],還含有能響應ABA調控的5個順式作用元件ABRE,2個與脅迫和水楊酸SA響應的順式作用元件W-box,5個與缺水、抗脫落酸、抗凍均有響應的結構MBS,1個與干旱、高鹽、低溫誘導相關的結構DRE,1個參與脫落酸應答的元件DPBFCOREDCDC3,1個與胚乳表達相關的結構Skn-1-motif,10個光響應元件ATCT-motif,5個與SA響應相關的元件GCCCORE,1個與光響應和MeJA響應相關的G-box。具體結構和數量見表2。
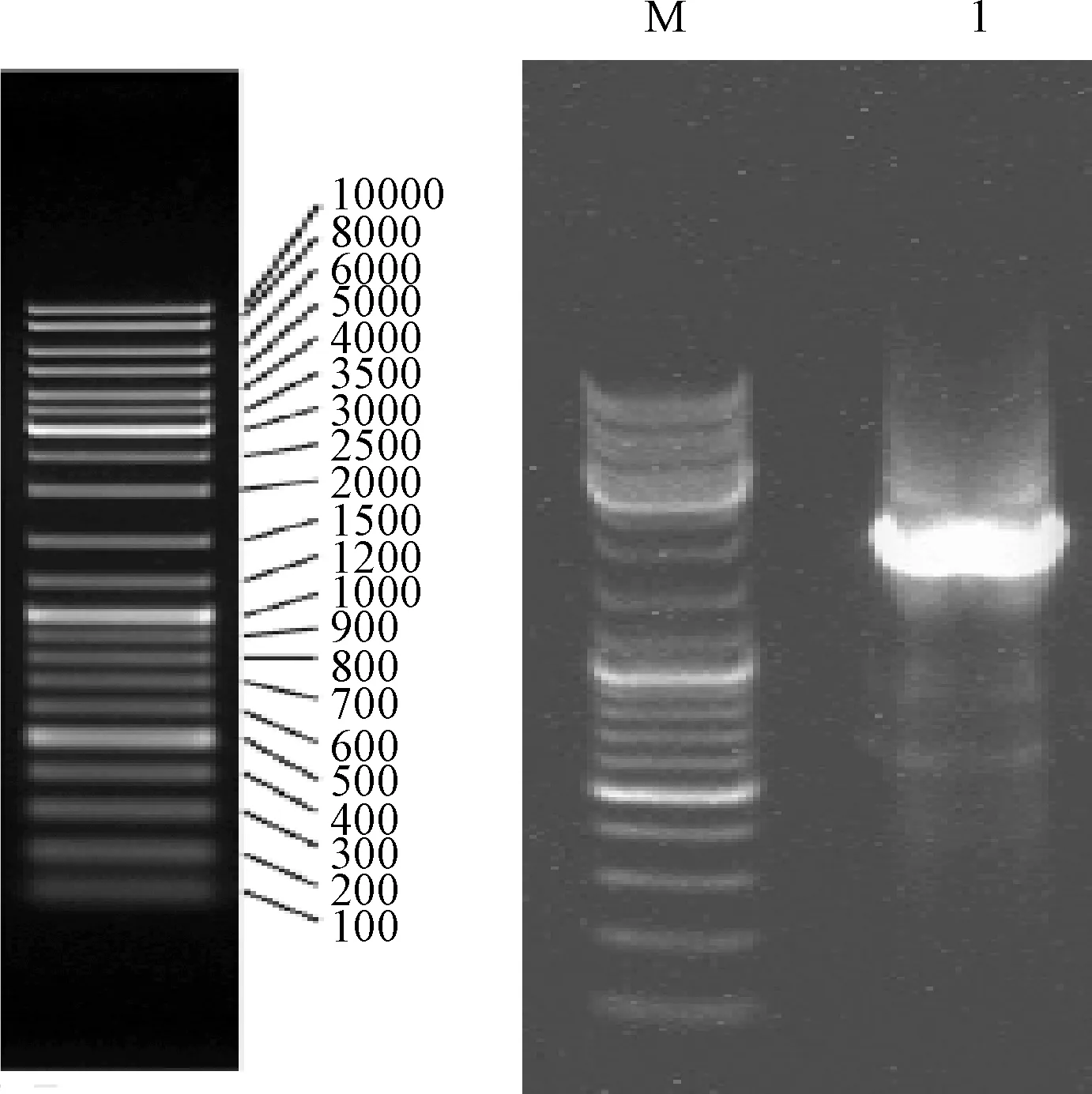
圖5 白羊草BiMYB52啟動子PCR擴增產物

表2 BiMYB52基因啟動子順式作用元件種類和數量及功能分析
2.4 逆境脅迫下白羊草BiMYB52基因的表達分析
利用RT-qPCR對白羊草BiMYB52基因在非生物逆境脅迫下的表達量進行檢測,結果表明,多種逆境脅迫均能誘導白羊草BiMYB52基因的增強表達。在20% PEG脅迫誘導下,BiMYB52的表達量隨時間上調,8 h表達量達到高峰,為對照的26倍,然后又下降(圖6A);NaCl脅迫下BiMYB52的表達量在8 h之前無明顯變化,8 h開始增加,12 h達到最大,此時表達量增加為對照的9倍,而后又迅速下降(圖6B);冷脅迫下(4℃)BiMYB52的表達量呈現先升高12 h達到峰值,后降低的趨勢(圖6C);外源ABA也能明顯誘導BiMYB52的表達,也呈現出先升高后降低的趨勢,8 h時表達量最大,是對照的4倍(圖6D);SA處理后,4 h出現第一高峰,隨后迅速下降(圖6E);MeJA處理后2 h就出現第一次高峰,而后第二次高峰出現在12 h,此時誘導的轉錄水平低于2 h(圖6F);這些結果表明,BiMYB52的表達受多種脅迫和激素影響。
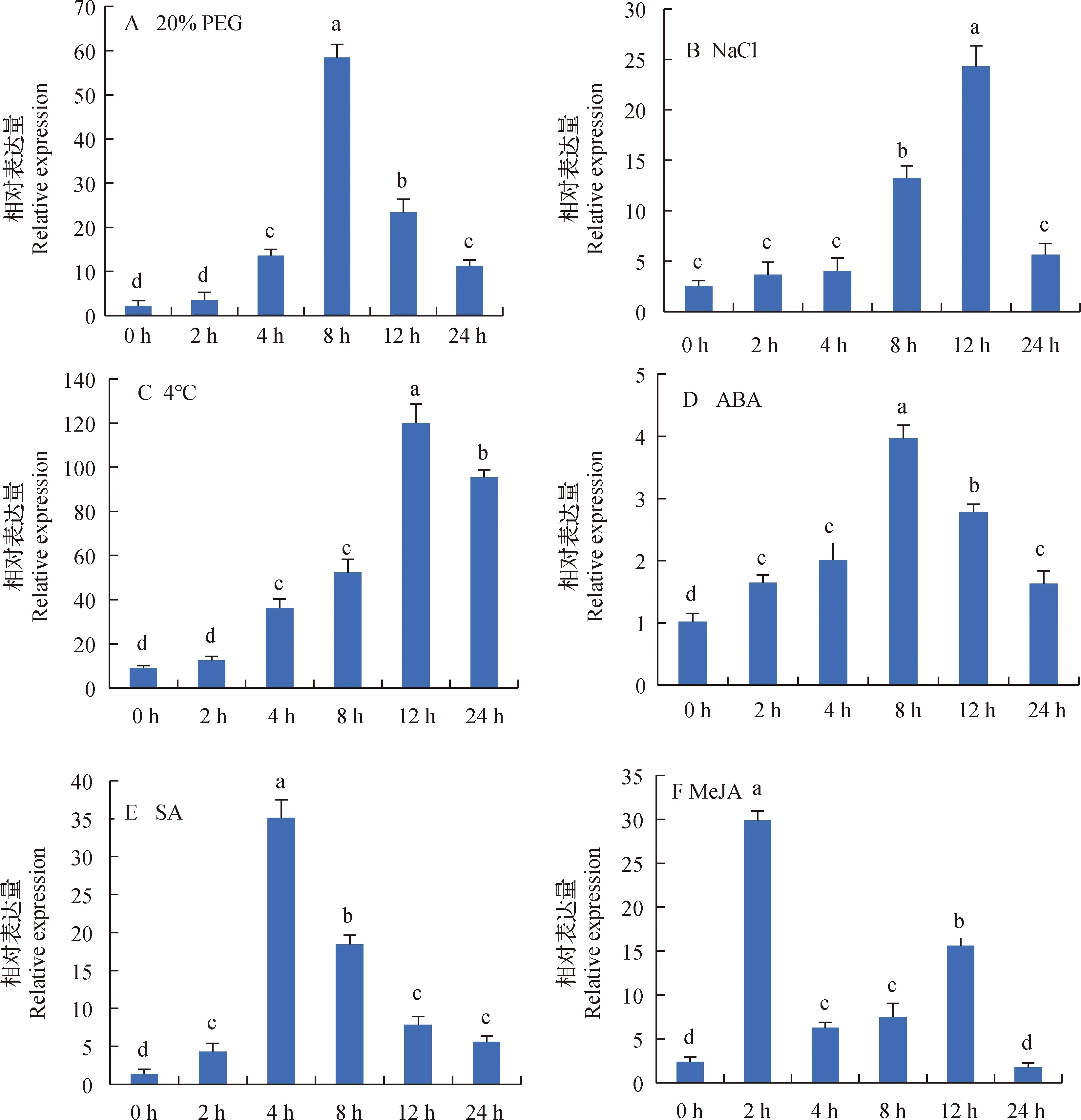
圖6 BiMYB52在不同脅迫誘導下的表達量變化分析
2.5 表達載體構建及遺傳轉化
采用PCR法擴增帶有Nco I和Xba I酶切位點的BiMYB52啟動子基因序列(圖7A),獲得大小約為2 167 bp目的片段,將該目的片段與經過Nco I和Xba I雙酶切的pCAMBIA1301載體進行連接轉化大腸桿菌DH5α,經PCR驗證,挑選陽性克隆測序,將測序正確的質粒轉化到農桿菌GV3101感受態細胞中進行菌落PCR鑒定(圖7B),得到與預期大小一致的片段,證明含有目的基因的pCAMBIA1301-BiMYB52植物表達載體已經構建完成。用花序侵染法轉化野生型擬南芥,在含有潮霉素的培養基篩選得到5個株系(圖8),以得到的轉基因擬南芥DNA為模板,采用引物HPT-F和HPT-R(表1)進行轉基因擬南芥PCR檢測,獲得與預期598 bp大小一致的片段(圖8)。選取BiMYB52-1,BiMYB52-2和BiMYB52-3轉基因株系進行干旱脅迫分析。
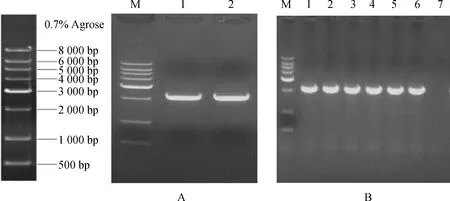
圖7 帶酶切位點BiMYB52啟動子的擴增和表達載體pCAMBIA1301-BiMYB52的PCR鑒定
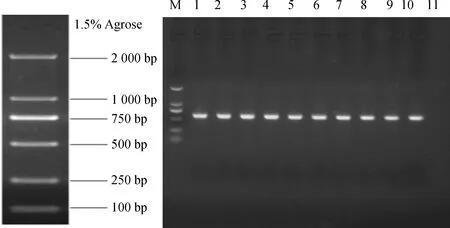
圖8 轉BiMYB52基因擬南芥T1代株系PCR鑒定
2.6 轉基因擬南芥抗旱性分析
為方便我們把BiMYB52-1,BiMYB52-2和BiMYB52-3轉基因株系分別命名為OE1,OE2和OE3。由圖9所示,野生型和轉基因BiMYB52擬南芥在干旱脅迫前后的存活率無明顯差異,干旱脅迫復水后,轉基因擬南芥OE1,OE2和OE3存活率較高,分別為80.4%,86.5%和71.3%,而野生型擬南芥的存活率僅為31.3%。圖10和11表明,正常供水條件下,轉基因擬南芥與野生型擬南芥丙二醛MDA和脯氨酸Pro含量無顯著差異,干旱脅迫條件下,轉基因擬南芥OE1,OE2和OE3丙二醛MDA含量均顯著低于野生型(P<0.05),而脯氨酸Pro含量均顯著高于野生型(P<0.05),說明轉基因擬南芥在干旱脅迫條件下積累的丙二醛MDA較少,但脯氨酸Pro含量較多。
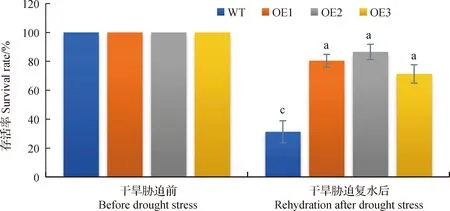
圖9 干旱脅迫復水后的存活率
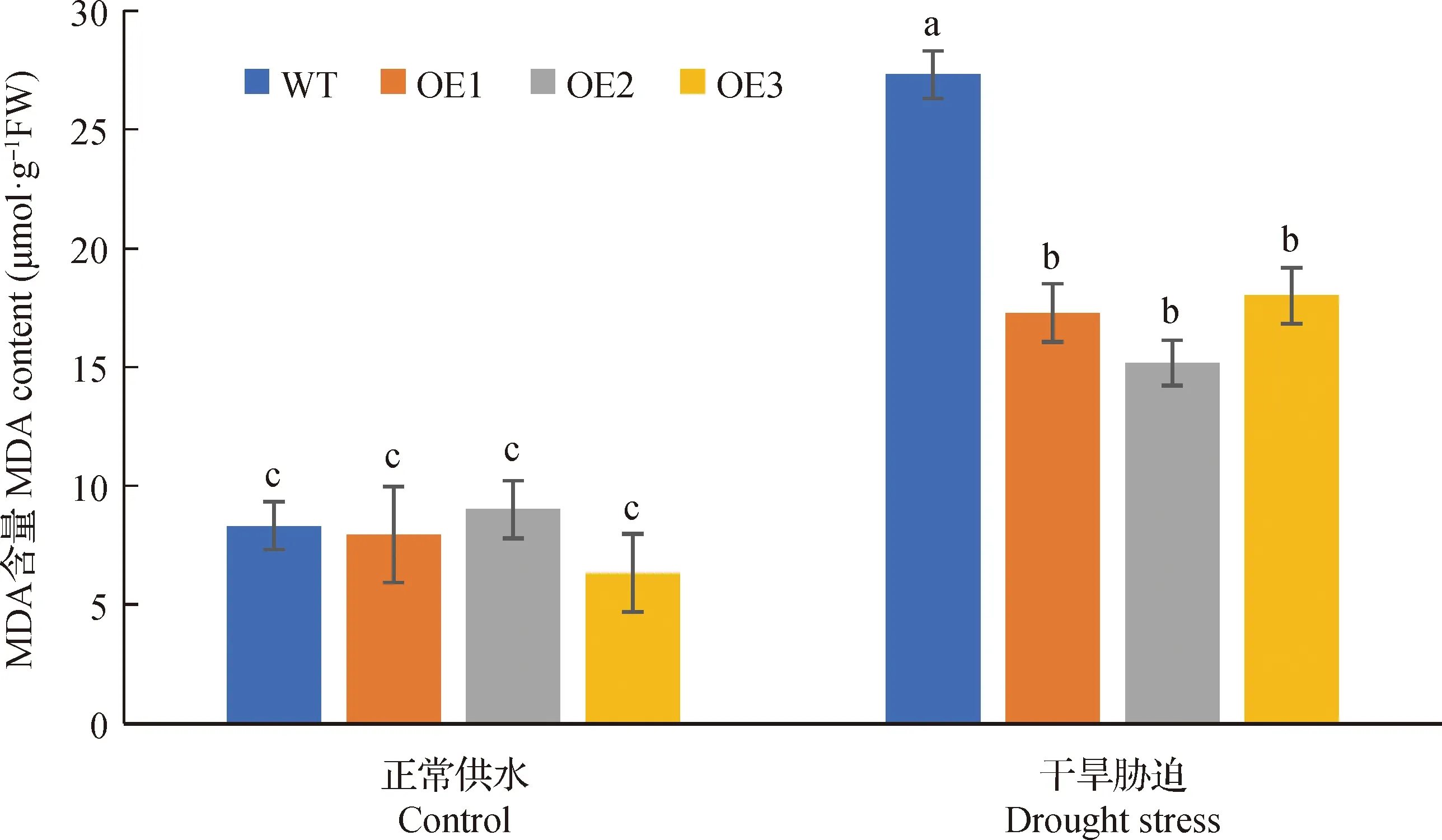
圖10 正常和干旱脅迫條件下野生型和轉基因擬南芥葉片的丙二醛(MDA)含量
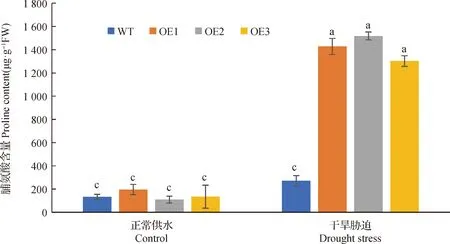
圖11 正常和干旱脅迫條件下野生型和轉基因擬南芥葉片的脯氨酸含量
3 討論
植物中MYB蛋白首次發現是在玉米蛋白微粒中分離出的參與花青素合成ZmMYB基因[19],后來隨著擬南芥MYB家族基因被逐漸鑒定出來,許多功能異同的MYB蛋白在多種植物中被分離和鑒定出來[20]。本研究利用前期轉錄組測序得到的一段MYB序列,從白羊草中克隆出1個BiMYB52基因,其cDNA全長1 149 bp,含714 bp的ORF,編碼237個氨基酸,其N端構成了R2,R3兩個典型的DNA結合結構域,形成2個HTH(螺旋轉角螺旋)結構[3],這種結構有助于與DNA分子結合進而發揮功能[21-22]。氨基酸序列比對結果顯示,BiMYB52與高粱SbMYB52(XP_002466556.1)的同源性最高,達到94.44%。
R2R3-MYB蛋白已經被證明對非生物脅迫的反應至關重要。過去的許多研究已經報道了一些R2R3-MYB蛋白與植物抗逆性相關的功能。例如,擬南芥AtMYB60是氣孔運動調節因子,受干旱脅迫的影響,過表達該基因會抑制對水分的敏感性[23],AtMYB96,AtMYB15和AtMYB2在干旱脅迫的誘導下,通過激活脫水應答基因(如RD22)的轉錄來充當耐旱的正調控因子[7,24],除擬南芥外,還在蘋果[25]、水稻[26]、小麥[27]等植物中發現了R2R3-MYB基因在其對干旱響應中起著重要作用。AtMYB20通過抑制PP2Cs表達來增強抗鹽性[28],TaMYB56-B和LcMYB1在轉基因擬南芥中能夠正調節應激反應和鹽反應[29]。不同物種中的MYB蛋白能夠響應冷、鹽和干旱脅迫響應。如GmMYB92[30]和TaMYB56-B控制鹽和冷反應,OsMYB4 調節干旱和寒冷反應[31]。因此,MYB蛋白質可能是植物對多種非生物脅迫反應的關鍵調控節點。眾所周知,ABA作為一種信號分子,在植物逆境脅迫響應過程中發揮著重要的作用。研究證明,擬南芥AtMYB60和AtMYB96參與調控依賴ABA的干旱脅迫反應,通過調節氣孔運動來提高植物抗旱能力[32-33],Ding等報道了擬南芥基因AtMYB15的過量表達可以調高擬南芥對ABA的敏感性,并提高了植物的抗旱性[34]。本研究發現在外源激素ABA,SA,MeJA和干旱、高鹽、低溫等逆境脅迫,均能誘導mRNA的積累,對轉基因BiMYB52擬南芥抗旱性的研究表明,干旱脅迫復水后,轉基因擬南芥存活率遠遠大于野生擬南芥;干旱脅迫條件下,轉基因擬南芥MDA含量的減少,說明干旱脅迫條件下轉基因擬南芥細胞膜透性減弱,這可以減緩干旱脅迫的植物傷害,脯氨酸含量的增加可提高植物的滲透調節能力,從而增加植物的耐旱性。說明BiMYB52基因可能通過體內ABA,SA和MeJA多種激素信號途徑來參與白羊草抗旱性調控。這是因為BiMYB52基因的啟動子區域上含有ABREs元件(ACGT),W-box,G-box和一些與干旱、鹽脅迫和低溫脅迫相關的順式作用元件。
4 結論
本研究以前期白羊草干旱脅迫條件下轉錄組測序中所獲得一段類MYB序列,利用基于拓撲異構酶快速擴增法從白羊草中克隆到R2R3-MYB型的基因BiMYB52,經生物信息學分析發現其N端具有較高的保守性。利用染色體步移技術獲得該基因的啟動子,通過對啟動子的分析對其進行了相應的脅迫處理,發現BiMYB52不僅受低溫、干旱和高鹽脅迫的誘導,同時外源激素ABA,SA和MeJA也能誘導其表達量增加。通過對轉基因擬南芥進行干旱脅迫,對轉基因植株干旱脅迫復水后存活率、丙二醛MDA和脯氨酸含量的測定表明轉基因擬南芥的抗旱性明顯優于野生擬南芥。這位進一步揭示白羊草BiMYB52基因在非生物脅迫中的調控作用奠定了基礎。

