一例鴨疫里默氏桿菌病的診斷與防治
白紅英,劉洋洋,曹嫚嫚
廣東茂名農林科技職業學院,廣東茂名 525000
鴨疫里默氏桿菌病是一種對雛鴨、雛鵝等家禽具有較強傳染性和危害性的細菌類疾病,能夠導致感染家禽出現氣囊炎、心包炎、肝周炎等典型病變,嚴重影響患病家禽的生長發育并具有致死性。通過研究發現,鴨疫里默氏桿菌具有多達21種,并且不同血清型的菌株之間缺乏交叉免疫防護效果,另外,與其他病原菌的繼發和并發感染頻出。因此養殖人員面臨著該病防治困難的問題,所以選擇合理的防治和用藥顯得至關重要。
1 鴨疫里默氏桿菌病案例分析
1.1 養殖場雛鴨發病概況
某飼養場養殖的1 800只雛鴨在16日齡時突發疫病,在3日內累計死亡雛鴨125只。發病的雛鴨在食量方面顯著降低,約450只雛鴨具有站立困難、雙腳軟弱無力、嗜睡、精神萎靡等病癥,眼睛、鼻子等部位多見黏液流出,糞便稀疏呈綠色與黃白色,部分雛鴨在瀕死狀態時展現出較為直觀的神經病癥,最終抽搐死亡。
1.2 死亡雛鴨病理分析
通過對10只病死的雛鴨進行解剖病理分析發現,病鴨漿膜處存在廣泛的纖維素性滲出,肝臟部位存在易剝離的灰白色偽膜,內部具有棕紅色、土黃色等多種顏色;胸壁明顯滲出淡黃色膠樣物質;膽囊內部膽汁充盈腫大;心臟心包積液增加,心包膜表面附著灰白、黃色等多種顏色的滲出物,心外膜滲出纖維素性物質;肺部發炎水腫;腎臟充血。部分病死雛鴨存在跗關節腫脹、腦膜炎等問題。
2 實驗室診斷分析方法
2.1 診斷對象及材料應用情況
為分析雛鴨感染病菌類型,選擇6只病鴨抽取肝臟組織以及心包積液用于檢測。檢測期間需應用的材料包括:PCR試劑、標準型DNA Marker(DL2000)、細菌基因組提取試劑盒、自制巧克力細菌培養基、核酸染料、TSA培養基、TSB培養基、麥康凱瓊脂培養基、革蘭氏染液、瑞氏染液、微量生化鑒定管、新生牛血清、藥敏紙片、瓊脂糖、綿羊全血(無菌脫纖維)。
2.2 細菌鑒定診斷方法
2.2.1 細菌培養方法
利用自制的巧克力培養基接種采集自病鴨的肝臟組織以及心包液,培養環境為37 ℃恒溫,內部二氧化碳比例為5%,24 h后對菌落生長情況進行觀察記錄。在無菌條件下進行單個菌落的選取工作,并以37 ℃恒溫環境分別在麥康凱、巧克力培養基中培養12~24 h。將單個菌落從純化后的菌落中選出,于TSB培養基中以37 ℃恒溫培養12~24 h,培養基中需添加5%比例的牛血清。培養完成后,通過革蘭氏染色鏡檢對培養的純培養物的染色特性和形態進行觀察分析。
2.2.2 利用生化試劑檢測鑒定
參考RA鑒定圖譜選取分離菌,在各類微量生化管(尿素、乳糖、賴氨酸等)中接種純培養物,在37 ℃恒溫環境中進行1~2d的培養,需將環境內二氧化碳濃度控制在5%,培養完畢后對反應結果進行觀察記錄。
2.2.3 利用PCR試劑檢測鑒定
在無菌條件下選擇2 mL分離菌的純培養物,按照標準開展細菌DNA提取工作,結合RA細菌外膜蛋白A對特異性引物進行設計,并利用PCR試劑基于分離菌總DNA進行擴增,具體操作過程中需遵循25 μL體系,依次進行預變性處理、變性處理、退火處理、延伸處理,時間分別為3 min、45 s、45 s、45 s,溫度分別為95、95、54、72 ℃,進行30次循環后開展10 min 72 ℃的延伸處理工作。利用1.2%瓊脂糖凝膠對擴增后的DNA進行電泳檢測,并由第三方開展PCR基因測序工作。
2.3 藥敏試驗
利用材料中的藥敏紙片開展藥敏試驗。在實際操作時,需在TSB培養基中接種單個純培養菌落,培養基需添加5%的牛血清,在37 ℃恒溫振蕩箱中培養,在180 r/min的振動箱轉速中進行16 h培養工作。選取100 μL菌液在巧克力培養基中涂抹,當菌液干燥后將藥敏紙片粘貼在培養基上,期間需用無菌鑷子操作,在37 ℃恒溫箱內進行1~2d的培養,箱內二氧化碳濃度需控制在5%,培養結束后對抑菌圈直徑進行測量,根據直徑數據對藥敏性進行判定。
3 診斷結果與防治方法
3.1 鑒定結果分析
生化測試結果表明,分離菌無法將蔗糖、乳糖等發酵,不會將賴氨酸等水解,對硝酸鹽還原、苯丙氨酸、硫化氫等檢測結果為陰性,對氧化酶、過氧化氫酶、尿素等檢測結果為陽性,各種試驗檢測結果與RA特征一致。
根據PCR擴增檢測結果得出,分離菌如預期一般具有663 bp的單一條帶,通過基因測序比對確認,檢測結果與已公布的RA細菌外膜蛋白A完全同源,確認病鴨所感染的細菌類型為RA。
3.2 藥敏試驗結果分析
為分析病鴨所感染RA對各類抗生素的敏感性,對常用的16種抗生素進行藥敏試驗得到結果如表1所示。結果表明,病鴨感染的RA對新霉素、卡那霉素以及哌拉西林三類抗生素具有較強的敏感性,等級為S;對青霉素、氟苯尼考、羧芐西林以及頭孢他定敏感性極低,在防治RA的過程中可以應用敏感性較高的卡那霉素、新霉素等抗生素開展治療工作。
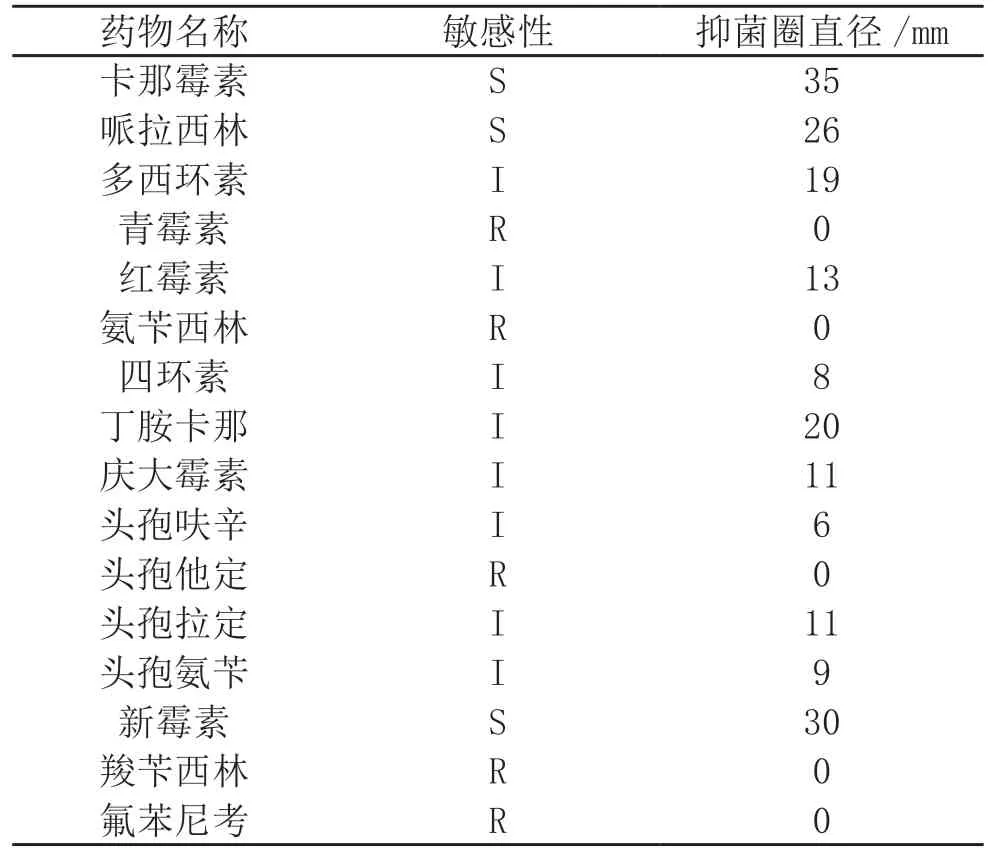
表1 分離菌藥敏試驗結果
3.3 疾病防治方法
根據藥敏試驗結果可以確認,病鴨的治療可以借助抗生素卡那霉素進行,由于大多數病鴨在飲水量、采食量方面受到較大影響,精神狀況不佳,故選擇肌肉注射的方式使用抗生素,鴨肌肉注射硫酸卡那霉素注射液30~40 mg/kg。如果病鴨的病情極為嚴重,則可以增加用藥頻次,選擇在注射抗生素1d后再次注射。注射完成后,養殖人員可以按照0.15g/kg的比例在水中添加20%的該類抗生素藥粉,同時將鴨益康作為輔助抗生素混合其中,作為飲用水供給病鴨使用5d。結果表明,注射藥液后,病鴨死亡率大幅度降低,身體條件得到改善,服用藥水5d后,無病鴨死亡情況,病鴨幾乎全部恢復正常。
4 鴨疫里默氏桿菌病應對措施
4.1 定期接種疫苗
為了實現對鴨疫里默氏桿菌病的有效應對,養殖人員可以采取定期接種的方式提升所養殖鴨、鵝等家禽的抗病能力。當種鴨接種疫苗后,雛鴨將會在更高母源抗體滴度的作用下得到更長久的保護,種鴨自身病菌攜帶量也會隨之降低,避免產生垂直傳播等問題,在保健藥物的共同作用下,能夠進一步強化自身的抵抗能力,下面對各種疫苗進行詳細論述。
滅活疫苗根據有無佐劑可以區分為兩類,相關研究表明,疫苗添加油乳劑能夠起到良好的保護效果,但容易因為接種對動物造成局部傷害;油佐劑相對甲醛滅活疫苗具有較高的免疫效果,抗體檢測數據指出,10日齡接種疫苗能夠具有更高的免疫效果,而且免疫次數應為2次。
4.2 日常預防措施
養殖人員需要重視日常管理對防治鴨疫里默氏桿菌病的積極作用,在規模化養殖期間,積極采取全進全出的飼養模式。在飼料方面需要結合雛鴨等動物的營養需求做好飼料配比工作,合理利用礦物質、維生素等增強動物自身免疫力。同時,養殖人員也需要做好環境消毒處理與相關隔離措施,避免污染的水源、飼料等因素造成鴨的感染而發病。
4.3 疫病發生時的措施
當發生鴨疫里默氏桿菌病時,養殖人員需要做好病死雛鴨等動物殘留物的無害化處理工作,加強對病鴨所處環境的消毒處理力度,做好健康雛鴨與病鴨的隔離,及時開展細菌藥敏試驗并根據藥物敏感性試驗結果,選擇合適藥物,實現對病鴨等患病動物的快速治療。
5 結語
本文通過病鴨剖解的方式對病鴨病理狀況進行了觀察分析,將病鴨心包液、肝臟等作為材料進行了生化鑒定與PCR檢測,確認病鴨所感染病菌為RA,通過藥敏試驗的方式確定了RA各類抗生素的敏感性,最終選擇利用卡那霉素抗生素完成了對病鴨的治療。鴨、鵝等動物養殖人員需要充分認識到RA病菌對雛鴨、雛鵝等動物的危害性,一方面采取注射疫苗、日常防控管理等措施降低發病概率,另一方面也需要掌握發病時的隔離、消毒以及治療措施,實現對RA病菌的有效防治。

