國外藥品生產遠程檢查模式介紹及啟示 Δ
史揚帆,付佳男,顏建周,邵蓉 (中國藥科大學國家藥物政策與醫藥產業經濟研究中心,南京 211198)
近年來,“長春長生問題疫苗”等事件的發生引起了我國藥監部門的高度重視,各地藥監部門開始對藥品生產現場傳統檢查模式中存在的不足之處進行探究。傳統檢查的核心是產品的原材料控制、生產過程控制和產品放行[1],直接在藥品生產現場尋找問題、發現問題和處理問題,導致技術審查工作量大、耗時長以及檢查方案前瞻性和自主性不強等問題。為了解決這些問題,國外對藥品生產現場遠程檢查模式開展了許多研究,并在2019年國際突發公共衛生事件中正式投入使用。筆者在本文中對國外典型國家和地區藥品生產現場遠程檢查模式的適用情形、實施流程、檢查技術以及相關注意點進行了梳理,旨在為構建我國藥品生產現場遠程檢查模式提供參考。
1 國外典型國家和地區藥品生產現場遠程檢查模式現狀
世界各國已經對藥品生產現場遠程檢查開展了大量研究。2019年國際突發公共衛生事件期間,為了應對公共衛生安全事件,已有不少國家或地區的藥品監管部門出臺了相關文件以指導藥監部門如何展開藥品生產現場遠程檢查,并且在世界范圍內展開了試點。其中,澳大利亞治療產品管理局(Therapeutic Goods Administration,TGA)的遠程檢查指南表達了通過完全遠程檢查或混合檢查的形式進行海外檢查的期望,而英國藥品和健康產品管理局(Medicines and Healthcare Products Regulatory Agency,MHRA)通過發布首個遠程檢查指南,強調了遠程檢查可以塑造全新的監管格局,即區別于傳統現場檢查的全新藥品監管方式[2]。相比之下,美國食品藥品監督管理局(Food and Drug Administration,FDA)、歐洲藥品管理局(European Medicines Agency,EMA)和日本醫藥品與醫療器械局(Pharmaceuticals and Medical Devices Agency,PMDA)在各自的指南中提出了藥品生產現場遠程檢查的具體實施要求,比如對遠程檢查的適用情形、實施流程、檢查技術以及注意點進行了規定,為開展遠程檢查制定了規范化標準。
1.1 遠程檢查的適用情形
大部分國家的藥品監管部門均指出,藥品生產現場遠程檢查并非適用于所有情形,該檢查形式只針對某些因危急情況而無法展開現場檢查的特殊情形。2019年國際突發公共衛生事件之前,EMA就提出了遠程檢查的適用情形,比如在與藥物警戒相關的檢查指導文件《在危機情況下對MAHs進行遠程藥物警戒檢查-需要考慮的要點》(Remote Pharmacovigilance Inspections of MAHs during a Crisis Situation-points to Consider)中指出,因健康損害風險和地方當局建議而限制進入藥品生產現場或者可能會對藥品生產現場產生污染的情況下可以開展遠程檢查[3]。歐洲藥品質量管理局(European Directorate for the Quality of Medicines & Healthcare,EDQM)則在2019年國際突發公共衛生事件期間明確將“實時遠程檢查”作為《藥品生產質量管理規范》(Good Manufacturing Practice of Medical Products,GMP)檢查的一種永久性措施,并指出實時遠程檢查的主要適用情形[4],主要包括:(1)旅行限制,如疫情流行和目的地國家安全問題;(2)在此前實施的現場檢查中顯示出良好合規性;(3)藥品生產活動中需要采取糾正和預防措施(corrective action and preventive action,CAPA)的環節,即在藥品生產活動中需要對存在或潛在的不合格原因進行調查分析,采取措施以防止問題再發生或避免發生的環節;(4)需要進行緊急GMP評估,但是這種情況下實時遠程檢查不會完全取代現場檢查。FDA的遠程檢查文件《COVID-19突發公共衛生事件期間藥品生產和生物研究監測設施遠程互動評估》(Remote Interactive Evaluations of Drug Manufacturing and Bioresearch Monitoring Facilities during the COVID-19 Public Health Emergency)也明確了遠程檢查的適用類型[5],主要包括預批準檢查、預許可檢查、審批后檢查、監督檢查、跟蹤和合規檢查以及生物研究檢查。在確定是否進行遠程檢查前,FDA項目辦公室會與受檢企業進行事先溝通,并對檢查目的、項目和類型進行審核,以確認進行遠程檢查的適宜性。而PMDA公布的遠程檢查文件《作為藥品和再生醫療產品合規性檢查一部分的遠程檢查程序》(Procedure for Remote Inspection as a Part of Compliance Inspection on Drugs and Regenerative Medical Products)只對藥品生產文件的合規性檢查進行了規定,并沒有過多對于遠程檢查適用情形的規定。
1.2 遠程檢查的實施流程
針對疫苗、血液制品等生物制品,出于生物安全的考慮,部分生產步驟會限制檢查員進入生產車間開展現場檢查。為解決該問題,美國國家科學基金會(National Science Foundation,NSF)開發了一種遠程檢查四步法,并將其應用于遠程的GMP檢查中[6]。具體步驟包括風險評估、遠程評估質量體系、遠程審計和現場評估,具體實施流程見圖1。FDA在該四步法的基礎上將遠程檢查流程分為計劃和實施兩大階段。在計劃階段,FDA項目辦公室需要選擇并通知生產企業開展遠程檢查的意圖,并確定生產企業的信息傳輸記錄以及進行遠程交互的能力。此外FDA還需要為遠程檢查做準備,一旦生產企業確認有意愿并有能力開展遠程檢查,FDA將安排一次簡短的線上會議與受檢企業共同確定檢查注意點。在實施階段,FDA則明確規定了相關信息技術和文件交互要求以確保遠程檢查順利進行。

圖1 NSF遠程檢查四步法的實施流程
相比之下,EMA發布的遠程檢查指南《關于GMP/GDP和PMF遠程評估的指導意見》(Guidance Related to GMP/GDP and PMF Distant Assessments)則提出了更加細致完整的實施流程[7],主要包括計劃階段、準備階段、組織階段和事后階段,具體實施流程見圖2。GDP指藥品優良運銷規范(Good Distribution Practice),PMF指主血漿文件(Plasma Master File)。在計劃階段,生產企業需要配備適當的平臺以便能夠及時提供數據(如較為安全的云服務器);生產企業與檢查員需要使用電話會議/視頻會議或其他方式以便生產企業和領域專家進行實時討論;現場操作人員需要實時共享現場使用的計算機屏幕,或向檢查員提供遠程訪問計算機系統的權限;生產企業需要提供生產現場攝像或視頻記錄以便檢查員遠程檢查生產操作、設備、設施和相關文件;生產企業與檢查員還需要配備有分會場/會議室和屏幕共享的實時視頻會議平臺、可與視頻會議平臺接口的智能眼鏡或其他移動攝像機,以及能夠安全共享文檔的云服務器等。在準備階段,EMA需要制定和公布遠程檢查計劃概述每個檢查員需要檢查的區域并分享現場檢查計劃和時間表,避免檢查員發生重復檢查和因時差無足夠時間進行實時討論的情況發生。組織階段的一般流程包括開展開幕會議、執行遠程檢查以及開展閉幕會議。最后的事后階段則是對遠程檢查中發現的問題進行回顧,并要求生產企業進行專項整改的過程。
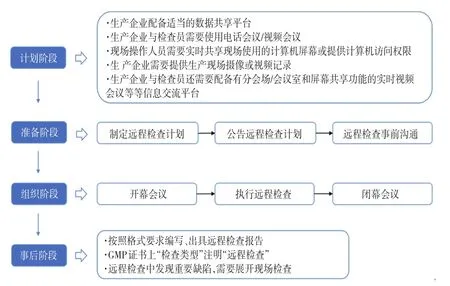
圖2 EMA遠程檢查的實施流程
PMDA發布的遠程檢查指南《作為藥品和再生醫療產品合規性檢查一部分的遠程檢查程序》(Procedure for Remote Inspection as a Part of Compliance Inspection on Drugs and Regenerative Medical Products)則注重對生產文件檢查的程序規定[8],其具體檢查流程見圖3。PMDA遠程檢查的核心步驟包括預檢查和主檢查兩個階段,進一步細分可以分為事前溝通、文件提交、預檢查、主檢查和檢查后階段。在事前溝通階段,PMDA需要確定遠程檢查的時間安排,并通過電子郵件或電話向生產企業明確檢查意圖、預檢查時間表和文件提交方法。在文件提交階段,檢查員需要在檢查當天或前1天告知生產企業檢查條件/范圍,生產企業需要向檢查員提交生產文件。在預檢查階段,檢查員對生產企業提交的生產文件進行檢查,如發現任何問題檢查員都應當詢問生產企業。在主檢查階段,檢查員需要通過視頻會議系統檢查預檢查階段未提交的文件并對發現的問題與生產企業進行談話。在檢查后階段,生產企業需要根據檢查員的指示和檢查結果采取行動。

圖3 PMDA遠程文件審查流程
1.3 遠程檢查的檢查技術
2019年國際公共衛生事件期間,歐盟采用了全新的遠程交互技術以幫助藥監部門進行藥品生產遠程檢查,比如EMA利用虛擬現實和混合現實平臺對賽默飛世爾科技公司運營的一系列用于腺伴隨病毒、慢病毒和各種其他病毒載體的懸浮液和黏附性制造平臺進行了遠程檢查[9];EDQM則利用實時遠程檢查工具足不出戶對印度2家制藥廠進行了遠程檢查,他們主要利用的技術包括360°攝像機、Matterport 3D技術和文件審查軟件(Microsoft Teams)等。由于PMDA與FDA在指南中指出的遠程檢查技術與EMA所使用的技術大同小異,比如監控攝像頭和文件共享工具等,下文不再進行分開論述。
1.3.1 360°攝像機 現場操作員將360°攝像機連接到遠程檢查員的手機或平板電腦上,然后將其安裝在靜脈輸液桿上,該設備可以在光滑地面上繞著現場設施旋轉,可實現對生產設施進行直播并向檢查員實時傳遞視頻。此外,攝像機本身的分辨率極高,可以在檢查過程中識別文檔、標簽和工作日志。該設備的優點在于可以根據生產車間的潔凈度需求進行適當清潔以便隨時攜帶設備進出車間。針對某些特殊情況,EMA還使用了全息鏡頭,這是一項虛擬現實技術,用于展示360°攝像機無法顯示的生產場所,比如生物安全柜等。該全息鏡頭可以實現對GMP設施的遠程檢查。
1.3.2 Matterport 3D技術 賽默飛世爾科技公司使用的另一項技術是Matterport 3D映射技術,這項技術通常被房地產經紀人用來繪制房屋地圖以供在線查看現場設施設備的大致布局狀況。EMA與賽默飛世爾科技公司利用該技術對生產車間進行虛擬地圖繪制,以便引導檢查員初步了解設施狀況。但是Matterport 3D技術僅用于引導檢查員進行遠程的設施參觀,幫助其初步了解現場設施設備布局,并不能取代360°攝像機和全息鏡頭的實時直播功能。
1.3.3 文件審查軟件 文件審查軟件是許多辦公室工作人員用于日常溝通的文件共享工具,賽默飛世爾科技公司利用該技術構建了一個虛擬文件室并以一種便于檢查員審核的方式管理文件,而且還讓企業自身把握文件的控制權來存儲關鍵文件。這種方式的優點在于檢查員可以使用與本地計算機應用程序相同的功能在網頁上訪問。生產企業將計算機中的文檔發布到文件審查軟件上,并授予檢查員臨時的網頁訪問權限,這樣各方都可以在自己的信息系統中管理文件以控制文件傳輸的泄露風險。
1.4 遠程檢查的注意點
為了避免遠程檢查過程出現程序性和技術性問題,生產企業、檢查員和檢查派出機構需共同關注遠程檢查中的以下注意點。
1.4.1 對信息設置訪問權限 FDA通常會在進行遠程檢查之前要求預先審查生產企業的相關文件和信息以確保檢查互動的高效進行,此外FDA還有可能會在遠程檢查期間隨時要求生產企業提供錄像等其他信息。為了防止在信息共享的過程中出現信息泄露,藥品生產企業需要對信息進行加密,并設置FDA的信息訪問權限。FDA在遠程檢查的準備階段會要求提前確定雙方共享信息和收集現場照片或視頻的方式,同時還要求確定檢查員需要獲得哪些生產區域的檢查權限,以便在保證信息安全的同時能夠保證遠程檢查順利進行。
1.4.2 對遠程檢查員進行培訓 遠程檢查過程中需要操作員和檢查員相互配合使用遠程檢查技術和設備,一般情況下未經過培訓的普通檢查員和操作員并不熟悉具體檢查流程和設備操作方法,而且雙方無法進行默契配合從而可能會影響檢查效率和效果。因此,FDA和EMA均要求對操作員和檢查員進行提前的專項培訓并開展模擬遠程檢查,確保操作員熟悉遠程檢查的基本流程并在正式的遠程檢查會議前與檢查員進行積極溝通,保證遠程檢查順利進行。
1.4.3 對檢查設備進行檢驗 為了避免出現設備問題阻礙遠程檢查順利進行,FDA和EMA均要求對檢查設備進行事前檢驗。EMA在文件中明確規定進行遠程檢查前,首先需要對所有檢查平臺和軟件進行檢驗,幫助檢查員和操作員了解虛擬檢查平臺,練習使用文件審查軟件下載文件;其次,生產企業需要與檢查團隊共同進行模擬檢查,檢查視頻和音頻質量狀況,在正式檢查前解決現場生產信息的傳輸問題;最后,檢查前需要檢驗文件審查技術問題,確保檢查員可以獲得生產文件,并有相關的安全保護措施保障生產文件傳輸的保密性。同樣地,PMDA也要求在開展生產文件的遠程檢查前需要對云系統和視頻會議系統進行檢驗,比如生產企業應當采取有效的預防措施,防止在用于連接的設備和線路上發生信號攔截或者未經授權的訪問等問題發生。如果在事前檢驗中系統出現重大安全問題,生產企業應當及時與PMDA進行溝通,考慮暫停或推遲遠程檢查,由雙方重新商討遠程檢查的啟動時間和方式。
2 我國藥品生產現場遠程檢查模式的現狀
由于遠程檢查一方面可以作為旅行限制期間無法抵達生產現場的臨時替代檢查方式,另一方面也可以在一定程度上解決現場檢查缺乏時效性的問題,因此我國十分關注藥品生產現場遠程檢查的應用,各省級藥監部門都在嘗試將遠程檢查作為日常檢查的替代手段。相比于FDA“遠程檢查”(remote inspection)或“遠程評估”(remote evaluation)以及歐盟“遠程評估”(distant assessment)的定義,我國的藥品生產遠程檢查更多被定義為非現場檢查[10]。比如河南省藥監局的藥品生產智慧監管系統“千里眼工程”本著“有用+精簡”原則,已通過固定視頻監控、遠程移動檢查、質量關鍵參數3種途徑,實現了非現場遠程監管的目的;浙江金華市藥品智慧檢查系統利用人工智能(artificial intelligence,AI)技術打造了藥品檢查數字應用軟件,實現了檢查員科學管理、檢查結果開發運用、企業風險預警三大功能。我國各省市具有代表性的遠程檢查系統見表1。

表1 我國各省市具有代表性的遠程檢查系統
綜上,雖然目前我國各省市針對遠程檢查已經開展了許多嘗試,但構建我國藥品生產遠程檢查模式還面臨一些挑戰。首先,現有的關于遠程檢查的大部分探索主要停留在對遠程檢查利用的可視化和數據共享技術以及其他智能化監管系統上,尚缺少對遠程檢查具體操作流程的系統化規定,這就可能影響遠程檢查的合規化與有序化進行。其次,并非所有項目都適合進行遠程檢查,我國目前缺少對遠程檢查適用情形的詳細規定,這也可能會影響遠程檢查效果。再次,我國目前的遠程檢查尚未將一些智能化技術應用到遠程檢查的生產信息采集過程中,這在一定程度上也會影響遠程檢查的效率。最后,由于遠程檢查的技術要求較高,對于未經歷過培訓的操作員和檢查員而言,缺乏系統化的培訓可能會導致其無法勝任遠程檢查工作等。
3 國外經驗對我國的啟示
3.1 出臺統一的藥品生產遠程檢查指南,明確遠程檢查適用情形
就目前我國的藥品檢查現狀而言,遠程檢查是無法完全替代現場檢查成為主要檢查方式的,這是由于有些項目對于檢查要求比較嚴格,遠程檢查無法很好地對這些項目開展針對性檢查,因此明確遠程檢查的適用情形對于確保遠程檢查的順利進行是十分重要的。建議我國可以在國家層面出臺統一的藥品生產遠程檢查指南,并且在指南中明確指出遠程檢查的具體適用情形,一方面可以參考國外典型國家和地區的經驗,將我國目前藥品檢查的主要種類即許可檢查、常規檢查、有因檢查和其他檢查進一步細化,比如在指南中規定對于因旅行限制(如疫情流行和目的地國家安全問題)、在此前實施的現場檢查中顯示出良好合規性、需要采取糾正和預防措施的生產環節、需要進行緊急的GMP評估等情形,經過檢查派出機構的風險評估后可以采取遠程檢查的方式代替現場檢查。另一方面,可以廣泛征集領域內相關專家的意見,在指南中規定如非必要,對于藥品生產過程中風險較高的環節和步驟以及疫苗、血液制品等生產條件和監管要求較為嚴格的重點藥品,不應當作為藥品生產遠程檢查的首要適用情形。
3.2 參考藥品生產企業意見制定藥品生產遠程檢查實施流程
藥品生產遠程檢查不僅需要檢查派出機構作為檢查主體,還需要藥品生產企業積極配合方可完成整個檢查流程。我國藥監部門可以借鑒國外典型國家和地區的非現場檢查工作的實踐,結合我國藥品檢查的實際情況研究制定統一的《藥品生產企業遠程檢查工作程序》等制度文件,并聚焦具體品種的質量風險,起草非現場檢查工作方案,明確從受檢企業申請展開遠程檢查、提交檢查材料到檢查派出機構展開遠程檢查以及檢查后整改評估等系統化流程。整個流程應當包括計劃、準備、組織和檢查后階段在內的主要檢查流程:在計劃階段,檢查派出機構需要與受檢企業進行溝通交流并對遠程檢查實施的可行性進行評估,由專家級檢查員組成的檢查組應提前與受檢企業召開溝通會,重點就提交資料的準備要求進行溝通;在準備階段,檢查派出機構需要與受檢企業進行事前的模擬檢查,再次研判分析風險情形和確認檢查重點,確認檢查設備以及關鍵人員已經準備到位并向企業公布檢查計劃和相關事宜,為高質高效開展遠程檢查奠定工作基礎;在組織階段,檢查員與操作員需要按照事先制定的計劃相互配合并按部就班地對各項目進行檢查;最后,在檢查后階段,則需要檢查派出機構對檢查中的問題進行回顧分析,告知受檢企業及時進行整改。
3.3 結合藥品生產企業信息化建設水平,使用智能化的遠程檢查技術
我國藥品生產遠程檢查利用的技術僅停留在安裝監控攝像頭以及數據共享系統上,對于特殊的傳感器以及智能化數據采集設備等的應用缺乏實踐。為提高遠程檢查的實施效果和效率,我國藥品檢查派出機構可嘗試依照檢查的具體要求,利用虛擬現實技術比如Matterport 3D技術等引導檢查員提前了解生產現場的大致狀況,也可以利用諸如360°攝像機等設備促使檢查員和操作員之間開展積極的互動,實時獲取生產現場的狀況。針對生產文件的審查,可以利用文檔查看器將紙質文件的實時投影傳輸給檢查員,并利用虛擬文件室管理生產文件,實現生產企業和檢查員之間的文件共享,同時采取信息保密措施保障生產信息的安全。但需要注意的是,我國藥品生產企業的信息化水準差異較大,因此檢查派出機構需要結合受檢企業的信息化水平采用合適的遠程檢查技術和設備展開遠程檢查。
3.4 制定專門的藥品生產遠程檢查培訓方案,培養專業的遠程檢查團隊
雖然我國正積極推進專業化藥品檢查員團隊的建設并且取得了顯著成效[16],但是由于在檢查過程中需要檢查員熟練掌握檢查技術,這對遠程檢查員的專業能力提出了更高要求。因此,我國藥監部門可以制定統一的藥品生產遠程檢查培訓方針,各省市藥監部門以及相應的藥品檢查派出機構可結合各地藥品生產企業的信息化水平,從藥品生產遠程檢查的具體要求出發,依照方針制定專門的藥品生產遠程檢查培訓方案,將遠程檢查員需要熟悉的檢查流程和使用的檢查技術等作為遠程檢查培訓的重點內容,由藥品檢查派出機構對遠程檢查員進行檢查流程的理論知識培訓以及檢查技術和設備的實踐操作培訓,并且定期組織遠程檢查的考核,確保檢查員能夠熟練掌握相關操作以保證遠程檢查順利進行,從而構建起一支既具備基礎檢查知識又掌握高新技術的遠程檢查團隊。
綜上所述,我國的藥品生產遠程檢查模式相較于國外仍處于起步階段,因此我國應當積極借鑒國外典型國家和地區遠程檢查的理論和實踐經驗,從上述4條啟示著手建立并完善適應我國國情的藥品生產遠程檢查模式。

