7-羥乙基白楊素對低壓缺氧致PC12細胞損傷的改善作用及機制 Δ
張冬梅,高迎春,張潔,景臨林,馬慧萍 (聯(lián)勤保障部隊第九四〇醫(yī)院藥劑科/全軍高原醫(yī)學實驗室,蘭州730050)
我國高原面積廣闊,具有重要的政治、軍事和經(jīng)濟地位。氣壓低、氧含量低是高原環(huán)境最主要的特征。大腦對低氧刺激尤為敏感,動物研究和臨床試驗表明,急性低壓缺氧可導致大腦皮質(zhì)神經(jīng)細胞、海馬神經(jīng)細胞損傷[1]。當腦神經(jīng)細胞缺氧時,氧氣及營養(yǎng)物質(zhì)消耗所導致的線粒體損傷、神經(jīng)細胞丟失、氧化應激或細胞壞死、凋亡、自噬是缺氧性損傷的關鍵環(huán)節(jié)[2―4],但目前關于高原低壓缺氧致神經(jīng)細胞損傷的機制及藥物研究較少,其預防和治療一直面臨著較大壓力。可見,探索低壓缺氧致神經(jīng)細胞損傷的發(fā)生機制并尋找抗低壓缺氧損傷藥物具有重要意義。
近年來有研究表明,黃酮類化合物具有改善缺氧損傷神經(jīng)的藥理作用,如抗氧化、抗炎、抗凋亡作用等[5―7]。白楊素(化學名5,7-二羥基黃酮)又名白楊黃素,是來源廣、毒性低的黃酮類化合物,具有抗焦慮、抗抑郁和保護神經(jīng)等多種生物活性,但其生物利用度較低[3]。為了改善白楊素的上述缺點,本課題組通過結構修飾合成了7-羥乙基白楊素[化學名5-羥基-7-羥乙氧基黃酮,英文名7-hydroxyethyl chrysin,以下簡稱“7-HEC”][8];藥理研究表明,7-HEC能改善低壓缺氧誘導的腦組織損傷、認知功能障礙,并能逆轉(zhuǎn)缺氧模型大鼠海馬神經(jīng)細胞損傷[9],但具體機制尚不清楚。PC12細胞是研究神經(jīng)生理和神經(jīng)藥理的常用細胞之一,本課題組為了更好地模擬高原環(huán)境,在單純?nèi)毖跄P偷幕A上進行改良,建立了PC12細胞低壓缺氧損傷模型,并證實了低壓缺氧可誘導該細胞凋亡[10]。研究指出,抗凋亡蛋白B細胞淋巴瘤2(B-cell lymphoma-2,Bcl-2)與促凋亡蛋白Bcl-2相關X蛋白(Bcl-2 associated X protein,Bax)的表達比值決定了細胞凋亡的進程,活化的胱天蛋白酶3(cleaved caspase-3)則是執(zhí)行細胞凋亡的關鍵因子,可見,caspase-3/Bax/Bcl-2通路是調(diào)控細胞凋亡的重要信號通路[11]。基于此,本研究擬探討7-HEC對低壓缺氧致PC12細胞損傷的保護作用,同時以caspase-3/Bax/Bcl-2通路為線索,探討該化合物改善低壓缺氧致PC12細胞損傷的分子機制,以期為7-HEC在高原低壓缺氧損傷防治領域中的應用提供參考。
1 材料
1.1 主要儀器
本研究所用主要儀器包括自制壓力控制型細胞缺氧培養(yǎng)箱(實用新型專利ZL201821672535[12])、EST-10-02型氧濃度測定儀(深圳市興源恒通科技有限公司)、CKX41型倒置相差顯微鏡(日本Olympus公司)、INC 153H9T6型三氣培養(yǎng)箱(德國Memmert公司)、Spectra-Maxi3型全自動熒光酶標儀(美國Molecular Devices公司)、ACEA NovoCyte型流式細胞儀(美國ACEA Biosciences公司)、ChemiDocMP Imaging System型凝膠成像分析系統(tǒng)(美國Bio-Rad公司)等。
1.2 主要藥品與試劑
7-HEC原料藥(純度98%)由本實驗室自制;DMEM高糖培養(yǎng)基購自美國HyClone公司;胎牛血清(fetal bovine serum,F(xiàn)BS)、0.25%胰酶消化液均購自美國Gibco公司;青霉素-鏈霉素雙抗購自蘭杰柯生物科技有限公司;乳酸脫氫酶(lactate dehydrogenase,LDH)試劑盒(批號20180728)、超氧化物歧化酶(superoxide dismutase,SOD)試劑盒(批號20190412)、丙二醛(malondialdehyde,MDA)試劑盒(批號20180728)均購自南京建成生物工程研究所;CCK-8細胞活力檢測試劑盒(批號PM508)購自日本Dojindo公司;Annexin Ⅴ-FITC細胞凋亡檢測試劑盒(批號10625-2)購自上海碧云天生物技術公司;DNA含量檢測試劑盒(細胞周期)(批號20210105)購自北京索萊寶科技有限公司;兔抗鼠Bax單克隆抗體(批號ab32503)、兔抗鼠Bcl-2多克隆抗體(批號ab196495)、兔cleaved caspase-3多克隆抗體(批號ab184787)均購自美國Abcam公司;鼠β-肌動蛋白(βactin)單克隆抗體(批號TA-09)、辣根過氧化物酶標記的山羊抗兔免疫球蛋白G二抗(批號ZB-2307)均購自北京中杉金橋生物技術有限公司。
1.3 細胞
大鼠腎上腺嗜鉻細胞瘤細胞系PC12購自中國科學院上海細胞庫。
2 方法
2.1 細胞培養(yǎng)
將PC12細胞接種于含10%FBS、1%青霉素-鏈霉素雙抗的DMEM高糖培養(yǎng)基(以下簡稱“完全培養(yǎng)基”)中,于37 ℃、5%CO2培養(yǎng)箱中培養(yǎng)。待細胞融合至80%~90%時,用0.25%胰酶消化并按1∶3比例傳代,取對數(shù)生長期的細胞進行后續(xù)實驗。
2.2 分組與處理
根據(jù)不同培養(yǎng)條件,將PC12細胞分為對照組、低壓缺氧組和7-HEC組。對照組細胞用含10%FBS的DMEM高糖培養(yǎng)基培養(yǎng)24 h;低壓缺氧組細胞根據(jù)前期確定的低壓缺氧模型條件[10],于 5%CO2、94%N2、1%O2、54 004 Pa(與5 000 m海拔處大氣壓相當)條件下培養(yǎng)24 h;7-HEC組細胞先用含7-HEC的完全培養(yǎng)基培養(yǎng)30 min后,再按低壓缺氧組方法培養(yǎng)24 h。
2.3 細胞存活率檢測
采用CCK-8法檢測。取生長良好且處于對數(shù)生長期的PC12細胞,用0.25%胰酶消化后,按每孔1×104個接種于96孔板中。將細胞分為對照組、低壓缺氧組、不同濃度7-HEC組(7-HEC終濃度為100、10、1、0.1、0.01 μmol/L,根據(jù)預實驗結果設置),每組設置6個復孔;同時設置不含細胞、不含藥物的空白組。于37oC、5%CO2條件下培養(yǎng)24 h后,棄去上清液,對照組和低壓缺氧組細胞加入完全培養(yǎng)基100 μL,7-HEC組細胞分別加入含7-HEC 100、10、1、0.1、0.01 μmol/L 的完全培養(yǎng)基 100 μL,按“2.2”項下方法處理。培養(yǎng)24 h后,每孔加入CCK-8試劑10 μL,于37 ℃下孵育1 h,使用酶標儀于450 nm波長處檢測各孔的光密度(OD)值并按下式計算細胞存活率:細胞存活率=(實驗組OD值-空白組OD值)/(對照組OD值-空白組OD值)×100%。
2.4 細胞中LDH、MDA含量和SOD活性檢測
取生長良好且處于對數(shù)生長期的PC12細胞,用0.25%胰酶消化后,按每孔2×106個接種于6孔板中。將細胞分為對照組、低壓缺氧組、7-HEC組(1 μmol/L,根據(jù)“2.3”項下結果設置),每組設置6個復孔。按“2.3”項下方法培養(yǎng)24 h,收集細胞和上清液,使用酶標儀以LDH試劑盒(L-P法)檢測上清液中LDH含量,以MDA試劑盒(TBA法)檢測細胞中MDA含量,以SOD試劑盒(WST-8法)檢測細胞中SOD活性,嚴格按照試劑盒說明書操作。
2.5 細胞凋亡和細胞周期檢測
2.5.1 細胞凋亡 采用Annexin Ⅴ-FITC/PI雙染流式細胞術檢測。取生長良好且處于對數(shù)生長期的PC12細胞,按“2.4”項下方法分組(每組設置3個復孔)、處理、培養(yǎng)。隨后,棄去上清液,細胞用4 ℃預冷的磷酸鹽緩沖液清洗2次,用不含乙二胺四乙酸的胰酶消化1 min,于室溫下以1 500 r/min離心5 min;用4 ℃預冷的磷酸鹽緩沖液清洗2次,以1 500 r/min離心5 min,棄去上清液;細胞用1×bingding buffer 400 μL重懸,制成密度為1×106個/mL的懸液;取上述懸液,加入Annexin Ⅴ-FITC試劑適量(每100 μL懸液加入Annexin Ⅴ-FITC試劑5 μL),輕輕混勻,室溫避光孵育15 min;加入PI試劑10 μL和1×binding buffer 400 μL,輕輕混勻,使用流式細胞儀檢測細胞凋亡率(%)。
2.5.2 細胞周期 采用流式細胞術檢測。取生長良好且處于對數(shù)生長期的PC12細胞,按“2.4”項下方法分組(每組設置3個復孔)、處理、培養(yǎng)。隨后,收集各組細胞,用磷酸鹽緩沖液清洗2次后,于-20 ℃ 75%乙醇中固定過夜;以1 500 r/min離心5 min,收集細胞,用磷酸鹽緩沖液清洗2次后,用RNaseA試劑重懸并于37 ℃下孵育30 min;加入PI試劑400 μL,于4 ℃下避光孵育30 min,使用流式細胞儀檢測各周期的分布情況。
2.6 細胞中凋亡相關蛋白表達檢測
采用Western blot方法檢測。取生長良好且處于對數(shù)生長期的PC12細胞,按“2.4”項下方法分組(每組設置3個復孔)、處理、培養(yǎng)。隨后,收集各組細胞,用磷酸鹽緩沖液洗滌2次,加入RIPA細胞裂解液100 μL,于冰浴中放置30 min,于4 ℃下以1 500 r/min離心15 min;取上清液,以BCA法進行定量后,加上樣緩沖液煮沸變性10 min,取變性蛋白樣品50 μg進行10%十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳并轉(zhuǎn)移至聚偏二氟乙烯膜上,用含50 g/L脫脂奶粉的TBST緩沖液室溫封閉1 h,加入cleaved caspase-3、Bcl-2、Bax、β-actin一抗(稀釋比例均為1∶1 000),4 ℃孵育過夜;用TBST緩沖液洗膜3次,加入二抗(稀釋比例為1∶5 000),室溫孵育1 h;用TBST緩沖液洗膜3次,以凝膠成像系統(tǒng)成像,以目標蛋白與內(nèi)參蛋白(β-actin)灰度值的比值表示目標蛋白的表達水平,并記錄Bax與Bcl-2表達水平的比值(Bax/Bcl-2比值),實驗重復3次。
2.7 統(tǒng)計學方法
使用GraphPad Prism 9.0軟件對數(shù)據(jù)進行統(tǒng)計分析。每組實驗至少重復3次。數(shù)據(jù)均以±s表示,多組間比較采用單因素方差分析,組間兩兩比較采用LSD-t檢驗。檢驗水準α=0.05。
3 結果
3.1 不同濃度7-HEC對低壓缺氧細胞存活率的影響
與對照組比較,低壓缺氧組細胞的存活率顯著降低(P<0.01);與低壓缺氧組比較,7-HEC 10、1、0.1 μmol/L組細胞的存活率均顯著升高(P<0.05或P<0.01),提示在上述濃度下,7-HEC可逆轉(zhuǎn)細胞存活率的降低,故選擇作用較明顯的1 μmol/L進行后續(xù)實驗。結果見圖1。

圖1 不同濃度7-HEC對低壓缺氧細胞存活率的影響(±s,n=6)
3.2 7-HEC對低壓缺氧細胞中LDH、MDA含量和SOD活性的影響
與對照組比較,低壓缺氧組細胞上清液中LDH含量和細胞中MDA含量均顯著升高,細胞中SOD活性顯著降低(P<0.01)。與低壓缺氧組比較,7-HEC組細胞上清液中LDH含量和細胞中MDA含量均顯著降低(P<0.01),細胞中SOD活性顯著升高(P<0.01)。結果見表1。
表1 7-HEC對低壓缺氧細胞中LDH、MDA含量和SOD活性的影響(±s,n=6)
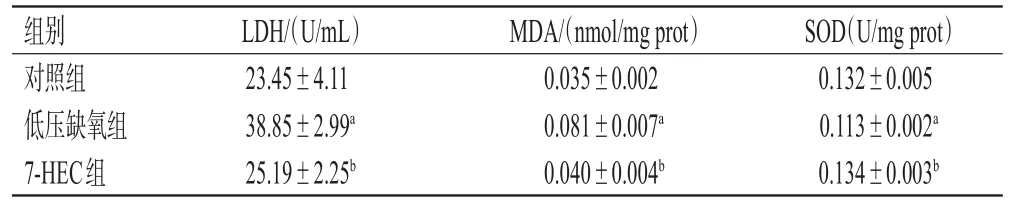
表1 7-HEC對低壓缺氧細胞中LDH、MDA含量和SOD活性的影響(±s,n=6)
a:與對照組比較,P<0.01;b:與低壓缺氧組比較,P<0.01
組別對照組低壓缺氧組7-HEC組LDH/(U/mL)23.45±4.11 38.85±2.99a 25.19±2.25b MDA/(nmol/mg prot)0.035±0.002 0.081±0.007a 0.040±0.004b SOD(U/mg prot)0.132±0.005 0.113±0.002a 0.134±0.003b
3.3 7-HEC對低壓缺氧細胞凋亡和細胞周期的影響
3.3.1 細胞凋亡 與對照組比較,低壓缺氧組細胞的凋亡率顯著升高(P<0.01);與低壓缺氧組比較,7-HEC組細胞的凋亡率顯著降低(P<0.01)。結果見圖2。

圖2 7-HEC對低壓低氧細胞凋亡的影響(±s,n=3)
3.3.2 細胞周期 與對照組比較,低壓缺氧組G1期細胞比例顯著升高,S期、G2期細胞比例均顯著降低(P<0.05或P<0.01);與低壓缺氧組比較,7-HEC組G1期細胞比例顯著降低,G2期細胞比例顯著升高(P<0.01)。結果見圖3。
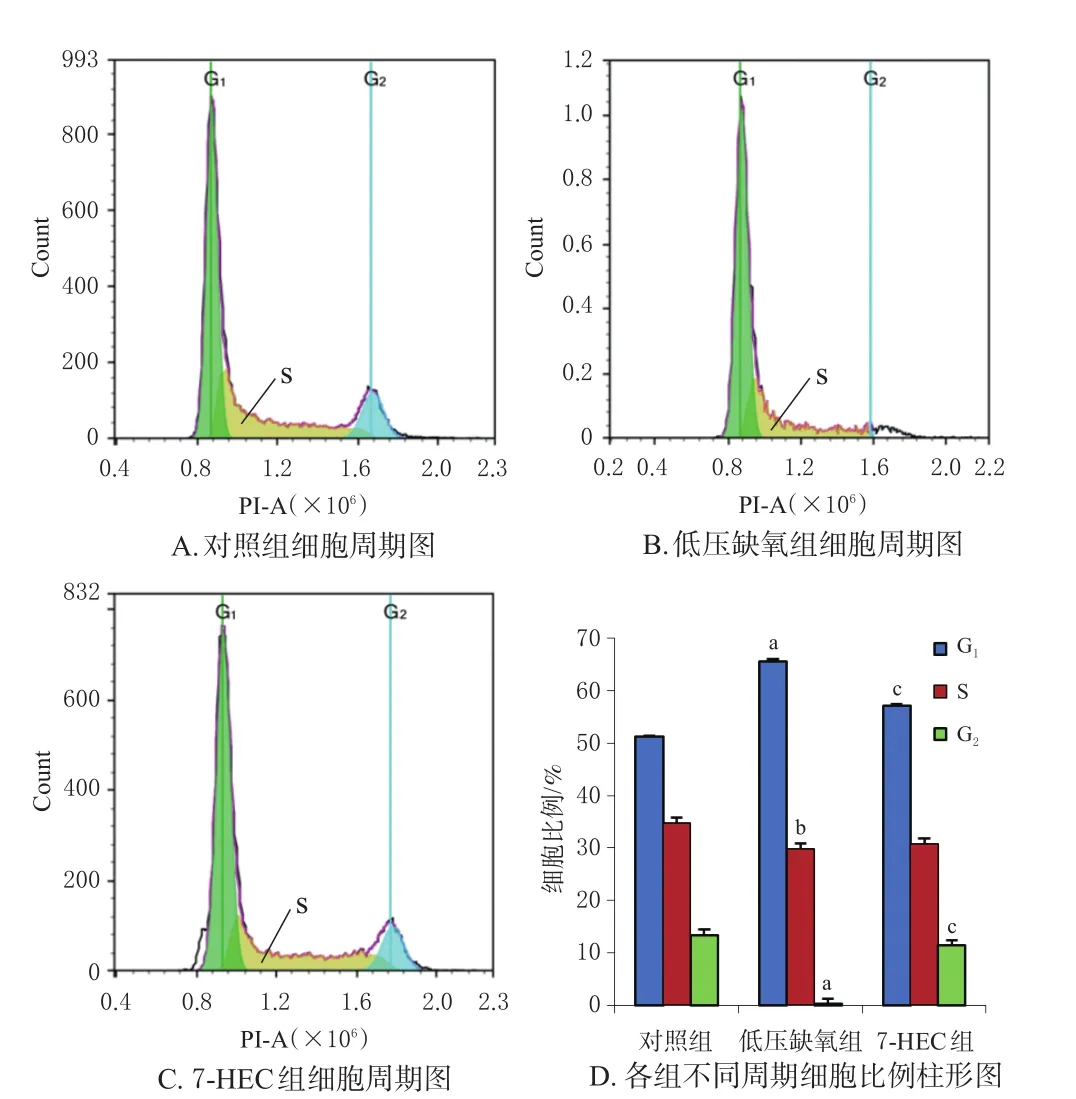
圖3 7-HEC對低壓缺氧細胞周期的影響(±s,n=3)
3.4 7-HEC對低壓缺氧細胞中凋亡相關蛋白表達的影響
與對照組比較,低壓缺氧組細胞中cleaved caspase-3蛋白的表達水平顯著升高,Bcl-2/Bax比值顯著降低(P<0.05或P<0.01);與低壓缺氧組比較,7-HEC組細胞中cleaved caspase-3蛋白的表達水平顯著降低,Bcl-2/Bax比值顯著升高(P<0.05或P<0.01)。結果見圖4。
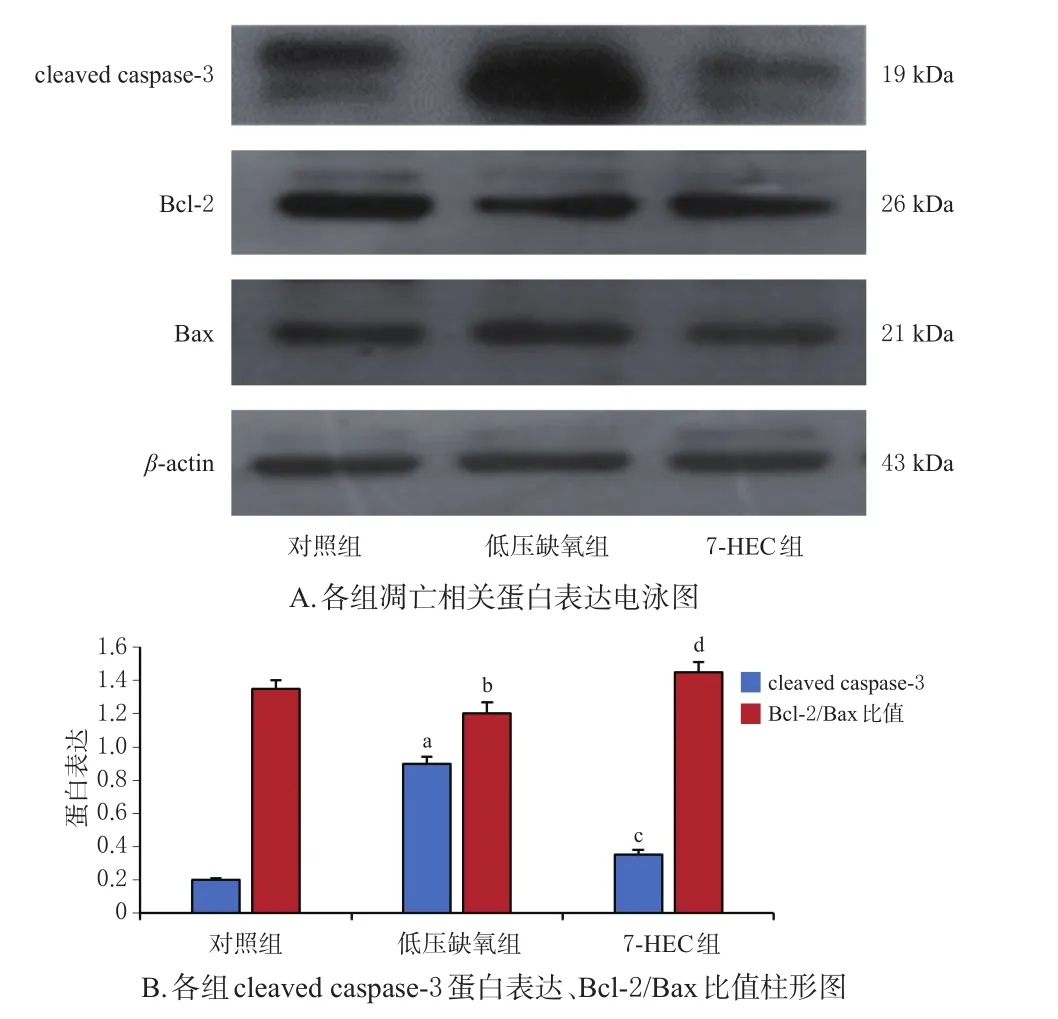
圖4 7-HEC對低壓低氧細胞中凋亡相關蛋白表達的影響(±s,n=3)
4 討論
本研究通過考察7-HEC對低壓缺氧PC12細胞增殖、抗氧化能力、細胞凋亡和細胞周期的影響,評價了該化合物對低壓缺氧致神經(jīng)細胞損傷的保護作用。細胞存活率檢測結果顯示,細胞在低壓缺氧(1%O2、54 004 Pa)條件下培養(yǎng)24 h后,其存活率明顯下降;經(jīng)0.01、0.1、1、10、100 μmol/L的7-HEC提前干預后,7-HEC 0.1、1、10 μmol/L組低壓缺氧細胞的存活率明顯提升,提示上述濃度的7-HEC可逆轉(zhuǎn)細胞存活率的降低;其中,1 μmol/L的活性最佳,故以該濃度作為后續(xù)研究的藥物濃度。
LDH是存在于正常細胞胞質(zhì)中的酶,當細胞膜受損后,LDH即被釋放到細胞外,故可通過檢測細胞上清液中LDH的含量來判斷細胞膜的受損程度[13]。本研究結果顯示,與對照組比較,低壓缺氧組細胞上清液中LDH含量顯著升高;與低壓缺氧組比較,7-HEC組細胞上清液中LDH含量顯著降低。這說明7-HEC對低壓性缺氧引起的細胞膜損傷具有改善作用。
有研究指出,MDA是脂質(zhì)過氧化的標志產(chǎn)物,其含量高低可反映氧化應激的嚴重程度,以及組織受氧自由基破壞的損傷程度;SOD是清除生物體內(nèi)氧自由基的重要物質(zhì),兼具修復細胞的功能,當細胞內(nèi)氧自由基水平升高時,SOD的生物合成及活性將有所增強,可用以間接反映機體氧自由基的生成量及清除氧自由基的能力[14]。本研究結果顯示,低壓缺氧組細胞中MDA含量較對照組顯著升高,SOD活性較對照組顯著降低,提示低壓缺氧細胞的脂質(zhì)過氧化反應增加,抗氧化能力減弱。與低壓缺氧組比較,7-HEC組細胞中MDA含量顯著降低,SOD活性顯著升高,提示該化合物可逆轉(zhuǎn)細胞脂質(zhì)過氧化反應增加、抗氧化能力減弱的現(xiàn)象,可通過調(diào)控細胞氧化/抗氧化失衡而發(fā)揮對低壓缺氧致細胞損傷的改善作用。
本研究應用Annexin Ⅴ-FITC/PI雙染流式細胞術檢測了低壓缺氧細胞的凋亡情況,結果顯示,與對照組比較,低壓缺氧組細胞的凋亡率顯著升高;與低壓缺氧組比較,7-HEC組細胞的凋亡率顯著降低。這表明低壓缺氧可誘導細胞凋亡,而7-HEC具有抑制細胞凋亡的作用。本研究應用流式細胞儀檢測了7-HEC對細胞周期的影響,結果顯示,低壓缺氧組G1期細胞比例較對照組顯著升高,S期、G2期細胞比例較對照組均顯著降低,提示在低壓缺氧條件下,細胞周期阻滯于G1期;經(jīng)7-HEC處理后,上述作用得到逆轉(zhuǎn),G1期的細胞比例明顯降低,G2期的細胞比例明顯上升,S期的細胞比例亦有上升趨勢,提示7-HEC可使進入DNA復制期的低壓缺氧細胞比例增加,可改善低壓缺氧引起的細胞周期阻滯。此結果與CCK-8實驗結果相符。有研究指出,處于G1期的細胞可對各種影響增殖與凋亡的信號進行整合和傳遞,進而決定細胞是否進行分裂、凋亡或延遲分裂,即進入G0期[15―16]。結合上述實驗結果顯示,7-HEC可能通過改善低壓缺氧致PC12細胞周期阻滯而提高細胞存活率、減少細胞凋亡和促進細胞增殖,但具體機制有待后續(xù)研究進一步驗證。
細胞凋亡是一種主動的程序性死亡方式,受抗凋亡蛋白和促凋亡蛋白的嚴格調(diào)控。通常情況下,抗凋亡蛋白Bcl-2和促凋亡蛋白Bax以相對穩(wěn)定的比例存在于細胞內(nèi),二者的表達失衡是造成細胞凋亡的關鍵因素:當Bax表達增多時,Bcl-2/Bax同源二聚體增多,在缺氧刺激下,細胞線粒體膜受損,作為凋亡執(zhí)行蛋白酶的caspase-3被釋放至胞質(zhì),當細胞發(fā)生凋亡時,caspase-3被活化成cleaved caspase-3,從而啟動和誘導凋亡;相反當Bcl-2高表達時,Bcl-2/Bax同源二聚體解離增多,細胞凋亡受到抑制[17]。本研究結果顯示,與對照組相比,低壓缺氧組細胞中cleaved caspase-3蛋白的表達水平顯著升高,Bcl-2/Bax比值顯著下降;與低壓缺氧組相比,7-HEC組細胞中cleaved caspase-3蛋白的表達水平顯著降低,Bcl-2/Bax比值顯著升高。這提示7-HEC可減少低壓缺氧誘導的細胞凋亡,其作用機制可能與抑制caspase-3/Bax/Bcl-2凋亡信號通路的激活有關。
綜上所述,7-HEC可明顯提高低壓缺氧細胞的存活率,降低上清液中LDH含量,改善細胞周期阻滯,降低細胞凋亡率,從而顯著減輕低壓缺氧誘導的細胞損傷,其作用機制可能與抑制caspase-3/Bax/Bcl-2凋亡信號通路的激活有關。本課題組將進一步從細胞分子水平分析7-HEC保護作用的具體機制,為該化合物應用于高原低壓缺氧損傷的防護提供基礎實驗數(shù)據(jù)和研究線索。

