白芍總苷對雷公藤多苷治療濕疹的增效減毒作用及機制 Δ
張明昊 ,王珍 ,高一盈 ,薛鵬坤 ,馬偉洋 ,董文霞 ,馬麗亞 ,張大偉 (.河南中醫藥大學醫學院,鄭州 450046;.河南中醫藥大學臨床技能實訓中心,鄭州 450046;.河南中醫藥大學第三附屬醫院婦產科,鄭州 450008)
濕疹是一種常見的炎癥性皮膚病,發病率逐年升高,具有皮損對稱分布、劇烈瘙癢、反復發作等特點[1]。目前,西醫常以糖皮質激素類藥物外用行局部治療,或者使用H1受體拮抗劑行全身治療,或者以糖皮質激素等免疫抑制劑行免疫治療(嚴重者);患者接受上述藥物治療后,其癥狀雖能在短期內得以緩解,但難以有效治愈,且停藥后易出現“反跳”現象并發生不良反應[2―3]。
雷公藤多苷(Tripterygium wilfordii polyglycoside,TWP)是提取自雷公藤Tripterygium wilfordii Hook. f.根部的脂溶性總苷,具有抗炎、抗腫瘤及調節免疫的作用[4]。白芍總苷(total glucosides of paeony,TGP)是提取自芍藥Paeonia lactiflora Pall.的糖苷類物質,是中藥白芍的有效成分,具有抗炎、抗氧化、保肝腎和調節免疫的作用,可用于濕疹的臨床治療[5]。本課題組前期研究發現,TWP(9.45 mg/kg)對濕疹模型大鼠有較好的干預作用,但會造成部分大鼠死亡[6]。該實驗所用劑量是根據成人用量(105 mg/d)折算而得,結合文獻報道的“成人口服TWP 60 mg/d連續1個月即會出現肝腎功能異常”[4],本課題組推測前期研究所用劑量致大鼠死亡可能與TWP的肝腎毒性有關。
p38絲裂原激活的蛋白激酶(p38 mitogen-activated protein kinase,p38 MAPK)通路是具有絲氨酸和酪氨酸雙重磷酸化功能的蛋白激酶通路,參與炎癥反應的調控及濕疹、皮炎等疾病的發生[7―8]。氧化應激在肝腎損傷過程中具有重要作用,超氧化物歧化酶(superoxide dismutase,SOD)等抗氧化酶耗竭將導致機體清除氧自由基的能力減弱,從而造成肝腎損傷[9]。考慮到抗炎是濕疹治療的一個重要思路,而氧化應激與肝腎損傷密切相關,故本實驗擬從p38 MAPK通路和抗氧化角度出發,基于TGP、TWP的抗炎作用和TGP的抗氧化、保肝腎作用,以臨床常用濕疹治療藥物氯雷他定為陽性對照,探討兩藥配伍后的抗炎增效和肝腎減毒作用,旨在為濕疹的臨床治療提供新的方向。
1 材料
1.1 主要儀器
本研究所用的主要儀器有SpectraMax iD3型酶標儀[美谷分子儀器(上海)有限公司],CX23型光學顯微鏡(日本Olympus公司),6300型化學發光儀(上海勤翔科學儀器有限公司),RM2235型石蠟切片機(德國Leica公司),YD-6D型組織包埋機、YD-A型組織攤片機、YD-B型組織烤片機(金華市科迪儀器設備有限公司),BV-2型垂直電泳儀、BT-2型轉印電泳儀(武漢賽維爾生物科技有限公司)等。
1.2 主要藥品與試劑
1.3 實驗動物
健康雄性SD大鼠,8周齡,體質量180~200 g,購自鄭州市惠濟區華興實驗動物養殖場,動物生產許可證號為SCXK(豫)2019-0002。所有大鼠均分籠飼養于河南中醫藥大學醫學機能實驗室(室溫20~22 ℃,相對濕度55%~60%,正常光照),并自由飲水、攝食。本實驗方案獲河南中醫藥大學實驗動物倫理委員會批準(編號DWLL202201010),實驗過程及動物處置嚴格遵守“3R”原則。
2 方法
2.1 分組、造模與給藥
取雄性SD大鼠50只,適應性飼養1周后,脫其腹部及背部毛,裸露皮膚(面積2 cm×2 cm),以DNFB-丙酮橄欖油溶液(體積比4∶1,下同)100 μL涂抹于大鼠腹部脫毛區致敏,每天1次,連續2 d。首次致敏5 d后,以DNFB-丙酮橄欖油溶液100 μL涂抹于大鼠背部脫毛區激發,同時以DNFB-丙酮橄欖油溶液5 μL涂抹于大鼠右耳內外側激發,每3天1次,共5次,以脫毛區出現紅斑、水腫、脫屑為標準,建立濕疹大鼠模型[10]。將50只濕疹模型大鼠隨機分為模型組、氯雷他定組、TWP組、TGP組和配伍組(TWP+TGP),每組10只;另取10只大鼠,作為正常組。氯雷他定、TWP、TGP成人(體質量70 kg)用量分別為10、105、1 800 mg,根據公式S大鼠/200g=0.018×S人/70 kg(S大鼠/200g、S人/70kg分別為大鼠、人用量),換算得大鼠氯雷他定、TWP、TGP的用量分別為0.9、9.45、162 mg/kg,故以此作為各藥物組的給藥劑量。上述藥物均以0.1%羧甲基纖維素鈉溶液為溶劑,制備相應混淆液并于首次致敏3 d后開始灌胃,各藥物組大鼠的灌胃體積為10 mL/kg;正常組和模型組大鼠灌胃等體積0.1%羧甲基纖維素鈉溶液,每天1次,連續21 d。
2.2 取材及處理
末次給藥24 h后,稱定各組大鼠體質量,并腹腔注射氨基甲酸乙酯1 g/kg進行麻醉,觀察大鼠背部皮膚外觀情況;于腹主動脈取血,以3 000 r/min離心10 min,取上清液于-80 ℃下保存;然后,沿耳基線剪下雙耳,用8 mm打孔器在左右耳中部同一位置打孔取圓形耳片,稱定質量;剖取大鼠背部皮膚組織,以生理鹽水沖洗后分為2份,其中1份用4%中性甲醛溶液固定,1份用液氮速凍后于-80 ℃下保存;剖取大鼠肝臟、腎臟,以生理鹽水清洗后用液氮速凍后于-80 ℃下保存。
2.3 大鼠一般情況觀察與濕疹嚴重度評分
觀察各組大鼠的一般情況并對其背部皮膚濕疹嚴重度進行評分。評分參考濕疹面積及嚴重度指數(eczema area and severity index,EASI)評分法[11]并略作改動,僅以紅斑、水腫的變化情況來評估藥物的干預效果,具體標準如下:紅斑、水腫的嚴重程度均包括無、輕微、中度、中重度、重度,分別記0、1、2、3、4分;綜合評分為紅斑、水腫評分的總和。
2.4 大鼠耳腫脹度檢測
稱定各組大鼠圓形耳片的質量,并按下式計算耳腫脹度:耳腫脹度(mg)=右耳片質量(mg)-左耳片質量(mg)。
2.5 大鼠皮膚組織形態學觀察
取“2.2”項下固定于中性甲醛溶液的背部皮膚組織,經梯度乙醇脫水、二甲苯透明、石蠟包埋后切片(4 μm),再經二甲苯脫蠟、蘇木精-伊紅(HE)染色、梯度乙醇脫水、二甲苯透明,以中性樹膠封片,置于光學顯微鏡下觀察皮膚組織病理學變化。大鼠背部皮膚病變程度評價參考Fukuda等[12]提出的組織病理學評分方法并略作改動,僅對表皮損傷、增厚、過度角化、真皮水腫和炎癥5個方面進行評分,具體標準如下:上述5個方面的嚴重程度均包括相對正常、輕度、中度、中度到顯著、顯著,分別記0、1、2、3、4分;病理評分為表皮損傷、增厚、過度角化、真皮水腫、炎癥程度評分的總和。
2.6 大鼠皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達水平及p38 MAPK蛋白磷酸化水平檢測
2.6.1 免疫組化實驗 取“2.5”項下的皮膚組織切片,經二甲苯脫蠟、水化后,用檸檬酸鹽緩沖液熱修復8 min,待降至室溫后依次用H2O2孵育(10 min)、磷酸鹽緩沖液浸洗、山羊血清孵育(30 min),然后滴加p38 MAPK、pp38 MAPK一抗(稀釋度均為1∶100),于4 ℃下孵育過夜。次日,將切片于37 ℃下復溫30 min,滴加HRP標記的山羊抗兔IgG二抗(稀釋度為1∶200)孵育20 min,用磷酸鹽緩沖液浸洗,以DAB顯色10 min;用水沖洗后,用蘇木精復染3 min,經鹽酸乙醇分化、水沖洗后,進行梯度乙醇脫水、二甲苯透明,以中性樹膠封片,置于光學顯微鏡下觀察。于400倍鏡下隨機選取1個視野,以棕黃色為陽性染色,采用Image-Pro Plus 6.0軟件檢測陽性染色區域的積分光密度(integrated optical density,IOD)值,以評價p38 MAPK、p-p38 MAPK蛋白的表達水平。
圖書館電子閱覽室在運營過程中,若想保證網絡賬號的有效管理,就必須要在合法的前提下享受網絡信息服務,要做好與電子郵件信息用戶的溝通,為其提供更為便捷的網絡服務,充分發揮電子閱覽室的功能,并加強管理與監督工作。
2.6.2 Western blot實驗 取“2.2”項下凍存的皮膚組織,加入含1%PMSF的RIPA裂解液,勻漿后,在4 ℃下以13 000 r/min離心15 min。取上清液,采用BCA蛋白定量法測定蛋白濃度。取蛋白樣品以5×上樣緩沖液稀釋,并于100 ℃下加熱50 min使變性。取變性蛋白適量,經十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳分離后轉移至聚偏二氟乙烯膜,以5%脫脂奶粉封閉2 h,加入p38 MAPK、p-p38 MAPK、β-actin一抗(稀釋度分別為1∶1 000、1∶1 000、1∶3 000),于4 ℃下孵育過夜;以TBST溶液清洗5 min×3次,加入HRP標記的山羊抗兔IgG二抗(稀釋度1∶1 000),于室溫下孵育30 min;以TBST溶液清洗5 min×3次,用ECL顯影。采用Image J 1.8.0軟件分析條帶灰度值,以p-p38 MAPK與p38 MAPK的灰度值比值(p-p38 MAPK/p38 MAPK)來表示p38 MAPK蛋白的磷酸化水平。
2.7 大鼠炎癥、肝腎功能、氧化應激指標檢測
取“2.2”項下各組大鼠的血清樣品適量,使用酶標儀檢測其血清中炎癥因子(IL-4、IFN-γ)和肝腎功能指標(GPT、GOT、SCr、BUN)水平;取“2.2”項下各組大鼠的肝、腎組織50 mg,制備勻漿后,使用酶標儀檢測其肝、腎組織中氧化應激指標(T-SOD、MDA)水平。嚴格按照試劑盒說明書方法操作。
2.8 統計學方法
采用SPSS 26.0軟件對數據進行統計分析。計量資料均以±s表示,多組間比較采用單因素方差分析,組間兩兩比較采用LSD-t檢驗(方差齊)或Dunnett’s檢驗(方差不齊)。檢驗水準α=0.05。
3 結果
3.1 大鼠背部皮膚觀察及濕疹嚴重度評分結果
正常組大鼠生存狀態良好,皮膚光滑完整,未見明顯異常;模型組大鼠背部造模區皮膚出現紅腫、丘疹、水皰、糜爛和滲出等濕疹癥狀;各藥物組大鼠背部造模區皮膚紅腫、糜爛和滲出癥狀均有所改善,丘疹和水皰均呈不同程度消散,皮膚較模型組明顯光滑。結果見圖1。
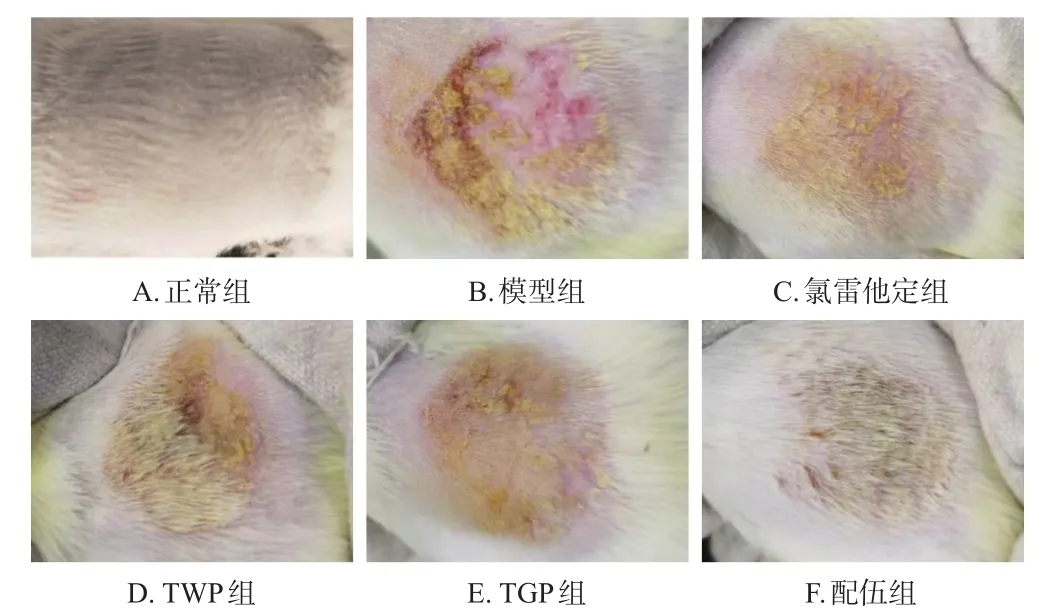
圖1 各組大鼠背部皮膚形態圖
與正常組比較,模型組大鼠背部皮膚的EASI評分顯著升高(P<0.05);與模型組比較,各藥物組大鼠背部皮膚的EASI評分均顯著降低(P<0.05)。結果見表1。
表1 各組大鼠背部皮膚EASI評分、耳腫脹度、病理評分的檢測結果(±s,n=10)
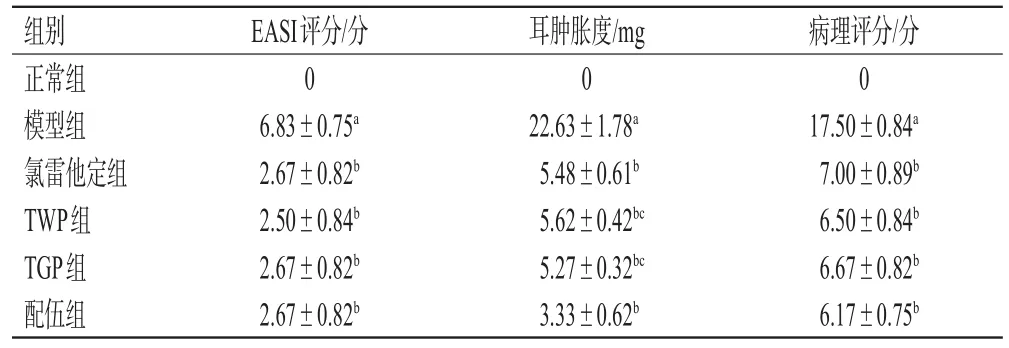
表1 各組大鼠背部皮膚EASI評分、耳腫脹度、病理評分的檢測結果(±s,n=10)
a:與正常組比較,P<0.05;b:與模型組比較,P<0.05;c:與配伍組比較,P<0.05
組別正常組模型組氯雷他定組TWP組TGP組配伍組EASI評分/分0 6.83±0.75a 2.67±0.82b 2.50±0.84b 2.67±0.82b 2.67±0.82b耳腫脹度/mg 0 22.63±1.78a 5.48±0.61b 5.62±0.42bc 5.27±0.32bc 3.33±0.62b病理評分/分0 17.50±0.84a 7.00±0.89b 6.50±0.84b 6.67±0.82b 6.17±0.75b
3.2 大鼠耳腫脹度檢測結果
與正常組比較,模型組大鼠的耳腫脹度顯著升高(P<0.05);與模型組比較,各藥物組大鼠的耳腫脹度均顯著降低,且配伍組顯著優于TWP、TGP組(P<0.05)。結果見表1。
3.3 大鼠背部皮膚組織形態學觀察及病理評分結果
模型組大鼠背部皮膚表皮厚度較正常組明顯增加,角化程度高,呈網狀并伴有海綿樣水腫,毛囊口可見角栓;真皮層可見血管輕度擴張、充血和炎癥細胞浸潤。氯雷他定組、TWP組、TGP組大鼠背部皮膚表皮均增厚,可見海綿樣水腫,且TWP組、TGP組大鼠毛囊口可見角栓。配伍組大鼠背部皮膚表皮輕微增厚,未見海綿樣水腫、空泡和炎癥細胞浸潤。結果見圖2。
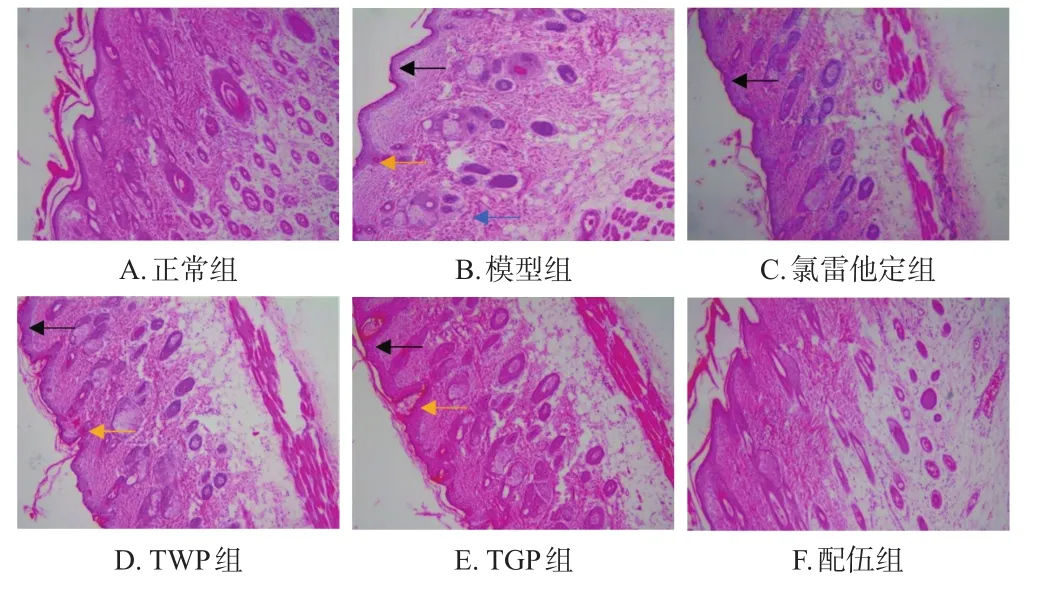
圖2 各組大鼠背部皮膚組織病理形態顯微圖(HE染色,×400)
與正常組比較,模型組大鼠背部皮膚的病理評分顯著升高(P<0.05);與模型組比較,各藥物組大鼠背部皮膚的病理評分顯著降低(P<0.05)。結果見表1。
3.4 大鼠皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達水平及p38 MAPK蛋白磷酸化水平的檢測結果
免疫組化實驗結果顯示,與正常組比較,模型組大鼠皮膚組織中p38 MAPK、p-p38 MAPK蛋白的表達水平均顯著升高(P<0.05);與模型組比較,各藥物組大鼠皮膚組織中p38 MAPK、p-p38 MAPK蛋白的表達水平均顯著降低,且配伍組上述指標均顯著低于TWP、TGP組(P<0.05)。結果見圖3、表2。
表2 各組大鼠背部皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達水平和p38 MAPK蛋白磷酸化水平的檢測結果(±s,n=10)
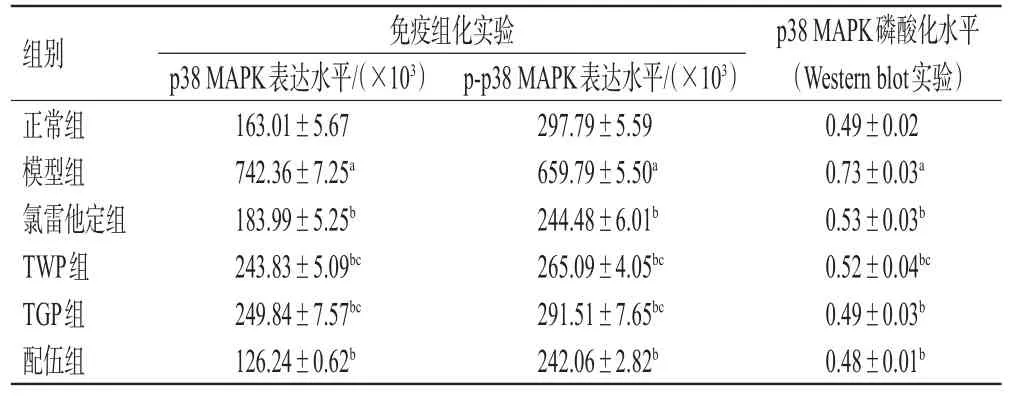
表2 各組大鼠背部皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達水平和p38 MAPK蛋白磷酸化水平的檢測結果(±s,n=10)
a:與正常組比較,P<0.05;b:與模型組比較,P<0.05;c:與配伍組比較,P<0.05
組別正常組模型組氯雷他定組TWP組TGP組配伍組p38 MAPK磷酸化水平(Western blot實驗)0.49±0.02 0.73±0.03a 0.53±0.03b 0.52±0.04bc 0.49±0.03b 0.48±0.01b免疫組化實驗p38 MAPK表達水平/(×103)163.01±5.67 742.36±7.25a 183.99±5.25b 243.83±5.09bc 249.84±7.57bc 126.24±0.62b p-p38 MAPK表達水平/(×103)297.79±5.59 659.79±5.50a 244.48±6.01b 265.09±4.05bc 291.51±7.65bc 242.06±2.82b

圖3 各組大鼠背部皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達的免疫組化圖(×400)
Western blot實驗結果顯示,與正常組比較,模型組大鼠皮膚組織中p38 MAPK蛋白的磷酸化水平顯著升高(P<0.05)。與模型組比較,各藥物組大鼠皮膚組織中p38 MAPK蛋白的磷酸化水平均顯著降低,且配伍組顯著低于TWP組(P<0.05)。結果見圖4、表2。
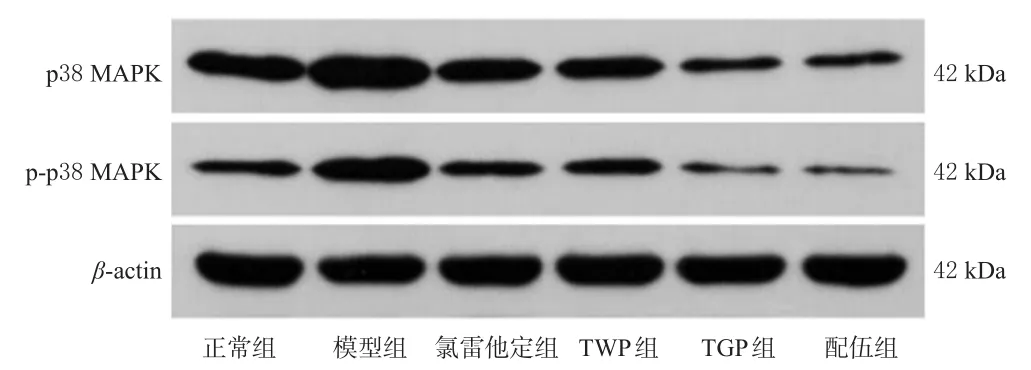
圖4 各組大鼠背部皮膚組織中p38 MAPK、p-p38 MAPK蛋白表達的電泳圖
3.5 大鼠炎癥、肝腎功能、氧化應激指標的檢測結果
與正常組比較,模型組大鼠血清中IL-4、IFN-γ水平均顯著升高(P<0.05);與模型組比較,各藥物組大鼠血清中IL-4、IFN-γ水平均顯著降低(P<0.05)。結果見表3。
表3 各組大鼠血清中炎癥指標的檢測結果(±s,n=10,pg/mL)

表3 各組大鼠血清中炎癥指標的檢測結果(±s,n=10,pg/mL)
a:與正常組比較,P<0.05;b:與模型組比較,P<0.05
組別正常組模型組氯雷他定組TWP組TGP組配伍組IFN-γ 166.98±4.21 262.33±5.36a 147.54±4.58b 143.98±5.01b 141.60±5.93b 140.38±4.00b IL-4 57.99±7.01 207.77±7.38a 123.75±5.99b 120.06±3.58b 124.61±8.38b 125.97±6.81b
與正常組比較,TWP組大鼠血清中GPT、GOT、SCr水平和除正常組外的其余組大鼠血清中BUN水平均顯著升高,TGP組大鼠血清中SCr水平顯著降低(P<0.05);與模型組比較,TWP組大鼠血清中GPT、GOT、SCr、BUN水平均顯著升高(P<0.05),TGP組大鼠血清中GOT、SCr水平和氯雷他定組大鼠血清中SCr水平均顯著降低(P<0.05),且配伍組上述指標水平均介于TWP組、TGP組之間(P<0.05)。結果見表4。
表4 各組大鼠血清中GPT、GOT、SCr、BUN水平的檢測結果(±s,n=10)
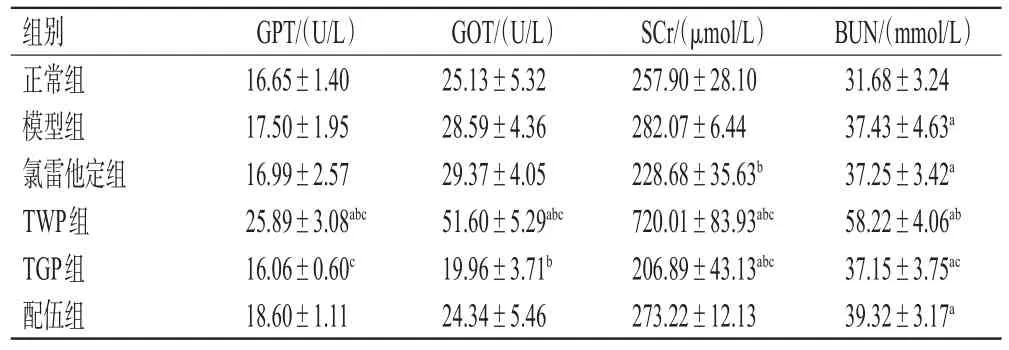
表4 各組大鼠血清中GPT、GOT、SCr、BUN水平的檢測結果(±s,n=10)
a:與正常組比較,P<0.05;b:與模型組比較,P<0.05;c:與配伍組比較,P<0.05
組別正常組模型組氯雷他定組TWP組TGP組配伍組GPT/(U/L)16.65±1.40 17.50±1.95 16.99±2.57 25.89±3.08abc 16.06±0.60c 18.60±1.11 GOT/(U/L)25.13±5.32 28.59±4.36 29.37±4.05 51.60±5.29abc 19.96±3.71b 24.34±5.46 SCr/(μmol/L)257.90±28.10 282.07±6.44 228.68±35.63b 720.01±83.93abc 206.89±43.13abc 273.22±12.13 BUN/(mmol/L)31.68±3.24 37.43±4.63a 37.25±3.42a 58.22±4.06ab 37.15±3.75ac 39.32±3.17a
與正常組和模型組比較,TWP組和配伍組大鼠肝、腎組織中T-SOD水平均顯著降低,MDA水平均顯著升高(P<0.05);配伍組上述指標均介于TWP組、TGP組之間(P<0.05)。結果見表5。
表5 各組大鼠肝、腎組織中T-SOD、MDA水平的檢測結果(±s,n=10)
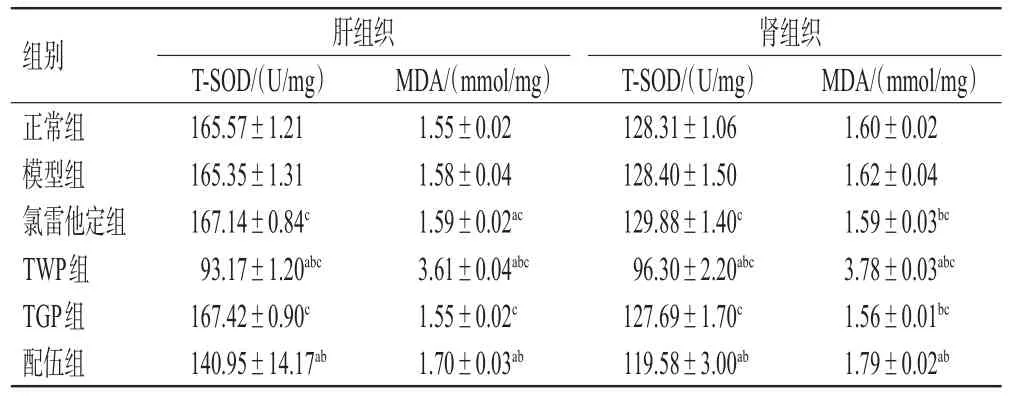
表5 各組大鼠肝、腎組織中T-SOD、MDA水平的檢測結果(±s,n=10)
a:與正常組比較,P<0.05;b:與模型組比較,P<0.05;c:與配伍組比較,P<0.05
組別正常組模型組氯雷他定組TWP組TGP組配伍組MDA/(mmol/mg)1.55±0.02 1.58±0.04 1.59±0.02ac 3.61±0.04abc 1.55±0.02c 1.70±0.03ab肝組織T-SOD/(U/mg)165.57±1.21 165.35±1.31 167.14±0.84c 93.17±1.20abc 167.42±0.90c 140.95±14.17ab腎組織T-SOD/(U/mg)128.31±1.06 128.40±1.50 129.88±1.40c 96.30±2.20abc 127.69±1.70c 119.58±3.00ab MDA/(mmol/mg)1.60±0.02 1.62±0.04 1.59±0.03bc 3.78±0.03abc 1.56±0.01bc 1.79±0.02ab
4 討論
濕疹是一種慢性過敏性皮膚病,以紅腫、瘙癢、剝皮、皮膚增厚等為主要特征。現有研究認為,機體經皮膚接受抗原刺激后,再次接觸相同抗原所致Ⅳ型變態反應與濕疹的發生密切相關[13―14]。本實驗采用DNFB高濃度腹部致敏+低濃度背部、耳部激發的方式構建了大鼠濕疹模型[10],結果顯示,濕疹模型大鼠耳腫脹度升高,表皮增厚且角化過度,真皮層可見炎癥細胞浸潤,表明造模成功。
研究指出,TWP可用于治療自身免疫及皮炎、濕疹等疾病,TGP可用于治療風濕性、免疫性疾病[4―5]。氯雷他定可通過抑制機體內炎癥介質的釋放而達到緩解濕疹癥狀的作用,是目前臨床治療濕疹的常用藥物之一[15]。因此,本實驗以此藥為陽性對照來考量TWP、TGP及兩藥配伍對濕疹模型大鼠的干預作用。結果顯示,TWP、TGP及兩藥配伍均能降低濕疹模型大鼠的EASI評分和耳腫脹度,并可使皮膚組織中海綿樣水腫和炎癥細胞浸潤程度減輕,且配伍組大鼠耳腫脹度的改善更明顯,表明TWP、TGP及兩藥配伍對濕疹模型大鼠的皮膚損傷均有較好的干預作用,且配伍組在耳腫脹度方面的干預效果優于TWP、TGP單用。
濕疹的發生與Th1/Th2細胞亞群分泌的細胞因子水平及其動態平衡有關,IL-4、IFN-γ作為Th1、Th2細胞的特征性因子,參與了濕疹的病理過程,并可反映Th1、Th2細胞免疫應答程度[16―17]。p38 MAPK通路是真核生物進化中相對保守的一條重要信號轉導通路,可參與細胞分化、細胞凋亡及炎癥反應等進程[8]。該通路的上游激酶首先磷酸化激活絲裂原激活的蛋白激酶激酶(mitogen-activated protein kinase kinase,MAPKK),活化的MAPKK可進一步磷酸化激活p38 MAPK;而p-p38 MAPK是重要的炎癥調控因子,可與多種靶蛋白結合,參與皮炎、濕疹等多種炎癥性疾病的發生過程[18―20]。本研究結果顯示,濕疹發生時,大鼠體內IL-4、IFN-γ水平,p38 MAPK、p-p38 MAPK蛋白的表達水平和p38 MAPK蛋白的磷酸化水平均顯著升高,提示IL-4、IFN-γ等促炎因子釋放增加,p38 MAPK通路異常激活,大鼠皮膚炎癥加重。經TWP、TGP及兩藥配伍干預后,大鼠上述指標均得以改善,且配伍組下調p38 MAPK、p-p38 MAPK蛋白表達及抑制p38 MAPK蛋白磷酸化的作用更明顯,提示TWP和TGP可通過阻斷p38 MAPK通路的激活來發揮抗炎作用,且兩藥配伍后抗炎作用有所疊加,這一抗炎增效與抑制促炎因子釋放和阻斷p38 MAPK通路激活有關。
TWP有明顯的肝腎毒性,以肝、腎功能損傷為主要表現[4]。GPT和GOT是衡量肝臟功能的重要指標,SCr和BUN是衡量腎臟功能的重要指標[5],故本研究以血清GPT、GOT、SCr、BUN水平變化來考察TWP的肝腎毒性和配伍TGP的減毒作用。結果顯示,TWP可使大鼠血清中GPT、GOT、SCr、BUN水平升高,提示其在干預過程中會導致大鼠出現不同程度的肝腎損傷;TGP可逆轉TWP致GPT、GOT、SCr、BUN水平升高的情況,即可部分減弱TWP的肝腎損傷。
氧化應激是肝腎損傷的重要因素之一,SOD是一種重要的氧自由基清除劑,能保護肝、腎免受自由基的損傷;MDA是活性氧致脂質過氧化反應的終末產物,可在一定程度上反映組織的氧化損傷程度[9]。本研究結果顯示,TWP可使大鼠肝、腎組織中T-SOD水平降低,MDA水平升高,提示TWP的肝、腎毒性可能與組織氧化應激水平的提升有關;TGP可逆轉TWP引起的氧化應激損傷,使大鼠肝、腎組織中T-SOD水平升高,MDA水平降低,提示TGP配伍TWP可通過提升機體的抗氧化能力來減弱TWP的肝腎毒性。
綜上所述,TGP配伍TWP對濕疹模型大鼠具有抗炎增效與肝腎減毒的作用,其機制可能與下調血清促炎因子的表達和抑制p38 MAPK通路的激活有關,可為兩藥配伍在濕疹治療方面的深入開發利用提供實驗依據。

