貯藏年限對不同居群白羊草種胚線粒體抗氧化性能的影響
朱夢馨, 曾 佳, 夏方山, 趙奧然, 李曉波, 王 勃, 李尹琳
(山西農業(yè)大學草業(yè)學院, 山西 太谷 030801)
種業(yè)是國家戰(zhàn)略性、基礎性核心產業(yè)[1-2],是發(fā)展草牧業(yè)的堅實支撐[3],而優(yōu)良鄉(xiāng)土草種質資源的收集、評價及創(chuàng)新利用是實現我國民族草種業(yè)高質量發(fā)展的重要基礎。白羊草(Bothriochloaischaemum)作為山西省及其周邊省區(qū)暖性灌草叢類草地的重要鄉(xiāng)土草種,具有高產耐牧、適口性好、飼用價值高等優(yōu)點[4],近年來已被作為重要的優(yōu)良牧草和生態(tài)草資源在山西及周邊省區(qū)廣泛種植,因而白羊草種子的需求量日益增加,使其良種繁育及貯藏越來越受到人們的關注。然而,種子生理成熟時,其種子活力也達到了頂峰,然后其內部便出現一系列不可逆的劣變,生理生化特性也發(fā)生變化,種子質量出現下降,致使其種用價值不斷降低[5]。因此,探究不同白羊草種質資源的耐貯藏性,進而選育出耐貯藏的白羊草新品種,是解決白羊草種質資源及其良種貯藏的重要途徑。
貯藏過程中種子活力的喪失是由活性氧(Reactive oxygen species,ROS)自由基的積累而引起的種子老化造成的[6]。線粒體是細胞的能量供應中心[7],在種子老化過程中發(fā)揮著重要的作用。線粒體老化學說[6]將老化、ROS和線粒體聯系起來,認為細胞老化過程離不開線粒體的參與。線粒體電子傳遞鏈上的復合物Ⅰ和復合物Ⅲ是ROS等自由基的主要產生位點[8],這已在大豆(Glycinemax)[9]和燕麥(Avenasativa)[10]等種子的老化研究中證實。此外,ROS自由基的大量積累會攻擊細胞膜、蛋白質等,導致細胞內生物大分子的氧化受損,刺激線粒體結構功能的改變,從而引起細胞內部代謝等功能的紊亂[11-12]。研究老化過程中的玉米(Zeamays)[13]種子發(fā)現,線粒體外膜修復能力逐漸降低,線粒體的細胞色素c氧化酶活性及線粒體細胞色素c氧化酶途徑的呼吸速率逐漸降低,表明種子老化破壞了線粒體膜的完整性及呼吸功能。研究人工老化的大豆[14]種子發(fā)現,隨著老化時間的延長,ROS含量逐漸增加,當ROS產生與清除失衡時便會引發(fā)氧化脅迫,使得種子胚軸線粒體膜結構嚴重解體,基質變稀,抗氧化酶活性逐漸降低,最終導致線粒體抗氧化系統崩潰,氧化損傷加劇。這與貯藏年限對老芒麥(Elymussibiricus)[15]種胚線粒體抗氧化功能的影響規(guī)律相似。
目前,種子老化與線粒體關系的研究已成為熱點問題,在多種牧草及作物種子上均已開展一定研究。然而,同種植物不同居群的染色體核型進化程度及遺傳多樣性存在著差異[16-17],卻尚未有貯藏年限對不同植物居群種胚線粒體抗氧化性能影響的相關報道。本試驗通過分析不同貯藏年限的不同居群白羊草種胚線粒體抗氧化酶活性及脂質過氧化程度的變化,探討不同居群白羊草種子的耐貯藏特性,以期為評價不同白羊草種質資源的耐貯藏性提供理論基礎,對白羊草種質資源的安全保存與創(chuàng)新利用具有十分重要的指導意義。
1 材料與方法
1.1 試驗材料
供試材料為2017,2018,2019及2020年收獲于山西農業(yè)大學草業(yè)學院校內實驗基地的山西省代縣、平魯、平定、柳林及太谷5個居群的白羊草種子,種子采集于每年10月進行,收獲后在含水量10%(鮮重基礎)條件下于-4℃冷庫中密封保存至2021年10月進行試驗,種子貯藏年限分別為1,2,3,4年。
1.2 生理指標的測定
種胚線粒體的提取參照Yin[18]的方法,略作改動,稱取不同貯藏年限及居群白羊草種子0.1 g,加入20 mL預冷的線粒體提取緩沖液,冰浴研磨5 min,4層紗布過濾后,反復離心洗滌獲得線粒體懸浮液。上述所有步驟均在0℃~4℃的條件下進行。每個處理設4次重復。
可溶性蛋白含量按照南京建成生物工程研究所試劑盒進行測定;超氧化物歧化酶(Superoxide dismutase,SOD)活性的測定參照Rao和Sresty[19]的方法,1 mL反應體系中加入10 μL線粒體進行測定;抗壞血酸過氧化物酶(Ascorbate peroxidase,APX)活性的測定參照Nakano和Asada[20]的方法,1 mL反應體系中加入10 μL線粒體進行測定;過氧化氫酶(Catalase,CAT)活性的測定參照Aebi[21]的方法,3.4 mL磷酸緩沖液加入10 μL線粒體和200 μL 0.1 mol·L-1H2O2;谷胱甘肽還原酶(Glutathione reductase,GR)活性的測定參照Madamanchi等[22]的方法,1.7 mL反應體系中加入10 μL線粒體進行測定;丙二醛(Malondialdehyde,MDA)含量測定參照Bailly等[23]的方法,加入10 μL線粒體進行測定。
1.3 數據統計分析
試驗數據在Excel 2019軟件中進行整理,用SPSS 26.0軟件對整理的數據進行方差分析,Duncans法進行多重比較(P<0.05),結果用平均值±標準誤表示。
2 結果與分析
2.1 貯藏年限對不同居群白羊草種胚線粒體SOD活性的影響
隨著貯藏年限的延長,各居群白羊草種胚線粒體SOD活性呈現逐漸降低的趨勢(表1),不同居群間存在差異。相較于貯藏第1年,代縣、平魯、平定及柳林居群的白羊草種胚線粒體SOD活性在貯藏第2年均出現顯著降低(P<0.05);貯藏第4年時,太谷居群的白羊草種胚線粒體SOD活性出現顯著降低(P<0.05),且顯著低于其他貯藏年限(P<0.05)。貯藏1~4年,太谷及平定居群白羊草種胚線粒體SOD活性均處在相對較高水平。
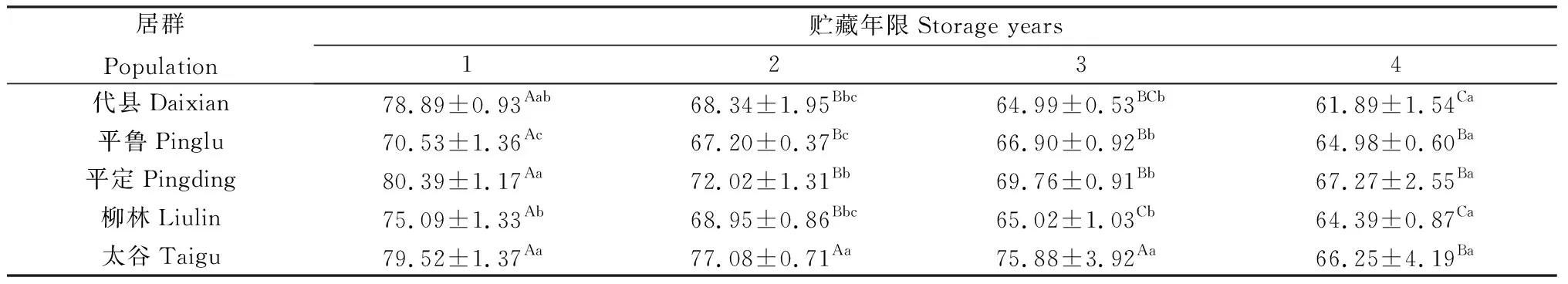
表1 貯藏年限對不同居群白羊草種胚線粒體SOD活性的影響Table 1 Effects of storage years on SOD activities of embryonic mitochondria in different populations of Bothriochloa ischaemum 單位:U·mg-1 protein
2.2 貯藏年限對不同居群白羊草種胚線粒體CAT活性的影響
隨著貯藏年限的延長,各居群白羊草種胚線粒體CAT活性呈現逐漸降低的趨勢(表2),不同居群間存在差異。相較于貯藏第1年,代縣、平魯、平定及柳林居群的白羊草種胚線粒體CAT活性在貯藏第2年均出現顯著降低(P<0.05);貯藏第4年時,太谷居群的白羊草種胚線粒體CAT活性出現顯著降低(P<0.05),且顯著低于其他貯藏年限(P<0.05)。貯藏1~4年,太谷及平定居群白羊草種胚線粒體CAT活性均處在相對較高水平。
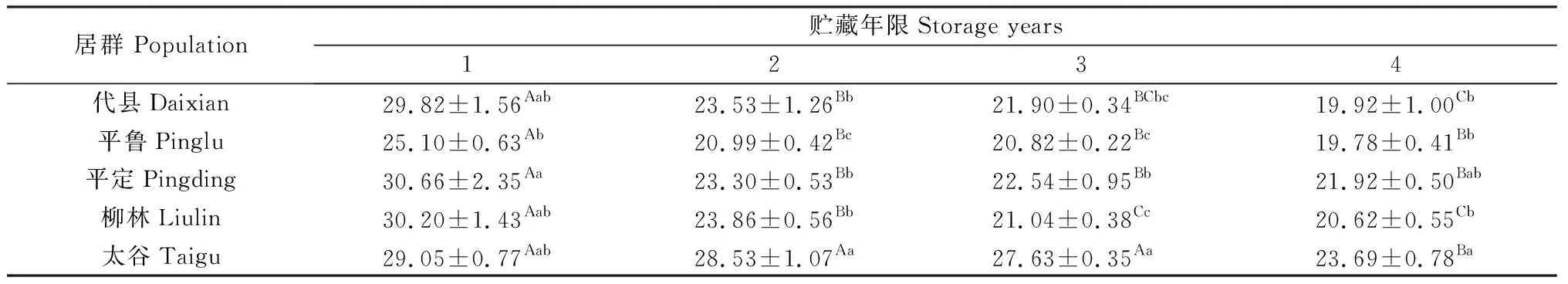
表2 貯藏年限對不同居群白羊草種胚線粒體CAT活性的影響Table 2 Effects of storage years on CAT activities of embryonic mitochondria in different populations of Bothriochloa ischaemum 單位:U·min-1·mg-1 protein
2.3 貯藏年限對不同居群白羊草種胚線粒體APX活性的影響
隨著貯藏年限的延長,各居群白羊草種胚線粒體APX活性呈現逐漸降低的趨勢(表3),不同居群間存在差異。相較于貯藏第1年,代縣、平魯、平定及柳林居群的白羊草種胚線粒體APX活性在貯藏第2年均出現顯著降低(P<0.05);貯藏第4年時,太谷居群的白羊草種胚線粒體APX活性出現顯著降低(P<0.05),且顯著低于其他貯藏年限(P<0.05)。貯藏1~4年,太谷及平定居群白羊草種胚線粒體APX活性均處在相對較高水平。
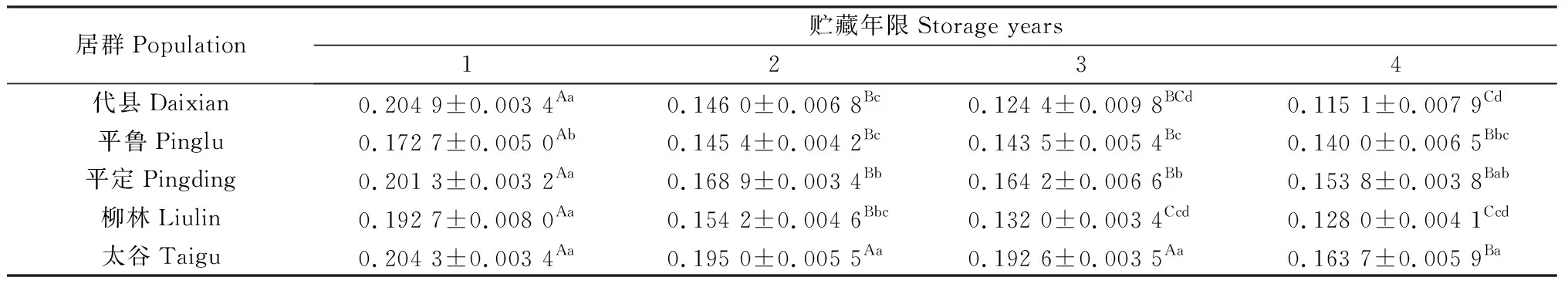
表3 貯藏年限對不同居群白羊草種胚線粒體APX活性的影響Table 3 Effects of storage years on APX activities of embryonic mitochondria in different populations of Bothriochloa ischaemum 單位:μmol·min-1·mg-1 protein
2.4 貯藏年限對不同居群白羊草種胚線粒體GR活性的影響
隨著貯藏年限的延長,各居群白羊草種胚線粒體GR活性呈現逐漸降低的趨勢(表4),不同居群間存在差異。相較于貯藏第1年,代縣、平魯、平定及柳林居群的白羊草種胚線粒體GR活性在貯藏第2年均出現顯著降低(P<0.05);貯藏第4年時,太谷居群的白羊草種胚線粒體GR活性出現顯著降低(P<0.05),且顯著低于其他貯藏年限(P<0.05)。貯藏1~4年,太谷及平定居群白羊草種胚線粒體GR活性均處在相對較高水平。

表4 貯藏年限對不同居群白羊草種胚線粒體GR活性的影響Table 4 Effects of storage years on GR activities of embryonic mitochondria in different populations of Bothriochloa ischaemum 單位:U·min-1·mg-1 protein
2.5 貯藏年限對不同居群白羊草種胚線粒體MDA含量的影響
隨著貯藏年限的延長,各居群白羊草種胚線粒體MDA含量呈現逐漸升高趨勢(表5),不同居群間存在差異。相較于貯藏第1年,代縣、平魯、平定及柳林居群的白羊草種胚線粒體MDA含量在貯藏第2年均出現顯著升高(P<0.05);貯藏第4年時,太谷居群的白羊草種胚線粒體MDA含量出現顯著升高(P<0.05),且顯著高于其他貯藏年限(P<0.05)。貯藏1~4年,太谷及平定居群白羊草種胚線粒體MDA含量均處在相對較低水平。

表5 貯藏年限對不同居群白羊草種胚線粒體MDA含量的影響Table 5 Effects of storage years on MDA contents of embryonic mitochondria in different populations of Bothriochloa ischaemum 單位:μmol·mg-1 protein
3 討論
種子的內部基因決定種子的潛在壽命,而種子活力的保持取決于外部環(huán)境因子的綜合影響[24-25],其中貯藏時間是影響種子活力的重要因素,隨著貯藏時間延長,種子老化程度加深,種子活力下降。在種子老化過程中,ROS不斷積累,誘導細胞發(fā)生膜質過氧化作用逐漸增強,膜結構受損[11],而MDA作為植物體內脂質過氧化的標志性產物,其含量的高低可以反映膜結構受損情況,從而衡量種子老化受損的程度[26]。同時,植物細胞中SOD,APX,CAT和GR等組成的抗氧化系統協同進行作用,清除細胞內積累的ROS,保護生物膜系統。在本試驗中,各居群白羊草種胚線粒體SOD,CAT,APX及GR活性隨貯藏時間的延長逐漸降低,白羊草種胚線粒體MDA含量隨貯藏時間的延長逐漸升高,這可能是由于隨著貯藏時間的延長,種子老化程度加深,種子內部ROS不斷積累,加劇了膜質過氧化作用,種胚線粒體MDA含量升高,這與前人在鳳丹(Paeoniaostii)[27]、大豆[28]等作物中的研究試驗結論相似。當細胞膜結構受到MDA脅迫時,白羊草種胚線粒體抗氧化酶活性被激活,增強了細胞質的抗氧化能力[29],能夠及時有效的清除ROS自由基,降低膜質過氧化程度,保護細胞免受其損害;但隨著種子老化程度加深,ROS富集到一定程度,便會打破植物體內ROS產生系統與消除系統間的動態(tài)平衡,導致過量的ROS無法被清除[30-31]。
不同居群白羊草種子的耐貯藏性也不同,其抗氧化酶活性變化也就不盡相同。代縣、平魯及柳林居群白羊草種胚線粒體SOD,CAT,APX及GR活性在貯藏第2年顯著降低(P<0.05),MDA含量顯著升高(P<0.05),這可能是由于積累的ROS會攻擊DNA、蛋白質等大分子,線粒體中抗氧化酶系統遭到破壞,抗氧化酶活性下降,消除線粒體中ROS的能力降低;同時,生物膜結構受損,種胚線粒體MDA含量逐漸升高,進而對細胞結構造成不可逆的氧化損傷,甚至導致細胞凋亡[32-33]。平定居群白羊草種胚線粒體MDA含量雖在貯藏第2年顯著升高(P<0.05),但其表現出較高的種胚線粒體SOD,CAT,APX及GR活性,能夠及時清除多余的ROS,可以緩解線粒體膜結構受損情況。貯藏1~3年,太谷居群白羊草種胚線粒體SOD,CAT,APX及GR活性處在較高水平,表現出較強的清除ROS的能力,這與其較低水平線粒體MDA含量相一致,說明線粒體膜結構受損程度較輕時,MDA含量較低,抗氧化酶清除ROS效率高,能夠更好地抵御種子老化損傷;而貯藏第4年,太谷居群白羊草種胚線粒體SOD,CAT,APX及GR活性顯著降低(P<0.05),MDA含量顯著升高(P<0.05),說明此時線粒體中抗氧化系統遭到嚴重破壞,積累的ROS未得到及時清除,膜質過氧化作用逐漸增強,線粒體膜結構嚴重受損,這可能是由不同居群長期所處的生態(tài)環(huán)境存在差異造成了其遺傳多樣性發(fā)生了變化[17]。
4 結論
白羊草種子線粒體抗氧化能力與貯藏時間關系密切。隨著貯藏時間的延長,不同居群白羊草種胚線粒體抗氧化能力均呈下降的趨勢,其耐貯藏特性表現也存在差異。太谷居群白羊草種子的耐貯藏時間可為3年,代縣、平魯、平定及柳林居群白羊草種子的耐貯藏時間以1年為佳。

