基于生物信息學及分子對接技術探究羌活勝濕湯治療強直性脊柱炎的作用機制?
李金政,霍鳳蕾,李志超,邱紅明
1 山東中醫藥大學中醫學院,山東 濟南 250014; 2 山東大學,山東 濟南 250100;3 山東中醫藥大學,山東 濟南 250355; 4 山東中醫藥大學附屬醫院,山東 濟南 250000
強直性脊柱炎(ankylosing spondylitis,AS)是與人類白細胞抗原有相關性的、以骶髂關節和脊柱附著點炎癥為主要癥狀的自身免疫系統疾病[1]。骶髂關節是本病最早累及的部位,主要表現為滑膜炎、軟骨變性、骨破壞等,晚期可致脊柱僵直和畸形,致殘率極高[2]。目前西醫在臨床上通常采用免疫抑制類藥物、糖皮質激素、生物制劑等治療AS,但均存在嚴重的不良反應[3]。隨著中醫學的發展,中藥治療AS的安全性和有效性得到了廣泛的認可,受到國內外越來越多的關注。
AS屬于祖國醫學“痹證”“背僂”等范疇。《素問·痹論篇》中記載:“風寒濕三氣雜至,合而為痹也……腎痹者,善脹,尻以代踵,脊以代頭。”[4]其描述的癥狀與AS晚期脊柱僵直、畸形等臨床癥狀相符合。羌活勝濕湯最早見于金代李東垣所著《內外傷辨惑論》,由羌活、獨活、川芎、甘草、蔓荊子、藁本、防風等七味藥組成。方中羌活、獨活祛風除濕、通利關節;川芎與羌活配伍,活血祛風,透關利節,治療督脈為病,脊強而厥;防風、藁本、蔓荊子祛風止痛;甘草調和諸藥,共奏祛風逐濕之功。羌活勝濕湯可有效地緩解AS患者疼痛、僵硬、屈伸不利等癥狀,是治療風寒濕痹阻所致的AS、風濕性關節炎、類風濕性關節炎等疾病的經典名方,在臨床上取得了滿意的療效[5]。
本研究基于生物信息學技術及分子對接技術,科學系統地探究羌活勝濕湯治療AS的作用機制,為該方的臨床應用提供理論支持,并進一步探索中藥組方治療AS的新方向與新思路。
1 資料與方法
1.1 GEO基因芯片數據分析AS差異表達基因以“ankylosing spondylitis”為關鍵詞檢索GEO數據庫并確定芯片號為GSE41038的數據集,該數據集包含了8個屬于AS及分類未定脊柱炎的膝關節滑膜組織樣本為實驗組,7個屬于骨關節炎及健康正常組織的膝關節滑膜組織樣本為對照組。采用生物信息學中RMA(robust multiarray average)算法背景校正和矩陣數據歸一化處理其原始文件,并利用R語言中limma包分析該數據集,結合P值和差異倍數(fold change,FC)進行篩選,將顯著差異基因的篩選條件設置為P<0.05,logFC絕對值>0.5,最終獲得AS的差異表達基因。
1.2 AS疾病靶基因預測以“ankylosing spondylitis”作為關鍵詞,采用疾病基因數據庫(DisGeNET)、人類基因數據庫(GeneCards)、孟德爾遺傳綜合數據庫(OMIM)、疾病數據庫(MalaCards)等多個數據庫對AS已知靶基因進行查找篩選。將合并后的疾病靶基因與R語言分析芯片獲得的差異表達基因取并集,刪除重復的靶基因后,即獲得已明確的AS發病過程的疾病靶點。
1.3 羌活勝濕湯有效成分篩選及靶點預測通過中藥藥理學平臺(TCMSP),以羌活、獨活、川芎、甘草、蔓荊子、藁本、防風等七味中藥檢索其化學成分,并以口服生物利用度(oral bioavailability,OB)≥30%和類藥性(drug likeness,DL)≥0.18作為篩選條件,將獲得的具有較高活性化合物導入蛋白質數據庫(Unitprot)進行處理。利用Cytoscape 3.7.2軟件,構建其有效成分的靶點網絡圖,并進行網絡拓撲分析。
1.4 羌活勝濕湯治療AS關鍵靶基因篩選將所篩選的羌活勝濕湯潛在靶基因與“1.2”項獲取的AS疾病靶基因交叉生成Venny圖,得出羌活勝濕湯治療AS的映射靶基因。抽取映射靶基因,借助Cytoscape 3.7.2軟件構建羌活勝濕湯治療AS的作用靶點PPI網絡圖,根據節點連接度(degree)值進行篩選,得到羌活勝濕湯治療AS的關鍵靶基因,揭示羌活勝濕湯治療AS的關鍵機制。
1.5 生物通路及富集分析將“1.4”項篩選出的關鍵靶基因導入基因注釋數據庫(DAVID),進行KEGG(kyoto encyclopedia of genes and genomes)通路分析以及GO(gene ontology)生物過程的富集分析。將篩選條件設置為P≤0.05,FDR≤0.05,且分別將篩選出的前10個GO條目與KEGG條目借助R語言ggplot2包繪制富集分析氣泡圖。
1.6 分子對接從有機小分子生物活性數據庫(Pubchem)下載“1.3”項篩選出的羌活勝濕湯主要有效成分的化合物結構,從蛋白質數據庫(RCSB PDB)下載“1.4”項篩選出的關鍵靶基因的蛋白質結構。使用Mgltools工具,通過加氫、計算電荷、合并非極性氫后,作為對接配體。設置Grid Box坐標和盒子大小,通過Autodock Vina 1.1.2工具進行分子對接,得分越低說明其對接的活性越好,并使用Pymol 2.3工具作圖分析。
2 結果
2.1 AS相關差異表達基因檢索通過AS差異表達基因分析結果顯示,發現704個mRNA存在差異表達,其中上調280個,下調424個,用R語言中heatmap與limma程序包繪制芯片原始的差異基因熱圖與火山圖。見圖1-2。

圖1 AS相關芯片差異基因聚類圖

圖2 AS相關芯片差異基因火山圖
2.2 篩選AS疾病靶基因采用“1.2”項所述多個數據庫,對AS已知靶基因進行檢索與篩選,合并后共獲得1323個疾病靶基因,將合并后的疾病靶基因與704個差異表達基因取并集并刪除重復值,獲得已明確的AS發病過程的疾病靶點共1950個。
2.3 羌活勝濕湯有效成分及作用靶點以OB≥30%,DL≥0.18為篩選標準,在TCMSP數據庫共檢索到七味中藥活性成分共計176個,其中羌活17個、獨活11個、川芎7個、蔓荊子27個、藁本1個、防風20個、甘草93個,相對應靶點共計3490個,刪除重復值后得到羌活勝濕湯最終靶點137個。借助Cytoscape構建羌活勝濕湯中七味藥物的有效成分-靶點網絡圖,見圖3。分析可知,槲皮素、β-谷甾醇、山柰酚、異紫花前胡內酯、歐前胡素等潛在的活性成分自由度較高,與多個作用靶點相互關聯,說明這些化合物是羌活勝濕湯治療AS的主要有效成分。

圖3 羌活勝濕湯有效成分-靶點網絡圖
2.4 羌活勝濕湯治療AS的PPI網絡圖將篩選的羌活勝濕湯潛在137個靶基因與“2.2”項獲取的1950個AS疾病靶基因交叉生成Venny圖,見圖4,通過Venny圖可以直觀發現羌活勝濕湯對AS的靶基因映射率為2.3%,該方共有137個有效靶點,其中映射靶點46個,作為羌活勝濕湯治療AS的直接或間接作用靶標基因,占據該方作用靶點的33.5%左右,表明該復方在治療AS方面具有顯著特異性。將這46個映射靶基因導入Cytoscape3.7.2軟件,構建羌活勝濕湯治療AS的作用靶點PPI網絡圖,根據節點連接度(degree)≥20為條件進行篩選,得到羌活勝濕湯治療AS的關鍵靶基因13個,見表1。所獲取的關鍵靶基因則是發揮治療AS作用的關鍵靶點,揭示出羌活勝濕湯治療AS的關鍵機制。

表1 羌活勝濕湯治療AS關鍵靶基因信息

圖4 “羌活勝濕湯-AS”映射靶基因Venny圖
2.5 GO生物過程結果及KEGG通路富集分析對“2.3”項獲得的13個關鍵靶基因采用DAVID數據庫進行GO生物過程和KEGG信號通路分析,得到分子功能、生物過程和細胞成分條目161個,KEGG通路55條,將篩選條件設置為P≤0.05,FDR≤0.05,并以P值升序排列,獲得排名前10的生物過程和10條信號通路,并將其以氣泡圖的形式展現出來,見圖6。

圖5 羌活勝濕湯治療AS關鍵靶基因PPI網絡圖

圖6 羌活勝濕湯治療AS關鍵靶基因的GO生物過程及KEGG信號通路氣泡圖
2.6 分子對接結果將“2.3”項獲得的羌活勝濕湯主要有效成分槲皮素、β-谷甾醇、山柰酚、異紫花前胡內酯、歐前胡素與“2.4”項中自由度值排名前五的關鍵靶基因IL-6、TNF-α、VEGFA、PTGS2、IL-1β做分子對接,見表2。配體與受體的結合能越低,說明結合可能性越大越穩定,打分值≤-5的成分具有潛在的活性,打分值≤-7的成分具強的穩定性及活性。結果如表2所示,羌活勝濕湯中主要有效成分在與關鍵靶基因對接過程中均進入了活性位點,表明該方主要有效成分和關鍵靶基因具有較強的結合能力,驗證了本研究數據的可靠性。根據表2可知,各靶基因對應各活性成分結合最穩定的是:槲皮素與IL-6、槲皮素與IL-1β、β-谷甾醇與VEGFA、β-谷甾醇與PTGS2、槲皮素與TNF-α,見圖7。

圖7 各活性成分與各關鍵靶基因最穩定結合圖
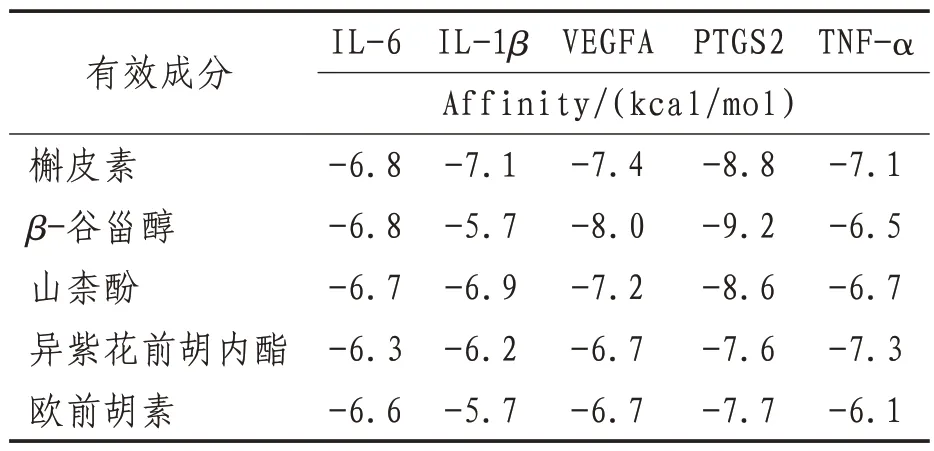
表2 分子對接打分結果
3 討論
本研究應用生物信息學技術,通過GEO數據庫篩選出AS患者與膝關節炎患者及正常人的差異基因,與各數據庫已知AS作用靶基因進行合并。構建了羌活勝濕湯治療AS的“藥物-有效成分-靶基因-疾病”網絡樣機制,并進一步通過分子對接技術驗證羌活勝濕湯中有效成分與關鍵靶基因的結合能力,系統闡述該方在治療AS上藥物、靶基因、通路與疾病的相關性。
通過TCMSP數據庫分析得出,槲皮素、β-谷甾醇、山柰酚、異紫花前胡內酯等可能是羌活勝濕湯治療AS的有效成分。槲皮素具有多重生物活性,其具有抗氧化、抗炎癥、保護骨關節等作用[6]。研究表明,槲皮素可能通過增強下游抗氧化基因的表達,影響IKK/NF-κB和MAPK信號通路,進而抑制炎性細胞因子的釋放,并且可顯著降低基質金屬肽酶13(matrix metallopeptidase-13,MMP-13)/基質金屬蛋白酶抑制劑1(tissue inhibitor of metalloproteinase-1,TIMP-1)的比例,抑制軟骨細胞外基質的降解,促進對關節軟骨的保護[7-8]。β-谷甾醇在抗氧化、抗炎、免疫調節等多個方面表現出良好的藥理作用[9]。β-谷甾醇具有強的抑制TNF-α、IL-1β和IL-6炎癥因子作用,并通過強的抗氧化活性,猝滅人體產生的ROS,經嗜酸粒細胞滲濾等緩和炎癥[10-11]。山柰酚具有抗炎癥、抗氧化等藥理作用,可有效降低IL-1β等因子的表達,使OA軟骨細胞促炎介質的表達明顯下降[12-13]。異紫花前胡內酯具有抗氧化、抗炎鎮痛、保護中樞神經等作用[14]。有研究表明[15],異紫花前胡內酯除可調節細胞周期相關蛋白表達外,還可以抑制血管內皮細胞生長因子(vascular endothelial growth factor,VEGF)的表達。而VEGF的表達可促進關節軟骨組織破壞,同時也與骨關節炎的發展呈正相關[16]。在目前的研究中,氧化應激穩態失衡被認為是導致AS發生發展的強效觸發因素[17]。而如何干預氧化應激在AS過程中的信號通路表達也是治療AS新的研究方向。本研究中的槲皮素、β-谷甾醇、山柰酚、異紫花前胡內酯均具有顯著的抗氧化作用,故存在以上有效成分作為抗氧化劑整體參與AS的抗氧化應激治療的可能,需要進一步研究證明。綜上所述,羌活勝濕湯中的槲皮素、β-谷甾醇、山柰酚、異紫花前胡內酯等有效成分,表現出調節各種細胞因子的表達、保護關節軟骨、緩和炎癥、抗氧化等作用,很可能是治療AS的有效成分。
在羌活勝濕湯治療AS的靶基因中,TNF-α、IL-6、IL-1β、VEGFA、CAT、ESR1、PTGS2等起到了關鍵靶基因的作用。AS是一種主要累及脊柱與骶髂關節的慢性炎性疾病,各種促炎細胞因子過度表達,影響各相關細胞因子,在骨質的破壞和新骨的形成過程中起重要作用。TNF-α作為炎癥的重要啟動因子,誘導IL-1β、IL-6、VEGF等因子的表達,貫穿炎癥反應發生發展的全過程,并通過調節自身免疫,在炎性骨吸收和自身免疫疾病等方面發揮作用[18]。IL-6是一種多效細胞因子,受到IL-1β的刺激而促進其表達,同時又誘導VEGF的表達而促進血管生成,在炎癥反應、自身免疫、血管滲透和組織再生等多方面發揮作用[19]。VEGFA通過增加血管通透性導致炎性滲透加重,促進新生血管形成,導致滑膜炎癥的快速發展及骨質的加速破壞,其與ESR1也存在正相關關系[20]。CAT作用與VEGF類似,同樣受到各促炎性因子的調控,并且在新生血管形成過程中有重要作用[21]。PTGS2可參與炎性反應、細胞凋亡和自身免疫,調控破骨細胞與成骨細胞的生成和分化,其表達受到上述多個細胞因子的影響[22-23]。由此可見,許多細胞因子的表達與AS過程息息相關,每個細胞因子均具有多效性,它們之間的效應又相互重疊、相互誘導、相互協調,在AS的免疫反應中構成了復雜的關系網絡,而網絡性正是細胞因子的典型特點之一。干預細胞因子的表達是治療AS的重要思路之一,而目前臨床上常用的單一針對某個細胞因子的拮抗劑,如TNF-α拮抗劑,其作用也僅僅局限于緩解部分癥狀,無法根治,且大多數患者出現停藥后反復的情況[24]。而羌活勝濕湯在臨床上取得的良好療效提醒我們:是否正是該方通過多成分、多靶點的作用機制,使得其多種有效成分干預了AS過程相關的多個細胞因子,在一定程度上起到了整體調控細胞因子網絡的作用。這與中醫學的整體觀念、辨證論治之理念不謀而合,中藥復方在整體性和微觀性相結合的優勢也為我們新的遣方應用及老方新用提供了線索。
從DAVID數據庫對13個關鍵靶基因進行富集分析的結果可知,羌活勝濕湯治療AS的生物學進程主要涉及細胞外間隙、脂多糖介導的信號通路、一氧化氮生物合成過程的正調控、血管生成、絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)活性的激活與級聯反應、缺氧反應、細胞因子的活性等。通過KEGG通路富集分析發現,明顯富集的TNF信號通路、FoxO信號通路、VEGF信號通路、炎癥性腸病、NF-kappa B信號通路、HIF-1信號通路、T細胞受體等信號通路可能是治療AS的關鍵通路。其中與各促炎因子相關的信號通路已有大量研究證明與AS發病機制有關,故不再贅述。FoxO信號通路、炎癥性腸病是在本研究中值得關注的信號通路。在包括AS在內的慢性免疫介導炎癥疾病中,參與細胞增殖和存活的基因和通路的異常調節對炎癥的發生和發展起到了關鍵作用[25]。叉頭框轉錄因子家族(forkhead box,FOX)的O亞族在維持細胞穩態上具有重要的作用,作為重要的信號整合因子,它將氧化應激、炎癥和激素變化等環境刺激轉化為參與許多生理和病理過程的動態基因表達程序,在骨和骨細胞中廣泛表達,是骨形成和骨重塑的關鍵調節因子[26]。研究表明,敲除FoxO的小鼠軟骨中參與抗氧化、自噬、氧化還原調節和適應能量應激的基因表達明顯減少,同時使FoxO在人軟骨細胞中過表達,結果發現自噬增強,炎癥介質和軟骨降解酶的表達減弱,并拮抗IL-1β的刺激作用[27]。由于羌活勝濕湯中的有效成分具有抗氧化作用,說明該方可能通過上調FoxO信號通路的表達,抑制促炎因子的釋放,提高機體抗氧化能力,保護細胞免受氧化應激損傷,進而起到治療AS的作用。炎癥性腸病是由免疫介導的胃腸道晚期炎癥。研究發現,AS患者中,炎癥性腸病的發病率約為6%~14%,由于這兩種情況可能是同時發生的,AS和炎癥性腸病被認為存在相似的發病機制[28-30]。基于臨床重疊的表現,證明兩者之間存在共同的介體,在炎癥與骨的穩態之間起作用。而羌活勝濕湯的作用靶點在炎癥性腸病通路的明顯富集,提示我們在臨床上,可通過挖掘相關聯疾病的重疊靶基因,篩選同時作用于這些靶基因的藥物,借助中醫學異病同治之理念組方用藥,不失為一種有效的組方途徑。
分子對接結果顯示,羌活勝濕湯中主要有效成分在與關鍵靶基因對接過程中均進入了活性位點,尤其在與VEGFA、PTGS2、TNF-α的對接過程中體現了穩定的結構與強的活性,表明該方對VEGFA、PTGS2、TNF-α的表達具有強抑制作用,起到了抑制促炎因子的釋放,調控骨的穩態及自身免疫的作用。基于分子對接結果,說明本研究數據及結果準確度較高,建立在此基礎上的網絡分析具有較高的置信度和參考價值。
隨著生物信息學技術提高、各種生物信息數據庫的建立,各種中藥活性成分的作用靶點與疾病靶基因之間的網絡樣作用關系愈加清晰。中醫藥治療AS的研究仍處于發展階段,需要更多高質量、多角度和詳細的數據理論支持臨床試驗。綜上所述,本研究通過生物信息學與分子對接技術揭示羌活勝濕湯治療AS的作用機制,以期為今后治療AS的有效中藥藥理研究與中藥組方配伍提供新思路。

