不同溶栓時(shí)間窗rt-PA治療急性缺血性腦卒中后神經(jīng)血管功能的變化特征
何肖君 戴雅玲 李鉆芳 陳樂(lè)文 林華偉 賈微微 楊敏光 梁勝祥 柳維林 陶靜
(福建中醫(yī)藥大學(xué) 1康復(fù)醫(yī)學(xué)院,福州 福建 350122;2康復(fù)產(chǎn)業(yè)研究院)
缺血性腦卒中也稱(chēng)腦梗死,是臨床最常見(jiàn)的腦卒中類(lèi)型,由于腦血管某一分支發(fā)生較長(zhǎng)時(shí)間或永久性堵塞,導(dǎo)致腦組織持續(xù)性缺血、缺氧而發(fā)生壞死、軟化,引起局灶性神經(jīng)功能缺損或永久性喪失〔1〕。腦卒中導(dǎo)致全球范圍內(nèi)每年616.73萬(wàn)人死亡〔2〕,中國(guó)每年新增250萬(wàn)腦卒中病例,年齡標(biāo)化后患病率為1.12%,運(yùn)動(dòng)功能障礙高達(dá)70%~80%〔3〕。腦卒中后患者功能障礙嚴(yán)重影響其生活質(zhì)量,急性發(fā)作期間及時(shí)有效治療與預(yù)后功能密切相關(guān)。溶栓治療被認(rèn)為是迄今為止最有效的治療手段,1996年美國(guó)FDA批準(zhǔn)重組化織型纖溶酶原激活劑(rt-PA)用于腦卒中發(fā)病后3 h內(nèi)靜脈溶栓的藥物,其通過(guò)溶解血管梗死的血栓從而恢復(fù)缺血腦組織的血液供應(yīng),并促進(jìn)神經(jīng)功能恢復(fù)〔4〕。但是受限于狹窄的治療時(shí)間窗,只有3%~5%的患者接受溶栓治療〔5〕。顱內(nèi)出血是溶栓治療最常見(jiàn)的并發(fā)癥,超時(shí)間窗靜脈溶栓治療易造成缺血再灌注損傷和神經(jīng)毒性〔6〕。2008年歐洲合作組急性腦卒中研究(ECASS)-Ⅲ試驗(yàn)明確,急性缺血性腦卒中靜脈溶栓治療時(shí)間窗擴(kuò)展至4.5 h〔7〕,2016年發(fā)表的ECASS-Ⅳ試驗(yàn)研究發(fā)現(xiàn)運(yùn)用磁共振灌注成像(PWI)結(jié)合磁共振彌散加權(quán)成像(DWI)篩選缺血半暗帶不匹配患者,4.5~9.0 h靜脈溶栓組較安慰劑組可有效提高血管再通率和改善神經(jīng)功能,提示rt-PA靜脈溶栓時(shí)間窗有望延長(zhǎng)〔8〕。2019年《新英格蘭醫(yī)學(xué)雜志》臨床研究表明,腦卒中發(fā)生后4.5~9.0 h或者帶著腦卒中癥狀醒來(lái)時(shí)(腦卒中發(fā)生時(shí)間不明)在磁共振成像(MRI)灌注成像引導(dǎo)下開(kāi)始rt-PA靜脈溶栓治療對(duì)患者有益〔9〕。
本研究開(kāi)展rt-PA靜脈治療不同時(shí)間窗的臨床前實(shí)驗(yàn),從神經(jīng)血管功能的角度揭示rt-PA在不同時(shí)間窗的病理學(xué)特征。
1 材料與方法
1.1實(shí)驗(yàn)動(dòng)物 8周齡SPF級(jí)健康雄性C57BL/6J小鼠,購(gòu)自上海斯萊克實(shí)驗(yàn)動(dòng)物責(zé)任有限公司〔SCXK(滬)2012-0002〕,體重22~26 g。由福建中醫(yī)藥大學(xué)實(shí)驗(yàn)動(dòng)物中心飼養(yǎng),模擬標(biāo)準(zhǔn)日夜系統(tǒng),自由攝食飲水。
實(shí)驗(yàn)過(guò)程所有動(dòng)物的處理均嚴(yán)格按照實(shí)驗(yàn)動(dòng)物使用指南進(jìn)行。
1.2主要實(shí)驗(yàn)試劑和儀器 7.0 T小動(dòng)物磁共振儀(德國(guó)布魯克公司);阿替普酶溶栓藥(德國(guó)勃林格殷格翰公司);激光散斑血流儀(瑞典帕瑞醫(yī)學(xué)公司)。
1.3小鼠缺血再灌注模型 采用改良線栓法〔9〕制備小鼠缺血再灌注模型:小鼠異氟烷全麻后,仰臥固定于37℃手術(shù)臺(tái)上,小心剃去頸部正中毛發(fā),碘伏酒精分別消毒頸部皮膚,頸部正中縱向切開(kāi)長(zhǎng)約1.5 cm,暴露左側(cè)頸總動(dòng)脈(CCA)、頸內(nèi)動(dòng)脈(ICA)及頸外動(dòng)脈(ECA)。首先分離CCA于其上掛線1;然后分離ECA血管及其分支,在其頭尾端掛上線2和3;分離ECA與ICA分支,于ICA穿線4。在ECA上距分叉1.0~1.5 mm用顯微剪剪一切口,將標(biāo)記好的線栓由此切口插入CCA中,剪斷ECA遠(yuǎn)心端的血管,將線栓從CCA拔出至分叉稍尾側(cè),右手將線栓轉(zhuǎn)向滑入ICA,插入深度1 cm左右,到達(dá)大腦中動(dòng)脈與前交通之間。最后將線3打緊以固定線栓,松開(kāi)線1。待缺血60 min后,緩慢拔出線栓,術(shù)后縫合切口。術(shù)中和術(shù)后保持室溫25℃左右,使其體溫維持在(37±1)℃,直到恢復(fù)活動(dòng)。手術(shù)結(jié)束后,動(dòng)物放置于室溫25℃環(huán)境下蘇醒,正常飲食。
1.4分組與給藥 在動(dòng)物模型制備完成后將小鼠隨機(jī)分為3組,每組6只。①缺血性腦卒中模型組:在缺血再灌注后不予藥物治療;②rt-PA治療4.5 h給藥組:在缺血再灌注后4.5 h尾靜脈注射rt-PA(0.9 mg/kg);③rt-PA治療9.0 h給藥組:在缺血再灌注后9.0 h尾靜脈注射rt-PA(0.9 mg/kg)。
1.5神經(jīng)功能缺損評(píng)估 每組小鼠在注射rt-PA 30 min后進(jìn)行改良神經(jīng)功能缺損評(píng)分(mNSS)。mNSS主要包括:運(yùn)動(dòng)、感覺(jué)、平衡和反射4個(gè)方面評(píng)估,正常得0分,每得1分代表無(wú)法完成測(cè)試或者無(wú)反射活動(dòng),總分為18分。
1.6腦血流量測(cè)定 每組在注射rt-PA 1 h后,采用激光散斑成像系統(tǒng)監(jiān)測(cè)小鼠腦血流量,小鼠異氟烷全麻后固定于腦立體定位儀上,剃去小鼠頭部的毛后,從頭部正中沿矢狀縫剪開(kāi)頭皮和筋膜,將鏡頭光纖固定于小鼠頭顱上方約11 cm處,設(shè)置采樣頻率5幀/s,獲取640×480像素圖像,然后通過(guò)系統(tǒng)將原始散斑圖轉(zhuǎn)化成血流圖。計(jì)算梗死側(cè)腦血流量(ΔCBF)=〔右側(cè)感興趣區(qū)腦血流(RrCBF)-左側(cè)感興趣區(qū)腦血流(LrCBF)〕/RrCBF。
1.7H-MRS檢測(cè) 在注射rt-PA 18 h后使用7.0 T小動(dòng)物磁共振掃描儀進(jìn)行小鼠腦部掃描,小鼠經(jīng)3%異氟烷麻醉后置于立體支架上,掃描期間用1.5%異氟烷持續(xù)麻醉,利用水循環(huán)加熱系統(tǒng)使小鼠體溫保持在37℃左右,并實(shí)時(shí)監(jiān)控呼吸頻率。先行常規(guī)定位掃描,而后進(jìn)行T2加權(quán)掃描(T2WI),掃描參數(shù)重復(fù)時(shí)間(TR)=4 200 ms,回波時(shí)間(TE)=35 ms,最后基于T2WI圖像選取梗死側(cè)初級(jí)運(yùn)動(dòng)皮層為感興趣區(qū)域進(jìn)行波譜掃描。掃描面積為1.5×1.5×1.5 mm3,勻場(chǎng)、壓水,使其半高峰寬值低于20 Hz,后選擇點(diǎn)分辨波譜脈沖序列(PRESS)進(jìn)行數(shù)據(jù)采集,掃描參數(shù)TR=1 500 ms,TE=144 ms。最后通過(guò)Topspin3.0軟件計(jì)算出各代謝產(chǎn)物峰下面積,以肌酸濃度值作為參照標(biāo)準(zhǔn),各代謝產(chǎn)物峰下面積與Cr比值即為代謝物濃度。
1.8尼氏染色 各組小鼠在注射rt-PA 24 h后進(jìn)行灌注取腦,制備5 μm冠狀切片。經(jīng)二甲苯脫蠟,梯度酒精脫水后按照尼氏染色試劑盒進(jìn)行操作。首先在腦片上滴加尼氏染色試劑A,置于56℃水浴箱孵育1 h;用磷酸鹽緩沖液(PBS)將腦片上試劑洗去,滴加試劑B分化10 s,在顯微鏡下觀察背景接近無(wú)色為止。純水洗5 min后晾干,中性樹(shù)脂封片,光學(xué)顯微鏡下拍片成像。
1.9免疫組化 組織切片后用檸檬酸鈉進(jìn)行組織抗原修復(fù),滴加50 μl過(guò)氧化酶阻斷溶液,室溫下孵育10 min,PBS沖洗3次;滴加 50 μl正常非免疫動(dòng)物血清,室溫下孵育10 min;滴加50 μl一抗血管內(nèi)皮生長(zhǎng)因子受體VEGFR-1+VEGFR-2 (1∶300),4℃過(guò)夜;室溫下復(fù)溫30 min,PBS沖洗3次;每張切片滴加50 μl二抗,室溫孵育10 min,PBS沖洗3次;滴加50 μl鏈霉菌抗生物素-過(guò)氧化物酶溶液,室溫下孵育10 min,PBS沖洗3次;滴加新鮮配制的DAB 顯色劑,室溫孵育10 s,自來(lái)水沖洗,蘇木素復(fù)染10 s,自來(lái)水沖洗返藍(lán)后封片。
1.10統(tǒng)計(jì)學(xué)方法 采用SPSS25.0軟件進(jìn)行方差分析,兩兩比較采用LSD法。
2 結(jié) 果
2.1不同時(shí)間窗rt-PA給藥治療急性缺血性腦卒中對(duì)血管功能的影響 結(jié)果顯示,與模型組ΔCBF/%〔(31.42±4.24)%〕比較,rt-PA治療4.5 h給藥組ΔCBF/%〔(25.23±4.63)%〕明顯上升(P<0.05),rt-PA治療9.0 h給藥組ΔCBF〔(32.68±4.12)%〕差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);與rt-PA治療9.0 h給藥組比較,rt-PA治療4.5 h給藥組ΔCBF有顯著改善P<0.001)。見(jiàn)圖1。
梗死側(cè)初級(jí)運(yùn)動(dòng)皮層VEGFR表達(dá)情況,免疫組化染色結(jié)果表明,模型組和rt-PA治療9.0 h給藥組可見(jiàn)少量VEGFR-1和VEGFR-2表達(dá)陽(yáng)性細(xì)胞;rt-PA治療4.5 h給藥組免疫陽(yáng)性細(xì)胞數(shù)量增多。見(jiàn)圖2。

圖1 激光散斑成像系統(tǒng)監(jiān)測(cè)各組腦血流量變化
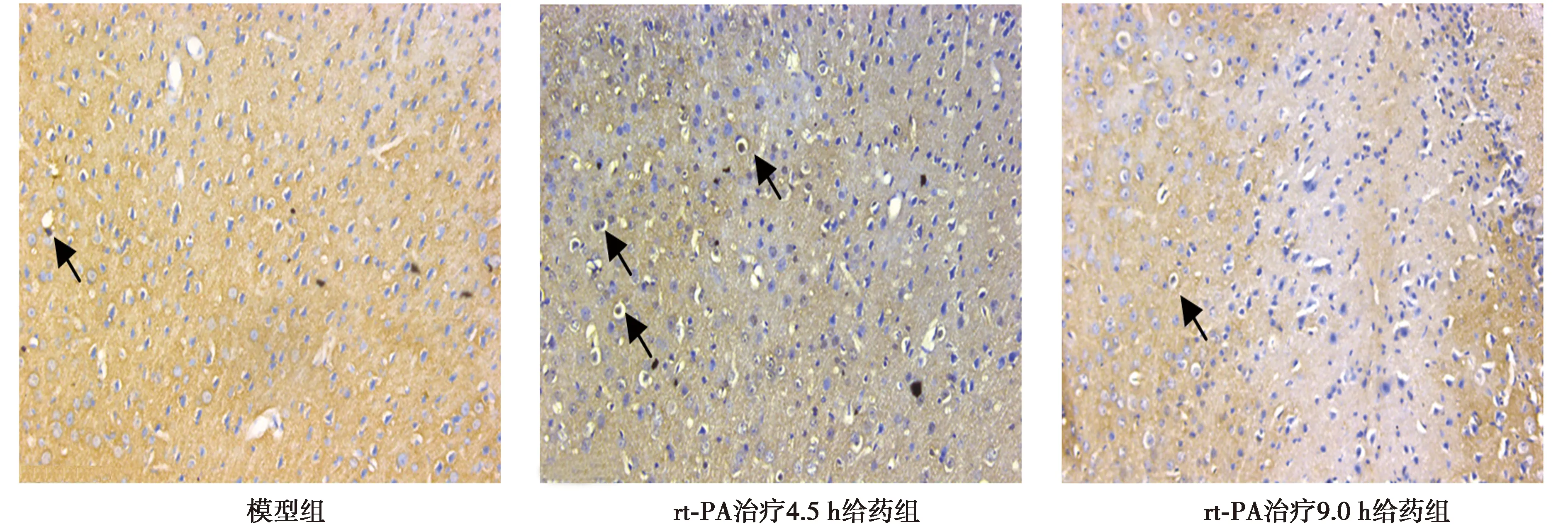
圖2 免疫組化法標(biāo)記各組VEGFR-1+VEGFR-2陽(yáng)性細(xì)胞數(shù)量(×200)
2.2不同時(shí)間窗rt-PA給藥治療急性缺血性腦卒中對(duì)神經(jīng)功能的影響
2.2.1梗死側(cè)初級(jí)運(yùn)動(dòng)皮層神經(jīng)元形態(tài)的變化 模型組iM1腦區(qū)神經(jīng)元出現(xiàn)空泡樣變性;rt-PA治療4.5 h給藥組iM1腦區(qū)神經(jīng)元排列相對(duì)整齊致密,胞體較大,尼氏體也較豐富;rt-PA治療9.0 h給藥組iM1腦區(qū)組織結(jié)構(gòu)松散,神經(jīng)細(xì)胞萎縮,核固縮。見(jiàn)圖3。
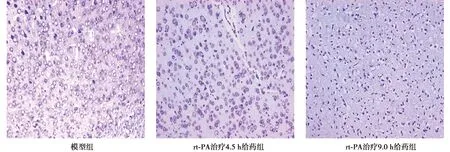
圖3 尼氏染色觀察各組神經(jīng)元形態(tài)(×200)
2.2.2梗死側(cè)初級(jí)運(yùn)動(dòng)皮層神經(jīng)代謝物質(zhì)Cho、NAA相對(duì)含量比較 rt-PA治療4.5 h給藥組的Cho相對(duì)含量較模型組和rt-PA治療9.0 h給藥組顯著升高(P<0.001),rt-PA治療4.5 h給藥組NAA相對(duì)含量較模型組、rt-PA治療9.0 h給藥組明顯升高(P<0.05,P<0.001)。見(jiàn)表1,圖4、5。
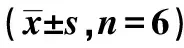
表1 各組梗死側(cè)M1區(qū)神經(jīng)代謝物質(zhì)Cho、NAA相對(duì) 含量比較

圖4 磁共振波譜成像峰值圖
2.3不同時(shí)間窗rt-PA給藥治療急性缺血性腦卒中對(duì)mNSS的影響 模型組mNSS(5.50±1.38)分、rt-PA治療4.5 h給藥組(6.00±1.41)分和rt-PA治療9.0 h給藥組(6.33±2.34)分,3組mNSS差異無(wú)統(tǒng)計(jì)學(xué)意義(F=0.338,P>0.05)。
3 討 論
缺血性腦卒中指腦供血突然中斷,導(dǎo)致腦組織因缺血缺氧造成不可逆神經(jīng)元壞死,而在梗死周邊區(qū)存在缺血程度較輕的潛在可逆性損傷區(qū)域?yàn)槿毖氚祹ВM快恢復(fù)缺血半暗帶血供對(duì)減輕腦組織的損傷至關(guān)重要〔10〕。臨床研究表明,單獨(dú)的神經(jīng)保護(hù)治療不足以恢復(fù)血流灌注和保護(hù)血管完整性〔11〕。2002年NINDS提出了“神經(jīng)血管單元”這一腦卒中治療的概念模型,神經(jīng)血管單元是一個(gè)功能上和結(jié)構(gòu)上相互依存的多細(xì)胞復(fù)合物,包括內(nèi)皮細(xì)胞、基底膜、周細(xì)胞、星形膠質(zhì)細(xì)胞和神經(jīng)元等〔12〕。已有研究表明,神經(jīng)血管單元是腦卒中后分子事件的靶標(biāo),并參與腦卒中病理機(jī)制發(fā)生〔13〕。
VEGF具有促進(jìn)血管內(nèi)皮細(xì)胞增殖作用,其在生理狀態(tài)下,僅在血管內(nèi)皮細(xì)胞有低水平表達(dá)。腦梗死后梗死灶和缺血半暗帶的VEGF表達(dá)增加,可促進(jìn)血管新生形成〔14〕。VEGFR是VEGF特異性的膜受體,其中VEGFR-1和VEGFR-2主要在血管內(nèi)皮細(xì)胞中表達(dá),是血管新生標(biāo)志物〔15,16〕。在缺血后數(shù)小時(shí)至數(shù)天內(nèi),VEGFR-1和VEGFR-2蛋白在海馬和皮質(zhì)神經(jīng)元表達(dá)增加〔17〕。研究表明,缺血可上調(diào)星型膠質(zhì)細(xì)胞的VEGF及其受體的表達(dá),促進(jìn)腦損傷后的神經(jīng)可塑性〔18〕。在缺血急性期運(yùn)用VEGF可以減少腦梗死面積和促進(jìn)神經(jīng)元再生〔19〕。對(duì)缺血性梗死動(dòng)物模型在腦梗死后3 h給予rt-PA溶栓治療,其梗死周邊區(qū)VEGF和突觸素表達(dá)增加,促進(jìn)神經(jīng)血管重塑〔20〕。進(jìn)一步發(fā)現(xiàn),rt-PA通過(guò)激活ERK2/p38信號(hào)通路,上調(diào)血管內(nèi)皮細(xì)胞VEGF的表達(dá)〔21〕。另有研究表明,腦中動(dòng)脈缺血模型(MCAO)大鼠在梗死后4 h以上,10 mg/kg tPA對(duì)其失去了效力,反而增加了梗死體積及加重出血性轉(zhuǎn)化〔22〕。
大腦皮層神經(jīng)元需要持續(xù)的氧供和攝取葡萄糖來(lái)滿足它們的代謝需求,因此皮層神經(jīng)元的存活依賴(lài)于感知和適應(yīng)低氧和低葡萄糖濃度的機(jī)制激活〔23〕。磁共振波譜(MRS)通過(guò)檢測(cè)腦缺血后的代謝產(chǎn)物反映腦缺血損傷的嚴(yán)重程度。NAA僅存在于神經(jīng)元和神經(jīng)軸突內(nèi),NAA的降低反映神經(jīng)元的丟失和損傷,可預(yù)測(cè)腦卒中神經(jīng)功能結(jié)局;Cho主要包括甘油磷酸膽堿、磷酸膽堿和膽堿等,是神經(jīng)遞質(zhì)乙酰膽堿的前體分子,參與神經(jīng)細(xì)胞膜構(gòu)成,神經(jīng)元數(shù)量增多可表現(xiàn)為Cho峰值增高〔24〕。運(yùn)用MRS觀察MCAO 模型小鼠在術(shù)后3、8、24 h的腦代謝物質(zhì)變化,發(fā)現(xiàn)NAA含量呈下降趨勢(shì),表明腦缺血造成神經(jīng)元損傷〔25〕。有研究表明,tMCAO模型小鼠自身可釋放內(nèi)源性tPA或運(yùn)用重組組織型tPA治療,通過(guò)激活神經(jīng)元中mTOR細(xì)胞信號(hào)傳導(dǎo)途徑增加對(duì)葡萄糖攝取利用,起到保護(hù)神經(jīng)元作用〔26〕。但是,rt-PA同時(shí)具有神經(jīng)毒性作用,主要取決于治療時(shí)間、劑量、神經(jīng)元類(lèi)型等因素〔27〕。
有研究對(duì)MCAO模型大鼠在腦梗死后2、6 h兩個(gè)時(shí)間點(diǎn)給予rt-PA治療,發(fā)現(xiàn)2 h給藥組較模型組腦梗死面積顯著減小,而6 h給藥組約50%大鼠出現(xiàn)出血性轉(zhuǎn)化,并伴隨著多形核白細(xì)胞的累積產(chǎn)生神經(jīng)毒性作用〔22〕。此外,對(duì)MCAO模型大鼠在梗死后5 h以10 mg/kg劑量給予rt-PA,治療組較安慰劑組具有神經(jīng)血管保護(hù)作用〔28〕。本研究結(jié)果與以上研究基本相符。而本實(shí)驗(yàn)結(jié)果可能與既往研究報(bào)道的神經(jīng)癥狀發(fā)生3 h后靜脈注射rt-PA,神經(jīng)功能的改善作用不能即刻體現(xiàn)有關(guān)〔29〕,未來(lái)研究應(yīng)延長(zhǎng)評(píng)估神經(jīng)功能的時(shí)間,以更全面觀察溶栓療效。
溶栓時(shí)間窗是腦卒中患者的生命窗,近來(lái)已有許多研究著力于rt-PA聯(lián)合其他治療方式來(lái)延長(zhǎng)溶栓時(shí)間窗,以為更多患者爭(zhēng)取治療時(shí)機(jī)。有研究在缺血性腦卒中大鼠梗死后6 h運(yùn)用rt-PA溶栓治療聯(lián)合腦梗死后30 min神經(jīng)保護(hù)藥物2-BFI,結(jié)果表明聯(lián)合治療下調(diào)促凋亡蛋白B細(xì)胞淋巴瘤(Bcl)-2相關(guān)X蛋白(Bax)表達(dá)和上調(diào)抗凋亡蛋白Bcl-2表達(dá),并且減少腦梗死面積,減輕神經(jīng)功能缺損,保護(hù)神經(jīng)血管單元完整性〔30〕。此外,也可通過(guò)聯(lián)合其他藥物,如他克莫司〔31〕和溴抑他汀〔32〕等,可抑制基質(zhì)金屬蛋白酶激活,保護(hù)微血管內(nèi)皮細(xì)胞完整性以降低血腦屏障通透性,減輕出血轉(zhuǎn)化,延長(zhǎng)溶栓時(shí)間窗至6 h。因此,要延長(zhǎng)rt-PA溶栓時(shí)間窗還需要聯(lián)合其他神經(jīng)血管單元保護(hù)藥物。
- 中國(guó)老年學(xué)雜志的其它文章
- 靶向腸道菌群及其代謝產(chǎn)物的動(dòng)脈粥樣硬化性疾病治療
- 經(jīng)顱多普勒監(jiān)測(cè)對(duì)肝大部切除術(shù)后肝性腦病的影響研究進(jìn)展
- 英國(guó)養(yǎng)老機(jī)構(gòu)市場(chǎng)化實(shí)踐對(duì)中國(guó)養(yǎng)老機(jī)構(gòu)公建民營(yíng)改革的啟示
- 視網(wǎng)膜靜脈周?chē)字形麽t(yī)藥物診治的研究進(jìn)展
- SUMO化調(diào)控突觸可塑性和介導(dǎo)認(rèn)知功能改變研究進(jìn)展
- 運(yùn)動(dòng)改善2型糖尿病患者乳酸代謝的研究進(jìn)展

