500 Internal Server Error
調強放療聯合甲磺酸阿帕替尼治療局部晚期胃癌的效果評價
么志軍 郭振江 巴楠 鄭力豪 孫滿滿 李文
[摘 ? 要] ? 目的:探討調強放療(intensity modulated radiation therapy,IMRT)技術聯合甲磺酸阿帕替尼治療局部晚期胃癌的臨床療效。方法:局部晚期胃癌患者124例,隨機分為觀察組和對照組各62例。對照組給予IMRT技術治療,觀察組在對照組基礎上聯合應用甲磺酸阿帕替尼治療。比較兩組治療2個月后臨床療效、治療前及治療2個月后血清腫瘤標志物水平、1年總生存率(overall survival,OS)和無進展生存率(progression free survival,PFS)以及治療毒副反應。結果:觀察組治療2個月后疾病控制率75.81%,客觀緩解率51.61%,分別高于對照組的58.06%及32.26%,差異均有統計學意義(P<0.05)。治療2個月后觀察組血清癌胚抗原(carcinoembryonic antigen,CEA)、糖類抗原199(carbohydrate antigen 199,CA199)和CA724水平分別為6.06±1.52 ng/mL、29.72±3.49 U/mL和6.85±1.03 U/mL,對照組分別為7.86±1.50 ng/mL、34.08±4.11 U/mL和9.20±1.52 U/mL,兩組均較治療前下降,但觀察組較對照組下降更為明顯,差異均有統計學意義(P<0.05)。觀察組1年PFS為74.19%,1年OS為77.42%,分別高于對照組的56.45%和56.45%,差異均有統計學意義(P<0.05)。兩組毒副反應發生率比較,差異均無統計學意義(P>0.05)。結論:IMRT技術聯合甲磺酸阿帕替尼治療局部晚期胃癌可提高短期臨床療效,降低腫瘤標志物水平,改善患者生存情況,安全性良好。
[關鍵詞] ? 局部晚期胃癌;調強放療;甲磺酸阿帕替尼;疾病控制率;客觀緩解率;無進展生存率;總生存率
[中圖分類號] ? R735.2 [文獻標志碼] ? B [DOI] ? 10.19767/j.cnki.32-1412.2023.06.009
胃癌為臨床常見的消化系統惡性腫瘤,由于早期癥狀缺乏特異性,大部分患者在確診時已為局部晚期,失去手術治療最佳時機[1]。與常規放療相比,調強放療(intensity modulated radiation therapy,IMRT)治療局部晚期胃癌毒副作用更小,照射效果更佳[2]。但IMRT技術的高度適形可能遺漏一部分靶區,增加疾病復發的風險。甲磺酸阿帕替尼為新型分子靶向藥物,通過抑制血管內皮細胞生長因子受體2(vascular endothelial growth factor receptor 2,VEGFR-2)來抑制腫瘤血管的生成[3]。目前IMRT技術聯合甲磺酸阿帕替尼治療老年食管癌、晚期肺癌的臨床療效已得到證實[4-5]。本研究選取我科2020年1月—2022年5月收治的局部晚期胃癌患者124例,探討IMRT技術聯合甲磺酸阿帕替尼的治療效果。
1 ? 資料與方法
1.1 ? 一般資料 ? 局部晚期胃癌患者124例,采用隨機數字表法分為觀察組與對照組各62例。觀察組男性38例,女性24例,年齡38~69歲,平均53.13±6.36歲;體質量指數15.8~24.4 kg/m2,平均19.71±2.02 kg/m2;病理類型:腺癌20例,腺鱗癌15例,髓樣癌14例,未分化細胞癌13例。對照組男性36例,女性26例,年齡41~68歲,平均52.97±6.46歲;體質量指數15.5~23.6 kg/m2,平均19.82±2.14 kg/m2;病理類型:腺癌19例,腺鱗癌14例,髓樣癌15例,未分化細胞癌14例。兩組一般資料比較,差異均無統計學意義(P>0.05),具有可比性。納入標準:(1)符合《內科學(第9版)》[6]中胃癌診斷標準,且經由胃鏡活檢確診;(2)影像學及消化道造影檢查明確均為賁門部Ⅲ、Ⅳ期胃癌;(3)無法耐受化療或經二線化療失敗者;(4)預計生存期>6個月;(5)卡氏功能狀態評分>70分;(6)患者及家屬均知情同意。排除標準:(1)合并嚴重心、肝、腎功能障礙或伴有其他惡性腫瘤;(2)病理類型為印戒細胞癌;(3)營養狀況差,無法耐受放療或靶向治療;(4)既往接受過靶向治療或放療;(5)伴有自身免疫性疾病或血液系統疾病;(6)哺乳期或妊娠期女性。本研究經醫院醫學倫理委員會批準。
1.2 ? 治療方法
1.2.1 ? 對照組:接受IMRT技術治療,治療前2 h囑患者禁食并口服0.9%氯化鈉注射液500 mL。采用熱塑膜固定患者體位,CT掃描并采集圖像,定位治療靶區及危及器官。使用Primus-Hi直線加速器(德國西門子股份公司)6 MV X線進行放射治療,設置照射野方向≥4個,單次放射劑量1.8~2.2 Gy,靶區及陽性淋巴結區總放射劑量為60~66 Gy,每天放射治療1次,5次/周。
1.2.2 ? 觀察組:患者在IMRT放療基礎上口服甲磺酸阿帕替尼片(江蘇恒瑞醫藥股份有限公司),初始劑量500 mg/次,1次/d, 1~2周后依據患者情況增加劑量,最高劑量為850 mg/次,于餐后半小時以溫開水送服,連續服用至疾病進展或不耐受。
1.3 ? 觀察指標 ? (1)臨床療效:治療2個月后患者復查影像學檢查,依據實體瘤療效評價標準[7]判定療效,所有靶病灶消失為完全緩解(complete response,CR);靶病灶直徑之和減少≥30%為部分緩解(partial response,PR);以整個研究過程中測得的最小靶病灶直徑之和為參照,直徑和相對增加≥20%且直徑和絕對值增加≥5 mm判定為疾病進展(progressive disease,PD);靶病灶有減少但程度未達到PR,或有增加但程度未達到PD判定為疾病穩定(stable disease,SD)。疾病控制率=(CR+PR+SD)例數/總例數×100%,客觀緩解率=(CR+PR)例數/總例數×100%。(2)腫瘤標志物:治療前、治療2個月后測定患者血清癌胚抗原(carcinoembryonic antigen,CEA)、糖類抗原199(carbohydrate antigen199,CA199)、CA724水平。(3)生存情況:治療開始后隨訪1年,通過電話、門診記錄患者生存時間、復發轉移發生情況,計算無進展生存率(progression free survival,PFS)及總生存率(overall survival,OS)。(4)毒副反應:觀察患者治療期間骨髓抑制、胃腸道反應(惡心、嘔吐、便秘、食欲不振等)、皮膚癥狀(局部皮膚瘙癢、皮膚干燥、毛發脫落等)、肝損傷、高血壓、蛋白尿發生情況。
1.4 ? 統計學處理 ? 應用SPSS 25.0統計學軟件處理分析數據。計量資料經Shapiro-Wilk正態性檢驗,符合正態分布的計量資料以x±s表示,組間比較采用獨立樣本t檢驗,組內比較采用配對樣本t檢驗;計數資料以n(%)表示,組間比較采用χ2檢驗或Fisher精確檢驗。P<0.05為差異有統計學意義。
2 ? 結 ? ? ?果
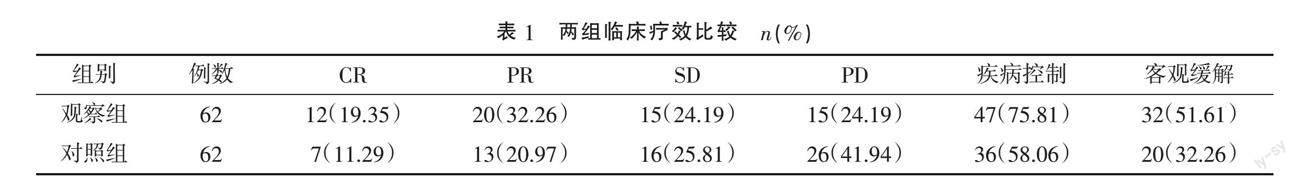
2.1 ? 兩組臨床療效比較 ? 觀察組疾病控制率及客觀緩解率分別為75.81%和51.61%,分別高于對照組的58.06%(χ2=4.409)和32.26%(χ2=4.769),差異均有統計學意義(P<0.05)。見表1。
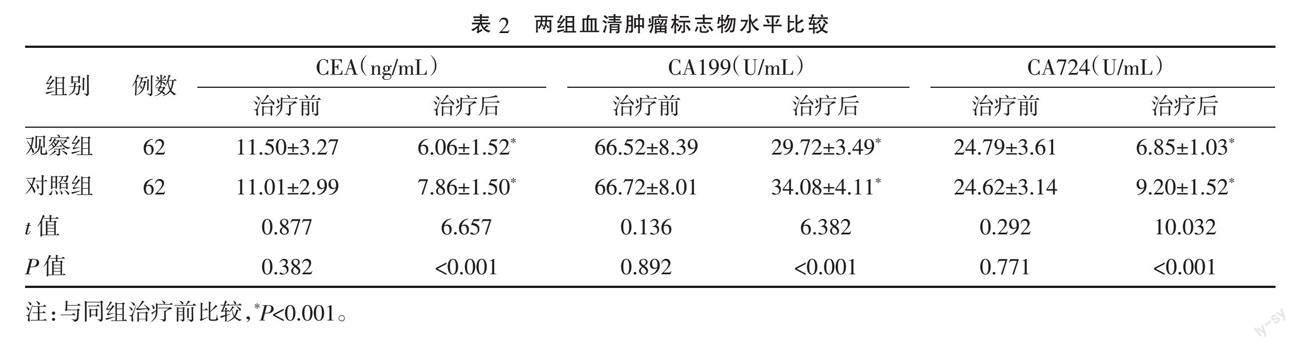
2.2 ? 兩組血清腫瘤標志物水平比較 ? 兩組治療前血清CEA、CA199、CA724水平比較,差異均無統計學意義(P>0.05);治療2個月后兩組CEA、CA199、CA724水平均較治療前下降,且觀察組下降較對照組更明顯,差異均有統計學意義(P<0.001)。見表2。
2.3 ? 兩組生存情況比較 ? 隨訪1年,觀察組16例疾病進展,1年PFS為74.19%,對照組27例疾病進展,1年PFS為56.45%,觀察組1年PFS高于對照組,差異有統計學意義(χ2=4.308,P=0.038);觀察組14例死亡,1年OS為77.42%,對照組27例死亡,1年OS為56.45%,觀察組1年OS高于對照組,差異有統計學意義(χ2=6.158,P=0.013)。
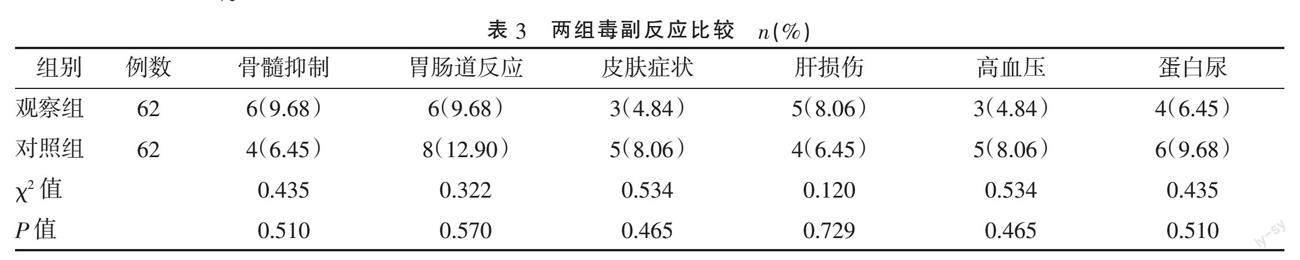
2.4 ? 兩組毒副反應比較 ? 兩組治療期間毒副反應發生率比較,差異均無統計學意義(P>0.05)。見表3。
3 ? 討 ? ? ?論
IMRT技術在改善局部晚期胃癌患者生存質量、延長生存時間方面具有顯著療效,但仍有部分患者治療效果不佳。當EGFR發生基因突變,導致EGFR通路失調,引起細胞異常增殖與轉移,形成惡性腫瘤[8]。因此,抗血管生成、抑制EGFR基因突變成為延緩局部晚期胃癌患者病情進展的治療靶點。甲磺酸阿帕替尼是針對EGFR突變的口服靶向藥物,可選擇性抑制EGFR活性,從而阻斷細胞增殖和分裂,達到治療目的[9]。
本研究結果顯示,觀察組治療2個月后疾病控制率75.81%及客觀緩解率51.61%,分別高于對照組的58.06%和32.26%,觀察組血清CEA、CA199、CA724水平較對照組下降更為明顯,觀察組1年PFS為74.19%,高于對照組56.45%,差異均有統計學意義(P<0.05),表明IMRT技術聯合甲磺酸阿帕替尼治療可提高局部晚期胃癌臨床療效,延長患者生存時間,與張濤等[10-11]研究結果一致。與傳統放療相比,IMRT改善了靶區定位、勾畫及放療的實施方位,可調節射線束強度和形狀,體內射線的空間分布在三維方向上與靶區外輪廓一致,每個小野均可得到均勻的放射劑量,提高了照射精準度,更全面殺滅腫瘤細胞,并有效減少對周圍正常組織結構的照射[12]。甲磺酸阿帕替尼作為口服抗血管生成藥物,通過與血管內皮生長因子競爭性結合VEGFR-2,阻斷血管內皮生長因子信號通路,進而抑制腫瘤細胞生長與分裂,誘導腫瘤細胞凋亡[13]。甲磺酸阿帕替尼與IMRT技術聯合應用可進一步減少腫瘤細胞增殖,固化放射殺滅腫瘤細胞的作用,抑制損傷腫瘤細胞修復,從而增加放療敏感性,延長生存時間[14]。此外,兩組治療期間毒副反應發生率比較,差異均無統計學意義(P>0.05),表明IMRT技術聯合甲磺酸阿帕替尼不會增加發生毒副反應風險,具有良好的安全性。
綜上所述,IMRT技術聯合甲磺酸阿帕替尼治療局部晚期胃癌可提高短期臨床療效,降低腫瘤標志物水平,延長患者生存時間,且不增加毒副反應,安全性良好。
[參考文獻]
[1] TAKAHARI D,KATAI H,TAKASHIMA A,et al. Perioperative TAS-118 plus oxaliplatin in patients with locally advanced gastric cancer:APOLLO-11 study[J]. Gastric Cancer,2023,26(4):614-625.
[2] 劉映,宋瑩,張惠玲. 胃癌術后調強放療自動與人工計劃的劑量學比較[J]. 中華腫瘤防治雜志,2021,28(3):223-229.
[3] 劉昊川,介亞瓊,韓新光. 放射性粒子植入聯合抗血管生成靶向治療在口腔頜面部惡性腫瘤患者中的應用效果[J]. 河南醫學研究,2022,31(9):1587-1591.
[4] 王玉芳,劉美榮,李明君. 調強放療聯合小劑量阿帕替尼治療老年食管癌的療效觀察[J]. 實用老年醫學,2022,36(2):146-149.
[5] 楊永凈,趙玲,許德權,等. 甲磺酸阿帕替尼聯合放療協同誘導結直腸癌細胞凋亡的體外研究及機制探討[J]. 中國腫瘤,2022,31(10):839-845.
[6] 葛均波,徐永健,王辰. 內科學[M]. 9版. 北京:人民衛生出版社,2018:364-367.
[7] EISENHAUER E A,THERASSE P,BOGAERTS J,et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J]. Eur J Cancer,2009,45(2):228-247.
[8] FATIMA I,BARMAN S,UPPADA J,et al. MASTL regulates EGFR signaling to impact pancreatic cancer progression[J].Oncogene,2021,40(38):5691-5704.
[9] 葉再生,曾奕,魏晟宏,等. 阿帕替尼聯合奧沙利鉑和替吉奧在胃癌腹膜轉移轉化治療中的安全性及近期療效觀察[J]. 中華胃腸外科雜志,2021,24(3):240-247.
[10] 張濤,惠華,徐海亭,等. 調強放療聯合甲磺酸阿帕替尼治療老年局部晚期賁門癌患者效果及對血管內皮生長因子受體的影響[J]. 腫瘤研究與臨床,2018,30(2):99-102,106.
[11] 趙美琴,蘇新華,楊杰,等. 欖香烯口服乳聯合甲碘酸阿帕替尼治療晚期胃癌的臨床觀察[J]. 南通大學學報(醫學版),2023,43(5):430-433.
[12] 杜峰,王光明,魏曾曾. 調強放療同步替吉奧或卡培他濱化療治療中老年晚期食管癌的臨床研究[J]. 中國醫刊,2022,57(4):389-392.
[13] 林文發,吳芳,蔡徐帆,等. 阿帕替尼聯合SOX方案對胃癌伴腹膜轉移患者進行轉化治療的臨床療效[J]. 中國醫師雜志,2022,24(3):341-345.
[14] 丁利芳,張惠潔. 阿帕替尼聯合SOX方案對晚期胃癌患者療效的影響[J]. 中國現代應用藥學,2022,39(5):653-657.
[收稿日期] 2023-07-04
(本文編輯 ? 王曉蘊)

