多中心切割2D-HPLC-QTOF法對表柔比星脂質體制劑中未知雜質的分離與結構推斷
計小凡 歐陽輝 馮育林 饒毅 羅曉健
摘要:目的 建立多中心切割(MHC)二維高效液相色譜-四級桿飛行時間質譜(2D-HPLC-QTOF)法分離和推斷表柔比星脂質體制劑中未知雜質的方法。方法 一維液相色譜采用Symmetry-C18 (250 mm×4.6 mm,5 μm)為色譜柱,以乙腈和甲醇(6:1)為流動相A,以加入十二烷基硫酸鈉的磷酸緩沖液為流動相B,流動相A與流動相B體積比為57:43進行等度洗脫;二維高效液相色譜采用Agilent Eclipse-C18 (50 mm×2.1 mm,1.8 μm)為色譜柱,以0.1%的甲酸水和乙腈為流動相,采用梯度洗脫。將一維液相色譜條件下分離的雜質峰進行多中心切割儲存在定量環中,并轉移至二維進行分離,以四極桿飛行時間質譜(QTOF)進行結構推斷。結果 該方法可以使表柔比星與雜質峰較好地分離,并且可以得到高質量雜質峰進行結構推斷。在表柔比星脂質體制劑中對6個未知雜質進行有效的推斷。結論 建立的多中心切割二維高效液相色譜-四極桿飛行時間質譜法可高效準確的分離并推斷表柔比星脂質體制劑中的未知雜質,特別是微量和難以分離的雜質,對表柔比星制劑的質量控制提供了新方法。
關鍵詞:2D-HPLC-QTOF;多中心切割;表柔比星脂質體;未知雜質
中圖分類號:R978.1文獻標志碼:A
Abstract? ? Objective To establish a method called multiple heart-cutting 2D-HPLC-QTOF to separate and identify the unknown impurities in epirubicin liposome. Methods One-dimension (1D) chromatographic condition was Symmetry-C18 column using acetonitrile and methanol (6:1) as mobile phase A and phosphate buffer solution with sodium lauryl sulfate as mobile phase B. The volume ratio of mobile phase A to mobile phase B was 57:43. Two-dimension (2D) chromatographic condition was Agilent Eclipse-C18 column using 0.1% formic acid solution as mobile phase A and acetonitrile as mobile phase B (gradient elution). Multiple impurity peaks separated by 1D liquid chromatography were cut by multi hearting-cutting and stored in quantitative loops, and then transferred to 2D for separation. The structures were identified by quadrupole time-of-flight mass spectrometry (QTOF). Results Using this method, good separation of epirubicin from impurity peaks was achieved, and high-quality impurity peaks were obtained for structural identification. Six unknown impurities were effectively identified in the epirubicin liposome. Conclusion The established method can efficiently and accurately separate and identify unknown impurities in the epirubicin liposome, especially the trace and hard-to-separate impurities, and provides a new method for quality control of the Epirubicin preparation.
Key words? ? 2D-HPLC-QTOF; Multiple heart-cutting; Epirubicin liposome; Unknown impurities
表柔比星(epirubicin,EPI,又稱表阿霉素)是一種蒽環類廣譜抗腫瘤抗生素[1],臨床常用其鹽酸鹽治療乳腺癌、卵巢癌、肺癌和肝癌等[2-4]。研究表明其療效與阿霉素相同或略高,但心臟毒性低于阿霉素[5]。近年來許多表柔比星及其鹽酸鹽的產品逐步上市,雖然注射劑療效確切但長期使用仍會出現骨髓抑制和心臟毒性等副作用。脂質體作為新型藥物載體在提高藥物靶向性、降低毒副作用、延長治療時間方面非常突出[6]。
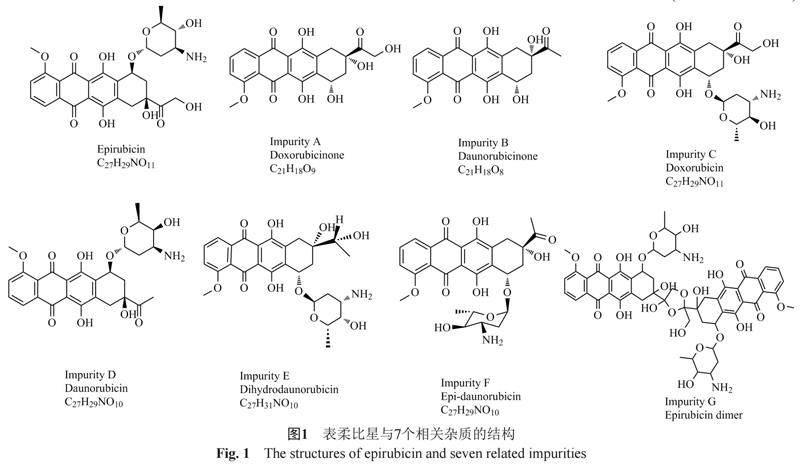
目前,各國藥典收載的鹽酸表柔比星和注射用鹽酸表柔比星有關物質檢測主要采用HPLC法[7-9],圖1列出了包括阿霉素在內的相關雜質共7種。檢測方法中因流動相含有磷酸和十二烷基硫酸鈉緩沖鹽,會對質譜檢測系統產生污染和離子抑制效應,無法與質譜直接聯用對表柔比星原料藥及其制劑的已知或未知雜質進行結構鑒定。邵武軍等[10]采用在線二維液相色譜-四極桿飛行時間質譜法對注射用鹽酸表柔比星長期穩定性留樣的未知峰進行定性分析,結果表示該未知雜質為鹽酸表柔比星二聚體,檢測方法簡便有效。
本試驗采用多中心切割(MHC)模式的2D-HPLC-QTOF聯用技術分離和推斷表柔比星脂質體制劑中的未知雜質。該方法可以實現對一維液相條件下分離的多個雜質峰進行中心切割,然后將這些中心切割儲存在定量環中,并將儲存的中心切割依次轉移到具有不同選擇性的二維進行分離,在實現共流出物得到有效分離的同時可以實現每個一維雜質峰都進行中心切割,避免雜質峰數據丟失。
1 儀器與試劑
1.1 儀器
Agilent 1290 型二維高效液相色譜儀(美國Agilent公司);Agilent 6530 型飛行時間質譜儀(美國Agilent公司);MILLI-Q超純水儀(美國Millipore公司)。
1.2 試劑
表柔比星(批號8514AOC00320)購自廣州安信醫藥有限公司;表柔比星脂質體(批號20170918)由江西本草天工科技有限公司提供;優級純十二烷基硫酸鈉購自美國Sigma公司;分析純磷酸購自國藥集團化學試劑有限公司;色譜級甲醇和乙腈購自美國Thermo Fisher Scientific公司;色譜級甲酸購自美國Sigma公司;超純水由MILLI-Q純水儀制備。
2 實驗方法
2.1 一維液相色譜條件
色譜柱:Symmetry-C18 (250 mm×4.6 mm,5 μm);流速:1 mL/min;柱溫:30℃;進樣量:20 μL;檢測波長:254 nm;流動相:A為乙腈:甲醇(6:1),B為緩沖液(稱取2.88 g十二烷基硫酸鈉,加磷酸1.36 mL,用水溶解并稀釋至1000 mL);等度洗脫A: B= 57: 43。
2.2 二維液相色譜條件
色譜柱:Agilent Eclipse-C18 (50 mm×2.1 mm,1.8 μm);流速:0.2 mL/min;柱溫:30℃;Loop環積:40 μL;檢測波長:254 nm;流動相A為0.1%甲酸水,流動相B為乙腈;洗脫程序為B相在8 min內由10%上升為90%。
2.3 質譜條件
離子化模式:電噴霧正離子化(ESI+);干燥氣溫度:325℃;霧化氣壓力:35 pai;干燥氣流速:8 L/min;毛細管電壓:3500 V;采集速率:2 Spectrum/Sec;質量范圍:50~1500 m/z。
2.4 樣品溶液的制備
取表柔比星原料藥適量,用甲醇溶解,搖勻,過濾,取濾液,制成濃度為20.52 μg/mL的表柔比星原料藥溶液,并用一維液相色譜條件進行分析。取表柔比星脂質體溶液用甲醇稀釋125倍,過濾,取濾液。空白脂質體用同樣的方法稀釋。取表柔比星脂質體樣品溶液在一維液相色譜條件下進行分析,通過一維液相色譜圖中目標雜質峰的保留時間設置多中心切割程序的切割時間,將目標雜質轉移至二維液相色譜條件下分析。
3 結果與討論
3.1 一維液相色譜分析結果
3.1.1 原料藥與空白脂質體
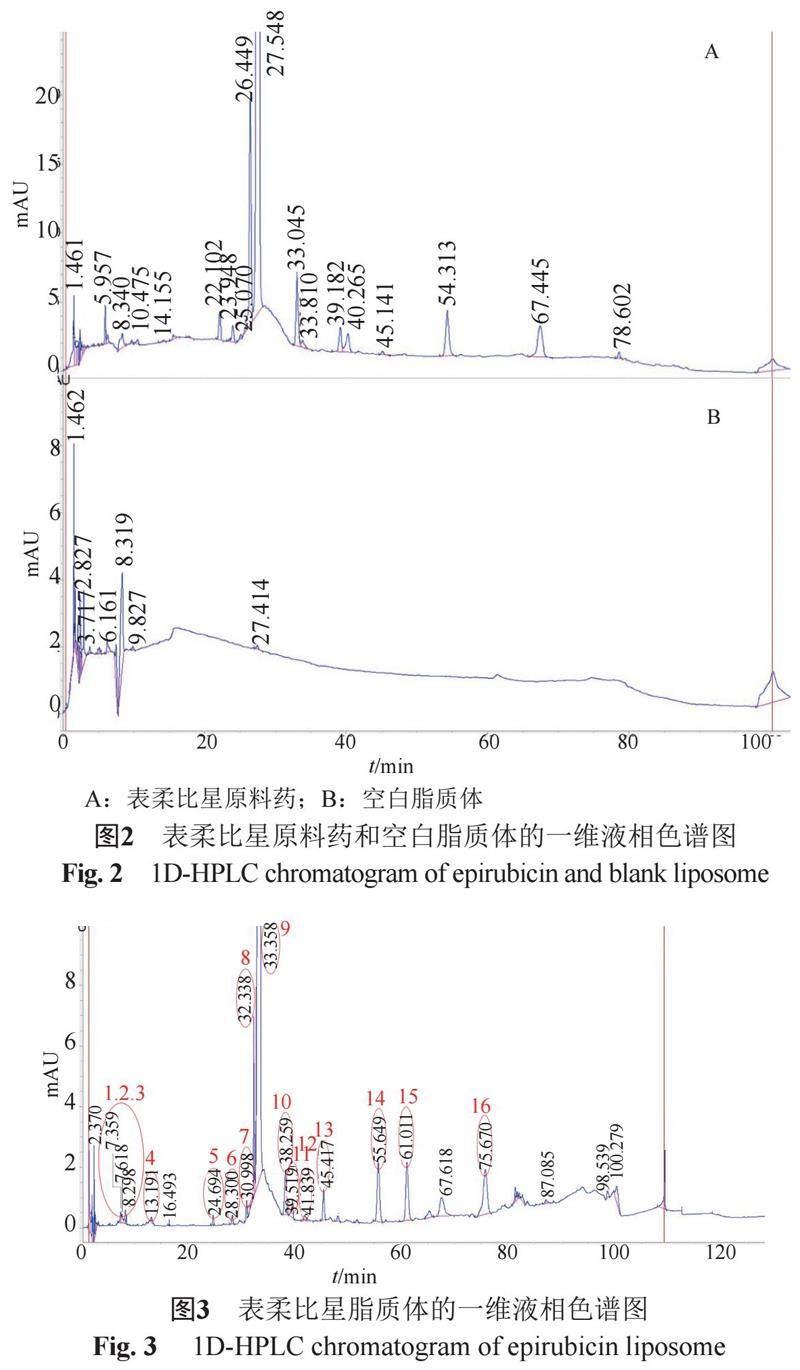
在加入緩沖鹽的液相色譜條件下,表柔比星原料藥的一維液相色譜圖如圖2A,主峰保留時間在27.548 min,并且能與其他雜質峰很好的分離,表明一維液相色譜條件的合理性。在相同的一維液相色譜條件下,分析空白脂質體的一維液相色譜行為。如圖2B所示,空白脂質體在7~8 min有干擾峰出現,可能會對此時間段出峰的雜質的鑒定有所干擾。同時圖中顯示空白脂質體在其他保留時間的區域無明顯干擾。
3.1.2 表柔比星脂質體
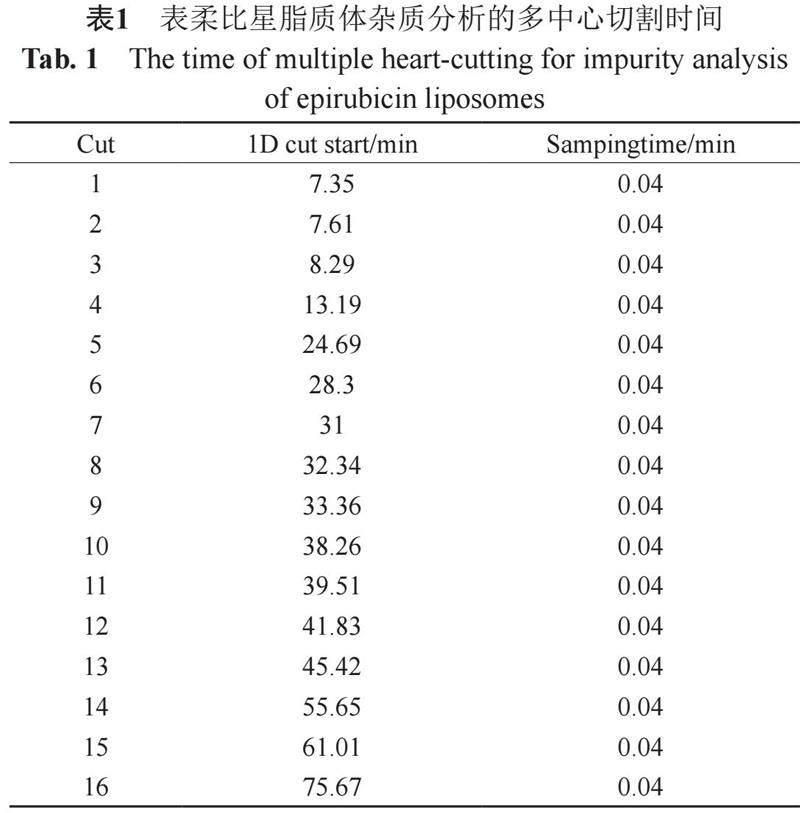
一維液相色譜分析結果可以確定目標雜質峰的保留時間,用于多中心切割模式的切割時間設置。表柔比星脂質體一維色譜圖如圖3,表柔比星主峰保留時間為33.3 min,編號為9。雜質峰分布及保留時間與原料藥中的基本一致,推測表柔比星脂質體制劑中的主要雜質來源于其原料藥,將各目標雜質峰標號為1~8和10~16。將主峰與各雜質峰引入二維體系進行分析的中心切割時間表如表1所示,共采集16個峰切入二維,每個峰采樣時間為0.04 min。
3.2 二維液相色譜與質譜聯用分析結果
在一維液相色譜條件下,表柔比星的主峰與雜質可以實現基本的分離,將主峰和各目標雜質峰切換到液相色譜條件可以直接與MS連接進行鑒定的二維中進一步分離,可以實現共流出物高效分離的同時進行質譜鑒定分析。
3.2.1 表柔比星主峰9的定性分析
將主峰9采集至二維液相色譜中進行分析(圖4A),保留時間為4.9 min,分子離子峰m/z為544.1808,通過MFG分子式計算功能綜合考慮精確質量數、同位素分布、價態、加鹽峰、碎片信息,在限定元素組成和得分的條件下,得出分子式為C27H29NO11,質量偏差-1.3 ppm(0.6 mDa),得分95.67,同時對比同位素峰測量與理論豐度,可以確定編號為9的峰是表柔比星主峰(圖4B)。
3.2.2 雜質7的定性分析
雜質7在一維液相色譜中的保留時間為31 min,切割到二維的保留時間為4.31 min(圖5)。通過EIC確認質譜對應離子為m/z 544.1829和m/z 397.0923(推 測為源內裂解),且與空白脂質體相比為表柔比星脂質體樣品特有(圖6)。計算雜質7的分子式為C27H29NO11,質量偏差-2.86 ppm(-1.6 mDa),推測雜質7為圖1中的雜質C阿霉素(圖7)。
3.2.3 雜質8的定性分析
雜質8在一維液相的保留時間為32.34 min,切閥后在4.34 min有254 nm的紫外吸收峰(圖8),EIC確認質譜對應離子為m/z 530.1663和m/z 383.0772(推測為源內裂解)(圖9)。與空白脂質體樣品比較,為表柔比星脂質體樣品特有峰。通過精確質量計算分子式為C26H27NO11,比主成分少-CH2,質量偏差1.48 ppm (-0.6 mDa),得分97.59。通過源內裂解脫去一分子氨基糖來推測雜質8可能是在主成分的基礎上丟失-CH2形成的,可能的結構如圖所示(圖10)。
3.2.4 雜質10的定性分析
雜質10在一維液相的保留時間為38.26 min,在切閥后5.88 min有254 nm的紫外吸收峰(圖11),EIC對應離子為m/z 337.0700,與空白脂質體相比確認為表柔比星脂質體樣品特有峰(圖12)。精確質量計算雜質分子式為C19H12O6,質量偏差2 ppm(0.7 mDa),可能的結構如圖所示(圖13)。
3.2.5 雜質13的定性分析
雜質13在一維液相的保留時間為45.42 min,切閥后在二維色譜圖上對應4.40 min的吸收峰(圖14),EIC確認質譜對應離子為m/z 542.1650。與空白脂質體樣品比較,為表柔比星脂質體樣品特有峰。通過精確質量計算分子式為C27H27NO11,比主成分少2個H,質量偏差-1.39 ppm,可能的結構如圖所示(圖15)。
3.2.6 雜質14的鑒定
雜質14在一維液相色譜中的保留時間為55.65 min,切閥后4.78 min有紫外吸收峰(圖16),質譜對應離子為m/z 1083.3228(圖17),與空白脂質體相比,確認為表柔比星脂質體樣品特有峰。通過精確質量計算雜質分子式為C54H54N2O22,質量偏差0.17 ppm,與雜質G相比少4H,可能的結構如圖所示(圖18)。
3.2.7 雜質15的鑒定
雜質15在一維液相色譜中的保留時間為61.01 min,在切閥后6.06 min有254 nm的紫外吸收峰(圖19),質譜對應離子m/z 1047.3030及二價信號m/z 524.1539,EIC確認化合物為樣品特有峰(圖20)。精確質量計算雜質分子式為C54H50N2O20,質量偏差0.83 ppm,與雜質G相比少H8O2,可能的結構如圖(圖21)。
3.2.8 其他雜質的分析
樣品中雜質1~3在一維液相中的保留時間分別為7.35、7.61和8.29 min。在二維液相色譜圖中均可提取到C21H18O9(雜質A)的[M+H]+,但因為含量太低,質譜干擾嚴重,無法進一步確認。推測可能由于空白脂質體的液相色譜行為在這段時間的干擾較強,導致無法分析。
雜質4和雜質12的一維液相保留時間分別為13.19 和41.83 min,由于一維液相色譜峰太低無法進行進一步分析。雜質5、11和16,一維液相保留時間分別為24.69、39.51和75.67 min,在切割到二維液相色譜中后因背景太高無法確認。
雜質6通過精確質量計算的分子式為C27H29NO11,質量偏差-2.89 ppm,推測是雜質7的異構體,但因為含量很低難以進一步確認。
4 結論
本文采用多中心切割模式的2D-HPLC-QTOF法分離表柔比星脂質體中的雜質,使用MFG分子式計算功能對未知雜質進行結構推測。本文分離出的雜質7和雜質10為常見同分異構體雜質和碎片雜質,雜質8和雜質13與主成分相比分別丟失-CH2和2H,雜質14和15是在表柔比星二聚體的基礎上丟失4H和H8O2,推斷部分雜質可能來源于原料藥。由于各雜質峰的二級質譜信號較低未能準確獲得因此無法確定各雜質峰手性中心的絕對構型,未來可針對各雜質進行立體結構的分析。本文所采用的多中心切割模式與普通中心切割模式相比,可以對每個一維目標峰進行中心切割,并且較高頻率的采樣可以對高度復雜的共流出物峰進行詳細分析。將二維液相色譜分離技術與QTOF質譜聯用,是分離鑒定未知雜質的有力手段。通過此方法共檢測出表柔比星脂質體溶液中6個雜質成分并推測出其平面結構,為表柔比星脂質體中雜質的分離鑒定提供了重要參考。
參 考 文 獻
Kumar D, Tomar R S, Deolia S K, et al. Isolation and characterization of degradation impurities in epirubicin hydrochloride injection[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2008, 869(1-2): 45-53.
Conte P F, Gennari A, Landucci E, et al. Role of epirubicin in advanced breast cancer[J]. Clin Breast Cancer, 2000, 1 (Suppl 1): S46-S51.
鄭彩微, 帥茨霞, 占麗飛, 等. 表阿霉素和順鉑介入治療晚期卵巢癌[J]. 溫州醫學院學報, 2000, 30(2): 117-118.
Song X L, Ju R J, Xiao Y, et al. Application of multifunctional targeting epirubicin liposomes in the treatment of non-small-cell lung cancer[J]. Int J Nanomedicine, 2017, 12: 7433-7451.
Launchbury A P, Habboubi N. Epirubicin and doxorubicin: a comparison of their characteristics, therapeutic activity and toxicity[J]. Cancer Treat Rev, 1993, 19(3): 197-228.
王燕. 新型脂質體作為中藥靶向載體在腫瘤治療中的作用[J]. 中國實驗方劑學雜志, 2010, 16(16): 212-215.
國家藥典委員會. 中國藥典2020年版二部[S]. 2020: 1191.
The United States Pharmacopoeia 43th Edition[S]. Rockville MD: The United States Pharmacopoeia Convention, 2020: 1653.
The European Pharmacopoeia 10.0[S]. Strasbourg: European Directorate for the Quality of Medicine & Health Care, 2020: 2514.
邵伍軍, 和燕玲, 金美春, 等. 2D-HPLC-QTOF法對注射用鹽酸表柔比星中二聚體的鑒定[J]. 中國抗生素雜志,? 2019, 44(2): 237-240.
基金項目:江西省創新人才團隊(No. 20165BCB19009);南昌市高層次科技創新人才“雙百計劃”;江西中醫藥大學校級科技創新團隊發展計劃;國家科技重大專項(No. 2017ZX09210004004)
作者簡介:計小凡,女,生于1998年,在讀碩士研究生,主要從事藥物分析和中藥藥效物質及其代謝研究,E-mail: 2804799585@qq.com

