早期經頸靜脈肝內門體分流術臨床應用及研究進展
王澤 黃金濤 仲斌演 沈健 朱曉黎
摘要:
經頸靜脈肝內門體分流術(TIPS)是經頸靜脈途徑在肝靜脈與門靜脈之間穿刺建立門體分流通道以此來降低門靜脈壓力,從而控制急性食管胃靜脈曲張出血(EGVB)。EGVB的預后在過去幾十年有了顯著的改善,目前內鏡下套扎聯合藥物治療被推薦為一線治療方案。過去十年EGVB管理的最新進展和研究聚焦在相對較新的“early”或“pre-emptive”TIPS概念,即在標準治療失敗風險較高的EGVB患者中,推薦早期TIPS(入院72 h內,理想情況下24 h內)治療。本文簡要介紹早期TIPS對控制出血、病死率以及肝性腦病的影響,早期TIPS適用的高危人群、干預的時機及成本效益,早期TIPS在真實世界中的應用以及國際指南和共識對早期TIPS的推薦。
關鍵詞:門體分流術, 經頸靜脈肝內; 食管和胃靜脈曲張; 出血
基金項目:
江蘇省社會發展面上項目(BE20221648); 蘇州市民生科技項目(SS202059)
Clinical application of early transjugular intrahepatic portosystemic shunt and related and research advances
WANG Ze, HUANG Jintao, ZHONG Binyan, SHEN Jian, ZHU Xiaoli. (Department of Interventional Radiology, The First Affiliated Hospital of Soochow University, Suzhou, Jiangsu 215000, China)
Corresponding author:
ZHU Xiaoli,zhuxiaoli90@163.com (ORCID:0000-0002-3507-2018)
Abstract:
Transjugular intrahepatic portosystemic shunt (TIPS) is a procedure to establish a portosystemic shunt between the hepatic vein and the portal vein via the jugular approach, so as to reduce portal venous pressure and control acute esophagogastric variceal bleeding (EGVB). The prognosis of EGVB has been improved significantly over the past few decades, and endoscopic variceal ligation combined with drug therapy is now recommended as the first-line treatment regimen for this disease. The latest research advances in the management of EGVB over the past decade have focused on the relatively new concept of “early” or “pre-emptive” TIPS, that is to say, early TIPS (within 72 hours after admission, ideally within 24 hours) is recommended for patients with EGVB who are at a relatively high risk of failure in standard treatment. This article briefly introduces the effect of early TIPS on controlling bleeding, mortality rate, and hepatic encephalopathy, the high-risk population for early TIPS, timing of intervention, cost effectiveness, the applications of early TIPS in a real-world setting, and recommendations for early TIPS in international guidelines and consensus statements.
Key words:
Portasystemic Shunt,? Transjugular Intrahepatic;?? Esophageal and Gastric Varices;?????? Hemorrhage
Research funding:
The Social Development General Program of Jiangsu Province (BE20221648); The Peoples livelihood Technology Program of Suzhou(SS202059)
門靜脈高壓定義為門靜脈與下腔靜脈之間的門靜脈壓力梯度(hepatic venous pressure gradient, HVPG)病理性升高,在肝硬化引起門靜脈高壓的情況下HVPG升高至正常限值(5 mmHg)以上。門靜脈高壓是肝硬化嚴重并發癥發生的基礎,如急性食管胃靜脈曲張出血(esophagogastric variceal bleeding, EGVB)、頑固性腹水、肝性腦病(HE)、門靜脈血栓等并發癥。EGVB占肝硬化所有上消化道出血的70%[1],已經被確認為肝硬化患者的常見死亡原因之一,6周病死率約為20%[2]。EGVB的預后在過去的幾十年得到顯著改善,目前內鏡下套扎術聯合藥物治療的標準化治療方案被推薦為EGVB的一線療法[3-5],然而高達10%~20%的患者對目前的標準治療沒有應答而導致持續性或復發性出血[5]。因此,此類接受標準治療方案失敗可能性較高的患者是目前臨床研究的重點對象,而經頸靜脈肝內門體分流術(TIPS)能夠使這部分高風險患者獲益。
TIPS是在影像設備導引下,經頸靜脈途徑在肝靜脈與門靜脈之間穿刺建立門體分流通道,使得一部分門靜脈血直接回流到下腔靜脈以此來降低門靜脈壓力,從而控制EGVB。TIPS手術最早是在20世紀60年代經頸靜脈肝內膽道造影術過程中發現的[6-7],1988年首例人體TIPS金屬支架置入獲得了成功[8]。隨著支架材料的發展和TIPS技術的改進,在21世紀初金屬裸支架轉變為聚四氟乙烯(polytetrafluoroethylene, PTFE)覆膜支架后支架通暢性得到顯著改善[9]。有研究報道采用Viatorr支架行TIPS術,結果顯示術后支架再狹窄率和HE發生率低,對肝功能影響小,療效確切。新一代可控擴張PTFE覆膜支架Viatorr CX支架的特點是通過支架內襯區域外部約束球囊可膨脹套控制擴張,使得球囊可在8~10 mm標記范圍內調節支架直徑,并保持選定直徑。TIPS從根源上降低門靜脈壓力,通過壓力下降和曲張靜脈栓塞來控制EGVB, 降低患者的再出血率、延長生存期,從而使患者生存獲益。
過去十年EGVB治療的最新進展和研究聚焦在相對新興的“early”或“pre-emptive”TIPS概念,即在接受標準治療后再出血風險較高的EGVB患者中,推薦早期TIPS(72 h內,理想情況下24 h)治療[3-4,10]。自從2004年“早期”TIPS這個概念提出以來[11],對于早期TIPS的療效始終存在爭議,幾項研究[11-13]試圖解決這一問題,證實了早期TIPS可以降低患者再出血的風險、延長患者的生存期,從而使此類患者生存獲益。但是,早期TIPS在臨床應用中的實際生存獲益仍存在不確定性,因此這一概念尚未被普遍采用,國際指南的推薦也各不相同。
本文簡要介紹早期TIPS的概念,早期TIPS對再出血、病死率以及HE的影響,早期TIPS適用的高危人群及成本效益,早期TIPS在真實世界中的臨床應用以及國際指南和共識對早期TIPS的推薦。
1 早期TIPS的概念
EGVB是門靜脈高壓最常見的并發癥之一,盡管藥物治療已經取得了相應進展, 但是仍有危及生命的風險[14]。研究[15]顯示接受血管活性藥物、內鏡治療以及預防抗生素治療后,仍有10%~15%的EGVB患者會發生持續性出血或早期再出血。在這些輕至中度再出血患者中,可以嘗試接受第二次內鏡套扎治療;對于持續或嚴重再出血的患者,挽救性TIPS則是首選療法[3-5,16]。然而研究表明盡管挽救性TIPS可以顯著降低再出血率[17-18],但病死率(30%~50%)仍然較高[19-21]。
挽救性TIPS治療后的高病死率提示一個問題:入院時預后較差的患者是否可以更快、更直接地從更積極的TIPS治療中獲益,因此早期TIPS的理念產生。早期TIPS即指接受標準治療(內鏡治療+藥物治療)后存在治療失敗高危風險的患者在入院72 h內(最佳是24 h)行TIPS治療。早期TIPS的合理性在于通過早期更為積極的治療措施預防治療失敗的患者再出血發生,并進一步使門靜脈高壓的發生率降低,從而降低患者的病死率。
因此,早期TIPS治療迫切需要確定接受標準治療后存在治療失敗風險較高的患者相對應的篩選標準,并“早期”干預以降低治療失敗率和再出血率,從而降低病死率。研究[22-23]顯示HVPG≥20 mmHg的患者發生無法控制EGVB或出現早期再出血的可能性是HVPG<20 mmHg患者的5倍,并且有更高的病死率。
Monescillo等[11]最先在一項多中心隨機對照試驗(RCT)中發表了關于早期TIPS的結果,該研究中HVPG≥20 mmHg被定義為高危患者并按照1∶1隨機分入早期TIPS組或傳統治療組,早期TIPS組患者從入院到TIPS手術的時間為(22.5±20.4)h。研究表明:與傳統治療比較,在選定的高危患者組中早期TIPS具有明確生存優勢的同時降低了治療失敗率。然而,盡管該研究證實了早期TIPS組有較好的1年生存率并降低了治療失敗率,但是這并沒有轉化為早期TIPS使用率的增加,因為非早期TIPS組中的患者在當時接受的是內鏡硬化療法而不是目前的標準治療方案(內鏡套扎療法+藥物治療)[24]。此外,本研究中早期TIPS組患者使用的裸金屬支架在此后的臨床實踐中已被更好的覆膜支架替代。
2010年,Garcia-Pagan等[12]將早期TIPS與目前標準治療(內鏡套扎+藥物治療)進行了比較,同時提出了一種更簡單、更具臨床意義的方法來鑒別高危患者:Child-Pugh評分和內鏡檢查[高危定義為肝硬化Child-Pugh C級(≤13分)或Child-Pugh B級伴活動性出血]。研究結果顯示早期TIPS組患者治療失敗和再出血率較標準治療組顯著降低,最終結果表現出明顯的生存優勢:早期TIPS組僅3%患者達到治療失敗或再出血的終點,而標準治療組為45%;早期TIPS組的1年生存率為86%,而標準治療組為61%(P<0.001)。 這個里程碑的研究是一個重大轉折點,早期TIPS在臨床實踐中的應用受到廣泛關注。此后,Thabut等[25]、Njei等[26]以及Lv等[13]分別總結了法國、美國以及中國關于早期TIPS的研究結果:高危標準治療失敗的肝硬化伴EGVB患者實施早期TIPS治療可以顯著改善患者預后。
關于早期TIPS的時間,在既往研究中該手術通常在出血后3天內進行,但在出血后5天內進行時也有研究[27]證實可以獲得同樣的效果。考慮到早期TIPS的作用主要是降低早期再出血率[13],因此建議在EGVB后應盡早行TIPS干預。歐洲的Baveno Ⅶ共識[3]、美國肝病學會[5]及我國的TIPS實踐指南[28]推薦:對于存在高危因素的患者應在72 h(最好24 h內)行TIPS治療。
2 早期TIPS獲益的人群
晚期肝硬化患者不僅門靜脈壓力升高,而且肝臟儲備能力也較差。因此,針對接受標準治療后再出血和治療失敗風險較高患者的標準化篩選對接受早期TIPS治療后是否獲益至關重要。Monescillo等[11]將HVPG≥20 mmHg定義為EGVB患者的高風險組,與HVPG<20 mmHg的患者(低危組)相比,高風險組患者治療失敗(50% vs 12%, P=0.000 1)、輸血需求(血單位:3.7±2.7 vs 2.2±2.3, P=0.002)、需要重癥監護(16% vs 3%, P<0.05)更多,生存率也更差。
在此背景下對其他已成熟的預后工具如Child-Pugh評分和終末期肝病模型(MELD)評分進行了相關研究。研究[29]顯示Child-Pugh A級患者的存活率為96%~100%,而Child-Pugh評分>13分的患者病死率很高。最近,MELD評分≥19分也被證明是預后不良的標志[12]。這些預后工具均被隨后的早期TIPS研究用于篩選高風險患者。
Conejo等[30]對接受標準治療的EGVB患者進行了一項大型回顧性研究。該研究通過三種不同的風險分層標準來比較病死率:早期TIPS標準[Child-Pugh C級(≤13分)或Child-Pugh B級伴活動性出血定義為高危];MELD評分標準(MELD評分≥19分表示高危)和Child C-C1標準(低風險定義為Child-Pugh A級或B級,或Child-Pugh C級伴肌酐<1 mg/dL,高風險為Child-Pugh C級伴肌酐≥1 mg/dL)。在915例患者中,523例被確認為理論上符合早期TIPS治療的條件,該組6周總體病死率為17%,研究者使用上述三個分層標準對死亡風險進行了分類。根據早期TIPS分類標準:高風險患者中約28.3%死亡,低風險的患者中僅7.0%死亡。然而,Child-Pugh B級患者的病死率(11.7%)顯著低于Child-Pugh C級患者(35.6%)(P=0.001)。此外,有或無活動性出血的Child-Pugh B級患者的病死率相似。MELD評分標準在區分病死率方面也表現良好,46.0%的高風險患者(MELD評分≥19分)死亡,8.1%的低風險患者(MELD評分<19分)死亡。同樣,Child-Pugh評分為高風險的患者病死率為51.9%,而低風險患者的病死率為10.9%。總體而言,Child-Pugh A級肝硬化或MELD評分≤11分的患者病死率低(2%~4%),Child-Pugh B級或MELD評分為12~18分的患者病死率中等(10%~12%),Child-Pugh C級或MELD 評分≥19分的患者病死率高(22%~46%)。三種評分系統在評估EGVB標準治療后死亡風險方面均表現良好,因此適合用來篩選能夠從早期TIPS獲益的患者。
在另一項多中心非隨機觀察性研究[31]中,研究者使用Child-Pugh評分、MELD評分、Child C-C1評分和早期TIPS標準比較了早期TIPS在不同風險類別中的生存優勢。根據每個分類標準將人群分為低風險組、中等風險組和高風險組。盡管整個隊列均顯示出在降低再出血率、提高生存期方面的優勢,但是早期TIPS的有益作用大多限于高風險患者,可能與這些患者會因為反復出血和隨后發生的多器官功能衰竭而死亡的風險最大有關。研究首次顯示:與標準治療組相比,MELD評分>19分與早期TIPS組的病死率降低密切相關。這與既往研究[32]結果不一致。該研究的另一個發現是早期TIPS與標準治療相比的獲益持續存在,即使因為復發性出血而需要行挽救性TIPS的治療組中也證實了TIPS作為早期干預的作用。該研究的結果也證實內鏡檢查時活動性出血與預后相關,實際上肝硬化患者Child-Pugh B級伴活動性出血代表了從TIPS早期干預獲益的高風險組,與之前的研究相反[12]。
在另一項涉及34家中心的觀察性研究[33]中,從早期TIPS中獲益的高風險患者僅限于Child-Pugh C級患者,而伴有活動性出血的Child-Pugh B級患者病死率低且未能從早期TIPS中獲益。
目前尚不清楚患者疾病嚴重到何種程度時不能考慮行早期TIPS治療,但可以肯定的是Child-Pugh評分≥14分,膽紅素水平≥80 μmol/L慎用[34]。目前歐洲的Baveno Ⅵ共識[3]、美國肝病學會[5]及我國的TIPS實踐指南[34]推薦早期TIPS獲益的人群為:Child-Pugh評分C級(≤13分)或Child-Pugh評分B級伴內鏡證實有活動性出血的肝硬化急性EGVB患者。
3 早期TIPS對再出血及病死率的影響
在早期TIPS的第一項RCT研究[11]中,因急性EGVB入院且HVPG≥20 mmHg的肝硬化患者被定義為治療失敗的高風險組,并隨機分配接受早期TIPS(入院后24 h內)治療或傳統治療。研究結果顯示:與傳統治療相比,早期TIPS顯著降低了治療失敗率和1年病死率。但是,對結果的解釋應考慮當時采用了不同于目前標準治療方案的傳統治療而具有的局限性,以及當時使用的支架是已經被目前PTFE覆膜支架替代的金屬裸支架。另一項歐洲多中心RCT研究[12]分析了早期TIPS(PTFE覆膜支架)治療肝硬化伴有EGVB患者的療效。該研究把Child-Pugh C級(10~13分)或Child-Pugh B級伴入院后初次內鏡檢查為活動性出血的患者定義為治療失敗的高危組,然后隨機分配至早期TIPS組或標準治療組。研究結果顯示:早期TIPS組1年內無治療失敗的比例顯著高于標準治療組(97% vs 50%,P<0.001);1年生存率也顯著更高,早期TIPS組為86%,而標準治療組為61%(P<0.001);兩組治療后HE的發生率無顯著統計學差異。與前面兩項RCT研究不同,最近的RCT研究[13]入組了肝硬化Child-Pugh C級(<14分)或Child-Pugh B級無論內鏡是否伴有活動性出血的患者,并且將生存獲益設定為主要終點。研究結果顯示:與標準治療組相比,早期TIPS 降低了病死率[調整后風險比(aHR)=0.44, 95%CI:0.22~0.88,P=0.02)和治療失敗率(aHR=0.25, 95%CI:0.12~0.54,P<0.000 1);兩組治療后HE的發生率相似(35% vs 36%,P>0.05)。
3項RCT研究均證明:早期TIPS不僅能降低肝硬化伴急性EGVB高危患者的再出血率,還能提高生存率,從而獲得生存獲益,同時早期TIPS組和標準治療組的HE發生率沒有統計學差異。基于這些研究結果,Baveno Ⅶ共識指出對于在初始藥物治療和內鏡治療后治療失敗風險較高的胃靜脈曲張出血患者[Child-Pugh C級(<14分)或Child-Pugh B伴活動性出血]必須考慮在72 h內(最好<24 h)進行早期TIPS治療。然而,一些觀察性研究[4,5,35-37]顯示早期TIPS對高危患者沒有生存獲益,因此美國肝病學會、歐洲肝病學會和韓國肝病學會的指南雖然均推薦早期TIPS, 但提示仍需要進一步研究。
一項薈萃分析[38](包括3項RCT和6項觀察性研究共2 878例患者)顯示: 與接受標準治療的患者相比,早期TIPS組的出血控制失敗(RR=0.15,95%CI:0.07~0.29)和再出血(RR= 0.40,95%CI:0.23~0.71)的發生率顯著降低;早期TIPS組在Child-Pugh B級伴有活動性出血的患者(RR=0.53,95%CI:0.31~0.93)和Child-Pugh C級患者(RR=0.55,95%CI:0.37~0.82)可以觀察到明顯的生存獲益,但在低危患者(Child-Pugh A級和Child-Pugh B 級不伴活動性出血)中未觀察到生存獲益(RR=0.93,95%CI:0.55~1.57)。
最新的一篇薈萃分析[39](納入3項RCT和4項觀察研究共1 327例患者,其中310例患者接受早期TIPS治療,1 017例患者接受標準治療)也支持這個觀點。研究顯示:與藥物聯合內鏡治療相比,早期TIPS顯著增加了肝硬化伴EGVB高風險患者的1年生存期的比例(HR=0.443,95%CI:0.323~0.607,P<0.001)。在Child-Pugh B級伴活動性出血(HR=0.524,95%CI:0.307~0.896,P=0.018))以及Child-Pugh C級(<14分)的患者(HR=0.374,95%CI:0.253~0.553,P<0.001)也分別觀察到了同樣的效應。同時,與藥物聯合內鏡相比,早期TIPS顯著改善了Child-Pugh C級和Child-Pugh B級伴活動性出血患者的出血情況以及腹水情況。
因此,早期TIPS可以顯著降低高危患者人群的再出血率,從而使患者得到生存獲益。
4 早期TIPS對HE的影響
HE是TIPS的常見并發癥,約1/3的患者在TIPS治療后發生HE[40]。因此,在考慮早期TIPS的任何獲益時必須考慮HE的發生風險。目前大多數研究[11,33,37,41]均顯示早期TIPS可顯著改善患者相關的臨床預后,且不會增加患者發生HE的風險。一項薈萃分析(7項研究,2 483例參與者)[38]顯示:早期TIPS組和標準治療組的HE發生率無顯著性差異(RR=1.13,95%CI:0.92~1.38);另一項薈萃分析[39]也顯示相較于標準治療組,早期TIPS沒有增加HE的發生風險。但是,觀察早期TIPS獲益的研究不可避免地會出現選擇偏倚,排除被視為HE高風險的患者(例如既往有發生過HE的患者等)。
值得注意的是,實際接受TIPS的患者所占的比例通常較小,而且這組患者通常都是基于不良預測特征(如年齡、既往HE和敗血癥病史等)嚴格排除標準后選擇的,所以該亞組患者與對照組相比發生HE的風險本質上更低[26,37]。同時,在大多數研究中,包括使用乳果糖和/或利福昔明在內的患者基線特征也沒有明確說明。此外,盡管顯性HE在大多數研究是有明確定義的,但是由于多數隱匿性HE表現出的癥狀是輕微且主觀的,所以很容易被漏掉。
因此對于早期TIPS在真實世界是否會增加HE發生率,還需要更多、更嚴謹的研究來進一步證實。
5 TIPS干預的時機
國際指南目前建議在經過篩選的“高風險”患者中使用早期TIPS進行治療。雖然這些指南針對“高風險”具有不同的定義[例如:Child-Pugh C級(<14分)[3-4,10,42-43]或Child-Pugh B級伴活動性出血[3,10,42],或MELD評分>19分[43]],但一致建議在內鏡檢查后72 h內行早期TIPS治療。早期TIPS已被證實可以改善再出血率,但其對生存率的影響仍不確定。
既往研究[44]顯示,食管胃靜脈曲張再出血的最常發生時間是在首次出血發生后的48~72 h。因此,在一項RCT[45]中,首先選擇了從內鏡檢查到行TIPS治療間隔72 h作為時間界點,研究早期TIPS與EGVB標準治療的影響。然而,最新有關于早期TIPS的RCT研究[12]顯示,35%的隨機接受早期TIPS的患者需要等待超過72 h行TIPS,盡管其生存率沒有受到影響,但提供麻醉和介入放射學支持被視為重大困難。
在最近的一項大型觀察性研究[46]中,只有6.7%的高風險患者在72 h內接受了TIPS治療,另外6.4%在72 h~42天接受了TIPS治療。在另一項類似的大型觀察性研究[33]中,只有9.8%的高風險患者接受了常規TIPS治療。據統計,其中9個中心的TIPS手術在真實世界中的可行性不一致。此類研究表明了在相對較短的72 h的時間窗內提供TIPS手術治療方案在真實世界中實踐的困難性。
一項英國多中心的隊列研究[47]早期TIPS的干預時機對患者預后的影響,研究結果表明:共83例患者接受72 h內早期TIPS治療,88例患者接受72 h后的早期TIPS治療。基線特征相似,不需要進行傾向匹配分析。72 h內和72 h后的早期TIPS組患者結局無差異。1年非移植生存率(69.9% vs 71.6%,P=0.73,HR=0.91,95%CI:0.52~1.58),長期生存期(P=0.52,HR=1.132,95%CI:0.77~1.65),食管胃靜脈曲張再出血(4.82% vs 11.36%,P=0.09,HR=0.411,95%CI:0.14~1.17),HE(43.93% vs 34.61%,P=0.26)和新發或惡化的腹水(16.6% vs 13.46%,P=0.79)均無顯著差異。但與72 h后早期TIPS相比,72 h內早期TIPS患者因肝衰竭導致的死亡明顯更為普遍(44% vs 16%,P=0.046,HR=2.79,95%CI:1.02~8.32)。總之,在72 h內行TIPS治療相較于在72 h~28天內接受TIPS治療并沒有益處。然而,72 h內的早期TIPS與1年內肝臟相關病死率的增加相關。本項研究中,雖然基線特征相似,但是研究者摒棄了患者的一般生命體征及休克指數等數據。在真實世界中,于72 h內行早期TIPS的患者可能更加危重,72 h~28天內行早期TIPS的患者一般情況或許更加平穩。因此有關于早期TIPS干預時機所導致的預后差異有待進一步研究。
6 早期TIPS的成本效益
既往研究[48]表明:與內鏡治療相比,TIPS治療的胃靜脈曲張再出血率較低,且對于預防食管胃靜脈曲張復發出血更具有成本效益。因此在考慮早期TIPS優于標準治療的潛在益處時,必須考慮其成本影響和經濟可行性。遺憾的是,迄今為止尚未對早期TIPS與標準治療在EGVB中的直接成本進行研究比較,僅在早期TIPS治療與標準治療的成本效益建模方面進行了一些研究比較。
在一項基于英國的經濟模型研究中,Harman等[49]對超過1年隨訪時間的回顧性隊列進行了成本-效果分析。有35%的EGVB患者被確定有資格進行早期TIPS治療,12個月隨訪的實際費用為138 473.50英鎊,假設再出血率為3.2%,那么早期TIPS可為每例患者每年節省534.70英鎊(P<0.000 1)。來自另外一項英國醫療保健國家數據庫的經濟模型研究[34]顯示,與內鏡套扎聯合藥物治療相比,早期TIPS估計可在2年期間為每例患者節省1 655英鎊。盡管一開始早期TIPS的費用比內鏡套扎組高出4 000英鎊以上,但是后續更少的內鏡治療、藥物治療、再出血事件和HE發生率使得所節省下來的費用遠遠超過了這個費用,同時早期TIPS組的病死率也更低。
TIPS手術的另一個潛在預期結局是腹水消退和相關生活質量的改善。EGVB高風險患者更可能并發腹水,因此考慮到對腹水的消退和再出血率降低的綜合作用,早期TIPS的長期利益成為了更有吸引力的選擇。
7 國際指南和共識中的早期TIPS
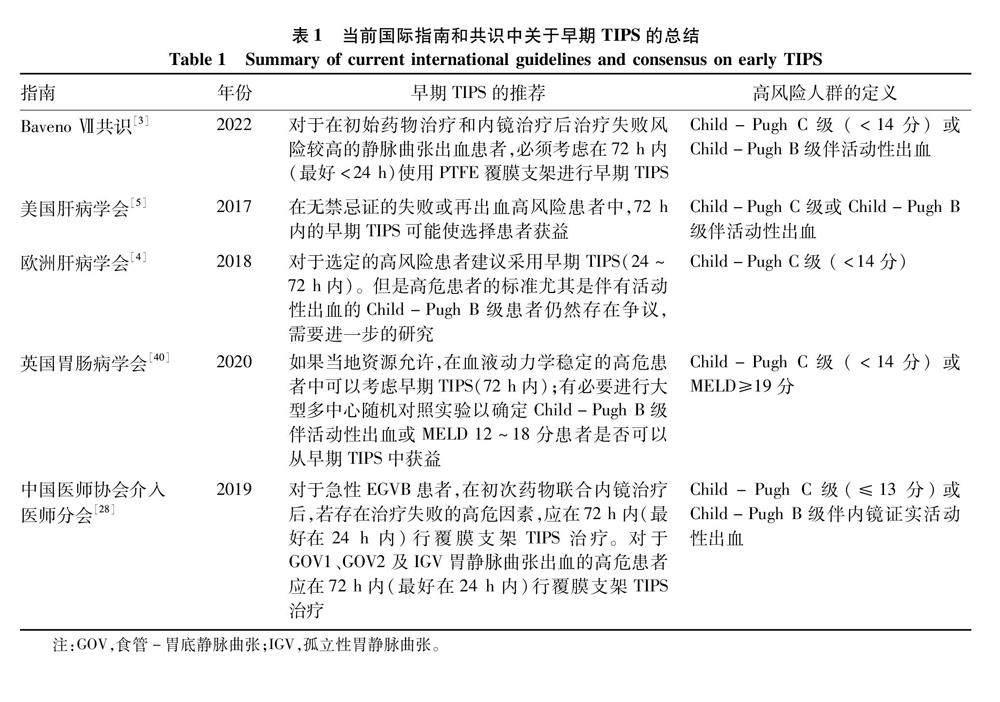
國際指南和共識對早期TIPS的推薦如下(表1)。
國際指南和共識均推薦對于在初始藥物治療和內鏡治療后失敗風險較高的EGVB患者在72 h內(最好<24 h)行早期TIPS,高危人群的定義為:Child-Pugh C級(≤13分)或Child-Pugh B級伴內鏡證實活動性出血。
8 早期TIPS在真實世界中的應用
盡管目前早期TIPS已經成為肝硬化EGVB患者的一種治療選擇,但是早期TIPS可能僅使少數高風險患者能夠獲益[50]。最近歐洲的一項大型多中心研究[33]顯示:雖然有多達671例(31%)患者符合早期TIPS治療的條件,但是最終只有66例(10%)患者實際接受了早期TIPS的治療。這與之前法國的一項對964例患者的研究[25]一致, 在這項研究中326例(35.0%)患者具有接受早期TIPS治療的資格,但是在真實世界里僅有22例(6.7%)患者最終接受了早期TIPS治療。
愿意接受早期TIPS治療的患者數量較少的主要原因可能是早期TIPS這項技術的可行性較低以及早期TIPS的有效獲益尚未處到廣泛認同。此外,臨床醫生的另一個共同顧慮是TIPS術后HE發生或者復發的潛在風險很高[51]。因此,在目前真實世界的臨床實踐中,具有接受早期TIPS資格的患者中最終僅有小部分患者接受了早期TIPS治療,TIPS目前仍然最常用于標準治療失敗后的挽救性治療,而不是作為早期的干預治療。
應該強調的是,選擇作為早期TIPS候選者的關鍵標準應該是患者能否從早期TIPS治療中獲益,而不是采用當前標準治療后是否存在持續性出血或早期再出血的高風險[13,50]。考慮到早期TIPS的潛在的臨床獲益,需要進一步設計更完善的研究來積累足夠的證據以確定早期TIPS候選者的標準,同時標準化手術操作步驟、圍手術期的護理以及患者的隨訪,這將有助于優化目前EGVB患者的治療策略,并使更多醫生相信早期TIPS的有效獲益[52-53]。
9 總結與展望
EGVB是肝硬化門靜脈高壓患者最嚴重、致命性的并發癥之一。早期TIPS在治療EGVB患者中展現了改善預后的優勢,6周和1年治療失敗率和再出血率在統計學上呈顯著性降低[13,26,31,33,36-37],且沒有提高HE的發病率,同時具有更好的成本效益。
早期TIPS的生存優勢已在許多研究中得到了證實,但這不是一個普遍的發現。值得注意的是,肝硬化EGVB患者長期生存結局的影響因素還有很多。首先,基礎肝病的嚴重程度和疾病病因的后續治療(比如抗病毒治療或持續戒酒等),都將對后續疾病的發展和預后產生影響。其次,各中心提供的內鏡治療和后續隨訪方案,以及EGVB患者的一般管理和進入ICU后的專業治療也都可能影響患者預后。最后,由于TIPS是一種高度專業化的干預措施,其可用性僅限于三級醫院,無法及時提供TIPS的治療也可能影響患者預后。值得鼓舞的是歐洲早期TIPS研究[26,33,41]中獲益的結果已在我國的研究[13,31]中得到了證實,這表明在人口統計學和病因學上不同的患者中觀察到了相似的獲益。TIPS是一種高度專業化的手術,因此進一步采用當前標準治療作為對照并以生存獲益作為主要終點的高質量的RCT研究是非常必要的,同時也可解決影響預后的其他因素。
鑒于EGVB患者的高病死率,因此確定存在治療失敗高危風險的患者亞組是至關重要的,正如Baveno Ⅶ共識[3]、中國醫師協會介入醫師分會最新指南[28]所示,需要進一步的研究來定義符合早期TIPS治療的高風險患者。早期TIPS顯著降低了肝硬化門靜脈高壓EGVB伴高危治療失敗因素者的再出血率,提高了生存期,從而使患者獲得生存獲益。隨著專用覆膜支架已經替代傳統的裸支架、構建較小直徑(8 mm)的分流道支架以及直徑可控覆膜支架的發展,極大改善了阻礙TIPS廣泛開展的兩大難點:分流道功能障礙、分流后較高的HE發生率。早期TIPS能否成為一線方案用于這些高危人群的治療,有待于高質量的多中心RCT來進一步驗證;早期TIPS除了對EGVB有積極作用外,還可帶來其他的獲益,如腹水及其相關并發癥的消退,這有待進一步研究探索;同時未來針對早期TIPS在酒精性肝炎、慢加急性肝衰竭患者中的作用、聯合曲張靜脈栓塞術等方面也有待進一步的研究。
利益沖突聲明:本文不存在任何利益沖突。
作者貢獻聲明:王澤負責查閱文獻和撰寫文章;黃金濤、鐘斌演、沈健參與修改文章;朱曉黎負責擬定寫作思路,指導撰寫文章并最后定稿。
參考文獻:
[1]BOSCH J, ABRALDES JG, ALBILLOS A, et al. Portal hypertension: recommendations for evaluation and treatment: consensus document sponsored by the Spanish Association for the Study of the Liver (AEEH) and the Biomedical Research Network Center for Liver and Digestive Diseases(CIBERehd)[J]. Gastroenterol Hepatol, 2012, 35(6): 421-450. DOI: 10.1016/j.gastrohep.2012.02.009.
[2]REVERTER E, TANDON P, AUGUSTIN S, et al. A MELD-based model to determine risk of mortality among patients with acute variceal bleeding[J]. Gastroenterology, 2014, 146(2): 412-419. e3. DOI: 10.1053/j.gastro.2013.10.018.
[3]de FRANCHIS R, BOSCH J, GARCIA-TSAO G, et al. Baveno VII - Renewing consensus in portal hypertension[J]. J Hepatol, 2022, 76(4): 959-974. DOI: 10.1016/j.jhep.2021.12.022.
[4]European Association for the Study of the Liver.EASL Clinical Practice Guidelines for the management of patients with decompensated cirrhosis[J]. J Hepatol, 2018, 69(2): 406-460. DOI: 10.1016/j.jhep.2018.03.024.
[5]GARCIA-TSAO G, ABRALDES JG, BERZIGOTTI A, et al. Portal hypertensive bleeding in cirrhosis: Risk stratification, diagnosis, and management: 2016 practice guidance by the American Association for the study of liver diseases[J]. Hepatology, 2017, 65(1): 310-335. DOI: 10.1002/hep.28906.
[6]ROSCH J, HANAFEE WN, SNOW H. Transjugular portal venography and radiologic portac- aval shunt: an experimental study[J].Radiology, 1969, 92(5): 1112-1114. DOI:10.1148/92.5. 1112.
[7]ROSCH J, HANAFEE W, SNOW H, et al. Transjugular intrahepatic portacaval shunt. An exp erimental work[J].Am J Surg, 1971, 121(5): 588-592. DOI: 10.1016/0002-9610(71)90147-4.
[8]RICHTER GM, NOELDGE G, PALMAZ JC, et al. The transjugular intrahepatic portosystemic stent-shunt (TIPSS): results of a pilot study[J]. Cardiovasc Intervent Radiol, 1990, 13(3): 200-207. DOI: 10.1007/BF02575474.
[9]SAAD WE. The history and future of transjugular intrahepatic portosystemic shunt: food for thought[J]. Semin Intervent Radiol, 2014, 31(3): 258-261. DOI: 10.1055/s-0034-1382794.
[10]TRIPATHI D, STANLEY AJ, HAYES PC, et al. U.K. guidelines on the management of variceal haemorrhage in cirrhotic patients[J]. Gut, 2015, 64(11): 1680-1704. DOI: 10.1136/gut- jnl-2015-309262.
[11]MONESCILLO A, MARTíNEZ-LAGARES F, RUIZ-DEL-ARBOL L, et al. Influence of portal hypertension and its early decompression by TIPS placement on the outcome of variceal bleeding[J]. Hepatology, 2004, 40(4): 793-801. DOI: 10.1002/hep.20386.
[12]GARCIA-PAGAN JC, CACA K, BUREAU C, et al. Early use of TIPS in patients with cirrhosis and variceal bleeding[J]. N Engl J Med, 2010, 362(25): 2370-2379. DOI: 10.1056/NEJMoa- 0910102.
[13]LV Y, YANG Z, LIU L, et al. Early TIPS with covered stents versus standard treatment for acute variceal bleeding in patients with advanced cirrhosis: a randomised controlled trial[J]. Lancet Gastroenterol Hepatol, 2019, 4(8): 587-598. DOI: 10.1016/S2468-1253(19)30090-1.
[14]JAIRATH V, REHAL S, LOGAN R, et al. Acute variceal haemorrhage in the United Kingdom: patient characteristics, management and outcomes in a nationwide audit[J]. Dig Liver Dis, 2014, 46(5): 419-426. DOI: 10.1016/j.dld.2013.12.010.
[15]GARCIA-TSAO G, BOSCH J. Management of varices and variceal hemorrhage in cirrhosis[J]. N Engl J Med, 2010, 362(9): 823-832. DOI: 10.1056/NEJMra0901512.
[16]Italian Association for the Study of the Liver (AISF).Portal hypertension and ascites: patient-and population-centered clinical practice guidelines by the Italian Association for the Study of the Liver (AISF)[J]. Dig Liver Dis, 2021, 53(9): 1089-1104. DOI: 10.1016/j.dld.2021.06.021.
[17]AZOULAY D, CASTAING D, MAJNO P, et al. Salvage transjugular intrahepatic portosystemic shunt for uncontrolled variceal bleeding in patients with decompensated cirrhosis[J]. J Hepatol, 2001, 35(5): 590-597. DOI: 10.1016/s0168-8278(01)00185-4.
[18]BANARES R, CASADO M, RODRIGUEZ-LAIZ JM, et al. Urgent transjugular intrahepatic por- tosystemic shunt for control of acute variceal bleeding[J]. Am J Gastroenterol, 1998, 93(1): 75-79. DOI: 10.1046/j.1365-2125.1998.t01-1-00689.x.
[19]ESCORSELL A, BAARES R,? GARCA-PAGN JC, et al. TIPS versus drug therapy in preventing variceal rebleeding in advanced cirrhosis: a randomized controlled trial[J]. Hepatology, 2002, 35(2): 385-392. DOI: 10.1053/jhep.2002.30418.
[20]BOSCH J. Salvage transjugular intrahepatic portosystemic shunt: is it really life-saving?[J]. J Hepatol, 2001, 35(5): 658-660. DOI: 10.1016/s0168-8278(01)00238-0.
[21]DAMICO G, PAGLIARO L, BOSCH J. The treatment of portal hypertension: a meta-analytic review[J]. Hepatology, 1995, 22(1): 332-354. DOI: 10.1002/hep.1840220145.
[22]MERLI M, NICOLINI G, ANGELONI S, et al. Incidence and natural history of small esophageal varices in cirrhotic patients[J]. J Hepatol, 2003, 38(3): 266-272. DOI: 10.1016/s0168- 8278(02)00420-8.
[23]DAMICO G, MORABITO A, DAMICO M, et al. Clinical states of cirrhosis and competing risks[J]. J Hepatol, 2018, 68(3): 563-576. DOI: 10.1016/j.jhep.2017.10.020.
[24]LAINE L, COOK D. Endoscopic ligation compared with sclerotherapy for treatment of esophageal variceal bleeding. A meta-analysis[J]. Ann Intern Med, 1995, 123(4): 280-287. DOI: 10.7326/0003-4819-123-4-199508150-00007.
[25]THABUT D, PAUWELS A, CARBONELL N, et al. Cirrhotic patients with portal hypertension-related bleeding and an indication for early-TIPS: a large multicentre audit with real-life results[J]. J Hepatol, 2017, 68(1): 73-81. DOI: 10.1016/j.jhep.2017.09.002.
[26]NJEI B, MCCARTY TR, LAINE L. Early transjugular intrahepatic portosystemic shunt in US patients hospitalized with acute esophageal variceal bleeding[J]. J Gastroenterol Hepatol, 2017, 32(4): 852-858. DOI: 10.1111/jgh.13593.
[27]SHADI AL H, TAREK S, BESHER S, et al. Early TIPS versus endoscopic therapy for secondary prophylaxis after management of acute esophageal variceal bleeding in cirrhotic patients: a meta-analysis of randomized controlled trials[J]. J Gastroenterol Hepatol, 2016, 31(9): 1519-1526. DOI: 10.1111/jgh.13303.
[28]The Chinese College of Interventionalists. CCI clinical practice guidelines: Management of TIPS for portal hypertension (2019 edition)[J]. J Clin Hepatol, 2019, 35(12): 2694-2699. DOI: 10.3969/j.issn.1001-5256.2019.12.010.
中國醫師協會介入醫師分會. 中國門靜脈高壓經頸靜脈肝內門體分流術臨床實踐指南(2019年版)[J]. 臨床肝膽病雜志, 2019, 35(12): 2694-2699. DOI: 10.3969/j.issn.1001-5256.2019.12.010.
[29]BAIGES A, MAGAZ M, TURON F, et al. Treatment of acute variceal bleeding in 2021-when to use transjugular intrahepatic portosystemic shunts?[J]. Clin Liver Dis, 2021, 25(2): 345-356. DOI: 10.1016/j.cld.2021.01.001.
[30]CONEJO I, GUARDASCIONE MA, TANDON P, et al. Multicenter external validation of risk stratification criteria for patients with variceal bleeding[J]. Clin Gastroenterol Hepatol, 2018, 16(1): 132-139. e8. DOI: 10.1016/j.cgh.2017.04.042.
[31]LV Y, ZUO L, ZHU X, et al. Identifying optimal candidates for early TIPS among patients with cirrhosis and acute variceal bleeding: a multicentre observational study[J]. Gut, 2019, 68(7): 1297-1310. DOI: 10.1136/gutjnl-2018-317057.
[32]HWANG GL, SZE DY. Survival in cirrhotic patients with high MELD Scores: the TIPping point[J]. Dig Dis Sci, 2017, 62(2): 296-298. DOI: 10.1007/s10620-016-4376-y.
[33]HERNNDEZ-GEA V, PROCOPET B, GIRLDEZ , et al. Preemptive-TIPS improves outcome in high-risk variceal bleeding: an observational study[J]. Hepatology, 2019, 69(1): 282-293. DOI: 10.1002/hep.30182.
[34]MANNING C, ELZUBEIR A, ALAM S. The role of pre-emptive transjugular intrahepatic portosystemic shunt in acute variceal bleeding: a literature review[J]. Ther Adv Chronic Dis, 2021, 12: 2040622321995771. DOI: 10.1177/2040622321995771.
[35]Korean Association for the Study of the Liver. KASL clinical practice guidelines for liver cirrhosis: Varices, hepatic encephalopathy, and related complications[J]. Clin Mol Hepatol, 2020, 26(2): 83-127. DOI: 10.3350/cmh.2019.0010n.
[36]RUDLER M, CLUZEL P, CORVEC TL, et al. Early-TIPSS placement prevents rebleeding in high-risk patients with variceal bleeding, without improving survival[J]. Aliment Pharmacol Ther, 2014, 40(9): 1074-1080. DOI: 10.1111/apt.12934.
[37]GARCIA-PAGN JC, DI PASCOLI M, CACA K, et al. Use of early-TIPS for high-risk variceal bleeding: results of a post-RCT surveillance study[J]. J Hepatol, 2013, 58(1): 45-50. DOI: 10.1016/j.jhep.2012.08.020.
[38]ZHOU GP, JIANG YZ, SUN LY, et al. Early transjugular intrahepatic portosystemic shunt for acute variceal bleeding: a systematic review and meta-analysis[J]. Eur Radiol, 2021, 31(7): 5390-5399. DOI: 10.1007/s00330-020-07525-x.
[39]NICOARA-FARCAU O, HAN G, RUDLER M, et al. Effects of early placement of transjugular portosystemic shunts in patients with high-risk acute variceal bleeding: a Meta analysis of individual patient data[J]. Gastroenterology, 2021, 160(1): 193-205. e10. DOI: 10. 1053/j.gastro.2020.09.026
[40]TRIPATHI D, STANLEY AJ, HAYES PC, et al. Transjugular intrahepatic portosystemic stent shunt in the management of portal hypertension[J]. Gut, 2020, 69(7): 1173-1192. DOI: 10.1136/gutjnl-2019-320221.
[41]DELTENRE P, TREPO E, RUDLER M, et al. Early transjugular intrahepatic portosystemic shunt in cirrhotic patients with acute variceal bleeding: a systematic review and meta analysis of controlled trials[J]. Eur J Gastroenterol Hepatol, 2015, 27(9): e1-e9. DOI: 10.1097/MEG.0000000000000403.
[42]GARCIA-TSAO G, ABRALDES JG, BERZIGOTTI A, et al. Portal hypertensive bleeding in cirrhosis: Risk stratification, diagnosis, and management: 2016 practice guidance by the American Association for the study of liver diseases[J]. Hepatology, 2017, 65(1): 310-335. DOI: 10.1002/hep.28906.
[43]TRIPATHI D, STANLEY AJ, HAYES PC, et al. Transjugular intrahepatic portosystemic stent-shunt in the management of portal hypertension[J]. Gut, 2020, 69(7): 1173-1192. DOI: 10.1136/gutjnl-2019-320221.
[44]de FRANCHIS R, PRIMIGNANI M. Why do varices bleed?[J]. Gastroenterol Clin North Am, 1992, 21(1): 85-101.
[45]GARCA-PAGN JC, CACA K, BUREAU C, et al. Early use of TIPS in patients with cirrhosis and variceal bleeding[J]. N Engl J Med, 2010, 362(25): 2370-2379. DOI: 10.1056/NEJMoa0910102.
[46]THABUT D, PAUWELS A, CARBONELL N, et al. Cirrhotic patients with portal hypertension-related bleeding and an indication for early-TIPS: a large multicentre audit with real-life results[J]. J Hepatol, 2017, 68(1): 73-81. DOI: 10.1016/j.jhep.2017.09.002.
[47]DUNNE P, FINKEL J, KHAN F, et al. Effect of time to pre- emptive transjugular intrahepatic portosystemic shunt on patient outcome, a UK multi- centre cohort study[J]. Aliment Pharmacol Ther, 2023, 57(2): 237-244. DOI: 10.1111/apt.17252.
[48]RUSSO MW, ZACKS SL, SANDLER RS, et al. Cost-effectiveness analysis of transjugular intrahepatic portosystemic shunt (TIPS) versus endoscopic therapy for the prevention of recurrent esophageal variceal bleeding[J]. Hepatology, 2000, 31(2): 358-363. DOI: 10.1002/hep.510310215.
[49]HARMAN DJ, MCCORRY RB, JACOB RP, et al. Economic modelling of early transjugular intrahepatic portosystemic shunt insertion for acute variceal haemorrhage[J]. Eur J Gastroenterol Hepatol, 2013, 25(2): 201-207. DOI: 10.1097/MEG.0b013e32835a4cb0.
[50]RSSLE M. Liver: Early TIPS in patients with cirrhosis and variceal bleeding[J]. Nat Rev Gastroenterol Hepatol, 2010, 7(10): 536-538. DOI: 10.1038/nrgastro.2010.147.
[51]HUNG ML, LEE EW. Role of transjugular intrahepatic portosystemic shunt in the management of portal hypertension: review and update of the literature[J]. Clin Liver Dis, 2019, 23(4): 737-754. DOI: 10.1016/j.cld.2019.07.004.
[52]HAYES PC, MOOKERJEE RP. Early TIPS for portal hypertensive related bleeding: Is resource or education the reason for failure to show clear survival benefit?[J]. J Hepatol, 2017. DOI: 10.1016/j.jhep.2017.11.001. [Online ahead of print]
[53]THABUT D, RUDLER M. Pre-emptive TIPS in high-risk patients with cirrhosis and variceal bleeding: is it finally time for a conclusion?[J]. Lancet Gastroenterol Hepatol, 2019, 4(8): 572-573. DOI: 10.1016/S2468-1253(19)30172-4.
收稿日期:
2022-05-16;錄用日期:2023-06-21
本文編輯:劉曉紅

