雙側海馬解剖、常見病變及發(fā)病機制研究進展
趙瑞清 康國偉 王倩 馮波
濱州醫(yī)學院附屬醫(yī)院神經內科,濱州 256600
海馬是一種易感的可塑性大腦結構,在學習、記憶的處理中起關鍵作用,并與情緒、恐懼、焦慮和壓力的調節(jié)密切相關[1]。人類海馬結構高度復雜,可能受到多種神經系統(tǒng)疾病急性或慢性病理過程的影響,導致單側或雙側海馬病變。研究表明,雙側海馬病變可能導致嚴重持續(xù)性、順行性遺忘[2]。本文綜述海馬的解剖和雙側海馬病變相關神經系統(tǒng)疾病,對臨床相關神經系統(tǒng)疾病的預防、診斷和治療具有十分重要的意義。
海馬的發(fā)現
1587年,Arantius在《De humano foetu Liber》中描述了海馬,觀察到大腦腦室內結構呈卷曲狀態(tài)后,使用術語“海馬體”。此后,其他作者如Winslow強調了海馬與公羊角的相似之處。Garengeot以古埃及神的名字命名海馬為安蒙角。Glogi引入了銀浸漬法以更好地研究海馬細胞結構。1998年,聯邦解剖學命名委員會(FCAT)將其命名為“海馬本體”(hippocampus proper)和/或“Ammon’s角”(CA)[3]。在本文中,術語“海馬”即海馬本體。
海馬的解剖、功能和血供
海馬是位于顳葉內側深處的細長凸起結構,大腦兩側各一個,沿著側腦室下角底部呈弓狀隆起[2]。成年人海馬長4~5 cm,寬約1 cm,在冠狀面上呈C形,與齒狀回(DG)構成S形,縱軸上由頭、體、尾部3部分組成,腦室部分位于側腦室的顳角,室外部分位于海馬旁回和鉤上的顳葉內側表面[4]。
在組織學上,根據細胞形狀及大小,海馬被分為CA1~4四個亞區(qū)。CA1區(qū)是其中最大區(qū)域,此區(qū)域90%神經元為錐體細胞,其余10%為中間神經元,其外側以前下托為界,內側以CA2區(qū)為界,是海馬信息處理的最后輸出地,對時間和空間記憶信息進行最終整合。CA2區(qū)為CA1區(qū)與CA3區(qū)之間的區(qū)域,朝向DG,具有相對致密狹窄的錐體細胞;人類海馬的常規(guī)制備中,CA2區(qū)的邊界很難確定,在社會認知記憶加工中起著重要作用。CA3區(qū)指向DG門部,內側受限于CA2區(qū),含有海馬區(qū)最大的錐體細胞,在情景記憶與聯想記憶中有快速編碼的能力。CA4區(qū)是CA3區(qū)的直接延續(xù),位于DG的凹陷中,目前對CA4區(qū)研究較少,功能尚不明確[5-8]。冠狀切面海馬亞區(qū)與齒狀回見圖1。
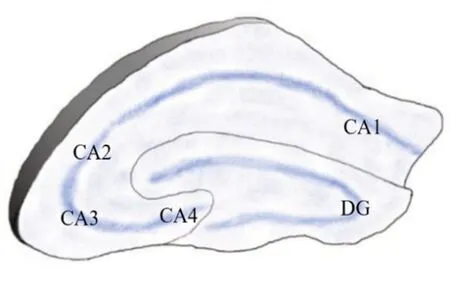
圖1 冠狀切面海馬亞區(qū)與齒狀回示意圖
通常海馬血液供給來自大腦后動脈和脈絡叢前動脈,關于海馬動脈起源及以上兩種動脈對海馬血供的貢獻,尚未形成一致意見。據報道,海馬血供主要來自大腦后動脈時,脈絡叢前動脈的貢獻因人而異。根據海馬動脈的分布區(qū)域命名,主要的供血動脈有3條,其中海馬前動脈供應海馬頭部,海馬中、后動脈分別供應海馬體、尾部。供應海馬的動脈位于腦室腔外,在海馬旁回背側的下丘腦區(qū),海馬動脈與海馬平行產生支動脈進入海馬[9-10]。海馬及其血液供應見圖2。
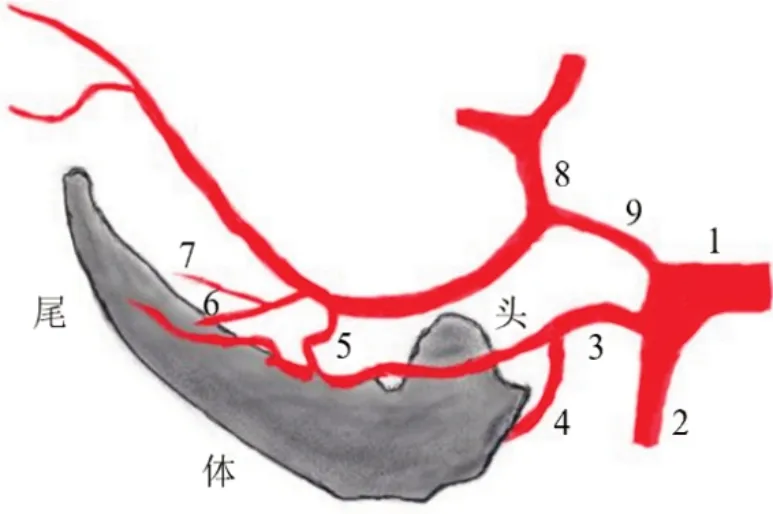
圖2 海馬及其血液供應示意圖
雙側海馬病變與神經系統(tǒng)疾病
1.衰老
衰老是一個不可逆的生物學過程,通常影響整個生物體,尤其大腦的衰老被廣泛研究。海馬隨著年齡的增長而減少,海馬萎縮逐漸導致的認知能力下降會對日常生活產生負面影響[11]。其機制尚不完全清楚,可能與神經元大小、復雜性和連接性減少、神經炎癥激活、神經營養(yǎng)因子及神經發(fā)生減少等相互關聯的機制有關[11-13]。膠質細胞和神經免疫途徑(包括與補體級聯、抗原呈遞及巨噬細胞和小膠質細胞激活相關的信號)在衰老機制中發(fā)揮著重要作用[14]。在衰老大腦中,觀察到巨噬細胞浸潤、小膠質細胞激活以及未能恢復內穩(wěn)態(tài)[11,13],星形膠質細胞失去執(zhí)行其正常功能的能力,釋放有毒因子,促進神經元和少突膠質細胞凋亡[15]。雖然免疫反應早期階段可能具有神經保護作用,但慢性激活可能有害,被認為會引起持續(xù)的神經炎癥,導致大腦中易感區(qū)域特別是海馬的結構性衰退[11,16]。神經元死亡可通過神經再生得到部分補償,然而隨著年齡增長,海馬神經受損[17]。神經營養(yǎng)因子和生長因子(如腦源性神經營養(yǎng)因子、成纖維細胞生長因子、胰島素樣生長因子-1、血管內皮生長因子)是神經發(fā)生的細胞外在調節(jié)因素,由于衰老的星形膠質細胞的局部產生相關因子減少和整體系統(tǒng)水平降低,這些因子及受體水平在衰老過程早期開始下降。此外,年齡引起的小膠質細胞激活和促炎因子對神經發(fā)生有負面影響。海馬也是糖皮質激素(GC)的主要靶點,人類海馬神經元和膠質細胞中均存在高水平的糖皮質激素受體蛋白α(GRα),分布于DG和CA亞區(qū)。海馬神經元GRα隨著衰老減少,而血液GC水平往往增加,產生低代謝、興奮性毒性等作用,可引起神經發(fā)生減少,加速海馬老化,并可在壓力、應激等條件下進一步加重海馬萎縮[18]。
2.缺血性腦卒中(CIS)
CIS是指腦部供血中斷并側支循環(huán)不足,引起腦組織缺血、缺氧,從而導致神經系統(tǒng)癥狀的臨床綜合征[19]。其主要原因有腦血栓形成、腦栓塞和血流動力學等機制[20]。雖然CIS是最常見的神經系統(tǒng)疾病之一,但海馬CIS很少見,尤其是雙側孤立性海馬梗死[21]。目前,孤立性海馬梗死的發(fā)病機制尚不清楚。Kumral等[22]曾報道,雙側孤立性海馬區(qū)梗死可能與心源性栓塞相關。Cole等[23]報道,基底動脈閉塞后雙側海馬灌注量低,盡管早期取栓,雙側海馬仍會發(fā)生梗死,分析原因為海馬對缺血性損傷具有選擇易感性。此外,腦缺血后神經病理現象持續(xù)時間遠遠超過最初的缺血損傷的急性期;在腦缺血后存活1年的動物中,嚴重的海馬萎縮表現為一種活躍的、緩慢進展的神經病理過程,最終導致認知障礙[24]。研究還發(fā)現,腦缺血后在海馬觀察到的神經病理圖像與阿爾茨海默病(AD)的神經退行性病變具有相同特征[25-26]。海馬缺血后神經病理過程緩慢進展,即從最初的缺血性變化和錐體神經元死亡,到β-淀粉樣蛋白(Aβ)和tau蛋白的產生和外滲,從系統(tǒng)循環(huán)中穿過缺血后的血腦屏障進入大腦,這些過程與海馬不敏感區(qū)域的慢性神經元凋亡有關,最終形成淀粉樣斑塊和神經纖維纏結,最后表現出類似于AD的特征[24,27-28]。
3.邊緣葉腦炎(LE)
LE是累及邊緣系統(tǒng)的炎癥性腦病,臨床特征包括急性或亞急性起病的認知障礙,其他癥狀包括精神癥狀、行為改變、癲癇發(fā)作及睡眠障礙等[29]。根據病因不同,可分為感染性LE、自身抗體介導性LE(ALE)和伴有自身免疫性疾病性LE[30]。感染性LE常見于病毒感染,以單純皰疹病毒1型(HSV-1)多見[31]。HSV-1可能通過以下3條途徑進入腦內:三叉神經或嗅神經介導的直接浸潤、中樞神經內潛伏感染再活化、中樞神經外再感染波及。3條途徑病變進展中都累及顳葉、海馬等大腦邊緣系統(tǒng)。HSV-1感染引發(fā)先天性免疫系統(tǒng)強烈反應,炎癥級聯招募先天免疫細胞并引發(fā)適應性免疫,進而導致受感染細胞壞死和凋亡[32]。ALE按其免疫病理學相關聯的抗體分類又可分為抗細胞表面或細胞外抗原的抗體相關LE和抗細胞內抗原的抗體相關LE。細胞表面或細胞外抗原包括N-甲基-D-天冬氨酸受體(NMDAR)、γ-氨基丁酸B受體(GABABR)、α-氨基-3-羥基-5-甲基-4-異惡唑丙酸受體(AMPAR)等受體及電壓門控鉀通道(VGKC)、水通道蛋白4(aquaporin 4,AQP4)等通道,其共同特征為可直接被機體免疫系統(tǒng)成分所接觸,進而產生相應抗體而致病。細胞內抗原,如Hu、Ri、Yo、GAD、Ma2、CV2等,被認為相應抗體無法接觸細胞內表位,神經癥狀可能由CD8+T細胞介導[31]。LE免疫機制包括抗體、補體或T細胞介導的免疫反應,根據自身抗體的不同而有不同程度變化。但也有學者發(fā)現,在符合ALE的臨床和副臨床標準患者血清中未檢測到抗體,然而其腦組織標本顯示出密集淋巴細胞浸潤物,提示自身免疫性腦炎[33]。在一項對ALE患者進行的一系列MRI研究中,最初觀察到內側顳葉(包括海馬)的腫脹,繼而為進行性萎縮,大多數患者持續(xù)存在高信號,這種炎癥后海馬萎縮會導致患者在疾病發(fā)展過程中出現持續(xù)性記憶障礙和神經功能障礙[34]。伴有自身免疫性疾病性LE包括系紅斑狼瘡性腦病、橋本腦病等,也可通過免疫機制導致邊緣系統(tǒng)的損害。
4.AD
AD是一種中樞神經系統(tǒng)退行性疾病,起病隱匿,引起認知功能和行為進行性損害[35]。AD頭顱MRI表現為內側顳葉萎縮,尤其在海馬[36]。在AD病程中,海馬萎縮與衰老、Aβ沉積、過度磷酸化tau蛋白、載脂蛋白E(APOE)4等密切相關。衰老是散發(fā)性AD發(fā)生的主要危險因素,盡管在大腦正常老化過程中海馬顯示出與年齡相關的體積減小,但AD患者海馬萎縮始終比其他區(qū)域明顯且易損傷。因此,海馬萎縮可作為AD病程中最具預測性和敏感性的生物學標志物之一[37]。AD的重要神經病理學特征是Aβ形成的神經炎性斑(NP)在細胞外沉積和過度磷酸化的tau蛋白形成的神經纖維纏結在神經元內逐漸沉積。研究表明,這些病理學改變與海馬萎縮密切相關,可引發(fā)氧化應激、微血管功能障礙和血腦屏障破壞,并且誘導大腦內炎性反應激活,最終導致突觸可塑性受損和神經細胞死亡[38]。此外,APOE的ε4等位基因是散發(fā)型AD的主要遺傳危險因素[39],APOEε4影響海馬萎縮的潛在機制不完全清楚。一項研究發(fā)現,年老的APOEε4小鼠中,可溶性和不可溶性Aβ均增加,該現象與海馬萎縮呈負相關,進而證明APOEε4可通過調節(jié)Aβ的產生和沉積在海馬萎縮中發(fā)揮重要作用[40]。另一項研究表明,APOE也可直接影響tau蛋白的發(fā)病機制、神經炎癥和其介導的神經變性,而不依賴于Aβ的病理[41]。
5.海馬硬化(HS)
HS是耐藥性顳葉癲癇(TLE)最常見的組織病理性改變,它與癲癇反復發(fā)作互為因果[42]。多項回顧性研究顯示,兒童早期腦損傷(熱性癲癇、創(chuàng)傷、缺氧和感染等)可能是初始誘發(fā)性損傷[43],也可能與遺傳易患性或LE相關[9]。部分患者還存在海馬或顳葉外的第2種病變,即“雙重病理”病變,包括皮質畸形、血管畸形和低級別神經膠質細胞腫瘤等。海馬區(qū)外病變產生癲癇發(fā)作或亞臨床發(fā)作活動,導致海馬神經元丟失[42]。HS患者經常有雙側(10%)海馬損傷:一側表現出明顯的HS特征,另一側具有不同程度的損害。雙側HS(BHS)與單側HS相比,表現出明顯的差異,如智力低下、癲癇持續(xù)狀態(tài)和精神錯亂的發(fā)生率增加[44]。HS宏觀上表現為海馬組織逐漸收縮和硬化,微觀上為星形膠質細胞增多和累及CA1、CA3及CA4亞區(qū)的神經元丟失,CA2亞區(qū)通常被保留下來,反映了常見的細胞保護機制[45]。HS其他改變包括DG顆粒細胞層的彌散(此現象似乎是癲癇患者特有)及DG分子層內苔蘚纖維(顆粒細胞軸突)的萌發(fā)。對癲癇持續(xù)發(fā)作后海馬損害的機制的認識主要來自癲癇持續(xù)狀態(tài)的動物模型。這些研究表明,其中一些海馬神經元損害是癲癇持續(xù)狀態(tài)期間發(fā)生的生理損害的繼發(fā)性損害,如缺氧、低血糖和低血壓,但大部分損害與這些因素無關,而是由于興奮性毒性,其中癲癇活動的存在通過激活谷氨酸受體介導神經元死亡,鈣過度內流主要通過NMDA受體,也可通過特定的AMPA受體亞型以及通過代謝性谷氨酸受體的激活,引起一系列級聯反應導致細胞死亡[46]。
6.放射性腦損傷(RBI)
RBI是頭頸部腫瘤患者放療后產生的中樞神經系統(tǒng)損害性疾病[47]。其中放射后顳葉壞死(TLN)是鼻咽癌放療后的后期并發(fā)癥之一[48],病變主要位于顳葉底部,向周圍延伸至側腦室旁,累及海馬等[9]。海馬易受輻射影響,早期即表現為輻射引起的損傷[49],晚期癥狀往往表現為記憶下降、認知障礙[50]。RBI主要病理表現為不同程度凝固性壞死、脫髓鞘改變及膠質增生[9,49]。RBI發(fā)病機制尚不清楚,可能涉及多種機制[49-52],具體如下。⑴血管內皮損傷:放療導致血管內皮細胞損傷、凋亡,導致血腦屏障破壞和血栓形成;此外,內皮細胞損傷釋放大量氧自由基,誘導低氧誘導因子1α和血管內皮生長因子上調,引起血管通透性增加,加劇血腦屏障破壞、血管性水腫、血小板和纖維蛋白血栓形成、血管閉塞和缺血性改變。⑵膠質細胞損傷:放療可直接損傷膠質細胞及其祖細胞,引起相應分子和細胞功能變化,導致血腦屏障破壞,腦水腫、缺氧加重,星形膠質增生和脫髓鞘改變。⑶神經元損傷:放療直接對細胞DNA和RNA造成損害,并通過誘導鈣內流,導致染色體疏松及細胞水腫,刺激神經元凋亡。⑷氧化應激、炎性反應誘發(fā)損傷:中樞神經系統(tǒng)內部和外部產生的氧化應激非常敏感,放療中電離輻射產生大量氧自由基導致組織細胞損傷。同時,放療可通過激活小膠質細胞和內皮細胞釋炎癥因子,形成炎性反應浸潤,導致腦內微環(huán)境改變。中樞神經系統(tǒng)各成分之間構成嚴密。放療通過以上多種機制直接殺傷海馬神經元和間接影響海馬微環(huán)境改變介導損傷。
綜上所述,雙側海馬病變與衰老、AD、CIS、LE、HS、RBI等多種神經系統(tǒng)疾病密切相關,多種機制可直接或間接導致雙側海馬病變。現已有多種抗炎藥物、營養(yǎng)神經藥物及免疫抑制劑等藥物應用于臨床,進一步探究導致雙側海馬病變的病因及潛在機制,為開發(fā)可行新治療靶點提供基礎。目前,對雙側海馬病變發(fā)生及發(fā)展的分子機制研究有限,眾多學者正進行大量持續(xù)性研究,期待相關研究成果能夠改善疾病預后。
作者貢獻聲明趙瑞清:研究實施,論文撰寫,數據采集,統(tǒng)計學分析;康國偉、王倩:數據采集,統(tǒng)計學分析;馮波:研究指導,論文修改,經費支持

