達格列凈通過miR-140-5p/FNDC5通路調控高糖誘導內皮細胞增殖、凋亡的機制研究
徐偉忠 陳愛華
糖尿病血管病變是一種最常見的糖尿病并發癥,慢性血管并發癥常伴有血管內皮功能障礙,這是糖尿病患者致殘、死亡的主要原因[1,2]。達格列凈(dapagliflozin,DAPA)是首個上市的鈉-葡萄糖協同轉運蛋白2(SGLT-2)抑制劑降糖藥物,目前市面上還有卡格列凈、恩格列凈、依格列凈、魯格列凈、托格列凈等SGLT-2抑制劑[3,4]。微小RNA(miRNA)是一種長度在18~25個核苷酸的內源性單鏈內編碼的保守小分子,其通過調控靶基因的轉錄、翻譯過程影響蛋白的表達,進而廣泛參與人類各種疾病的發展[5,6]。miR-140-5p是新發現的一種糖尿病失調miRNA[7],但是其在糖尿病血管病變中的作用及潛在的機制是否與DAPA之間存在關聯尚未可知。本研究擬以高糖誘導的內皮細胞為研究對象,觀察DAPA對其中miR-140-5p、FNDC5的表達及miR-140-5p、FNDC5對內皮細胞增殖、凋亡的影響,揭示DAPA發揮治療作用與miR-140-5p/FNDC5之間的關系。
1 材料與方法
1.1 材料 人臍靜脈血管內皮細胞HUVEC購自美國菌種保藏中心;達格列凈(商品名:安達唐)購自阿斯利康制藥有限公司;Lipofectamin 3000轉染試劑購自賽默飛世爾科技(中國)公司;細胞計數試劑盒(cell counting kit,CCK8)購自日本同仁化學研究所;膜聯蛋白V-異硫氰酸熒光素(annexin v-fluoresceine isothiocyanate,annexin V-FITC)/碘化丙錠(propidium iodide,PI)細胞凋亡檢測試劑盒購自上海碧云天研究所;DNA/RNA抽提試劑盒、實時熒光定量聚合酶鏈反應(real time fluorescence quantitative polymerase chain reaction,RT-qPCR)試劑盒均購自日本Takera;雙熒光素酶報告基因試劑盒購自上海信裕。
1.2 方法
1.2.1 細胞培養:人臍靜脈血管內皮細胞HUVEC用DMEM培養基(混有10%胎牛血清+1%青鏈霉素)培養,在5%CO2的37℃恒溫細胞培養箱中常規培養。隔天更換1次培養液。
1.2.2 細胞轉染與分組:葡萄糖(5.5、30 mmol/L)處理HUVEC細胞6 h分別標記為 正常NG組、高糖HG組。達格列凈DAPA(20、40、80 μmol/L)孵育2 h的HG組細胞分別標記為20 μmol/L組、40 μmol/L組、80 μmol/L組。使用5倍量的Lipofectamin 3000脂質體將agomiRNA組(轉染agomiRNA)、agomiR-140-5p組(轉染agomiR-140-5p)、antagomiRNA組(轉染antagomiRNA)、antagomiR-140-5p組(轉染antagomiR-140-5p)、si-NC組(轉染si-NC)、si-FNDC5組(轉染si-FNDC5)、pcDNA組(轉染pcDNA)、pcDNA-FNDC5組(轉染pcDNA-FNDC5)、80 μmol/L+agomiRNA組(轉染agomiRNA再用80 μmol/L處理)、80 μmol/L+agomiR-140-5p組(轉染agomiR-140-5p再用80 μmol/L的DAPA處理)、80 μmol/L+agomiR-140-5p+pcDNA組(共轉染agomiR-140-5p和pcDNA并用80 μmol/L的DAPA處理)、80 μmol/L+agomiR-140-5p+pcDNA-FNDC5組(共轉染agomiR-140-5p和pcDNA-FNDC5并用80 μmol/L的DAPA處理)轉染至內皮細胞,12 h后,更換新培養液進行HG處理或80 μmol/L的DAPA處理。RT-qPCR實驗檢測細胞的轉染情況。
1.2.3 CCK8實驗檢測細胞增殖:收集細胞,用培養液調整密度0.5×105個/ml,取200 μl分裝置96孔板,培養12 h。取CCK8液10 μl,微微震蕩混勻,避光孵育20 min。酶標儀調至490 nm波長,在此波長下檢測細胞吸光值(OD490)。細胞增殖率(%)=(OD490實驗組/OD490對照組-1)×100%。
1.2.4 流式細胞術檢測細胞凋亡:收集細胞,預冷PBS洗滌5次,500 μl結合緩沖液懸浮細胞。取Annexin V-FITC(10 μl)、PI(10 μl)充分混合,避光孵育15 min,結束后快速上流式細胞儀分析細胞凋亡。細胞總凋亡率=早期凋亡率+晚期凋亡率。
1.2.5 WB實驗檢測細胞FNDC5、Ki67、PCNA、caspase-3的蛋白表達:收集前面處理好的細胞,RIPA裂解液冰上充分裂解,提取總蛋白。BCA法定量,沸水浴變性。SDS-PAGE進行蛋白電泳,按照流程電泳-封閉-轉膜-封閉-Ⅰ抗孵育-Ⅱ抗孵育-顯影曝光操作。最后用Image J軟件分析條帶的灰度,用條帶的相對灰度值表示蛋白的相對表達量。一抗稀釋倍數:兔抗FNDC5多抗,1∶1 500;兔抗Ki67多抗,1∶1 000;兔抗PCNA多抗,1∶1 000;兔抗caspase-3多抗,1∶1 000。二抗稀釋倍數:HRP標記的二抗,1∶500。一抗孵育條件:37℃,搖床孵育3 h,充分洗膜。二抗孵育條件:37℃,2 h。
1.2.6 RT-qPCR試驗檢測細胞miR-140-5p、FNDC5的表達:收集細胞,使用試劑盒提取總RNA并合成cDNA,-20℃保存備用。按照RT-qPCR試劑盒說明書要求操作檢測cDNA中miR-140-5p、FNDC5的水平。U6、GAPDH作為內參,2-ΔΔCt法計算樣本中miR-140-5p、FNDC5的相對表達水平。
1.2.7 雙熒光素酶報告基因試驗檢測細胞熒光活性:使用Targetscan(http://www.targetscan.org/)預測miR-140-5p的下游靶基因,發現FNDC5與miR-140-5p之間存在互補的結合序列。根據預測到的結合位點合成含有結合位點的片段(FNDC5 3′ UTR-WT)和不含結合位點的片段(FNDC5 3′ UTR-MUT),插入熒光載體,構建熒光報告基因載體。將載體與agomiRNA、agomiR-140-5p、antagomiRNA、antagomiR-140-5p轉染至內皮細胞,使用雙熒光素酶報告試劑盒,嚴格按照說明書要求操作檢測細胞的熒光活性。

2 結果
2.1 不同濃度DAPA對高糖誘導的內皮細胞生存的影響 與NG組比較,HG組細胞增殖率顯著降低,凋亡率顯著升高,Ki67、PCNA的蛋白表達均顯著降低,caspase-3的蛋白表達顯著升高(P<0.05)。與HG組比較,40、80 μmol/L組細胞增殖率顯著升高,凋亡率顯著降低,Ki67、PCNA的蛋白表達均顯著升高,caspase-3的蛋白表達顯著降低(P<0.05)。見圖1,表1。

表1 DAPA對高糖誘導內皮細胞增殖、凋亡的影響 n=9,
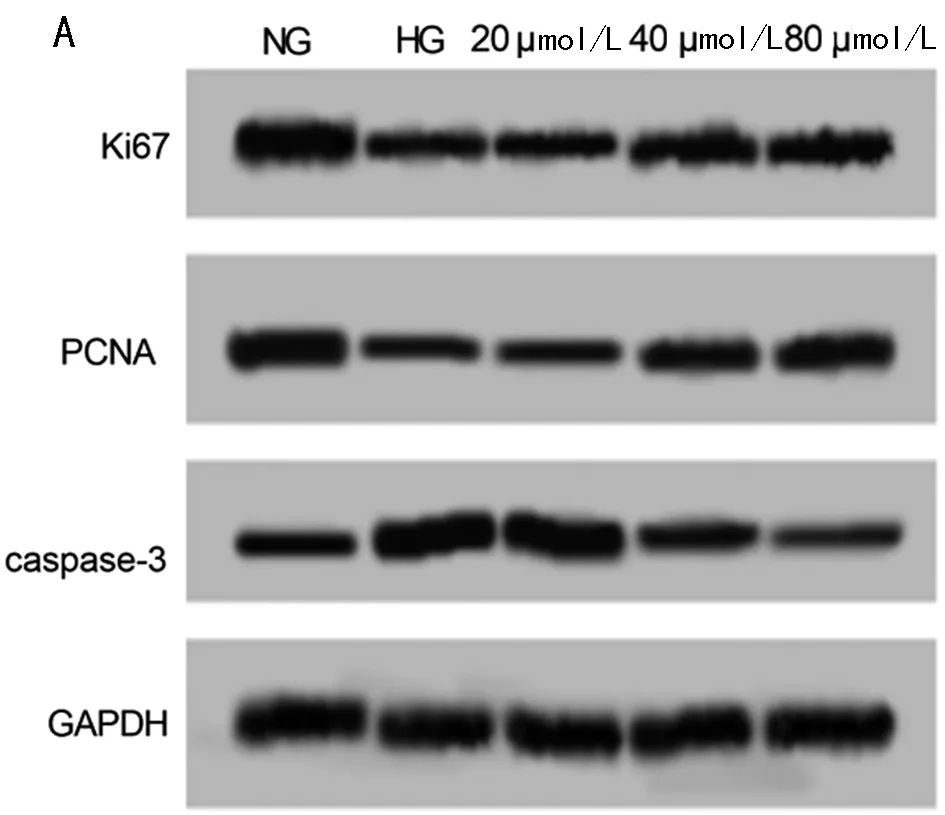
圖1 不同濃度DAPA處理的高糖誘導內皮細胞凋亡及增殖、凋亡相關蛋白表達;A Ki67、PCNA、caspase-3的蛋白圖;B DAPA處理的高糖誘導內皮細胞凋亡圖
2.2 不同濃度DAPA對高糖誘導的內皮細胞中miR-140-5p、FNDC5表達的影響 與NG組比較,HG組細胞miR-140-5p表達顯著升高,FNDC5的mRNA和蛋白表達均顯著降低(P<0.05)。與HG組比較,40、80 μmol/L 組細胞miR-140-5p表達顯著降低,FNDC5的mRNA和蛋白表達均顯著升高(P<0.05)。見圖2,表2。

表2 DAPA對高糖誘導內皮細胞miR-140-5p、FNDC5表達的影響n=9,
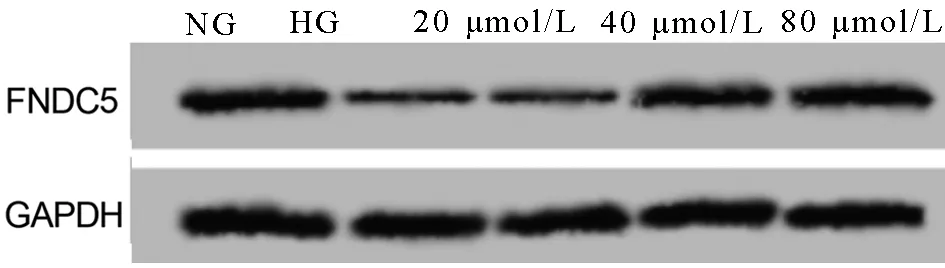
圖2 DAPA處理的高糖誘導內皮細胞FNDC5蛋白圖
2.3 miR-140-5p對高糖誘導的內皮細胞存活的影響 與agomiRNA組比較,agomiR-140-5p組細胞增殖率顯著降低,凋亡率顯著升高,Ki67、PCNA的蛋白表達均顯著降低(P<0.05),caspase-3的蛋白表達顯著升高(P<0.05)。與antagomiRNA組比較,antagomiR-140-5p組細胞增殖率顯著升高,凋亡率顯著降低,Ki67、PCNA的蛋白表達均顯著升高,caspase-3的蛋白表達顯著降低,差異均有統計學意義(P<0.05)。見圖3,表3。

表3 miR-140-5p對高糖誘導的內皮細胞增殖、凋亡的影響 n=9,
2.4 FNDC5對高糖誘導的內皮細胞存活的影響 與si-NC組比較,si-FNDC5組細胞增殖率顯著降低,凋亡率顯著升高,Ki67、PCNA的蛋白表達均顯著降低,caspase-3的蛋白表達顯著升高(P<0.05)。與pcDNA組比較,pcDNA-FNDC5組細胞增殖率顯著升高,凋亡率顯著降低,Ki67、PCNA的蛋白表達均顯著升高,caspase-3的蛋白表達顯著降低(P<0.05)。見圖4,表4。

表4 FNDC5對高糖誘導的內皮細胞增殖、凋亡的影響 n=9,
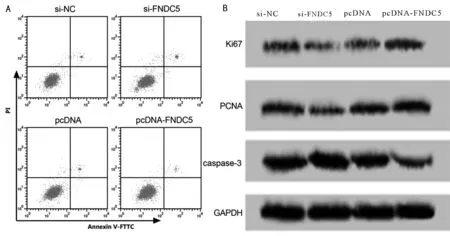
圖4 FNDC5對高糖誘導內皮細胞凋亡及增殖、凋亡相關蛋白的表達;A FNDC5處理的高糖誘導內皮細胞凋亡圖;B Ki67、PCNA、caspase-3的蛋白圖
2.5 miR-140-5p靶向FNDC5 Targetscan(http://www.targetscan.org/)預測到miR-140-5p與FNDC5之間互補的結合位點。雙熒光素酶報告實驗,與agomiRNA組比較,agomiR-140-5p組FNDC5 3’UTR-WT細胞的熒光活性顯著降低(P<0.05)。與agomiRNA組比較,agomiR-140-5p組細胞FNDC5的mRNA和蛋白表達均顯著降低(P<0.05),與antagomiRNA組比較,antagomiR-140-5p組細胞FNDC5的mRNA和蛋白表達均顯著升高,差異有統計學意義(P<0.05)。見圖5,表5。

表5 miR-140-5p對熒光素酶相對活性、FNDC5 mRNA和蛋白相對表達的影響 n=3,
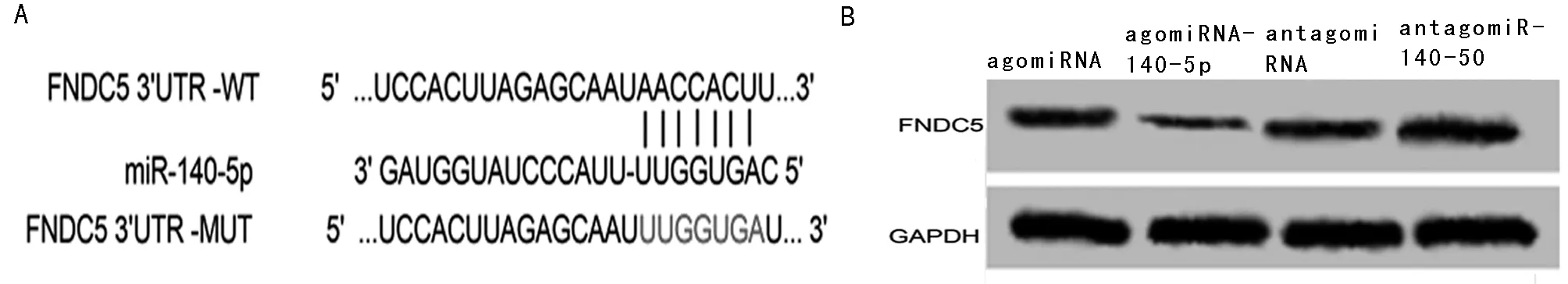
圖5 miR-140-5p靶向FNDC5;A miR-140-5p與FNDC5的互補序列;B miR-140-5p調控FNDC5蛋白表達
2.6 過表達FNDC5對DAPA、miR-140-5p調控高糖誘導的內皮細胞存活功能的作用 與80 μmol/L+agomiRNA組比較,80 μmol/L+agomiR-140-5p組細胞增殖率顯著降低,凋亡率顯著升高,Ki67、PCNA蛋白表達均顯著降低,caspase-3蛋白表達顯著升高(P<0.05)。與80 μmol/L+agomiR-140-5p+pcDNA組比較,80 μmol/L+agomiR-140-5p +pcDNA-FNDC5組細胞增殖率顯著升高,凋亡率顯著降低,Ki67、PCNA蛋白表達均顯著升高,caspase-3蛋白表達顯著降低(P<0.05)。見圖6,表6。

表6 過表達FNDC5和miR-140-5p對DAPA調控高糖誘導內皮細胞增殖、凋亡的影響n=9,
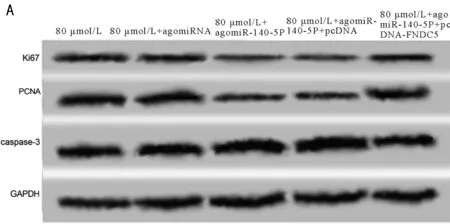
圖6 過表達FNDC5和miR-140-5p對DAPA調控高糖誘導內皮細胞凋亡及增殖、凋亡相關蛋白的表達;A 凋亡圖;B Ki67、PCNA、caspase-3的蛋白圖
3 討論
DAPA屬于SGLT-2抑制劑之一,現已在世界范圍內廣泛用于T2DM的臨床治療[8]。但是DAPA發揮保護作用的相關機制尚未十分清楚。miR-140參與人類很多疾病的發生發展過程,包括糖尿病[9]。但是miR-140在糖尿病中的作用機制尚未十分清楚。Fan等[10]研究發現,異氟醚能夠加重糖尿病大鼠的認知障礙,上調miR-140-5p,且抑制miR-140-5p可減輕異氟醚對糖尿病大鼠的認知損傷,發揮神經保護作用,同時上調分類連接蛋白12(SNX12),揭示抑制miR-140-5p能夠通過上調SNX12減輕異氟醚的糖尿病神經毒性。Zou等[11]發現,梓醇對糖尿病心肌病小鼠具有保護作用,其作用機制為通過調節糖尿病心肌病小鼠體內的長非編碼RNA核旁小斑組裝轉錄物1(NEAT1)/miR-140-5p/組蛋白去乙酰化酶4(HDAC4)通路減輕心肌損傷。結果顯示,miR-140-5p在高糖誘導的小鼠心肌細胞中表達降低,過表達miR-140-5p可挽救NEAT1誘導的心肌細胞凋亡。
本研究發現,miR-140-5p在HG誘導的內皮細胞中高表達,并且過表達miR-140-5p加重高糖對內皮細胞的增殖抑制和凋亡促進作用,而抑制miR-140-5p則可減弱高糖對內皮細胞生存的損害作用。這個研究結果與Fan的實驗結果相一致,與Zou的研究結果相悖。進一步研究發現,miR-140-5p靶向負調控PDX1,暗示PDX1可能參與了miR-140-5p對高糖誘導內皮細胞存活的保護作用。
很多研究均報道稱,FNDC5有利于T2DM血糖恢復[12,13]。Lin等[14]發現,在高糖(HG)/高脂肪(HF)處理的心肌細胞中,FNDC5/虹膜蛋白表達顯著降低,HG/HF處理的H9C2細胞中一氧化氮合酶(iNOS)、NADPH氧化酶2(NOX2)、3-硝基酪氨酸(3-NT)、活性氧(ROS)和過氧亞硝酸鹽(ONOO-)的水平均明顯升高,促進氧化/亞硝化應激,FNDC5/虹膜蛋白是T2DM的潛在治療靶點。Jiang等[15]研究發現,在鏈脲佐菌素(STZ)誘導的1型糖尿病小鼠、高脂飲食(HFD)誘導的肥胖小鼠和糖尿病小鼠中,皮下脂肪中循環虹膜素和FNDC5表達下調,血漿虹膜素水平與皮下脂肪FNDC5表達呈正相關,表明皮下脂肪源性FNDC5/虹膜蛋白在代謝性疾病中起調節作用。本研究結果顯示:FNDC5在HG誘導的內皮細胞中表達下調,這與前人的研究結果相吻合。敲減FNDC5抑制內皮細胞增殖,促進凋亡,而過表達FNDC5則具有相反的保護內皮細胞作用。這說明FNDC5有益于高糖環境下內皮細胞的存活。重要的是,過表達FNDC5還能夠減輕miR-140-5p對內皮細胞存活的損害作用,加強DAPA對內皮細胞的保護功能。
綜上所述,達格列凈促進高糖誘導的內皮細胞增殖,抑制凋亡,有助于內皮細胞在高糖環境下的存活,產生這種作用的機制與抑制miR-140-5p/FNDC5通路有關,為T2DM的治療提供理論支持。

