泰它西普治療IgA腎病的有效性及安全性分析
董寅迪, 吳 歌, 李冠華
(鄭州大學(xué)第一附屬醫(yī)院 腎內(nèi)科, 河南 鄭州, 450052)
IgA腎病(IgAN)指免疫病理顯示以IgA為主的免疫球蛋白在腎小球系膜區(qū)沉積的自身免疫性疾病。IgAN是導(dǎo)致終末期腎病的原因之一, 20%~40%的IgAN患者在出現(xiàn)首次臨床表現(xiàn)后的10~20年內(nèi)發(fā)生終末期腎病(ESRD)[1]。IgAN臨床表現(xiàn)及病理均多種、多樣,其致病機(jī)制較復(fù)雜,其中B細(xì)胞的異常活化發(fā)揮了重要作用。早期CD20+B細(xì)胞產(chǎn)生少量抗體[半乳糖缺陷型IgA 1(GD-IgA1)], 而CD38+漿細(xì)胞既能產(chǎn)生GD-IgA1, 又能產(chǎn)生大量自身抗體(抗GD-IgA1)[2]。抗體和自身抗體形成免疫復(fù)合物,在腎小球系膜區(qū)沉積并積累,通過激活補(bǔ)體進(jìn)而誘發(fā)炎癥,最終導(dǎo)致腎功能喪失和ESRD[3-4]。新的治療方法通過抑制B細(xì)胞或CD38+漿細(xì)胞活化或促進(jìn)其耗竭靶向治療IgAN。
泰它西普是將鈣調(diào)親環(huán)素配體相互作用分子(TACI)胞外特定的可溶部分與人IgG1 Fc段相融合的重組蛋白[5], 能夠結(jié)合B淋巴細(xì)胞刺激因子(BLys/BAFF)和增殖誘導(dǎo)配體(APRIL), 從而多靶點(diǎn)抑制B細(xì)胞成熟分化和漿細(xì)胞抗體產(chǎn)生,抑制Gd-IgA1產(chǎn)生,發(fā)揮免疫抑制作用[6]。目前,臨床將該藥用于治療B細(xì)胞介導(dǎo)的自身免疫性疾病,如系統(tǒng)性紅斑狼瘡[7]。泰它西普治療類風(fēng)濕性關(guān)節(jié)炎[8]和多發(fā)性硬化癥的研究尚處于臨床研究中。本研究旨在評(píng)估泰它西普在單中心臨床實(shí)踐中治療IgAN的有效性和安全性。
1 資料與方法
1.1 一般資料
回顧性選取鄭州大學(xué)第一附屬醫(yī)院2022年2—10月使用泰它西普治療的IgAN患者9例,其每周皮下注射泰它西普160 mg,隨訪時(shí)間不短于12周。
納入標(biāo)準(zhǔn): ① 腎穿刺病理活檢證實(shí)為IgAN者; ② 年齡不小于18周歲且不大于65周歲者; ③ 估算腎小球?yàn)V過率(eGFR)≥35 mL/(min·1.73 m2)(使用CKD-EPI公式); ④ 經(jīng)過3個(gè)月血管緊張素轉(zhuǎn)化酶抑制劑(ACEI)/血管緊張素受體阻滯劑(ARB)等優(yōu)化治療后,尿蛋白與肌酐比值(UPCR)不小于0.5 g/g者。排除標(biāo)準(zhǔn): ① 繼發(fā)性IgAN者,如紫癜性腎炎、慢性肝病腎損害等; ② 克羅恩病、潰瘍性結(jié)腸炎、乳糜瀉等胃腸道疾病者; ③ 自身免疫性疾病免疫者,如系統(tǒng)性紅斑狼瘡、類風(fēng)濕關(guān)節(jié)炎、干燥綜合征等疾病; ④ 感染性疾病者,如慢性病毒感染(乙肝病毒、丙肝病毒)、慢性黏膜感染等疾病; ⑤ 腫瘤性疾病者,如骨髓瘤、淋巴瘤等疾病。
本研究符合人體試驗(yàn)倫理學(xué)標(biāo)準(zhǔn),并通過鄭州大學(xué)第一附屬醫(yī)院科研和臨床試驗(yàn)倫理委員會(huì)審核,臨床試驗(yàn)注明編號(hào)2022-KY-1397。
1.2 方法
本研究為回顧性分析,對(duì)于所有療效分析的基線標(biāo)準(zhǔn)定義為第1次給藥之前的最后1次評(píng)估。主要觀察終點(diǎn)為隨訪期間UPCR、eGFR較基線的變化。次要觀察終點(diǎn)為血清白蛋白、免疫球蛋白在隨訪期間的變化。① 隨訪12周前后指標(biāo)比較: 比較隨訪12周前后患者血壓、尿紅細(xì)胞計(jì)數(shù)、UPCR、血清肌酐、eGFR指標(biāo)變化。② 次要指標(biāo)比較: 比較治療前后血清白蛋白、血清尿酸、總膽固醇、甘油三酯等變化。療效評(píng)價(jià)情況: ① 完全緩解(CR), UPCR≤0.3 g/g, 且腎功能穩(wěn)定(eGFR波動(dòng)≤30%); ② 部分緩解(PR), UPCR減少≥50%, 且腎功能穩(wěn)定,但未達(dá)到完全緩解; ③ 無效,未達(dá)到完全緩解和部分緩解的標(biāo)準(zhǔn)。蛋白尿分級(jí)標(biāo)準(zhǔn)(根據(jù)UPCR): 輕度蛋白尿, >0.15 g/g且<1.0 g/g, 中度蛋白尿, ≥1.0 g/g且<3.5 g/g, 大量蛋白尿, ≥3.5 g/g。
1.3 觀察指標(biāo)
臨床資料包括疾病病程、年齡、性別、體質(zhì)量指數(shù)及目前用藥、高血壓病史、收縮壓等。實(shí)驗(yàn)室檢查指標(biāo): 尿紅細(xì)胞計(jì)數(shù)、UPCR、血尿素氮、血清肌酐、血清尿酸、eGFR、血清白蛋白、總膽固醇、甘油三酯、血白細(xì)胞、血紅蛋白、血小板、免疫球蛋白(IgA、IgG、IgM)、補(bǔ)體C3和補(bǔ)體C4等。每4周收集1次上述指標(biāo)。
病理資料: 病理結(jié)果按IgAN牛津病理分型標(biāo)準(zhǔn),收集腎小球硬化、新月體、系膜增生、毛細(xì)血管內(nèi)增生、間質(zhì)纖維化等腎活檢結(jié)果。① 系膜細(xì)胞增殖(M): PSA染色下, ≥50%的腎小球系膜區(qū)內(nèi)可見>3個(gè)系膜細(xì)胞則為M1, 否則為M0; ② 毛細(xì)血管內(nèi)增生(E): 腎小球毛細(xì)血管袢內(nèi)細(xì)胞增生導(dǎo)致管腔狹窄,若存在則為E1, 否則為E0; ③ 腎小球節(jié)段硬化(S): 存在腎小球節(jié)段硬化或粘連則為S1, 否則為S0; ④ 腎小管萎縮/間質(zhì)纖維化(T): 皮質(zhì)區(qū)細(xì)胞外基質(zhì)增多導(dǎo)致管腔狹窄,根據(jù)受累面積百分比分別為T0(≤25%)、T1(>25%~50%)、T2(>50%); ⑤ 細(xì)胞或混合性新月體(C): 根據(jù)占腎小球總數(shù)的百分比分別為C0(無)、C1(<25%)、C2(≥25%)。
記錄隨訪過程中的不良事件(AE)。AE: 即用藥后對(duì)機(jī)體可能產(chǎn)生的不良影響,包括非感染性、感染性及超敏反應(yīng)。感染性AE指皮膚、呼吸道、消化道、泌尿道等部位感染,非感染性AE指注射部位局部瘙癢、疼痛、硬結(jié)形成等不適。超敏反應(yīng)定義為與泰它西普相關(guān)的AE, 在給藥后6~48 h內(nèi)發(fā)生,與泰它西普的關(guān)系由醫(yī)生判斷確定。
1.4 統(tǒng)計(jì)學(xué)分析

2 結(jié) 果
2.1 一般資料
共納入9例患者,男7例(77.78%), 女2例(22.22%); 基線年齡(41.89±12.63)歲,中位病程1.42(0.88, 5.00)年。納入的9例IgAN患者均表現(xiàn)為持續(xù)性蛋白尿, 1例合并間斷性肉眼血尿(11.11%), 4例合并腎功能不全(44.44%), 5例合并高血壓(55.56%)。基線中位UPCR為0.91(0.59, 1.83) g/g, 尿紅細(xì)胞為4.00 (1.00, 34.00)個(gè)/HP, 血清肌酐(120.11±39.58) μmol/L, 血清尿酸為(385.56±130.80)μmol/L, eGFR為(67.33±25.11) mL/(min·1.73 m2), 血清白蛋白為(41.34±5.66) g/L, 血清免疫球蛋白IgA(3.26±0.86) g/L。基線合并用藥情況: 3例(33.33%)服用他克莫司、6例(66.67%)使用ACEI/ARB類藥物, 4例(44.44%)服用抗瘧藥, 3例(33.33%)服用降脂藥, 7例(77.78%)服用百令膠囊, 6例(66.67%)服用貝前列素鈉, 4例(44.44%)服用非布司他,合并用藥在12周研究過程中未有調(diào)整,見表1。

表1 IgAN患者基線臨床特點(diǎn)
2.2 治療12周臨床指標(biāo)變化情況
用藥12周后,中位UPCR由治療前0.91(0.59, 1.83) g/g下降至0.54(0.35, 0.59) g/g, 差異有統(tǒng)計(jì)學(xué)意義(P=0.008)。中位血清肌酐治療前為106.00(88.50, 139.50) μmol/L, 治療后為112.00(99.00, 135.50) μmol/L, 差異無統(tǒng)計(jì)學(xué)意義。
(P=0.605)。eGFR均值治療前為(67.33±25.11) mL/(min·1.73 m2), 治療后為(63.72±18.30) mL/(min·1.73 m2), 差異無統(tǒng)計(jì)學(xué)意義(P=0.069)。隨訪12周, 9例IgAN患者治療前后血紅蛋白、血糖、血脂、血清尿酸、血清白蛋白比較,差異無統(tǒng)計(jì)學(xué)意義(P>0.05), 見表2。

表2 9例IgAN患者泰它西普治療12周后臨床指標(biāo)與基線比較
2.3 泰它西普治療前后隨訪情況
治療第4、8、12周時(shí)UPCR均數(shù)小于基線,差異有統(tǒng)計(jì)學(xué)意義(F=10.032,P=0.008)。治療第4、8、12周時(shí)血清尿酸均數(shù)與基線比較,差異無統(tǒng)計(jì)學(xué)意義(F=1.121,P=0.329)。治療第4、8、12周時(shí)eGFR均數(shù)與基線比較,差異無統(tǒng)計(jì)學(xué)意義(F=2.046,P=0.134)。9例患者未規(guī)律隨訪B淋巴細(xì)胞計(jì)數(shù),其降低統(tǒng)計(jì)意義有限,未對(duì)該指標(biāo)進(jìn)行統(tǒng)計(jì)學(xué)分析。見表3。
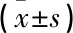
表3 9例IgAN患者泰它西普治療前后隨訪情況
2.4 臨床療效和不良事件發(fā)生情況
9例患者治療12周,其中6例患者獲得臨床緩解,緩解率為66.67%。1例發(fā)生不良事件,為皮膚感染。隨訪期間無嚴(yán)重不良事件、輸液反應(yīng)和非感染性事件發(fā)生。
3 討 論
本研究評(píng)估了泰它西普在IgAN患者治療中的療效及安全性,結(jié)果顯示, 9例患者治療12周,其中6例患者獲得臨床緩解。總不良事件發(fā)生1例,在治療第12周出現(xiàn)皮膚感染,總體耐受性良好。本研究中, 1例青年IgAN患者,病程7年,持續(xù)性輕中度蛋白尿,既往分別接受糖皮質(zhì)激素、環(huán)孢素、嗎替麥考酚酯、他克莫司治療,病情易反復(fù),治療效果欠佳。基線已使用ACEI及羥氯喹3月余,尿蛋白未見改善,在合并使用泰它西普治療后,蛋白尿逐步下降,治療12周尿蛋白較基線下降59.39%, 腎功能持續(xù)維持穩(wěn)定。
本研究中, 4例患者表現(xiàn)為腎炎綜合征合并腎功能不全,基線均為中度蛋白尿。1例初診IgAN患者,病程3個(gè)月,病理提示局灶增生性IgAN, 缺血性腎損傷。1例病程9個(gè)月的IgAN復(fù)發(fā)患者,病理表現(xiàn)局灶增生性IgAN, 重度缺血性腎損傷,既往應(yīng)用羥氯喹及嗎替麥考酚酯。1例難治性IgAN, 病程7年,病理提示局灶增生性IgAN, 既往應(yīng)用激素聯(lián)合免疫抑制劑治療。1例病史2年,病理提示局灶增生壞死性IgAN。經(jīng)過12周治療,上述患者尿蛋白明顯下降,達(dá)到臨床部分緩解水平(均小于0.7 g/g), 腎功能維持穩(wěn)定,無不良反應(yīng)事件發(fā)生。一項(xiàng)泰它西普Ⅱ期臨床研究[9]顯示,泰它西普可顯著減少IgAN患者蛋白尿。本研究提示,對(duì)于中度蛋白尿合并腎功能不全的IgAN患者,泰它西普具有較好的療效及安全性。
本研究中, 3例IgAN患者合并使用免疫抑制劑(他克莫司),病程分別為1、1、5年,基線尿蛋白為0.69、0.60、0.91 g/g, 病理分別為局灶增生性IgAN、輕度系膜增生性IgAN、局灶增生性IgAN伴缺血性腎損傷,基線腎功能未見異常。經(jīng)12周治療后,尿蛋白水平持續(xù)穩(wěn)定下降,但差異無統(tǒng)計(jì)學(xué)意義,提示對(duì)于合并使用免疫抑制劑的輕度蛋白尿患者,聯(lián)合泰它西普治療效果不顯著,其原因可能是由于患者體內(nèi)長(zhǎng)期免疫抑制狀態(tài), B淋巴細(xì)胞長(zhǎng)期低水平,泰它西普未能發(fā)揮相應(yīng)療效。此外,目前,他克莫司治療IgAN的療效尚不明確。相關(guān)研究[10]中,對(duì)他克莫司治療IgAN的療效評(píng)估顯示,經(jīng)6個(gè)月治療,他克莫司組完全緩解率僅為35%。本研究顯示,對(duì)于輕度蛋白尿IgAN患者,泰它西普聯(lián)合免疫抑制劑治療效果不顯著。本研究中, 9例IgAN患者經(jīng)過泰它西普160 mg治療12周的蛋白尿水平較基線顯著降低(P<0.05), 且腎功能保持穩(wěn)定。但有關(guān)泰它西普Ⅱ期臨床研究[9]顯示, 14例IgAN患者經(jīng)過泰它西普240 mg治療24周,平均尿蛋白水平較基線降低49%; 16例IgAN患者經(jīng)過泰它西普160 mg治療,尿蛋白較基線降低25%。該研究結(jié)果與本研究不一致,考慮可能與納入標(biāo)本量較少,納入患者病理活動(dòng)度不同有關(guān)。上述結(jié)果初步提示,泰它西普對(duì)IgAN具有較好的療效,可為治療IgAN提供一種新的治療方案,但具體治療有效劑量有待進(jìn)一步探討。
IgAN一般給予支持治療、激素和/或免疫抑制劑。免疫抑制劑被建議用于有進(jìn)展高風(fēng)險(xiǎn)的IgAN患者[11]。雖然這類藥物普遍具有良好的耐受性,但也可引起致命感染、肝腎毒性等。相關(guān)研究[12]比較了利妥昔單抗聯(lián)合標(biāo)準(zhǔn)治療與標(biāo)準(zhǔn)治療對(duì)IgAN的療效,結(jié)果提示,利妥昔單抗對(duì)IgAN缺乏療效。與阿塞西普相比,泰它西普生物學(xué)活性更強(qiáng)[13]。
本研究中, 1例患者在治療第12周時(shí)出現(xiàn)皮膚感染。一項(xiàng)泰它西普聯(lián)合常規(guī)藥物治療中重度活動(dòng)性系統(tǒng)性紅斑狼瘡患者的研究[14]表明,泰它西普在總體不良事件發(fā)生率上與安慰劑無顯著差異。泰它西普治療IgAN Ⅱ期研究[9]提示,泰它西普組與安慰劑組用藥后不良反應(yīng)發(fā)生情況比較無顯著差異,均為輕、中度不良反應(yīng),無重度不良反應(yīng)事件。相關(guān)研究[15-16]顯示,使用泰它西普治療自身免疫系統(tǒng)疾病療效尚可,安全性高。
本研究存在局限性,本研究缺乏對(duì)照人群,同時(shí)納入樣本量較小及觀察時(shí)間較短,仍需擴(kuò)大樣本量、延長(zhǎng)觀察時(shí)間,以進(jìn)一步評(píng)估泰它西普對(duì)于IgAN患者的療效及安全性。此外,研究未能連續(xù)監(jiān)測(cè)到B細(xì)胞亞群濃度。
- 實(shí)用臨床醫(yī)藥雜志的其它文章
- 驅(qū)動(dòng)基因陽性非小細(xì)胞肺癌的免疫檢查點(diǎn)抑制劑治療的研究進(jìn)展
- 幽門螺桿菌相關(guān)性胃癌與非編碼核糖核酸的研究進(jìn)展
- 利妥昔單抗治療對(duì)特發(fā)性膜性腎病患者外周血T淋巴細(xì)胞亞群影響的研究進(jìn)展
- 多參數(shù)磁共振成像與經(jīng)直腸超聲認(rèn)知融合技術(shù)在前列腺靶向穿刺活檢中的應(yīng)用研究進(jìn)展
- 開顱術(shù)后創(chuàng)口感染的病原學(xué)分析、風(fēng)險(xiǎn)模型構(gòu)建及預(yù)見式護(hù)理
- 某中醫(yī)院重癥監(jiān)護(hù)病房醫(yī)院感染現(xiàn)狀及患者預(yù)后分析

