維持性血液透析患者發生營養不良的風險預測模型構建
魏 敏, 劉 軍
(江蘇省淮安市第二人民醫院 腎臟內科, 江蘇 淮安, 223002)
目前,維持性血液透析已成為終末期腎病患者的主要治療手段[1]。全球維持性血液透析患者數量正在迅速增加,透析患者數量每年增加6%。由于透析引起的分解代謝作用,包括氨基酸丟失、飲食攝入不足、炎癥和代謝性酸中毒,維持性血液透析患者存在營養不良的風險[2]。據報道[3-4], 維持性血液透析患者營養不良的發生率為15%~75%, 其中6%~8%的患者患有嚴重營養不良,其是影響透析患者生存的主要因素之一。因此,評估維持性血液透析患者發生營養不良的高風險人群,對臨床制訂合理的治療方案意義重大。列線圖可根據多因素回歸分析疾病的危險因素進行繪制,并通過計算總得分的形式直觀展示患者出現相應疾病的概率,易于臨床高效、快速篩選高危人群,并制訂有效干預措施。本研究分析行維持性血液透析患者的資料及其影響因素,并建立列線圖,以期為維持性血液透析患者營養不良的臨床早期篩選提供指導。
1 資料與方法
1.1 一般資料
收集2019年12月—2021年12月在本院接受維持性血液透析的255例患者資料進行回顧性分析,將納入患者按照6∶4比例分為建模組153例及驗證組102例。將建模組患者根據是否發生營養不良[采用主觀綜合營養評估(SGA)法[5]評估患者營養狀態,評估內容包括胃腸道癥狀、肌肉消耗、體質量變化、皮下脂肪以及飲食變化等, A級為營養正常, B級為輕中度營養不良, C級為重度營養不良]分為營養不良組83例和無營養不良組70例。
納入標準: ① 年齡≥18歲者; ② 至少接受6個月的血液透析者; ③ 在過去4周內沒有使用補充營養的藥物,且沒有酗酒、吸煙或吸毒成癮者。排除標準: ① 患有活動性惡性腫瘤者; ② 有急性傳染病或炎癥性疾病者; ③ 患有嚴重心律失常、肝臟和胃腸道疾病者。本研究經本院倫理委員會批準。
1.2 方法和觀察指標
收集患者性別、工作狀況、婚姻狀況、有無家人照顧、家庭月收入、教育水平及有無合并糖尿病、有無合并高血壓、有無高通量透析、營養知識知曉度(由專業營養師或醫護人員制作營養學知識調查問卷,共設10道題目,總分10分,得分≥7分為營養知識知曉度高,反之為營養知識知曉度低)、有無蛋白質能量攝入不足[患者每天能量攝入量<125 kJ/(kg·d)及每天蛋白攝入量<1.2 g/(kg·d)為蛋白質能量攝入不足,反之為攝入充足]、原發疾病種類(慢性腎小球炎、梗阻性腎病、糖尿病腎病、高血壓腎病等)、有無睡眠質量差[采用匹茲堡睡眠質量指數(PSQI)量表[6]進行評估,總分>7分定義為睡眠質量差]、有無抑郁[采用漢密爾頓抑郁癥評定量表(HAMD)[7]評定患者病情,按照HAMD評分可以分為: <7分為無抑郁, ≥7分為抑郁]、社會支持(采用社會支持評定量表[8], 共10個條目,總分<38.4分為社會支持程度低)、社會支持、職業、透析頻率、總尿素清除指數(Kt/v)、透析齡、體質量指數(BMI)、殘余尿量、上臂中部周徑(MAC)、超敏C反應蛋白、血紅蛋白(Hb)、血肌酐(Scr)、尿素氮(BUN)、降鈣素原(PCT)、碳酸氫根(HCO3-)、甲狀旁腺激素(PTH)。
1.3 統計學分析

2 結 果
2.1 建模組發生營養不良的單因素分析
收集患者資料進行單因素分析,結果顯示,工作狀況、有無合并糖尿病、營養知識知曉度、有無蛋白質能量攝入不足、透析頻率、Kt/v、透析齡、年齡、BMI、MAC、超敏C反應蛋白、Scr、PCT、HCO3-、PTH為影響維持性血液透析患者發生營養不良的因素(P<0.05), 而營養不良組與無營養不良組患者性別、婚姻狀況、有無家人照顧、家庭月收入、教育水平、有無合并高血壓、有無高通量透析、原發疾病、有無睡眠質量差、有無抑郁、社會支持、職業、殘余尿量、Hb、BUN比較,差異無統計學意義(P>0.05)。見表1。
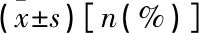
表1 建模組發生營養不良的單因素分析
2.2 維持性血液透析患者發生營養不良的危險因素
將發生營養不良作為因變量(未發生=0, 發生=1), 根據單因素分析中有統計學意義的變量作為自變量進行分析(工作狀況等),變量賦值方式見表2。多因素Logistic回歸分析結果顯示,蛋白質能量攝入不足(OR=8.732)、Kt/v(OR=9.756)、年齡(OR=1.142)、透析齡(OR=1.537)、超敏C反應蛋白(OR=1.671)是營養不良發生的危險因素(P<0.05), 見表3。

表2 變量賦值方式

表3 多因素Logistic回歸分析影響維持性血液透析患者發生營養不良的危險因素
2.3 建立列線圖預測模型
根據多因素Logistic回歸分析結果,使用R軟件建立影響維持性血液透析患者發生營養不良發生的列線圖預測模型,結果顯示,年齡每增加5歲,增加6.5分的權重; 透析齡每增加2個月,增加8.1分的權重; 超敏C反應蛋白每增加2 mg/L, 增加9.9分的權重; 蛋白質能量攝入不足增加21.3分, Kt/v<1.2增加22.3分。見圖1。

圖1 維持性血液透析患者發生營養不良的列線圖預測模型
2.4 評估維持性血液透析患者發生營養不良的列線圖預測模型
繪制校準曲線評估模型的結果顯示,建模組χ2=7.425,P=0.492; 驗證組χ2=6.398,P=0.603。繪制ROC曲線評估模型的結果顯示,建模組曲線下面積為0.877(95%CI: 0.818~0.936), 敏感度為84.34%, 特異度為80.00%; 驗證組曲線下面積為0.825(95%CI: 0.747~0.903), 敏感度為89.09%, 特異度為61.70%。見圖2。

A: 建模組校準曲線; B: 驗證組校準曲線; C: 建模組ROC曲線; D: 驗證組ROC曲線。圖2 列線圖預測模型評估校準曲線和ROC曲線
3 討 論
營養不良是接受血液透析的終末期腎病患者的常見疾病[9-10], 指對組織至關重要的大量營養元素或特定微量營養素需求過剩或營養不足的狀態[11]。維持性血液透析患者發生營養不良,不僅可影響治療效果,甚至可導致死亡[12]。因此,對營養不良發生的影響因素進行有效分析具有重要意義。
本研究收集在本院進行維持性血液透析的患者資料進行分析,結果顯示, 153例患者中, 83例出現營養不良,占比54.25%, 與畢明明等[13]研究結果基本一致。通過多因素Logistic回歸分析發現,蛋白質能量攝入不足、Kt/v、年齡、透析齡、超敏C反應蛋白為影響維持性血液透析患者發生營養不良的影響因素。分析原因為: ① 患者隨著年齡增長,其胃腸道功能下降、對營養攝入能力下降及飲食結構受限,無法攝入人體正常需要的蛋白質及熱量[14], 從而容易出現營養不良; 因此老年維持性血液透析患者是臨床工作中重點監測對象,應針對老年患者提前干預,盡早給予患者有效的營養健康教育和干預措施。② 蛋白質能量攝入不足是維持性血液透析患者發生營養不良的重要原因,由于患者在透析過程中可能會發生口味改變、厭食等情況,且患者承擔巨大的心理負擔,其消化功能也隨之減退,造成患者發生營養不良。③ 研究[15]發現,隨著患者透析時間延長,其并發癥發生率也隨之升高,加上患者在透析期間體內微量元素、氨基酸等重要營養物質流失,致使體內蛋白質分解、消耗及合成減少,造成負氮平衡,最終導致營養不良; 因此應加強管理患者,盡早發現患者發生并發癥的原因,并采取個性化預防措施,在透析間期,按照要求嚴格控制患者體質量,同時加強患者的健康教育,指導患者合理飲食。④ Kt/v是反映患者透析充分的指標[16],由于營養不良的個體體積較小,因此其易受Kt/v增加的影響,即使在透析有效的情況下也可能存在營養不良。因此,護士在臨床工作中需要對透析不足的患者進行深入分析,并與醫生共同制定更科學、更個性化的透析計劃,以減少透析不足的發生。同時,在患者透析治療前2 h進行鍛煉,可有效提高透析的充分性,可指導患者在透析過程中進行中低強度的漸進式阻力運動(如臥位騎自行車運動),并根據患者的耐受水平每周逐漸應用阻力,逐步提高其透析充分性,已預防營養不良。⑤ 超敏C反應蛋白是微炎癥反應的主要標志物之一。如果患者機體長期發生慢性炎癥,會刺激巨噬細胞分泌組織因子,促進超敏C反應蛋白釋放,這些炎性因子可通過減少胃酸分泌及減弱腸道蠕動,降低患者的營養攝入,引發營養不良,造成病情惡化[17-18]。臨床醫護人員應加強對上述相關因素的警戒,以降低維持性血液透析患者營養不良的風險,改善其透析結局。
列線圖模型作為臨床統計圖形化、可視化模型,可將復雜的多因素分析結果轉變為帶刻度線段,進行臨床風險評估,更加客觀和具體。本研究根據多因素Logistic回歸分析篩選出5個獨立危險因素。通過繪制ROC曲線及校準曲線評估模型,結果顯示,該模型的區分度及有效性較好。此外,本研究選取同時期在本院接受治療的患者作為驗證組,繪制校準曲線及ROC曲線行外部驗證,顯示該模型區分度及有效性較好,表明該模型的判別和校正能力較好。
綜上所述,本研究建立的列線圖預測模型區分度及有效性較好,可用于臨床醫護人員個體化預測維持性血液透析患者營養不良的發生風險。但本研究為回顧性分析,納入因素固定且有限,可能導致結果存在偏倚,尚需在今后的研究中納入更多因素,以完善列線圖預測模型。

