植物乳桿菌與地衣芽孢桿菌復合微貯稻草發酵早期菌群結構變化及功能分析
任文義 李婭楠 楊雙鳴 張力莉 徐曉鋒
(寧夏大學農學院,寧夏 銀川 750021)
飼料成本是制約現代養殖業發展的重要因素之一[1]。我國的稻草資源豐富,但稻草的品質差,反芻動物利用效率低。稻草主要由纖維素和半纖維素組成,還含有木質素、含氮化合物和粗灰分等[2]。若能找到合適的處理方法,能夠提高稻草的利用率。
微貯技術是利用一些酶制劑和益生菌,在合適條件下對秸稈進行厭氧發酵處理,此過程產生熱量、酸和酶;產生熱量會提高發酵的溫度,酸可以使稻草柔軟蓬松,降低發酵pH 值,較低的pH 值和較高的溫度可為纖維素分解酶、半纖維素分解酶和木質素分解酶提供適宜的酶解環境[3]。趙林果等[4]發現,利用白腐菌及黑曲霉所產的纖維素復合酶處理稻草48 h,能夠使稻草中的纖維素、半纖維素和木質素分別降解53.8%、57.8%、44.5%。微貯飼料化加工可以最大程度保存稻草的營養價值,在一定程度上提高稻草適口性。植物乳桿菌是目前微貯飼料生產中最常用的微生物制劑之一。乳酸菌可以抑制酵母菌和霉菌的生長,避免微貯飼料好氧降解造成的營養損失[5-7]。地衣芽孢桿菌是一種常見于土壤的革蘭氏陽性嗜熱細菌[8],具有獨特的生物氧捕獲機制,能夠快速創造厭氧環境,產生抗菌活性物質,抑制病菌的生長和繁殖[9]。但地衣芽孢桿菌與植物乳桿菌組合利用的研究相對較少,對微貯的作用有待進一步研究。本試驗旨在研究地衣芽孢桿菌與植物乳桿菌復合微貯稻草,基于16S rRNA技術找到發酵過程中細菌群落動態和預測的代謝途徑,分析微貯過程中菌群變化,探討其分子機制,為實際生產中稻草資源的利用提供參考。
1 材料與方法
1.1 試驗材料
稻草采自寧夏,干物質(DM)含量為94.49%,粗蛋白質(CP)含量為3.45%,中性洗滌纖維(NDF)含量為59.51%,酸性洗滌纖維(ADF)含量為33.59%。
植物乳桿菌為凍干型粉劑,活菌數為1.39×1010CFU/g,地衣芽孢桿菌為凍干型粉劑,活菌數為1.30×1011CFU/g,均購自山東中科嘉億生物工程有限公司。
1.2 試驗設計
試驗采用完全隨機設計,微貯稻草隨機分為5 組,每組6個重復。試驗設計見表1。試驗期30 d。

表1 微貯稻草試驗設計
1.3 微貯稻草的制作
以粉碎2~3 cm 左右的稻草為原料,利用小規模發酵法進行微貯,蔗糖、菌劑、蒸餾水均按照表1進行配制,使用噴壺均勻噴灑至稻草樣品,在乙醇消毒的塑料容器中充分混勻。裝入35 cm × 45 cm的聚乙烯發酵袋中,每袋500 g,每組6個重復,使用真空包裝機抽真空,密封。室溫條件(28±3)℃下避光貯藏。于微貯第30 d 后開袋,測定營養指標。
1.4 測定指標及方法
1.4.1 營養成分
微貯30 d后的稻草開袋取樣,65 ℃烘干48 h,粉碎,過40 目標準篩。采用烘干法(GB/T 6435—2014)測定干物質(DM),采用凱氏定氮法(沛歐SKD-100)(GB/T 6432—2018)測定粗蛋白(CP)含量,采用Van Soest 洗滌法測定中性洗滌纖維(NDF)、酸性洗滌纖維(ADF)含量。樣品開袋后,混勻,從每袋中取微貯稻草20 g,加入180 mL蒸餾水,使用多功能攪拌機均質30 s,使用4 層紗布過濾至三角瓶中,使用雷磁臺式酸度計測定濾液pH值。
1.4.2 隸屬函數分析
將DM、CP、NDF、ADF、pH 值采用模糊數學的隸屬函數理論,綜合評價其微貯品質[10-11]。其中DM、CP為正隸屬函數,NDF、ADF、pH值為反隸屬函數。隸屬函數均值越大,說明微貯稻草品質越好。
1.4.3 微生物測序及生物信息學分析
根據模糊隸屬函數分析將最優組合即復合菌組Ⅲ的1、3、7、15、30 d微貯樣品進行細菌變化規律研究及功能預測分析。樣品的DNA提取、PCR擴增、構建文庫及測序由廣州基迪奧生物科技有限公司完成,測序平臺為Illumina Hiseq 2500測序平臺。測序得到的原始數據經過質控得到有效數據,進行后續分析。
1.5 數據統計與分析
試驗數據采用Excel 2019 處理,SAS 9.4 統計軟件進行單因素方差分析,Duncan's 法進行多重比較,結果以平均值和標準誤表示,P<0.05表示差異顯著。
根據OTU 的物種注釋和豐度信息,使用PICRUSt 2軟件對細菌的KEGG 進行功能注釋,并統計每個通路豐度信息。使用Origin 2022軟件作圖。
2 結果與分析
2.1 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草營養成分的影響(見表2)
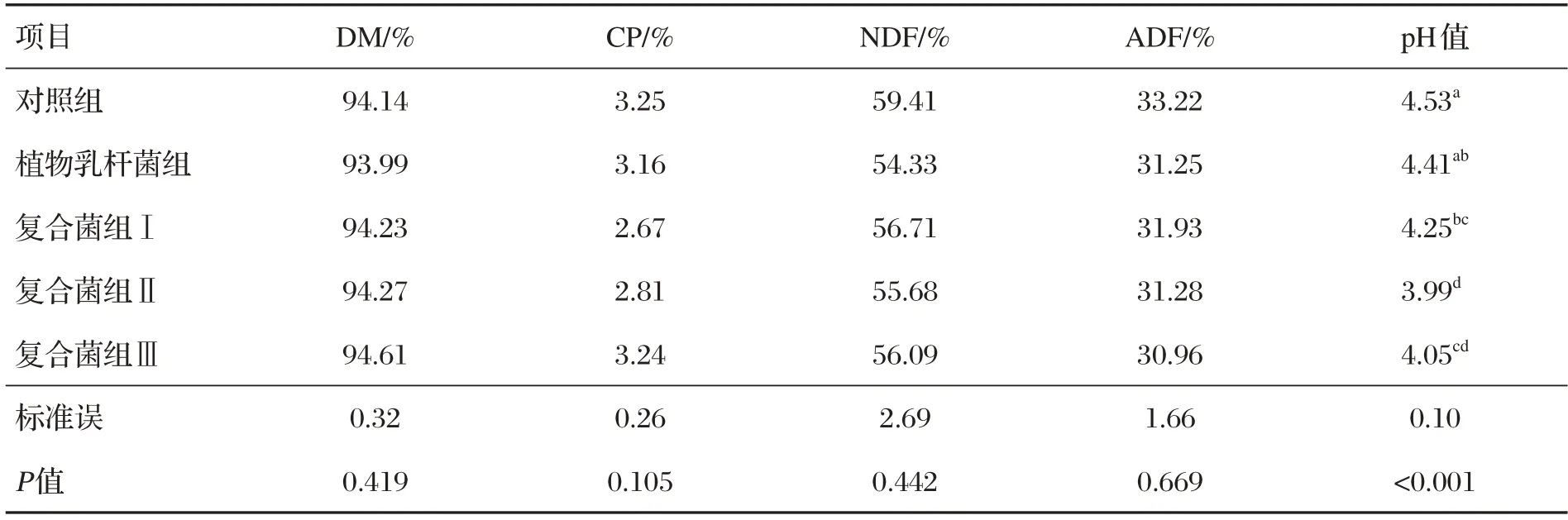
表2 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草營養成分的影響
由表2 可知,微貯30 d 后,植物乳桿菌組、復合菌組Ⅰ、復合菌組Ⅱ、復合菌組Ⅲ微貯稻草的NDF 含量分別比對照組降低了8.6%、4.6%、6.3%、5.6%(P>0.05),ADF含量分別比對照組降低了5.9%、3.9%、5.8%、6.8%(P>0.05)。與對照組相比,復合菌組Ⅰ、復合菌組Ⅱ、復合菌組Ⅲ微貯稻草的pH 值分別降低了6.2%、11.9%、10.6%(P<0.05)。
2.2 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草品質的隸屬函數值的影響(見表3)
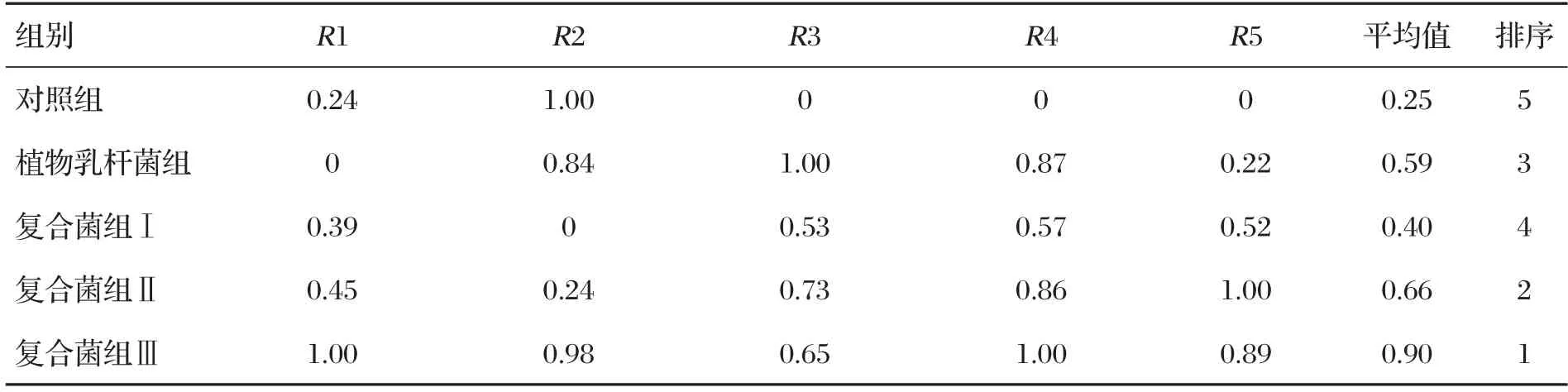
表3 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草品質的隸屬函數值的影響
由表3 可知,復合菌組Ⅲ稻草微貯的隸屬函數平均值綜合表現最優。
2.3 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草發酵過程中細菌Alpha多樣性的影響(見表4)

表4 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草發酵過程中細菌Alpha多樣性的影響
由表4 可知,微貯第7 d 時,微貯稻草的Shannon 指數最高,微貯第30 d 的Shannon 指數顯著低于第1、3、7、15 d(P<0.05)。微貯第7 d 時,微貯稻草的Simpson指數最低,微貯第7、15 d的Simpson指數顯著低于第1 d(P<0.05)。研究表明,稻草微貯過程中細菌群落多樣性在第7 d時最高,第30 d時最低。
微貯稻草的Chao 1和Ace指數呈先升高后降低趨勢,第7 d最高,微貯第7、15 d的Chao 1、Ace指數顯著高于第1 d(P<0.05)。研究表明,稻草微貯過程中細菌群落豐富度呈先升高后降低趨勢,第7 d時豐富度最高。
2.4 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草發酵過程中細菌組成的影響(見表5、圖1)
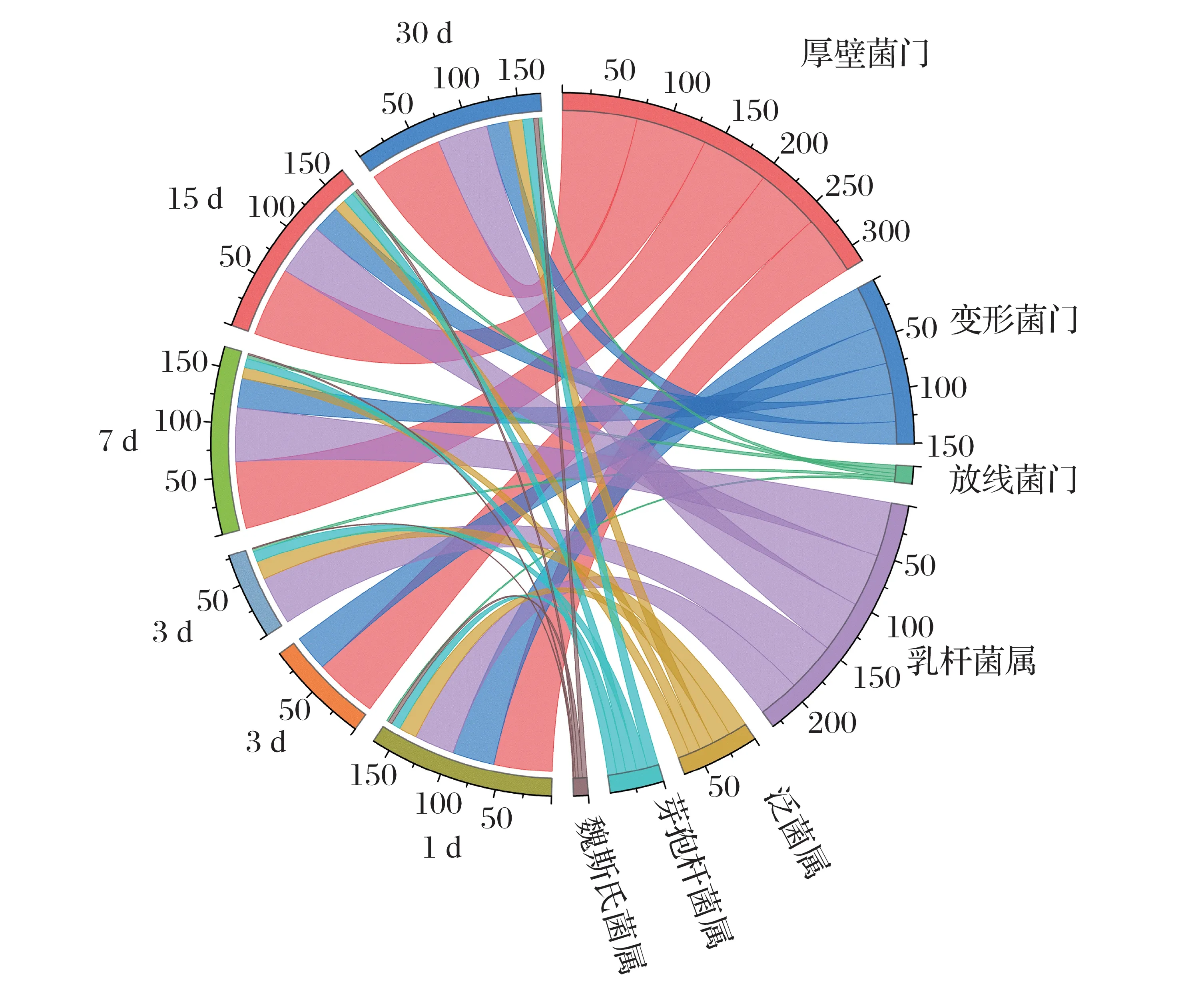
圖1 稻草發酵過程中細菌門水平和屬水平和弦圖
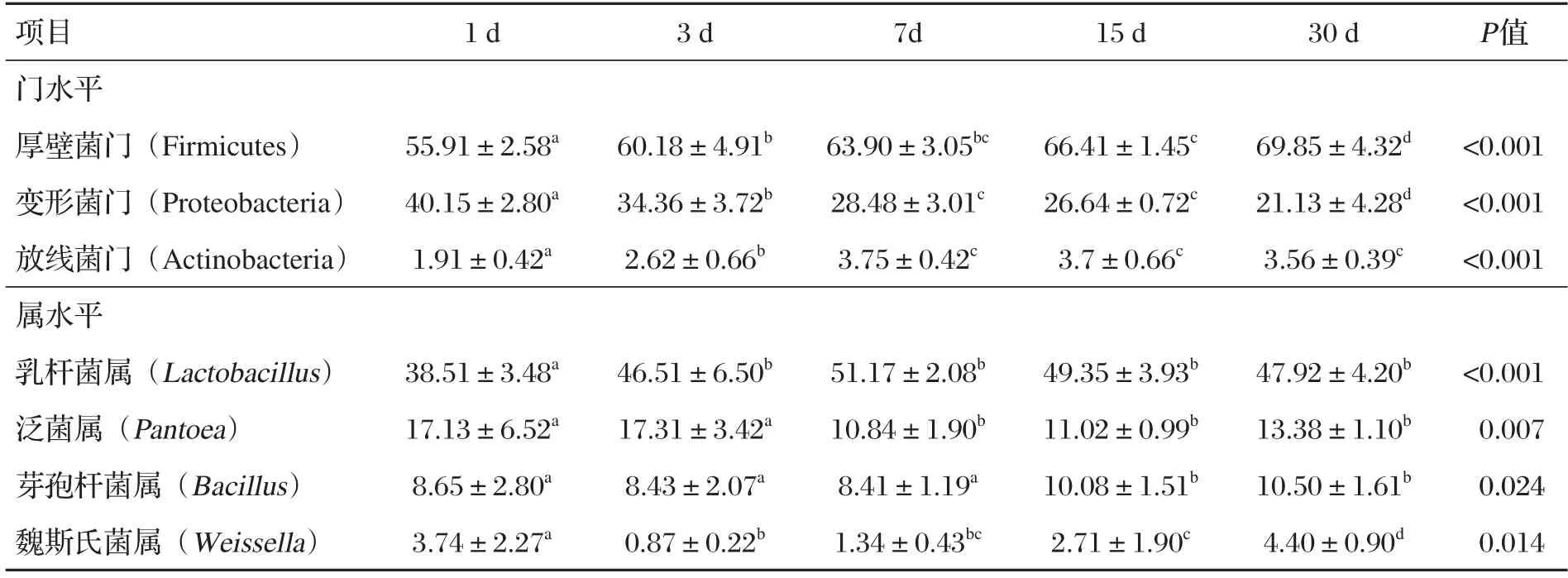
表5 稻草發酵過程中細菌群落的相對豐度 單位:%
由表5、圖1可知,在門水平上,稻草發酵過程中的優勢菌門為厚壁菌門、變形菌門、放線菌門;厚壁菌門隨發酵時間增加而增加;變形菌門隨發酵時間增加而減少;放線菌門呈先增加后減少趨勢,在第7 d時相對豐度最高。在屬水平上,稻草發酵過程中的優勢菌屬為乳桿菌屬、泛菌屬、芽孢桿菌屬、魏斯氏菌屬;發酵第1~3 d,乳桿菌屬和泛菌屬增加,芽孢桿菌屬和魏斯氏菌屬減少;第3~7 d,乳桿菌屬繼續增加達到最高,而泛菌屬、芽孢桿菌屬開始減少,魏斯氏菌屬開始增加;第7~30 d,乳桿菌屬減少,泛菌屬、芽孢桿菌屬和魏斯氏菌屬增加。
2.5 稻草發酵過程中微生物功能預測(見圖2)

圖2 稻草發酵過程中微生物功能預測
用PIRUSt的方法與KEGG數據庫比對預測細菌功能選取6條Level 2層級代謝通路和14條Level 3層級代謝通路繪制豐度圖。由圖2 可知,稻草發酵過程主要涉及的Level 2 層級功能通路包括碳水化合物、氨基酸、輔酶因子和維生素、脂質和能量代謝等;Level 3 層級功能通路包括脂肪酸生物合成、D-丙氨酸代謝和磷酸戊糖途徑等。稻草發酵過程中,溶酶體、鞘脂類代謝、其他多糖降解、糖胺聚糖降解、磷酸鹽和磷酸鹽代謝等途徑存在明顯差異。
3 討論
3.1 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草營養成分的影響
在微貯飼料中加入添加劑有助于乳酸菌的增殖,阻礙需氧菌和厭氧菌的增加,從而降低飼料pH 值,減少DM損失[12]。本研究中,與對照組相比,稻草微貯中單獨添加植物乳桿菌并未顯著降低發酵pH值;與對照組和植物乳桿菌組相比,地衣芽孢桿菌與植物乳桿菌復合后顯著降低了稻草發酵pH值,可能與地衣芽孢桿菌獨特的生物氧捕獲機制快速創造了厭氧環境有關[8]。pH 值是評估發酵飼料發酵程度的重要參數,較低的pH值可確保更好的有氧穩定性,并抑制進一步發酵,pH值降至低于4.5,有助于抑制病原微生物。范子豪[13]研究發現,地衣芽孢桿菌在酸性環境中可以正常生長,在有氧狀態下的生長速度遠大于無氧狀態,在無氧狀態下可以利用營養物質產生乳酸。因此,在微貯飼料中加入地衣芽孢桿菌可以快速消耗氧氣,有助于乳酸菌生長,產生的乳酸可以快速降低發酵pH值。
Mara 等[14]研究發現,地衣芽孢桿菌具有很強的降解纖維的能力,具有促進ADF 分解的作用。本試驗中,添加地衣芽孢桿菌與植物乳桿菌組微貯稻草的NDF和ADF含量均低于對照組,原因可能是地衣芽孢桿菌與植物乳桿菌在降解植物纖維成分方面具有協同作用。NDF 和ADF 有助于生成可溶性碳水化合物,是一種良好的乳酸菌生長促進劑底物,可促進更多乳酸產生,促進發酵過程。此外,結構碳水化合物組分的分解可以提高微貯飼料的消化率。
3.2 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草發酵過程中菌群變化規律的影響
微貯飼料微生物是影響其發酵品質的關鍵因素,原料表面附著的微生物還是外源添加的微生物在微貯發酵過程中均對微生物群落的演替起重要作用[15]。本試驗中,稻草微貯細菌群落的Shannon、Chao1 和Ace 指數在發酵7 d時最高,表明此時稻草發酵中細菌群落豐富度和多樣性最高。在本研究中,厚壁菌和變形菌是稻草微貯飼料中豐度最高的前兩個門,與之前的研究結果一致[16-19]。厚壁菌是革蘭氏陽性菌,主要包括產孢子菌、不產孢子菌和支原體菌,能夠降解大分子物質,如纖維素、淀粉、蛋白質等,增加厚壁菌的豐度會提高產酸能力,從而降低pH值,進一步分解ADF[20]。Li等[21]研究發現,使用乳酸菌和糖蜜對本地牧草進行微貯,在微貯的早期階段(前7 d),乳酸菌的相對豐度增加,隨著微貯時間的延長,細菌群落的豐富度下降。Ni 等[22]研究發現,大豆在微貯前7 d乳酸菌數量顯著增加,在14 d后減少。本研究中,稻草在微貯前7 d,乳桿菌屬豐度隨著發酵時間的增加而增加,可能是因為地衣芽孢桿菌與植物乳桿菌復合微貯降低了pH值,抑制了有害微生物的生長,促進了乳桿菌的生長。添加植物乳桿菌可以直接增加乳桿菌屬的豐度,而地衣芽孢桿菌可以通過其獨特的生物氧捕獲機制,快速創造厭氧環境,促進乳桿菌屬的快速生長繁殖[23]。魏斯氏菌是發酵飼料中最常見的異型發酵細菌之一,能夠產生與乳桿菌屬等量的有機酸。研究表明,泛菌屬、芽孢桿菌屬和魏斯氏菌屬等是發酵飼料中的主要菌屬,但其豐度與環境和地理位置密切相關[24-26]。
3.3 地衣芽孢桿菌與植物乳桿菌復合微貯對稻草發酵過程中菌群功能預測的影響
乳酸菌將稻草中可用的碳水化合物發酵為丙酮酸,在厭氧條件下丙酮酸在胞質中還原生成乳酸,完成糖的無氧氧化。當飼料中的葡萄糖和果糖水平隨著植物呼吸或微生物利用而下降時,只有多糖降解可以增加葡萄糖含量。許冬梅[27]研究發現,添加布氏乳桿菌后,玉米青貯發酵中期糖胺聚糖降解上調,且主要貢獻微生物為乳酸桿菌屬。本研究發現,在發酵第7 d時糖胺聚糖降解途徑顯著上調,此時乳酸桿菌屬達到最高。本研究中,發酵第7 d 時,D-精氨酸和D-鳥氨酸代謝途徑開始上調,表明此時氨基酸的脫氨作用加強,生成的酮酸開始作為菌群發酵的碳源。Keshri等[28]研究發現,氨基酸代謝水平可能反映微貯飼料中細菌種群重新合成氨基酸的能力。磷酸鹽和磷酸鹽代謝途徑的變化可能是由乳酸菌引起,乳酸菌發酵產生的有機酸可溶解磷復合物而具有解磷作用[29]。
乳酸菌和低氧壓力產生的有機酸會阻止許多霉菌和有害細菌的生長。霉菌和有害細菌在發酵飼料生長,對線粒體功能產生毒性。Rezabakhsh 等[30]研究發現,線粒體和溶酶體功能障礙,細胞內腺嘌呤核苷三磷酸(ATP)耗竭和過多的活性氧(ROS)生成是霉菌產生毒素的機制。ROS 生成的增加可以使呼吸鏈和三羧酸循環受到抑制,破壞細胞結構[31]。硫辛酸是一種二硫醇,可通過其兩個巰基部分保護機體免受氧化應激。研究表明,硫辛酸及其還原形式二氫硫辛酸可直接清除ROS 和活性氮(RNS),保護細胞免受氧化應激[32-34]。本研究中,硫辛酸的代謝在發酵7 d上調,15 d時開始下調。鞘脂可調節生物膜的生物物理特性,鞘脂類代謝的大部分路徑都發生在溶酶體中。溶酶體中鞘脂及其代謝產物會抑制脂質循環,這直接影響細胞膜(包括線粒體內膜)的脂質組成[35]。本研究中,溶酶體新陳代謝和鞘脂類代謝途徑在發酵7 d上調,15 d時開始下調。本試驗條件下,稻草發酵的7~15 d,硫辛酸、溶酶體和鞘脂類的代謝與霉菌的變化有關。Rocchetti 等[36]研究基于霉菌毒素污染的玉米青貯飼料飼喂奶牛后牛乳中代謝組的變化,結果表明,鞘脂以及嘌呤和嘧啶衍生的代謝物是受影響最大的化學類別。許多研究表明,霉菌毒素污染的飼料會破壞鞘脂類代謝[37-38]。
4 結論
本研究條件下,植物乳桿菌復合地衣芽孢桿菌微貯稻草發酵優于單獨添加植物乳桿菌的效果。

