離子選擇性電極法測定工業碳酸鈉中氯化物的研究
陳魏,王家珍,張及亮,李智,余雅芹
(1.湖北中檢檢測有限公司,湖北 武漢 430056;2.中國檢驗認證集團湖北有限公司,湖北 武漢 430022)
0 引言
工業碳酸鈉(Na2CO3),又稱為純堿,國際貿易中又名蘇打或堿灰。工業碳酸鈉是用于玻璃制造的重要化工原料[1]。氯化鈉是碳酸鈉的主要雜質之一,由于其生產工藝上的原因,或多或少都會含有少量氯化物(以氯化鈉計)。而氯化鈉是高強度離子晶體,其熔點和沸點分別達到800 ℃和1413 ℃,如果含量太高會影響玻璃的熔融反應過程,造成玻璃的品質下降[2-3],因此必須準確測定工業碳酸鈉中的氯化物含量。
目前測定碳酸鈉中氯化物的方法主要有離子選擇電極法、電位滴定法和汞量法等。國家標準GB/T 210—2022 《工業碳酸鈉》對氯化物的測定提供了兩種可選方法,即汞量法和電位滴定法[4]。汞量法由于使用到了劇毒化學藥品硝酸汞,它對實驗人員及生態環境有一定程度的危害,且滴定操作較為繁瑣耗時,滴定終點的判斷受個人主觀影響較大,故該方法的使用仍存在一定的局限性;而電位滴定法的操作同樣較為繁瑣,在實驗過程中,需要記錄大量的電位值數據,滴定管很難全程控制每次的滴定體積控制在0.10 mL,且滴定終點需通過計算電位值的突躍來判斷,一旦出現偏差,就會對結果的準確性產生不利影響。而離子選擇電極法具有操作簡單、安全無害、高效準確等優點,可對樣品直接進行測定,目前已被廣泛的運用于氯化物的測定[5-6]。因此,本文建立離子選擇電極法來測定工業碳酸鈉中的氯化物含量。
1 實驗部分
1.1 方法原理
試樣在pH值在5~6之間情況下,用乙酸鹽緩沖溶液調節總離子強度,以氯離子選擇電極和飽和甘汞電極測量電位。由于電極對溶液中的氯離子有良好的選擇性,且試樣中氯離子含量的對數值與電極電位存在線性關系,符合能斯特方程,通過測定樣品中氯離子的電位值,即可計算出其氯離子濃度。
1.2 主要儀器與試劑
離子計(型號XSJ-216F),測量精度0.01 mV,上海雷磁;氯離子選擇電極(型號PCl-1-01)和飽和甘汞電極(型號217),上海雷磁;電子天平(型號AUW120),精度0.0001 g,日本島津;控溫電磁攪拌器(型號GH-09),上海國華。
碳酸鈉、硝酸、冰乙酸、硝酸鉀均為優級純,國藥集團;基準碳酸鈉,主含量為99.95%~100.05%,天津科密歐;水中氯離子溶液標準物質[GBW(E)082683]:1000 μg/mL,北京壇墨質檢;實驗所用水均為電阻率18.2 MΩ·cm的超純水。
1.3 實驗步驟
1.3.1 標準曲線的配制及測定
用單標移液管吸取水中氯離子溶液標準物質10.00 mL,轉移至100 mL容量瓶中,用超純水稀釋至刻度,此溶液為氯離子標準儲備溶液,濃度為100 μg/mL。用刻度移液管分別移取0.0、2.5、5.0、10.0、25.0 mL氯離子標準儲備溶液和5.0、25.0 mL水中氯離子溶液標準物質至7個50 mL容量瓶中,再分別加入5 mL乙酸鹽緩沖溶液(100 g硝酸鉀和50 mL乙酸,溶解后用氫氧化鈉溶液調節pH值為5~6),用超純水稀釋至刻度,搖勻,即可得到氯離子標準工作溶液,其濃度分別為0、5、10、20、50、100、500 μg/mL。
將上述氯離子標準工作溶液分別轉移至100 mL燒杯中,將預熱半小時以上的氯離子選擇電極和飽和甘汞電極,按照低濃度到高濃度的順序,依次插入到氯離子標準工作溶液中(需使電極液膜充分浸入)。加入磁力攪拌子,用電磁攪拌器進行勻速攪拌,避免產生的氣泡接觸到電極。待讀數穩定(1 min內電極電位小于0.2 mV)[7]后,分別記錄電位值。每次測定前,需用超純水清洗電極,并用濾紙擦干。以氯離子濃度的對數(logC)為橫坐標,以待測溶液的電位值為縱坐標,在半對數坐標系上建立標準曲線。
1.3.2 樣品溶液的制備及測定
稱取約2 g(精確至0.0001 g)已于270~300 ℃干燥至恒重的樣品置于50 mL容量瓶中。加入5 mL硝酸溶液(1+1),并根據樣品情況用硝酸溶液(1+1)或氫氧化鈉溶液(100 g/L)調節pH值為5~6左右,加入5 mL乙酸鹽緩沖溶液,用水稀釋至刻度,搖勻。
將制備的上述樣品溶液轉移至100 mL燒杯中,插入氯離子選擇電極和飽和甘汞電極,加入磁力攪拌子,用電磁攪拌器進行勻速攪拌,避免產生的氣泡接觸到電極。待讀數穩定后,記錄樣品溶液的電位值。注意樣品溶液和氯離子標準工作溶液的溫差不宜超過1 ℃。根據樣品溶液測得的電位值,通過標準曲線方程,計算氯離子含量。
1.3.3 結果計算
氯化物的質量分數(以NaCl計)w,數值以%表示,按下列公示計算:
式中:C為由校準曲線測得樣品中的氯離子含量(μg/mL);V為樣品溶液定容的體積(mL);1.66為氯離子濃度換算成氯化鈉濃度的換算系數;m為樣品稱樣量(g)。
2 結果與討論
2.1 標準曲線的繪制
根據1.3.1完成氯離子標準工作溶液的測定,每個濃度的標準工作溶液的測試數據詳見表1。以氯離子濃度的對數(lgC)為橫坐標,以待測溶液的電位值為縱坐標,在半對數坐標系上建立標準曲線,詳見圖1。曲線方程為:y=-56.47x+177.6,相關系數R=0.9999。從以上數據可以得出,在0~500 μg/mL的濃度范圍內,電極對氯離子有良好的響應,并且能夠滿足各種品級碳酸鈉中氯化物的檢測需求。

圖1 氯離子標準曲線
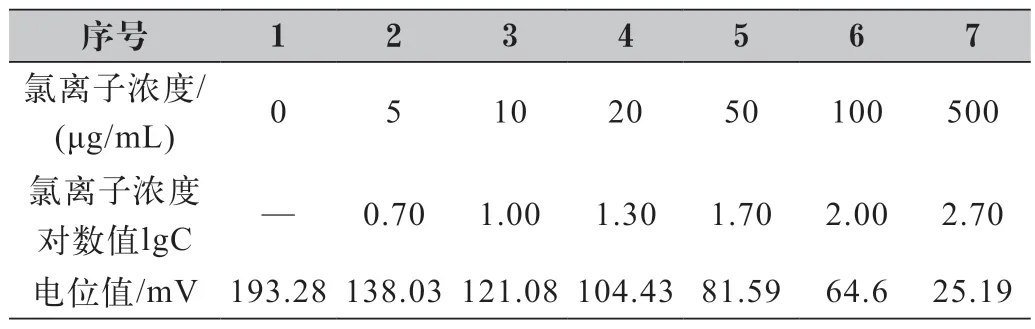
表1 氯離子標準工作溶液測試數據
2.2 pH值對檢測結果的影響
按照1.3.1步驟,配制7組濃度為10 μg/mL的氯離子標準工作溶液,在定容前,用硝酸溶液(1+1)或氫氧化鈉溶液(100 g/L)調節上述7個氯離子標準工作溶液的pH值依次為4.0±0.1、5.0±0.1、6.0±0.1、7.0±0.1、8.0±0.1、9.0±0.1和10.0±0.1,然后分別進行測試,每組數據測定6次,以平均值為最終結果,測試數據詳見表2。從這些數據可以看出,氯離子在pH值為4~6的范圍內變化不大,在pH值為5~6的范圍內最接近理論值,而在pH值為8~10的堿性條件下,與實際值則相差較大。因此pH值控制在5~6的范圍內最為適宜。

表2 不同pH值的對測試結果的影響(n=6)
2.3 溫度對檢測結果的影響
按照1.3.1步驟,配制6組濃度為10 μg/mL的氯離子標準工作溶液,在測試前,用控溫電磁攪拌器將待測氯離子標準工作溶液的溫度維持在15、20、25、30、35、40 ℃,然后分別進行測試,每組數據測定6次,以平均值為最終結果,測試數據詳見表3。實驗結果表明,溫度對測試結果有一定的影響,隨著溫度的升高,氯離子測試濃度隨之升高,因此為了保證結果的準確性,在測定標準溶液和樣品時,要保證測量時段溫度恒定,前后溫差最好控制在±5 ℃范圍內,就可以有效抵消由溫度變動對結果造成的影響。
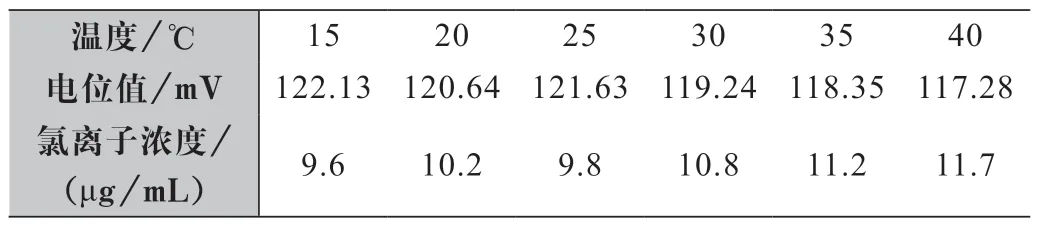
表3 不同溫度對測試結果的影響(n=6)
2.4 檢出限的測定
參考HJ 168—2020 《環境監測分析方法標準制修訂技術導則》[8]附錄A.1.4離子選擇電極法要求,檢出限的確定準則為:在沒有前處理的情況下,當校準曲線直線部分外延的延長線與通過空白電位且平行于濃度軸的直線相交時,其交點所對應的濃度值即為該離子選擇電極法的檢出限。稱取2 g基準碳酸鈉作為空白樣品,按照1.3.2的步驟對空白樣品平行測定6次,其平均電位值為193.28 mV,將此電位值在標準曲線圖上標記,沿該電位點作平行于 x 軸(氯離子濃度)的直線交于曲線直線部分延長線對應的濃度值為0.53 μg/mL,當碳酸鈉稱樣量為2 g時,本方法的檢出限為0.0022%。
2.5 精密度和回收率的測定
考慮到樣品基準效應,將基準碳酸鈉作為空白加標樣品,設置3組加標水平,在2 g基準碳酸鈉中分別加入1.50、5.00、15.0 mL水中氯離子溶液標準物質(1000 μg/mL),配制成氯離子濃度分別為0.124%、0.415%、1.245%的三組樣品,按照1.3.2的步驟對加標樣品進行測試,每組樣品平行測定6次。得出的精密度和準確度數據詳見表4,三組加標樣品測定的相對標準偏差在0.99%~2.41%的范圍內,加標回收率在96.5%~99.3%的范圍內。滿足GB/T 27417—2017《合格評定 化學分析方法確認和驗證指南》[9]中對精密度和回收率的要求。
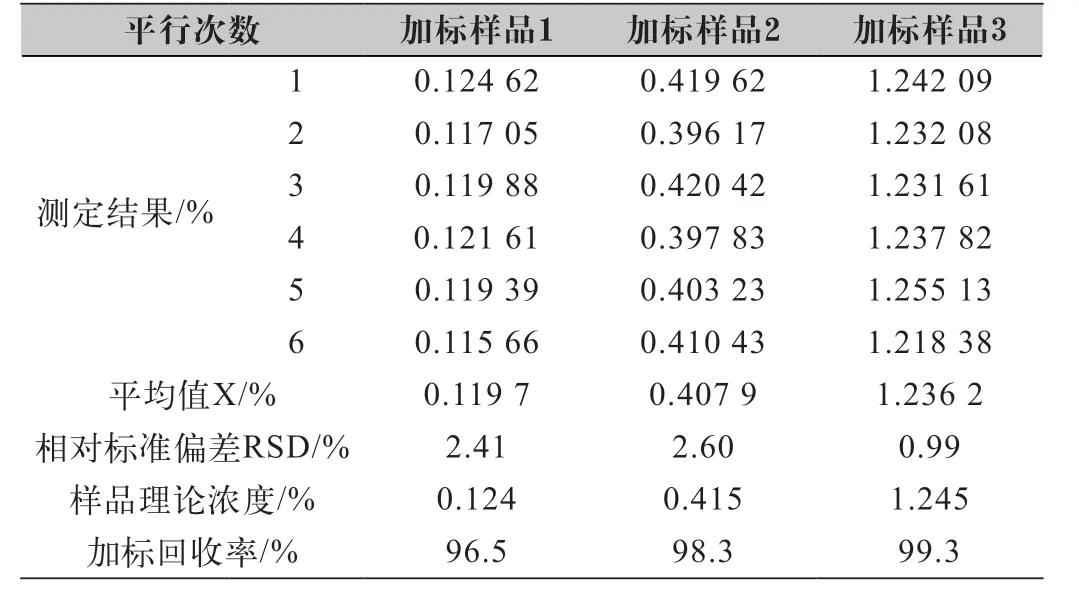
表4 配制樣品精密度和準確度測試結果
3 結語
本文建立的氯離子選擇電極-標準曲線法可以有效測定工業碳酸鈉中的氯化物含量,并能夠滿足各種品級碳酸鈉中氯化物的檢測需求。同時還對影響實驗結果的因素,如pH值和溫度對結果的影響進行探討,并給出了最適條件。另外通過方法學實驗表明,本方法特異性強、線性范圍寬、檢出限低、精密度好、回收率高,為工業碳酸鈉中氯化物的測定提供了一種可供選擇的技術方法。

