靶向治療聯(lián)合化療對轉移性結直腸癌患者的效果及腫瘤標志物、Th1/Th2細胞因子的影響
陳香梅 劉太鋒
結直腸癌為臨床常見惡性腫瘤。其發(fā)病率在所有惡性腫瘤中位居第三,死亡率排名第四[1]。現(xiàn)階段,臨床上常采用外科手術治療結直腸癌,如腹腔鏡手術,因具有創(chuàng)傷小、術后恢復快等優(yōu)勢而得到廣泛應用,但該手術僅適合早期結直腸癌患者,對于晚期轉移性結直腸癌(metastatic colorectal cancer,mCRC)患者,其效果并不理想[2,3]。臨床針對mCRC患者以化療為主,并為了進一步增強治療效果,建議聯(lián)合靶向抗腫瘤單克隆抗體類藥物西妥昔單抗或貝伐珠單抗。據此,本研究選取106例mCRC患者作為研究對象,旨在探討西妥昔單抗和貝伐珠單抗聯(lián)合化療治療mCRC的療效及對腫瘤標志物、Th1Th2細胞因子的影響。
1 資料與方法
1.1 一般資料 選取2017年1月至2020年7月于本院接受診治且隨訪至2022年7月的106例mCRC患者作為研究對象,按照治療方法不同分為A組(予以西妥昔單抗聯(lián)合化療治療,n=21),B組(予以貝伐珠單抗聯(lián)合化療治療,n=42),C組(予以單純化療,n=43)。A組中,男11例,女10例;年齡35~68歲,平均(50.45±2.78)歲;病程3~5年,平均(4.02±1.45)年。B組中,男23例,女21例;年齡36~68歲,平均(50.51±2.74)歲;病程2~5年,平均(3.85±1.28)年。C組中,男23例、女20例;年齡36~69歲,平均(50.62±2.84)歲;病程3~6年,平均(4.07±1.41)年。3組一般資料比較,差異無統(tǒng)計學意義(P>0.05)。
1.2 納入與排除標準
1.2.1 納入標準:①經臨床確診為結直腸癌,TNM分期為Ⅳ期;②左半結直腸癌行基因檢測,西妥昔單抗組RAS、BRAF為野生型;③認知功能正常;④年齡>18歲;⑤預期生存時間>6個月。
1.2.2 排除標準:①已出現(xiàn)遠處轉移或其他惡性腫瘤;②對化療藥物耐藥者或過敏者;③患有嚴重心功能不全等疾病。
1.3 方法 A組患者均選擇含氟尿嘧啶或其衍生物的化療方案治療,具體為mFOLFOX6(奧沙利鉑85 mg/m2,靜脈滴注2 h,第1天;亞葉酸鈣400 mg/m2,靜脈滴注2 h,第1天;5-氟尿嘧啶400 mg/m2,靜脈推注,第1天,然后總量2 400 mg/m2持續(xù)泵入46~48 h,每2周重復);CapIRI(伊立替康180 mg/m2,靜脈滴注90 min,第1天;卡培他濱1 000 mg/m2,口服,2次/d,第1~7天,每2周重復);或FOLFIRI(伊立替康180 mg/m2,靜脈滴注90 min,第1天;亞葉酸鈣400 mg/m2,靜脈滴注2 h,第1天;5-氟尿嘧啶400 mg/m2,靜脈推注,第1天,然后總量2 400 mg/m2持續(xù)泵入46~48 h,每2周重復。其中,A組予以西妥昔單抗聯(lián)合化療,西妥昔單抗500 mg/m2,靜脈輸注,第1天,輸注時間超過2 h,每2周重復。B組予以貝伐珠單抗聯(lián)合化療,貝伐珠單抗5 mg/kg靜脈輸注,第1天,每2周重復。C組予以單純予以mFOLFOX6或CapIRI或FOLFIRI方案化療療。其中,西妥昔單抗和貝伐珠單抗先于化療藥物使用,共治療8個周期。
1.4 觀察指標
1.4.1 療效判定:參照2007年國家工作組織標準[4]進行評估:完全緩解(CR):病灶消失,無新病灶出現(xiàn),持續(xù)1個月;部分緩解(PR):病灶縮小率≥50%,持續(xù)1個月;疾病穩(wěn)定(SD):病灶縮小率<50%或擴大率≤25%;疾病進展(PD):病灶擴大率≥25%;總有效率=(CR+PR)/總例數×100%。
1.4.2 實驗室指標:于治療前和治療8個周期后采集患者靜脈血,采用電化學發(fā)光分析法測定甲胎蛋白(Alpha fetoprotein,AFP)、癌胚抗原(Carcinoembryonic antigen,CEA)、糖類抗原72-4(Carbohydrate antigen 72-4,CA72-4)、糖類抗原125(Carbohydrate antigen125,CA125)、糖類抗原199(Carbohydrate antigen199,CA199),選擇羅氏E-801分析儀,檢測試劑采用上海羅氏診斷公司,操作流程由我院檢驗師嚴格按照說明書進行;采用流式細胞計數法測定白介素-2(interleukin-2,IL-2)、干擾素-γ(interferon-gamma,INF-γ)、IL-4、IL-10,選擇貝克曼流式細胞儀,檢測試劑采用青島瑞斯凱爾公司,操作流程由我院檢驗師嚴格按照說明書進行。
1.4.3 不良反應:根據美國國立癌癥研究所常見毒性分級標準5.0版(NCI-CTCAE5.0)[5]對化療后的毒副反應進行分級,記錄患者化療期間有無出現(xiàn)Ⅰ~Ⅳ級骨髓抑制、肝功能損害、胃腸道反應、皮疹、心臟毒性;其中骨髓抑制的表現(xiàn)包括白細胞、血紅蛋白、血小板計數下降等;胃腸道表現(xiàn)包括惡心、嘔吐等;肝功能損害包括血清轉氨酶升高。
1.4.4 生存狀況:對患者進行為期2年的隨訪,記錄其生存率和生存時間。

2 結果
2.1 3組臨床療效比較 3組總有效率比較,差異有統(tǒng)計學意義(P<0.05);A組和B組的有效率高于C組(P<0.05)。見表1。

表1 3組臨床療效比較 例(%)
2.2 3組腫瘤標志物比較 治療前,3組AFP、CEA、CA72-4、CA125、CA199比較,差異無統(tǒng)計學意義(P>0.05);治療后,A、B組的AFP、CEA、CA72-4、CA125、CA199低于C組(P<0.05)。見表2。
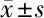
表2 3組腫瘤標志物比較
2.3 3組Th1/Th2細胞因子比較 治療前,3組IL-2、INF-γ、IL-4、IL-10比較,差異無統(tǒng)計學意義(P>0.05);治療后,A組和B組的IL-2、INF-γ高于C組,而IL-4、IL-10低于C組(P<0.05)。見表3。
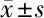
表3 3組Th1/Th2細胞因子比較 ng/L,
2.4 3組不良反應比較 在A組中,出現(xiàn)不良反應共11例,發(fā)生率52.38%,未出現(xiàn)任何不良反應患者10例;其中出現(xiàn)Ⅰ級不良反應患者共10例,兼具骨髓抑制、肝功能損害、胃腸道反應共7例,兼具骨髓抑制、皮疹、心臟毒性共2例,單純出現(xiàn)骨髓抑制共1例;出現(xiàn)Ⅱ級不良反應患者共1例,兼具骨髓抑制、皮疹共1例。在B組中,出現(xiàn)不良反應共23例,發(fā)生率54.76%,未出現(xiàn)任何不良反應患者19例;其中出現(xiàn)Ⅰ級不良反應患者共15例,兼具骨髓抑制、肝功能損害、胃腸道反應、皮疹共10例,兼具骨髓抑制、胃腸道反應共1例,兼具胃腸道反應、皮疹共1例,兼具心臟毒性、骨髓抑制共2例、兼具胃腸道反應和心臟毒性共2例;出現(xiàn)Ⅱ級不良反應患者共4例,兼具胃腸道反應、皮疹共1例、兼具肝功能損害、心臟毒性共1例,單純出現(xiàn)胃腸道反應共1例,單純出現(xiàn)皮疹共1例。在C組中,出現(xiàn)不良反應共36例,發(fā)生率83.72%,未出現(xiàn)任何不良反應患者7例;其中出現(xiàn)Ⅰ級不良反應患者共32例,兼具骨髓抑制、肝功能損害、胃腸道反應共17例,兼具骨髓抑制、皮疹、心臟毒性共9例,單純出現(xiàn)骨髓抑制共6例;出現(xiàn)Ⅱ級不良反應患者共4例,單純出現(xiàn)骨髓抑制和皮疹各2例。3組不良反應發(fā)生率比較,差異有統(tǒng)計學意義(t=7.953,P=0.019)。見表4。

表4 3組毒副反應發(fā)生率比較 例
2.5 2年生存率和生存時間比較 A、B組2年生存率、生存時間高于C組(P<0.05)。見表5,圖1。

圖1 2組生存曲線分析

表5 3組2年生存率和生存時間比較
3 討論
臨床對于mCRC患者多采用化療手段治療,即利用化學藥物阻止癌細胞增殖、浸潤、轉移,并達到殺滅癌細胞的目的[6]。mFOLFOX6方案是由奧沙利鉑、5-氟尿嘧啶、亞葉酸鈣藥物組成,CapIRI方案由伊立替康、卡培他濱組成,FOLFIRI方案由伊立替康、5-氟尿嘧啶、亞葉酸鈣組成,為臨床治療mCRC的常用化療方案。其中,奧沙利鉑為二氨基環(huán)己烷的鉑類復合物,通過阻斷癌細胞DNA復制和轉錄,使癌細胞凋亡[7]。5-氟尿嘧啶則是通過抑制胸苷酸合成酶,破壞癌細胞DNA、RNA合成[8]。亞葉酸鈣具有增強5-氟尿嘧啶抗癌活性作用,能通過提高三元復合物穩(wěn)定性,增強5-氟尿嘧啶對胸苷酸合成酶的抑制作用,而胸苷酸合成酶的抑制又能通過阻斷脫氧嘧啶核苷酸轉化為胸腺嘧啶核苷酸,干擾癌細胞DNA、RNA合成[9]。伊立替康為喜樹堿類似物,針對其藥理作用分析,發(fā)現(xiàn)該藥物是通過抑制核拓撲異構酶I,干擾DNA合成及有絲分裂。但經臨床調查發(fā)現(xiàn),并不是所有患者采用上述化療方案治療均能獲得較好的臨床效果[10],故而提出聯(lián)合靶向藥物治療,并已成為臨床治療mCRC的新趨勢。
貝伐珠單抗和西妥昔單抗均屬于靶向抗腫瘤單克隆抗體類藥物。其中,貝伐珠單抗是一種來源于血管內皮生長因子(vascular endothelial growth factor,VEGF)的重組人源化IgG1單克隆抗體,針對其作用機制分析,發(fā)現(xiàn)貝伐珠單抗是通過競爭性結合VEGF,阻止表面受體其與VEGF結合而降低其活性,抑制新生血管生成[11]。據臨床研究發(fā)現(xiàn),新生血管為腫瘤細胞組織生長和轉移的基礎,抑制VEGF表達水平對抗腫瘤侵襲、轉移具有促進作用[12];故而認為抑制VEGF表達可作為治療結直腸癌的新靶點。此外,貝伐珠單抗還具有破壞腫瘤成熟和滲漏血管作用,通過促使腫瘤血管正常化,提高藥物利用率及降低耐藥性[13]。西妥昔單抗是人鼠嵌合型的單克隆抗體,針對其作用機制分析,發(fā)現(xiàn)該藥物是通過競爭性抑制表皮生長因子受體(EGFR)與內源性配體結合,阻斷EGFR信號通路傳導,抑制腫瘤細胞增殖,并誘導其凋亡[14]。有文獻報道,EGFR高表達是影響結直腸癌患者的預后的危險因素[15]。而抑制EGFR表達對阻止腫瘤細胞增殖、遷移及血管生長具有重要意義。與常規(guī)化療相比,靶向抗體類藥物具有靶向抗腫瘤作用,可提高mCRC對放化療的敏感性,達到精準靶向治療,聯(lián)合化療可以明顯延長mCRC的生存時間。
基于上述兩種靶向藥物療效分析,本研究結果顯示,西妥昔單抗和貝伐珠單抗聯(lián)合化療治療的A組和B組,其總有效率、2年生存率及生存時間均高于單純化療的C組。貝伐珠單抗有效減少或者終止腫瘤新生血管的形成;在RAS、BRAF野生型的左半結直腸癌中,EGFR高表達或異常表達,西妥昔單抗抑制EGFR,進而抑制腫瘤細胞增殖、生長和轉移[16],且西妥昔單抗可恢復耐藥細胞對化療藥物的敏感性,可與放化療聯(lián)合發(fā)揮協(xié)同抗腫瘤作用。AFP是一種酸性糖蛋白,在正常情況下其含量極低,但受腫瘤細胞生長、浸潤、轉移等影響,其表達顯著上升,故而臨床將其作為診斷結直腸癌的輔助指標。CEA為腫瘤細胞的黏附分子,當細胞發(fā)生癌變時,CEA受其調控可大量產生,并釋放入血,導致血清CEA增多;而CEA表達的上升又能通過干擾細胞的正常黏附力,增加癌細胞的移動性,加快惡性腫瘤增殖和轉移。因此臨床認為動態(tài)檢測其水平變化,對診斷惡性腫瘤和監(jiān)測腫瘤復發(fā)或轉移具有重要意義。CA199、CA72-4、CA125均屬于糖類蛋白,受腫瘤細胞增殖、浸潤影響,其表達水平顯著升高。在本研究結果中可見,3組患者治療前的血清AFP、CEA、CA72-4、CA125、CA199水平呈異常升高趨勢。但經治療后其表達水平明顯下降,提示西妥昔單和貝伐珠單抗聯(lián)合化療治療mCRC更有效。
據臨床研究發(fā)現(xiàn),結直腸癌患者多伴有Th1/Th2免疫漂移,為機體細胞免疫紊亂常見類型。即是指Th1細胞向Th2細胞漂移,使Th2細胞因子占主導位置,通過抑制Th1細胞介導的免疫功能,降低機體抗腫瘤作用,導致腫瘤細胞免疫逃逸。其中,IL-2、INF-γ由Th1細胞分泌,能通過誘導多種免疫細胞分化,介導機體細胞免疫功能[17]。IL-4、IL-10由Th2細胞分泌,其在抑制機體免疫功能、誘導炎性反應中具有重要作用,同時也參與了腫瘤的發(fā)生發(fā)展[18]。上述已說到受腫瘤細胞因子,患者可出現(xiàn)免疫功能紊亂情況,即表現(xiàn)為Th2細胞因子表達上調,Th1細胞因子表達下降。本研究結果顯示,3組患者治療前的IL-2、INF-γ處于異常下降狀態(tài),IL-4、IL-10處于異常升高狀態(tài),證實了上述說法的可靠性。但經治療后,上述指標均有所變化,本研究中,A組和B組的IL-2、INF-γ顯著高于C組,IL-4、IL-10顯著低于C組,提示靶向單抗類藥物西妥昔單和貝伐珠單抗聯(lián)合化療對改善結直腸癌患者免疫功能效果更為理想,可能與西妥昔單和貝伐珠單抗抑制腫瘤細胞增殖,誘導其凋亡效果更為顯著有關,通過降低腫瘤細胞對機體免疫功能影響,糾正Th1/Th2免疫漂移。且安全性較高,不良反應多發(fā)于Ⅰ~Ⅱ級,
綜上所述,西妥昔單抗和貝伐珠單抗分別聯(lián)合化療治療mCRC具有較為理想效果,可有效降低腫瘤標志物,改善免疫功能及延長患者生存時間。

