電針聯合延胡索水提物對絕經后骨質疏松大鼠的改善作用
溫志剛 路帥 馬欣
1. 河北省中醫院骨傷二科,河北 石家莊 050000
2.石家莊市中醫院,河北 石家莊 050000
3.河北省第八人民醫院,河北 石家莊 050000
絕經后骨質疏松癥是一種被認為與卵巢激素缺乏相關的骨質疏松癥,是迄今為止與年齡相關的骨質流失的最常見原因。目前西醫主要以雌激素替代療法為主,但存在不良反應多、致癌風險高等缺點。電針作為一種特定的中醫療法,是在普通針灸的基礎上使用現代技術來模擬醫者完成相應的運針并給予患者長時間規律的電刺激,具有操作方便、無副作用等優點,在臨床上得到廣泛應用[1]。電針在骨質疏松癥中的治療效果已被大量臨床和動物實驗研究所證實。將針灸療法與藥物治療結合起來已成為目前臨床上治療骨質疏松癥的研究熱點。延胡索是罌粟科細紫堇屬植物的干燥塊莖,也被稱為“元胡”。作為傳統中藥,延胡索有行氣活血、化瘀通絡的功效。包含延胡索的中藥制劑已被用于治療腰椎間盤突出、風濕性關節炎和頸椎病[2]。現代藥理學研究[3]發現,延胡索的主要化學成分是生物堿,具有抗炎、抗腫瘤、抗凋亡和鎮痛等多種生物學作用。Ling等[4]發現,延胡索提取物通過抑制細胞凋亡來減少心肌缺血再灌注大鼠的心臟功能。Wang等[5]發現,延胡索提取物巴馬汀通過抑制炎癥小體的活化和半胱天冬酶-1的形成來減輕痛風性關節炎的炎癥反應。然而,延胡索水提物在骨質疏松癥中的作用及相關機制尚未明確。本研究探討了電針聯合延胡索水提物對骨質疏松大鼠的保護作用,并初步探究其可能的潛在機制。
1 材料與方法
1.1 材料
1.1.1實驗動物:48只成年雌性SD大鼠購自購自華蘭生物工程股份有限公司[許可證號SYXK(豫)2018-0014],體重300~330 g,8~10周齡。將大鼠飼養在標準實驗室條件下,自由獲取食物和水,室溫為22 ℃,濕度約為45 % ~ 55 %。所有實驗程序均經本院倫理委員會批準,并按照國家有關規定進行。動物倫理審查號為(院科倫審:AEWC -2001281)。
1.1.2藥物及試劑:延胡索中藥飲片購自張仲景大藥房,經河南食品藥品檢驗所檢驗為真品。IP細胞裂解液(貨號P0013)、蛋白濃度測定試劑盒(貨號P0010)購自碧云天生物技術研究所;抗GSK-3β抗體(貨號ab93926)、抗DVL抗體(貨號ab233003)、抗Runx2抗體(貨號ab236639)、抗Wnt3a抗體(貨號ab219412)、抗β-catenin抗體(貨號ab68183)、抗GAPDH抗體(貨號ab9485)購自美國Abcam公司。骨保護素(Osteoprotegerin,OPG;貨號MOP00)和核因子-κB配體的受體激活劑(Receptor activator of nuclear factor-κB ligand,RANKL;貨號462-TR)酶聯免疫吸附試劑盒購自美國R&D Systems公司;酶聯免疫檢測儀(DNM9606)購自北京普朗新技術有限公司。SDZ-III型華佗牌電子針療儀購自蘇州醫療用品廠有限公司;MEDIX90雙能X線骨密度檢測儀購自法國奧斯托公司。
1.2 方法
1.2.1延胡索有效成分的提取及處理:延胡索提取物采用水提方式制備,方法如下:取延胡索中藥飲片500 g,加入1 800 mL水,大火燒開后浸泡1 h,再次大火燒開后,文火煮1 h。靜置冷卻至室溫后,經100目濾布過濾收集水提液。經高效液相色譜(HPLC)分析發現,延胡索水提取物的主要成分詳見圖1。
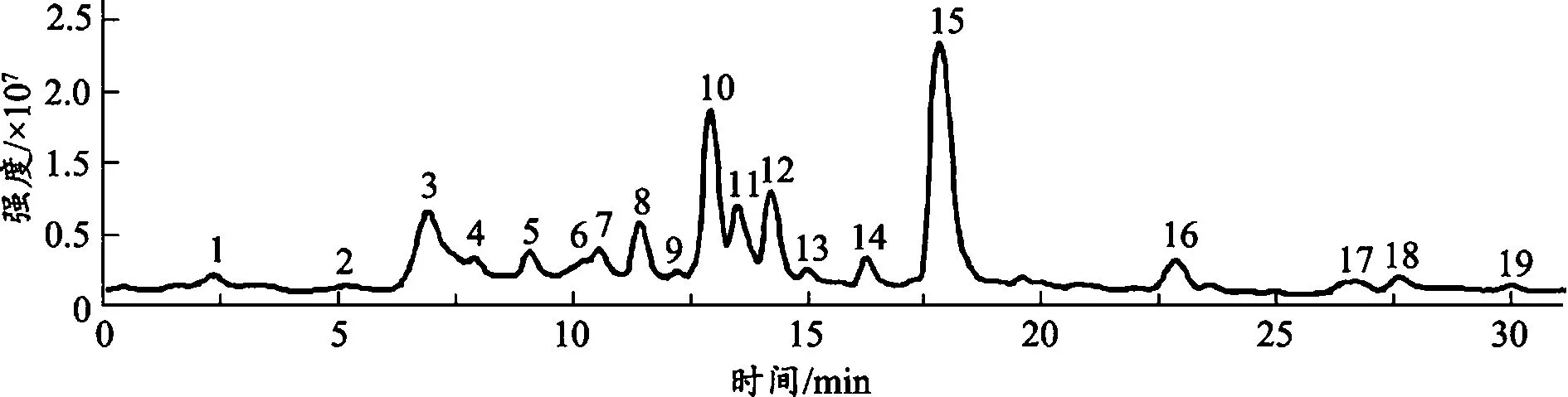
圖1 延胡索水提物的HPLC圖
1.2.2骨質疏松癥模型及分組:采用雙側卵巢切除法[6]制備骨質疏松癥大鼠模型,共40只。簡而言之,用2 %戊巴比妥鈉麻醉大鼠,然后切除兩個卵巢。同時,Sham組(假手術組,8只)的大鼠只切除了卵巢附近的脂肪組織。手術后,以青霉素5萬 U/d的劑量進行肌肉注射,每次持續3 d。手術一周后,將卵巢切除大鼠隨機分為五組(每組8只):模型組、雌二醇組、電針組、延胡索組和針藥組。
1.2.3干預方法:按照人鼠等效劑量,雌二醇組給予戊酸雌二醇50 μg/(kg·d)灌胃,每天一次。電針組根據參考文獻[7]取穴,將毫針刺入腎俞穴、三陰交穴、關元穴和足三里穴后,連接電針儀,連續波、設置刺激強度2 mA,2 Hz/100 Hz,每次15 min,每天一次。延胡索組給予延胡索水提物灌胃治療,根據參考文獻[8],選擇劑量為0.5 g/kg。針藥組先通過灌胃延胡索水提物0.5 g/kg,間隔15 min后進行電針治療,處理方法同上。Sham組和模型組每日給予等體積生理鹽水。連續治療12周。
1.3 標本采集
治療結束后,將大鼠經腹腔注射3 %戊巴比妥鈉(每100 g體質量0.1 mL)麻醉后,腹主動脈取血,3 000 r/min離心10 min后將血清置于- 20 ℃保存。大鼠放血致死后,剝離大鼠右側股骨遠端干骺端、右側股骨組織以及股骨遠端部分骨組織,一部分置于10 % EDTA溶液(pH 7.4)中在4 ℃下固定3周,用于觀察骨組織形態;另一部分置于- 80 ℃保存,用于蛋白免疫印跡分析。
1.4 檢測指標
1.4.1骨密度測定:使用骨密度儀掃描剝離的大鼠右側股骨遠端干骺端,記錄各組大鼠的骨密度(bone mineral density, BMD)值。
1.4.2骨組織形態及骨小梁微結構測定:將經DETA溶液固定的股骨組織脫鈣后,用石蠟包埋,并在冠狀面切割成3 μm厚的切片。切片經二甲苯脫蠟、梯度乙醇水合、行常規蘇木精-伊紅(HE)染色后,于顯微鏡下觀察組織形態學變化,并進行定性分析。通過微型CT測量脛骨遠端結構,測量的參數包括骨小梁的平均厚度(Tb.Th)、骨小梁面積百分比(Tb.Ar,%)、骨小梁數量(Tb.N)和骨小梁分離度(Tb.Sp)。具體操作根據CT操作手冊進行。
1.4.3酶聯免疫吸附測定(ELISA):根據ELISA試劑盒說明書檢測血清中骨特異性堿性磷酸酶(bone-specific alkaline phosphatase,BALP)、核結合因子-α1(core-binding factor subunit- α1,CBF-α1)、I型前膠原氨基端前肽(precollagen type I amino-terminal prepropeptide,PINP)、骨鈣素(osteocalcin,OC)、骨保護素(osteoprotegerin,OPG)和核因子-κB配體的受體激活劑(receptor activator of nuclear factor-κB ligand,RANKL)的含量。
1.4.4蛋白免疫印跡分析:將骨組織用含有蛋白酶抑制劑的裂解緩沖液裂解。將裂解物以12 000g離心15 min。收集上清液,使用雙辛可寧酸定量測定法測定蛋白質濃度。將蛋白質與負載緩沖液混合,并在100 ℃下孵育6 min。將等量的蛋白質(50 μg)進行10 %十二烷基硫酸鈉聚丙烯酰胺凝膠電泳,然后轉移至孔徑為0.45 μm的聚偏氟乙烯膜上。將膜與抗Runx2、抗Wnt3a、抗β-catenin、抗GAPDH抗體于4 ℃下孵育過夜。洗滌后,將膜與二級抗體辣根過氧化物酶綴合的抗小鼠(或兔)IgG在室溫下孵育1 h。ECL試劑顯影后,使用Image Lab軟件對免疫反應帶的像素強度進行量化。以GAPDH作為內部參照。
1.5 統計分析
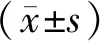
2 結果
2.1 體重和骨密度的比較
治療前,各組之間大鼠的體重和骨密度值均無明顯差異(P>0.05)。治療后,與Sham組相比,模型組大鼠的骨密度值明顯降低,差異有統計學意義(P<0.05)。治療后,與模型組相比,雌二醇、電針、延胡索、針藥組大鼠的骨密度值明顯升高,且針藥組大鼠的骨密度值顯著高于電針組和延胡索組,差異均有統計學意義(P<0.05)。見表1。

表1 各組大鼠治療前后體重和骨密度的比較
2.2 骨組織形態及骨小梁微結構參數的比較
如HE染色所示(圖2),Sham組顯示出完整的骨小梁結構,且骨小梁排列有序、直徑正常、罕見空骨陷窩。與Sham組相比,模型組骨小梁結構紊亂、骨小梁變薄,且空骨陷安窩增加,并觀察到輕微骨折。與模型組相比,雌二醇、電針、延胡索、針藥組的骨組織形態損傷明顯減輕。進一步比較骨小梁微結構參數發現(表2),與Sham組相比,模型組大鼠的Tb.Th、Tb.Ar和Tb.N均明顯降低,而Tb.Sp明顯增加,差異均有統計學意義(P<0.05)。干預12周后,與模型組相比,雌二醇、電針、延胡索、針藥組大鼠的Tb.Th、Tb.Ar和Tb.N均明顯增加,而Tb.Sp明顯降低,差異均有統計學意義(P<0.05)。此外,針藥組的干預效果明顯優于電針組和延胡索組,差異有統計學意義(P<0.05)。

表2 各組大鼠治療后骨小梁微結構參數的比較
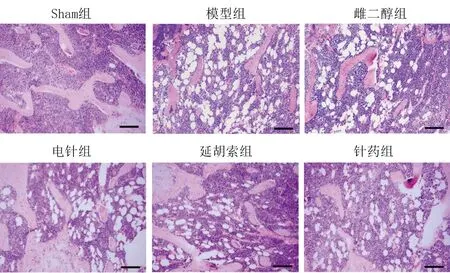
圖2 各組大鼠股骨組織HE染色(×400)
2.3 骨代謝標志物的比較
與Sham組相比,模型組大鼠骨代謝標志物BALP、CBF-α-1、PINP和OC含量均明顯降低,差異有統計學意義(P<0.05)。干預12周后,與模型組相比,雌二醇、電針、延胡索、針藥組大鼠的BALP、CBF-α-1、PINP和OC水平均明顯升高,且針藥組大鼠骨代謝標志物水平顯著高于電針組和延胡索組,差異均有統計學意義(P<0.05)。見表3。
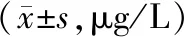
表3 各組大鼠治療后骨代謝標志物含量的比較
2.4 各組大鼠血清OPG和RANKL水平的比較
與Sham組相比,模型組大鼠血清OPG水平明顯降低,而RANKL水平明顯升高,差異有統計學意義(P<0.05)。治療后,與模型組相比,雌二醇、電針、延胡索、針藥組大鼠血清OPG水平明顯升高,而RANKL水平明顯降低(P<0.05)。針藥組血清OPG水平明顯高于、RANKL水平明顯低于電針組和延胡索組(P<0.05)。見表4。
表4 各組大鼠血清OPG和RANKL水平的比較
2.5 各組大鼠股骨遠端骨組織中Runx2、Wnt3a和β-catenin蛋白表達的比較
與Sham組相比,模型組大鼠骨組織中Runx2、Wnt3a和β-catenin蛋白表達明顯降低,而GSK-3β和DVL1蛋白表達顯著升高,差異有統計學意義(P<0.05)。與模型組相比,雌二醇、電針、延胡索、針藥組大鼠骨組織中Runx2、Wnt3a和β-catenin蛋白表達明顯升高,而GSK-3β和DVL1蛋白表達顯著降低,且針藥組Runx2、Wnt3a和β-catenin蛋白的表達顯著高于電針組和延胡索組,而GSK-3β和DVL1蛋白表達顯著低于電針組和延胡索組,差異均有統計學意義(P<0.05)。見圖3、表5。

表5 各組大鼠股骨遠端骨組織中Runx2、Wnt3a和β-catenin蛋白表達的比較
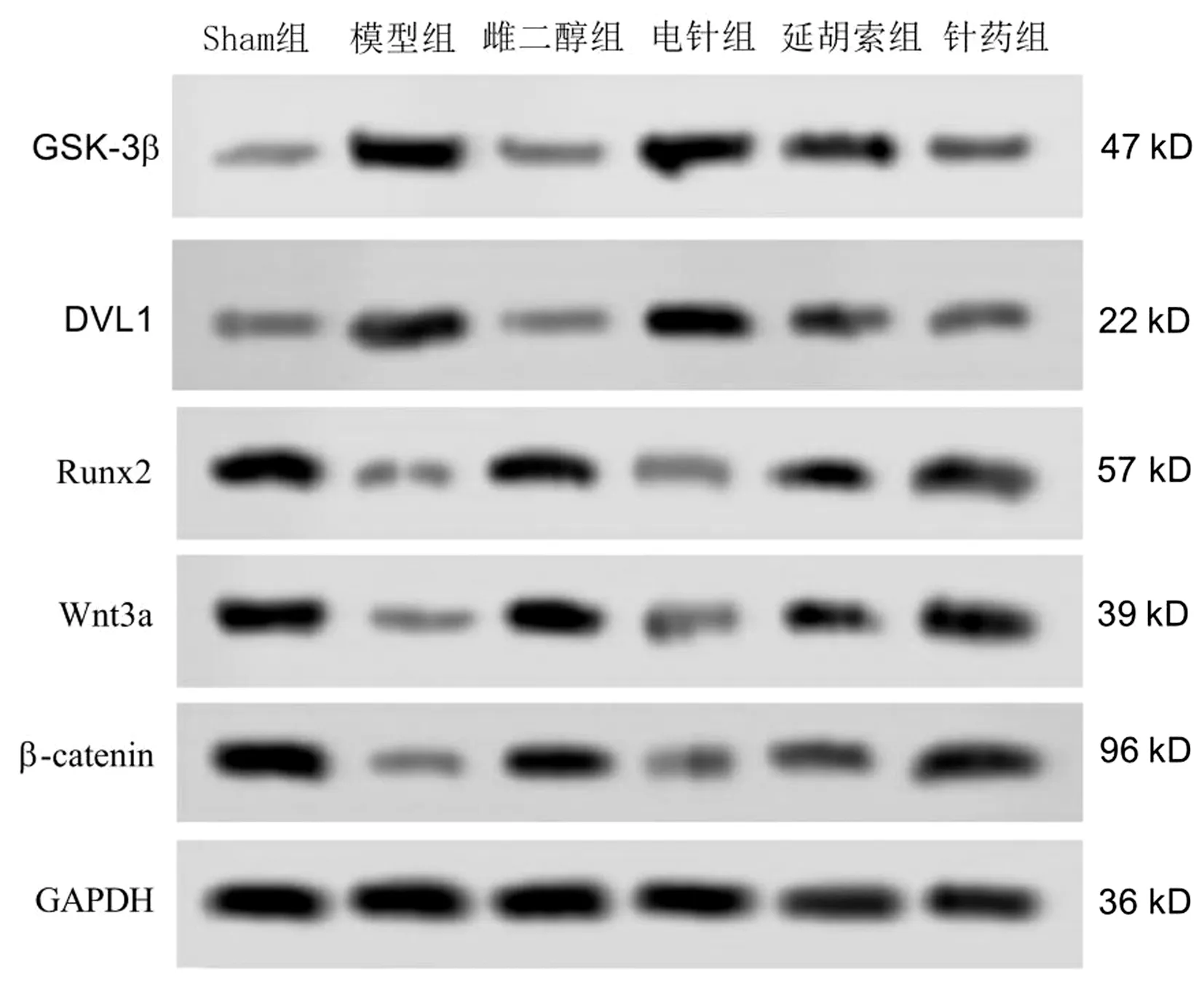
圖3 蛋白免疫印跡檢測股骨遠端骨組織中GSK-3β、DVL1、Runx2、Wnt3a和β-catenin蛋白的表達
3 討論
針灸和中藥作為中醫學的兩大療法,被廣泛用于疾病的治療。電針作為一種改良的針灸方法,其原理是調節陰陽、消除氣滯和氣血瘀的通道和側支。基于中醫學原理,腎俞穴、三陰交穴、關元穴和足三里穴是預防和治療絕經后婦女骨質疏松癥最常用的傳統穴位[9]。動物研究[10]表明,電針預處理可防止卵巢切除術導致的骨丟失和骨結構惡化,并促進骨愈合和骨痂形成。此外,電針刺激不僅可以增加骨密度,還可以防止卵巢切除引起的骨質流失[11]。延胡索作為傳統中藥之一,其水提物中含多種化學成分,其中延胡索乙素、脫氫紫堇堿、鹽酸小檗堿等都被證實是鈣離子拮抗劑[12]。研究[13]已證實,口服延胡索提取物能夠降低大鼠耳朵腫脹,提示其具有良好的抗炎作用。此外,延胡索提取物在多種腫瘤細胞中的抗癌細胞增殖作用也被證實[14]。然而,延胡索提取物在骨質疏松癥中的作用尚未見報道。本研究發現,電針刺激和延胡索水提物治療均能夠減輕骨組織形態損傷和骨小梁結構損傷,提示電針和延胡索水提物治療能夠改善骨質疏松癥中發生的病理變化。PINP、CBF-α1和OC的水平降低會影響骨代謝過程中的骨形成[7]。本研究發現電針和延胡索水提物治療均能夠增加骨質疏松癥大鼠血清ALP和BGP水平、增加骨密度,提示電針和延胡索水提物能夠改善骨代謝。
目前研究認為,針藥并用能夠在保證治療效果的基礎上減輕針灸的刺激量、降低藥物的毒副作用[15]。本研究中電針與延胡索水提物聯用能夠發揮出比單獨治療更好的抗骨質疏松癥效果。既往研究[16]指出,電針能夠提高中藥作用的敏感性和靶向性。一項薈萃分析[17]顯示,電針與中藥或西藥結合可以改善單一干預方式的不足之處,提高整體療效。基于既往研究推測,電針刺激“腎俞穴”“三陰交穴”“關元穴”和“足三里穴”可治本扶正、益腎調經,防止卵巢切除術導致的骨丟失和骨結構惡化;延胡索提取物可減輕促使骨質疏松發生的病理因素;二者結合在治療骨質疏松癥時可起到協同增效作用。
絕經后骨質疏松癥的致病機制十分復雜,與多種細胞信號轉導途徑有關。OPG/RANKL系統是骨生物學史上最重要的發現之一,被證明參與了骨代謝的調節[18]。RANKL作為腫瘤壞死因子配體家族的膜結合分子,參與促進破骨細胞的形成并抑制成骨細胞的增殖和分化,為破骨細胞祖細胞提供重要信號[19]。RANKL與其受體結合,誘導破骨細胞生存和成熟破骨細胞活化。OPG是RANKL的誘餌受體,由成骨細胞合成和分泌。其通過阻斷RANKL與其受體之間的相互作用,抑制破骨細胞的形成和成熟破骨細胞的活化。本研究發現,電針和延胡索水提物治療導致OPG表達上調、RANKL表達上調。基于既往研究推測電針和延胡索水提物可能通過激活成骨細胞的形成并抑制破骨細胞的形成,從而改善卵巢切除術誘導的骨質疏松癥。
Wnt/β-catenin信號通路在骨生長和骨重塑的調節中發揮關鍵作用[20]。Wnt信號缺失時,GSK-3β、酪蛋白激酶1(CK1)和軸蛋白(Axin)會構成降解復合物,介導β-catenin的泛素化和降解。在異常持續激活時,Wnt配體與細胞表面卷曲蛋白和低密度脂蛋白受體相關蛋白組成的受體復合物相互作用,經DVL傳遞信號后,導致降解復合物的失活,進而抑制β-catenin的降解。β-catenin是Wnt信號通路經典途徑的核心蛋白分子。β-catenin在細胞核中積累,并與淋巴增強子結合因子-1/轉錄因子結合,以上調Wnt靶基因的表達,如Runx2,進而引發多種效應,包括成骨細胞的增殖和分化。靶向Wnt/β-catenin信號途徑已成為骨質疏松靶向治療的研究熱點之一。范懷玲等[21]發現,電針刺激能夠激活Wnt/β-catenin信號通路來改善骨質疏松。與既往研究一致,本研究也發現電針治療能夠上調Runx2、Wnt2a和β-catenin的表達,并下調GSK-3β和DVL1的蛋白表達,提示其對Wnt信號途徑的激活。此外,延胡索水提物治療也能夠激活Wnt信號途徑,且電針與延胡索水提物聯合治療對Wnt信號途徑的激活效應比單一處理更明顯。基于這些研究,推測電針和延胡索水提物聯合能夠協同增效,至少部分是激活Wnt/β-catenin通路來抑制卵巢切除術誘導的骨質疏松癥。
綜上所述,本研究發現,電針刺激與延胡索水提物聯合治療能夠減少骨質疏松癥大鼠的骨量損失、增加骨密度、改善骨組織的微觀結構和骨代謝,從而減輕卵巢切除術誘導的骨質疏松癥,其可能是通過調控OPG/RANKL和Wnt/β-catenin途徑來實現。此外,電針刺激與延胡索水提物結合能夠起到協同增效作用,這一新發現可能為骨質疏松癥的治療提供新思路。然而,考慮到臨床應用中患者需接受長時間電針刺激,可能存在依從性較差的缺點,因此仍需結合臨床病例進行深入研究。

