大承氣湯對腸源性膿毒癥小鼠的保護作用及機制Δ
鐘 旋 ,李袁袁 ,林榮鋒 #,姚韻婕 ,劉偉瓊 ,羅毅平 ,凌家俊 (.廣東省婦幼保健院成人重癥監護室,廣州 544;.廣州中醫藥大學中藥學院,廣州 50006;3.東莞廣州中醫藥大學研究院,廣東 東莞 53808)
膿毒癥是全身性炎癥反應綜合征,可發展為嚴重的膿毒血癥和膿毒癥休克[1]。其可引起機體過度的炎癥反應,造成多器官損傷,進而引發多器官功能障礙,使患者病死率升高[2]。膿毒癥的臨床治療非常棘手,主要采用非特異性治療(如液體復蘇、肺保護性通氣、控制感染、改善血流動力學等)和對癥治療(如防治器官功能衰竭和休克等)[3]。由于目前尚無特異性治療方法,其病死率仍然高達36.6%[4]。中醫可采用通腑降下法治療膿毒癥,大承氣湯是該治法的代表方劑之一。大承氣湯源于張仲景《傷寒論》,由大黃、枳實、厚樸和芒硝組成,是《中國膿毒癥早期預防和阻斷急診專家共識》治療腑氣不通型膿毒癥的推薦用藥[4]。已有文獻報道,大承氣湯可縮短膿毒癥患者的機械通氣及住ICU時間,改善急性生理和慢性健康狀況Ⅱ(acute physiology and chronic health evaluation Ⅱ,APACHEⅡ)評分和膿毒癥相關序貫器官衰竭(sequential organ failure assessment,SOFA)評分,提高治愈率[5],且對膿毒癥胃腸損傷[6]、膿毒癥肺損傷[5]、急性胰腺炎并發肝損傷[7]等疾病均具有較好的治療效果,但其作用機制尚不清楚,且相關的基礎研究較少。采用中藥配方顆粒制備的大承氣湯在保持傳統湯劑成分特點的基礎上,不僅成分穩定可控,還具有較明確的藥動學數據[8]。基于此,本研究擬采用中藥配方顆粒制備大承氣湯,并開展其改善膿毒癥的藥效學研究。
Toll 樣受體4(Toll-like receptor 4,TLR4)是最早被人們發現且研究最為廣泛的TLR家族成員,其在膿毒癥的發病機制中扮演著重要的角色[9]。膿毒癥發生時,TLR4可通過識別并結合病原微生物細胞壁上的脂多糖激活其下游髓分化因子88(myeloid differentiation factor 88,MyD88)依賴性通路,進而促進白細胞介素6(interleukin-6,IL-6)、腫瘤壞死因子α(tumor necrosis factor-α,TNF-α)等炎癥因子的釋放[10]。因此,TLR4/MyD88信號通路在膿毒癥的發病機制中發揮了重要作用。本研究以經典的盲腸穿刺法復制腸源性膿毒癥模型小鼠,考察大承氣湯對腸源性膿毒癥小鼠的保護作用,并從TLR4/MyD88信號通路探討其可能機制,以期為大承氣湯治療膿毒癥的機制研究提供實驗參考。
1 材料
1.1 主要儀器
本研究所用主要儀器有ST16 型離心機(美國Thermo Fisher Scientific 公司)、DG5033A 型多功能酶標儀(南京東華電子科技有限公司)、JB-P5 型石蠟組織包埋機(武漢俊杰電子有限公司)、RM2016 型病理切片儀(上海徠卡儀器有限公司)、7500型熒光定量聚合酶鏈式反應(PCR)儀(美國Applied Biosystems 公司)、SMA4000型微量核酸定量儀(美國Merinton公司)。
1.2 主要藥品與試劑
大黃、枳實、厚樸、芒硝的配方顆粒購自四川新綠色藥業科技發展有限公司,參考大承氣湯處方(大黃12 g、枳實12 g、厚樸24 g、芒硝9 g),按文獻[8]方法加入煮沸的蒸餾水適量,配制成質量濃度分別為1、0.5 g/mL的大承氣湯藥液(以生藥量計),備用。注射用烏司他丁(批號032104073,規格100 000 U)購自廣東天普生化醫藥股份有限公司;戊巴比妥鈉(批號1905020301)購自美國Sigma公司;TNF-α 酶聯免疫吸附試驗(ELISA)試劑盒(批號RX202412M)、IL-6 ELISA試劑盒(批號RX203049M)均購自泉州睿信生物科技有限公司;TRIzol Reagent 試劑盒(批號DP424)購自天根生化科技(北京)有限公司;逆轉錄試劑盒(批號K1622)購自美國Thermo Fisher Scientific 公司;熒光實時定量PCR 檢測試劑盒(批號AOPR-1200)購自廣州復能基因有限公司。
1.3 實驗動物
本研究所用動物為C57BL/6J雄性小鼠,共60只,體重為23~25 g,由廣州中醫藥大學動物實驗中心提供,動物生產許可證號為SCXK(粵)2019-0202。動物飼養于廣州中醫藥大學中藥學院SPF級動物房(溫度為24~26 ℃,濕度為45%~55%,自然晝夜節律光照),自由獲取食物和水。本實驗經過廣東省婦幼保健院醫學倫理委員會批準,批準號為廣東省婦幼保健院醫倫第[202001070]號。
2 方法
2.1 實驗分組、造模與給藥
將60 只C57BL/6J 小鼠按體重隨機分為6 組,分別為假手術(Sham)組、假手術+大承氣湯高劑量(Sham+DCQD-H)組、模型(CLP)組、大承氣湯低劑量(DCQDL)組、大承氣湯高劑量(DCQD-H)組、陽性對照(Positive)組,每組10只。CLP組、DCQD-L組、DCQD-H組和Positive組小鼠均以盲腸結扎穿刺法建立腸源性膿毒癥模型[11]。DCQD-L組和DCQD-H組在術前3 d和術后7 d每天灌胃給予大承氣湯(劑量分別為4、8 g/kg[12],按生藥量計);Positive 組在術前2 h 腹腔注射烏司他丁1 次,術后7 d 每日腹腔注射烏司他丁1 次,劑量均為50 000 U/kg[13]。Sham 組僅暴露盲腸,不做結扎及穿刺;Sham+DCQD-H組僅暴露盲腸,不做結扎及穿刺,并在術前3 d和術后7 d每天灌胃給予大承氣湯8 g/kg(按生藥量計);Sham 組和CLP 組每天均灌胃和腹腔注射生理鹽水各0.2 mL,連續10 d。
2.2 小鼠膿毒癥評分與7 d生存率評估
采用小鼠膿毒癥評分評價各組小鼠膿毒癥嚴重程度[14]。根據小鼠外觀、行為表現、意識水平、對刺激的反應、睜眼反應、呼吸頻率和呼吸質量等情況進行綜合評分,分值越高,表明膿毒癥越嚴重。術后7 d每天對各組小鼠進行膿毒癥評分,并觀察其存活情況,繪制7 d生存曲線用以評估其7 d生存率。
2.3 標本采集
當小鼠的膿毒癥評分超過21 分或小鼠的呼吸頻率和呼吸質量得分超過3分時,視為死亡,此時及時進行取材[15]:摘眼球取血,收集血清備用。將小鼠處死,剖取肝、肺、腎、回腸組織,分批剪取適量組織裝入凍存管并迅速浸入液氮中,然后放入80 ℃冰箱中保存,備用;另取一部分組織浸入4%多聚甲醛溶液中固定,備用。其余小鼠于末次給藥1 h后采用相同方法取材。
2.4 小鼠血清和回腸組織中TNF-α、IL-6水平的測定
取“2.3”項下小鼠血清和回腸組織樣品適量(每組選取6只小鼠的樣本),采用ELISA法測定其中TNF-α、IL-6水平,具體步驟嚴格按試劑盒說明書操作。
2.5 小鼠肝、肺、腎、回腸組織的病理學形態觀察
采用蘇木精-伊紅(HE)染色法進行觀察。取“2.3”項下固定于4%多聚甲醛溶液中的小鼠肝、肺、腎、回腸組織(每組選取3 只小鼠的樣本),經常規石蠟包埋、切片、HE染色后,置于光學顯微鏡下觀察各組織的病理學形態并評分[16]。
2.6 小鼠回腸組織中TLR4、MyD88 mRNA 表達水平的檢測
取“2.3”項下小鼠回腸組織樣品適量(每組選取6只小鼠的樣品),使用TRIzol 試劑按照說明書要求提取小鼠回腸組織總RNA,使用逆轉錄試劑盒合成cDNA,再按照熒光實時定量PCR檢測試劑盒制備反應體系,反應條件為:95℃ 10 min;95℃ 10 s,55℃ 20 s,72℃ 35 s;循環40個周期。繪制熔解曲線,采用2-ΔΔCt法,以actb為內參,計算TLR4、MyD88 mRNA 的表達水平。引物序列由廣州四和生物科技股份有限公司合成,具體見表1。

表1 引物序列及擴增產物長度
2.7 統計學方法
采用SPSS 26.0 軟件、GraphPad Prism 9 醫學繪圖軟件進行分析,數據以±s表示。多組間比較采用單因素方差分析,進一步兩兩比較采用LSD-t檢驗。檢驗水準α=0.05。
3 結果
3.1 小鼠膿毒癥評分和7 d生存率測定結果
膿毒癥評分結果見圖1A。Sham 組和Sham+DCQD-H組小鼠的行為正常,精神佳,反應靈敏,呼吸正常,毛發光滑且發亮,眼睛完全睜開。與Sham 組比較,CLP 組小鼠膿毒癥評分顯著升高(P<0.01),毛發豎立,行動緩慢,精神萎靡,對外界刺激(如聲音、觸摸)反應遲鈍或行動伴隨著震顫,眼睛半閉或緊閉,偶有白色分泌物,呼吸頻率和質量較差。與CLP組比較,DCQD-L組、DCQD-H 組和Positive 組小鼠膿毒癥評分均顯著降低(P<0.01),且上述癥狀均有所改善或緩解。
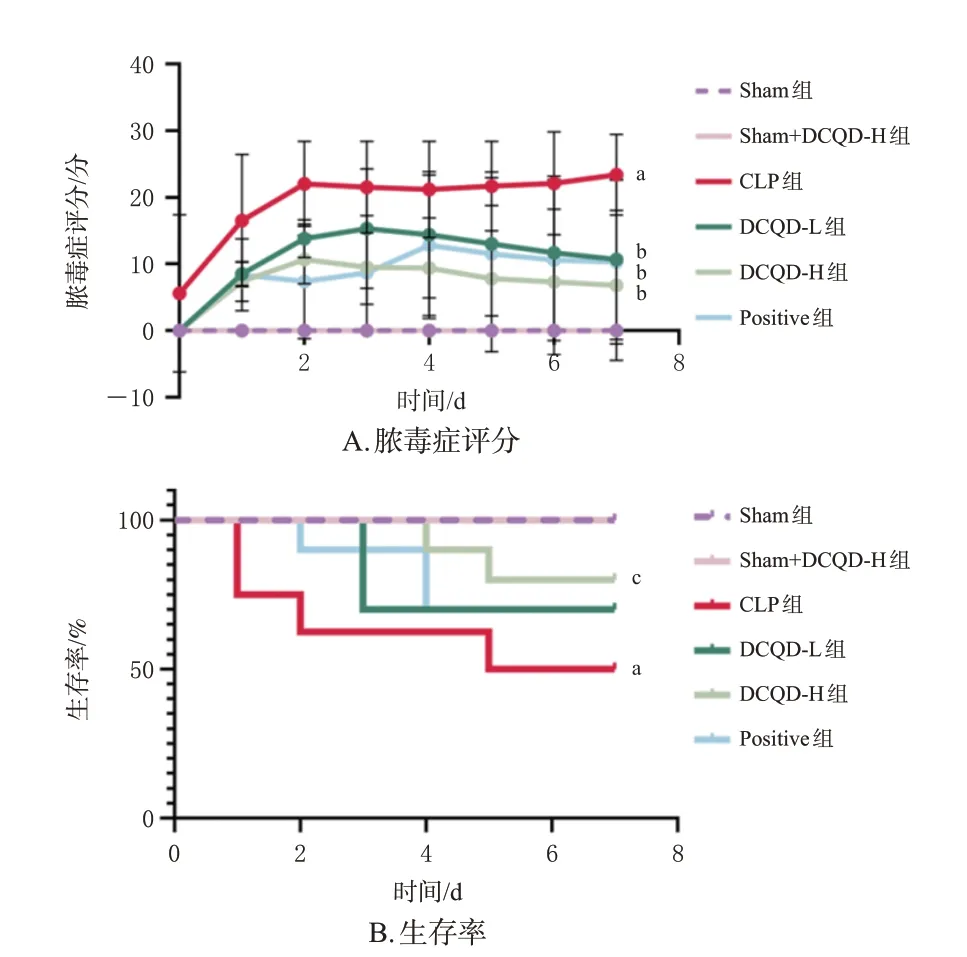
圖1 各組小鼠的膿毒癥評分和7 d 生存率測定結果(±s,n=10)
小鼠7 d 生存率測定結果見圖1B。Sham 組和Sham+DCQD-H組均無小鼠死亡。與Sham組比較,CLP組小鼠7 d生存率顯著降低(P<0.01),僅為40%;與CLP組比較,DCQD-L 組、DCQD-H 組、Positive 組小鼠7 d 生存率均有不同程度的升高,分別為70%、80%、70%,其中DCQD-H組小鼠7 d生存率顯著升高(P<0.05)。
3.2 小鼠血清和回腸組織中TNF-α、IL-6 水平的檢測結果
與Sham 組比較,CLP 組小鼠血清和回腸組織中TNF-α、IL-6 水平均顯著升高(P<0.01)。與CLP 組比較,DCQD-L 組、DCQD-H 組和Positive 組小鼠血清和回腸組織中TNF-α、IL-6水平(DCQD-L組回腸組織中IL-6除外)均顯著降低(P<0.05或P<0.01)。結果見圖2。
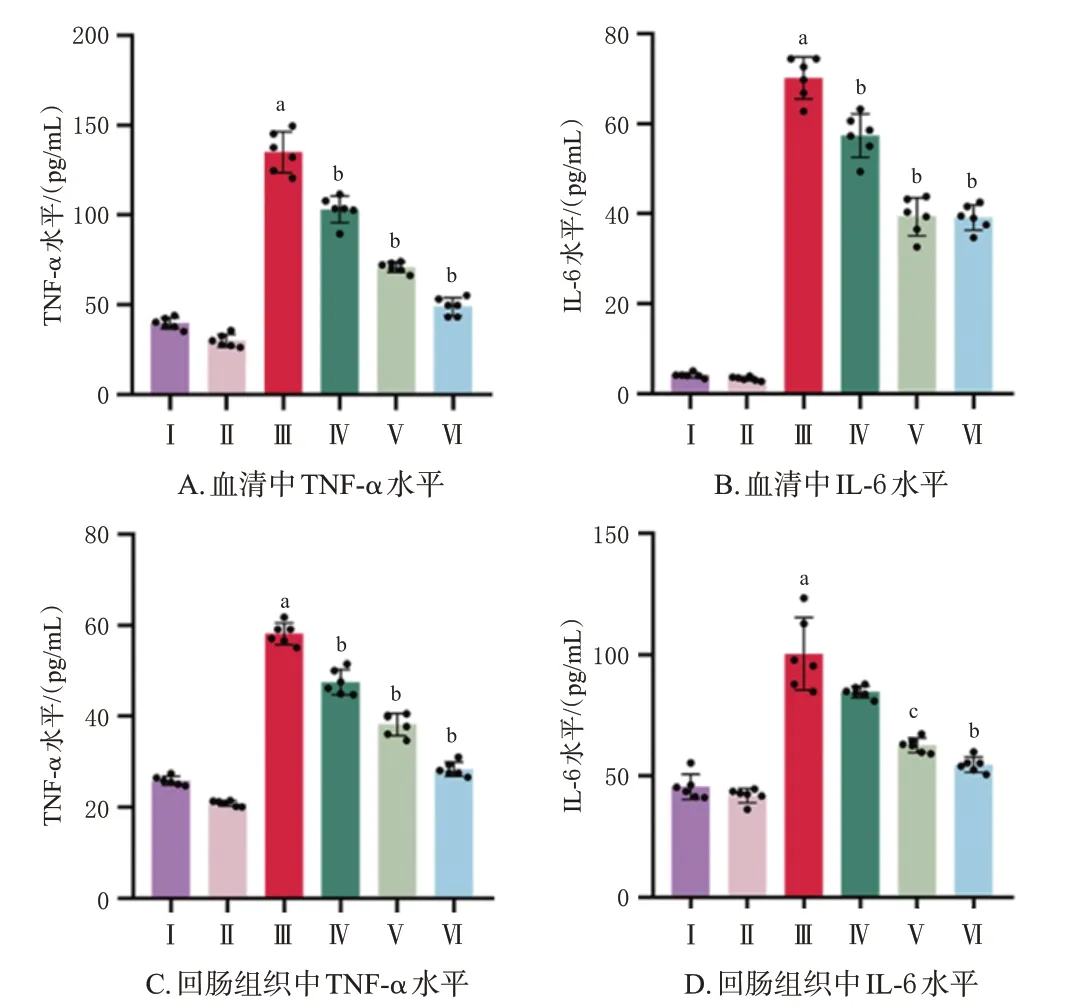
圖2 各組小鼠血清和回腸組織中TNF-α、IL-6 水平的檢測結果(±s,n=6)
3.3 小鼠肝、肺、腎、回腸組織的病理學變化結果
肝組織HE染色結果顯示,Sham組和Sham+DCQDH組小鼠肝細胞圍繞中央靜脈呈放射狀排列,未見明顯的形態結構改變;CLP組小鼠肝細胞排列疏松且雜亂不齊,細胞多腫脹,伴有出血,可見大面積的炎癥浸潤和細胞凋亡;DCQD-L 組、DCQD-H 組和Positive 組小鼠肝細胞損傷明顯改善,炎癥浸潤和凋亡減少,中央靜脈微擴張、排列相對整齊,結果見圖3A。

圖3 各組小鼠肝、肺、腎、回腸組織的病理學形態觀察結果
肺組織HE染色結果顯示,Sham組和Sham+DCQDH組小鼠肺泡壁間隙薄,肺泡大、形態正常,無明顯的損傷;CLP 組小鼠肺泡壁增厚,肺泡縮小且多見水腫、出血,可見明顯的炎癥浸潤;DCQD-L 組、DCQD-H 組和Positive 組小鼠肺組織損傷有所緩解,肺泡萎縮、出血、水腫均有不同程度的改善,結果見圖3B。腎組織HE染色結果顯示,Sham 組和Sham+DCQD-H 組小鼠腎組織形態正常,未見明顯的損傷及炎癥浸潤,可見完好的腎小球和腎小管;CLP 組小鼠可見腎小管管腔擴張,腎小管上皮細胞呈空泡樣變性,腎間質多見水腫、出血,有明顯的炎癥損傷;DCQD-L 組、DCQD-H 組和Positive 組小鼠腎組織損傷得到改善,腎小管管腔擴張減弱、空泡樣變性減少,結果見圖3C。回腸組織HE 染色結果顯示,Sham 組和Sham+DCQD-H 組小鼠回腸組織形態正常,完整的腸絨毛數量多,未見明顯損傷;CLP 組小鼠回腸組織可見較多尖銳或破損的腸絨毛,表現出明顯的炎癥損傷;DCQD-L 組、DCQD-H 組和Positive 組小鼠回腸組織損傷及水腫均有明顯改善,結果見圖3D。另外,與Sham 組比較,Sham+DCQD-H 組小鼠肝、肺、腎、回腸組織損傷評分差異無統計學意義(P>0.05),CLP 組小鼠肝、肺、腎、回腸組織損傷評分均顯著升高(P<0.01);與CLP 組比較,DCQD-L 組、DCQD-H 組和Positive 組小鼠肝、肺、腎、回腸組織損傷評分均顯著降低(P<0.01),結果見圖4。

圖4 各組小鼠組織損傷評分結果(±s,n=3)
3.4 小鼠回腸組織中TLR4、MyD88 mRNA 表達水平的檢測結果
與Sham 組比較,CLP 組小鼠回腸組織中TLR4、MyD88 mRNA表達水平均顯著升高(P<0.01)。與CLP組比較,DCQD-L 組、DCQD-H 組和Positive 組小鼠回腸組織中TLR4、MyD88 mRNA表達水平均顯著降低(P<0.01)。結果見圖5。
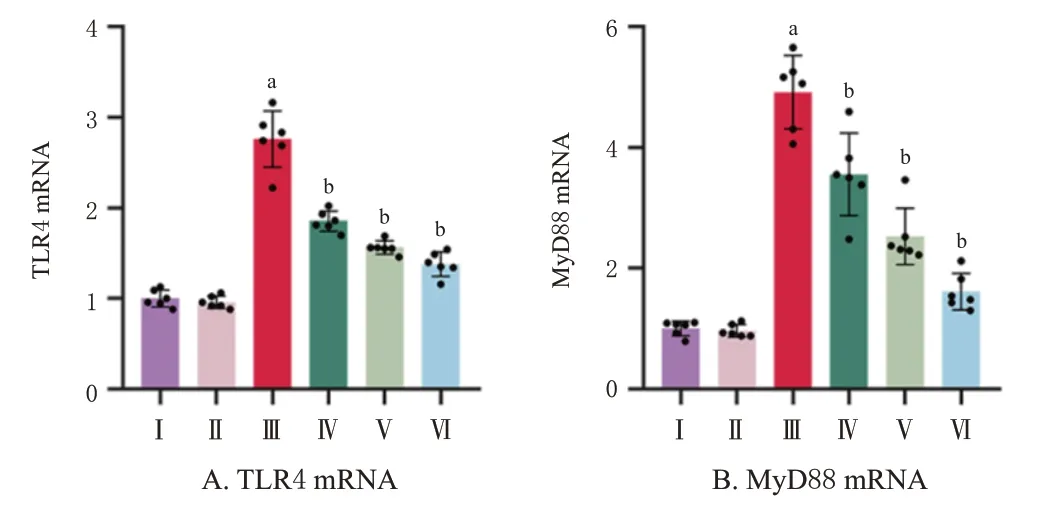
圖5 各組小鼠回腸組織中TLR4、MyD88 mRNA 表達水平的檢測結果(±s,n=6)
4 討論
TNF-α、IL-6均為重要的炎癥因子,常被視為衡量膿毒癥嚴重程度的指標[10]。本研究結果顯示,大承氣湯可抑制膿毒癥引發的血清炎癥因子TNF-α、IL-6 的升高,改善膿毒癥所致的肝、肺、腎、回腸組織的炎癥浸潤,提示其對全身性炎癥反應具有顯著的抑制作用。本研究結果與相關文獻對大承氣湯治療急性或重癥胰腺炎、炎性腸梗阻、肺炎的報道相符[7,17]。
膿毒癥常引起包括肝、肺、腎、回腸組織在內的多器官衰竭,其治療關鍵在于降低多器官功能障礙綜合征(multiple organ dysfunction syndrome,MODS)的發生率[18],因此本研究考察了大承氣湯對肝、肺、腎、回腸組織損傷的影響,結果顯示,其對肝、肺、腎、回腸組織均具有保護作用,尤其是對腸道的保護作用較好。胃腸道不僅是促進膿毒癥病情進展的關鍵器官,更是膿毒癥最常受累的靶器官[11],腸功能損傷的防治是截斷膿毒癥迅速進展為MODS的核心[19]。大承氣湯已被證實對腸梗阻、胃腸動力不足、腸缺血再灌注損傷等多種腸道疾病具有治療作用[20],且其成分可能對腸存在靶向性[21]。本研究亦證實,大承氣湯可改善腸源性膿毒癥所致的腸道炎癥損傷、浸潤、水腫、出血,較好地保護小腸絨毛的完整。
TLR4信號通路在先天的免疫反應和急性或慢性炎癥性疾病中發揮著重要的作用[22]。當膿毒癥發生時,往往會激活TLR4/MyD88 信號通路,引起動物模型中TLR4、MyD88 mRNA水平的顯著升高,進而促進炎癥因子大量釋放[23]。本研究結果顯示,大承氣湯可顯著下調膿毒癥模型小鼠回腸組織中TLR4、MyD88 mRNA 表達水平,提示其作用機制可能與抑制TLR4/MyD88信號通路有關。
綜上所述,大承氣湯對腸源性膿毒癥模型小鼠具有保護作用,其作用機制可能與抑制全身炎癥、減輕多器官損傷以及下調TLR4/MyD88信號通路有關。

