禿葉黃檗果實祛痰止咳物質基礎的初步研究Δ
張桂榮 ,李楊松 ,羅 婕 ,張 瑾 ,楊轉珍 ,朱寶潔 ,江莉媛 ,呂光華 ,龍 飛 #(1.成都中醫藥大學藥學院,成都 611137;2.西南特色中藥資源國家重點實驗室,成都 611137)
蕓香科黃檗屬植物在全球約有4 種,主產于亞洲東部,在我國有2 個種及1 個變種:黃檗Phellodendron amurenseRupr.、川黃檗P.chinenseSchneid.及變種禿葉黃檗P.chinensevar.glabriusculumSchneid.。《中國藥典》自2005年版起,將川黃柏與關黃柏列為2種藥材,以“川黃柏”作“黃柏”,關黃柏單列[1]。黃檗為中藥關黃柏的基原植物,主要分布在黑龍江、河北、山西、內蒙古、陜西等地[2]。川黃檗為中藥黃柏的基原植物,因被過度開采使用導致其野生資源急劇減少。調查發現,至20世紀末,野生的川黃檗植物基本消失殆盡,而今中藥黃柏的主流商品來源實則為變種禿葉黃檗,主要分布在四川、重慶、貴州、湖北、湖南和云南等地[3]。
禿葉黃檗的樹皮作為黃柏藥材使用,具有清熱燥濕、瀉火除蒸、解毒療瘡的功效,主要用于治療濕熱瀉痢、熱淋澀痛、骨蒸勞熱、盜汗、遺精、瘡瘍腫毒等病癥[4]。據文獻報道,黃檗屬植物除樹皮可作藥用之外,其果實也可入藥[5—6]。李煥榮等[7]研究發現,黃檗的果實中含有揮發油類、酚酸類、生物堿類和三萜類成分,其水煎液和揮發油均有祛痰止咳作用,民間多用于治療慢性支氣管炎[5—6]。另有研究發現,禿葉黃檗果實的主要成分包括揮發油類、生物堿類和三萜類化合物[8],但其作藥用還未見報道。本研究擬通過氨水引咳和藥物祛痰小鼠模型實驗研究禿葉黃檗果實的祛痰止咳作用;利用氣相色譜-質譜聯用(GC-MS)和超高效液相色譜-質譜(UPLCMS)聯用技術對禿葉黃檗果實的揮發油和非揮發性部位進行成分分析;并在藥效研究和成分分析鑒定的基礎上,通過網絡藥理學進一步探索禿葉黃檗果實祛痰止咳的物質基礎及作用機制,為禿葉黃檗果實資源的綜合利用研究提供依據。
1 材料
1.1 主要儀器
本研究所用主要儀器包括7890A-5975C 系列GCMS 聯用儀(美國Agilent 公司)、Vanquish 型超高效液相色譜聯用Q-Exactive 四極桿-靜電場軌道阱高分辨質譜儀(美國Thermo Fisher Scientific公司)、SQP型十萬分之一天平[賽多利斯科學儀器(北京)有限公司]、Spectra-Max i3x型酶標儀[美谷分子儀器(上海)有限公司]等。
1.2 主要藥品與試劑
藥材樣品采自四川省雅安市滎經縣,經成都中醫藥大學藥學院龍飛副教授鑒定為蕓香科黃檗屬植物禿葉黃檗P.chinensevar.glabriusculumSchneid.的成熟果實,低溫干燥后密封儲存。甜菜堿、小檗堿、小檗紅堿、綠原酸、木犀草素對照品(批號分別為CYR-T0049200815、CYRX0024210628、CYR-X004021022、CYR-L0098200419、CYR-M0072200308)均購自四川萃益潤生物科技有限公司,熊果苷、檸檬苦素、紅景天苷、山柰酚、延胡索乙素、秦皮甲素、巴馬汀、黃柏酮、黃柏堿、吳茱萸堿對照品(批號分別為PS020727、PS010363、PS011476、PS011676、PS000988、PS012121、PS020011、PS010197、PS000447、PS012147)均購自成都普思生物科技股份有限公司,葫蘆巴堿對照品(批號RDD-H05711801010)購自成都瑞芬思德丹生物科技有限公司,鹽酸藥根堿對照品(批號20081905)購自成都普菲德生物技術有限公司,槲皮素對照品(批號CHB190110)購自成都克洛瑪生物科技有限公司,所有對照品的純度均≥98%。氫溴酸右美沙芬片(批號51-221211,規格15 mg)購自北京天衡藥物研究院南陽天衡制藥廠;氯化銨(分析純)購自成都市科隆化學品有限公司。乙腈、甲醇、甲酸均為色譜純,其余試劑均為分析純,水為超純水。
1.3 動物
本研究所用動物為SPF 級健康KM 小鼠,共70 只,雌雄各半,體重18~22 g,購自北京SPF生物科技有限公司,動物生產許可證號為SCXK(京)2019-0010。將小鼠飼養于成都中醫藥大學中醫藥管理局中藥藥理三級科研實驗室。適應性飼養1周后用于實驗。本實驗方案經成都中醫藥大學實驗動物倫理委員會批準,倫理批號為2021-80。
2 方法與結果
2.1 試藥的制備
2.1.1 禿葉黃檗果實水煎液試藥
稱取禿葉黃檗果實粉末(過三號篩)200 g,用10 倍體積的水回流煎煮2 h,用紗布過濾后濾渣再用6倍體積的超純水回流煎煮2 h,合并2 次煎液,減壓濃縮定容至100 mL,得生藥量為2 g/mL的禿葉黃檗果實浸膏,臨用時用生理鹽水稀釋至給藥濃度。
2.1.2 禿葉黃檗果實揮發油試藥
稱取禿葉黃檗果實粉末(過三號篩)100 g,加入10倍體積的水,采用水蒸氣蒸餾法提取揮發油,揮發油得率為1.43%,臨用時用2%聚山梨酯80稀釋至給藥濃度。
2.2 禿葉黃檗果實水煎液和揮發油的止咳祛痰活性考察
2.2.1 止咳活性考察
采用氨水引咳實驗進行考察,具體操作參照文獻[9]。取小鼠60只,雌雄各半,隨機分為6組:正常對照組(生理鹽水),右美沙芬組(陽性對照氫溴酸右美沙芬片,15 mg/kg),禿葉黃檗果實水煎液高、低劑量組(后文簡稱為“水煎液高、低劑量組”,給藥劑量以生藥量計分別為12、3 g/kg),禿葉黃檗果實揮發油高、低劑量組(后文簡稱為“揮發油高、低劑量組”,給藥劑量以揮發油量計分別為0.8、0.2 g/kg),每組10只。灌胃相應藥物/生理鹽水,每天1次,連續7 d。末次灌胃后0.5 h,將小鼠放入1 000 mL燒杯中,再迅速放入注有0.4 mL濃氨水的棉球刺激小鼠,以小鼠腹肌強烈收縮且張嘴為咳嗽動作指標,記錄其咳嗽潛伏期和2 min內咳嗽次數。采用SPSS 26.0軟件對數據進行統計分析。實驗結果以±s表示,多組間比較采用單因素方差分析,進一步的組間兩兩比較采用LSD-t檢驗;檢驗水準α=0.05。結果顯示,與正常對照組比較,各給藥組小鼠的咳嗽潛伏期均顯著延長(P<0.05 或P<0.01),右美沙芬組、水煎液高劑量組和揮發油高劑量組小鼠2 min內咳嗽次數均顯著減少(P<0.05或P<0.01)。結果見表1。
表1 各組小鼠的咳嗽潛伏期、2 min內咳嗽次數及氣管中酚紅分泌量測定結果(±s,n=10)
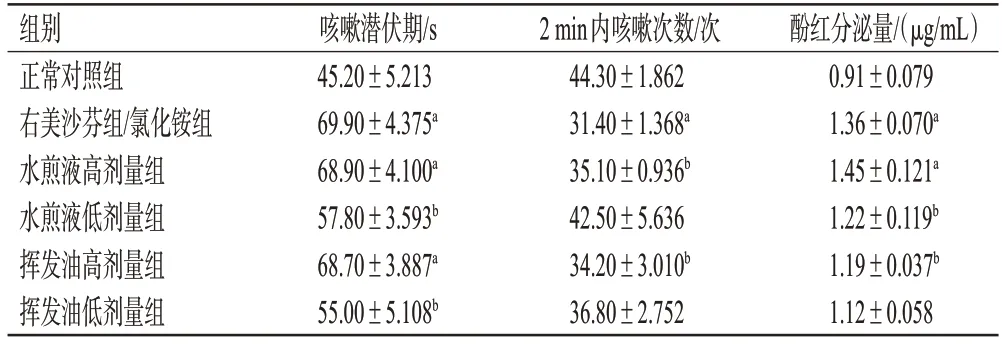
表1 各組小鼠的咳嗽潛伏期、2 min內咳嗽次數及氣管中酚紅分泌量測定結果(±s,n=10)
a:與正常對照組比較,P<0.01;b:與正常對照組比較,P<0.05。
組別正常對照組右美沙芬組/氯化銨組水煎液高劑量組水煎液低劑量組揮發油高劑量組揮發油低劑量組酚紅分泌量/(μg/mL)0.91±0.079 1.36±0.070a 1.45±0.121a 1.22±0.119b 1.19±0.037b 1.12±0.058咳嗽潛伏期/s 45.20±5.213 69.90±4.375a 68.90±4.100a 57.80±3.593b 68.70±3.887a 55.00±5.108b 2 min內咳嗽次數/次44.30±1.862 31.40±1.368a 35.10±0.936b 42.50±5.636 34.20±3.010b 36.80±2.752
2.2.2 祛痰活性考察
采用藥物祛痰小鼠實驗進行考察。動物選取及給藥方式同“2.2.1”項,陽性對照藥變更為氯化銨(1 g/kg)。末次給藥0.5 h 后,各組小鼠按1 g/kg 腹腔注射5%酚紅溶液,0.5 h后頸椎脫臼處死小鼠。取下氣管放入2 mL生理鹽水中,加1 mol/L NaOH 溶液0.2 mL,以3 000 r/min離心15 min,取上清液于酶標儀546 nm波長處測定光密度(OD)值。根據標準曲線Y=0.059 6X-0.028 3(R2=0.996 9)(式中X為酚紅質量濃度,Y為OD 值)計算氣管中酚紅分泌量。數據結果按“2.2.1”項下方法進行統計學分析。結果顯示,與正常對照組比較,氯化銨組和水煎液高劑量組、水煎液低劑量組、揮發油高劑量組小鼠氣管中的酚紅分泌量均顯著增加(P<0.05或P<0.01)。結果見表1。
2.3 禿葉黃檗果實揮發油的GC-MS成分分析
2.3.1 色譜條件
色譜柱為Agilent HP-5MS 柱(30 m×250 μm×0.25 μm);采用程序升溫:初始溫度50 ℃,保持2 min,以4 ℃/min 升溫至280 ℃,保持2 min;進樣口溫度為280 ℃;載氣為氦氣,流速為1.0 mL/min;分流比為20∶1;進樣量為1 μL。
2.3.2 質譜條件
電離方法為電子轟擊電離(electron ionization,EI);電子能量為70 eV;離子源溫度為230 ℃;質量掃描范圍為20~450;質譜檢索標準庫為NIST14。
2.3.3 GC-MS分析供試品溶液的制備
取禿葉黃檗果實打粉,過三號篩,精密稱取粉末約100 g,采用水蒸氣蒸餾法提取揮發油,得淡黃色揮發油液體約1.5 mL。加入無水硫酸鈉約0.5 g,靜置過夜,以除去水分。取揮發油約1.0 mL置于10 mL容量瓶中,用無水乙醚定容,以0.22 μm微孔濾膜過濾,即得。
2.3.4 數據處理及結果分析
將所得質譜裂解數據信息與NIST14 數據庫匹配,得到匹配度≥90%的化合物共38 個,總離子流圖見圖1。其中,相對百分含量>1%的主要化合物有8個,分別為α-蒎烯(1.27%)、月桂烯(64.08%)、石竹烯(1.07%)、germacrene D(2.77%)、isospathulenol(1.08%)、α-cadinol(1.32%)、4(15),5,10(14)-大根香葉三烯-1-醇(1.24%)、金合歡醇(1.29%),具體化合物的匹配度與相對百分含量信息見表2。
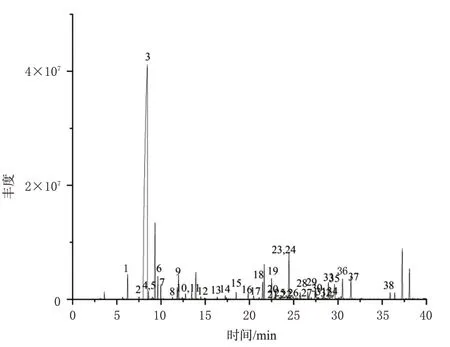
圖1 禿葉黃檗果實揮發油的GC-MS總離子流圖
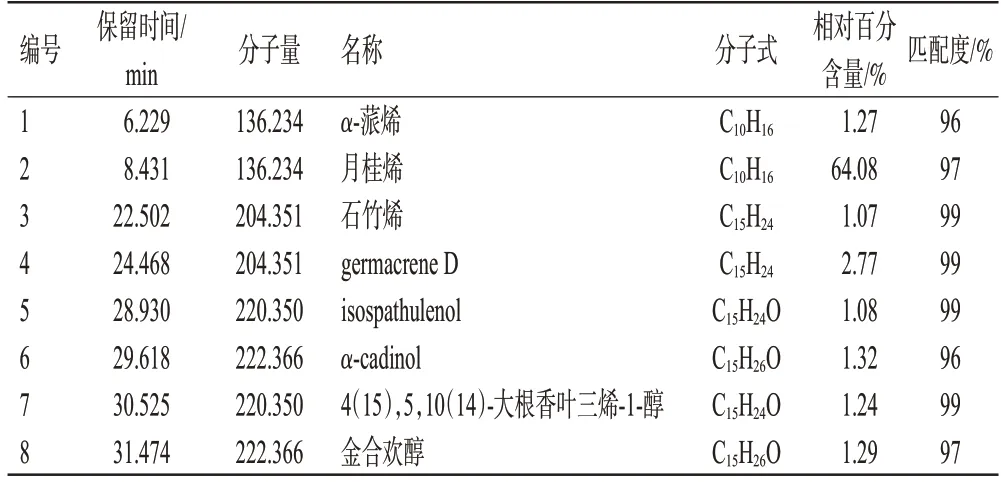
表2 禿葉黃檗果實主要揮發油成分及其相對百分含量
2.4 禿葉黃檗果實非揮發油的UPLC-Q-Orbitrap HRMS成分分析
2.4.1 色譜條件
采用Thermo Acclaim RSLC 120 C18色譜柱(100 mm×3 mm×2.2 μm),以0.1%甲酸溶液(A)-0.1%甲酸乙腈溶液(B)為流動相進行梯度洗脫(0~5 min,5%B→8%B;5~12 min,8%B;12~13 min,8%B→10%B;13~17 min,10%B;17~25 min,10%B→15%B;25~28 min,15%B→22%B;28~32 min,22%B→25%B;32~35 min,25%B;35~42 min,25%B→28%B;42~48 min,28%B→30%B;48~52 min,30%B→55%B;52~63 min,55%B→100%B);流速為0.2 mL/min;柱溫為35 ℃;進樣量為2 μL。
2.4.2 質譜條件
采用電噴霧離子源,在正、負離子模式下檢測。噴霧電壓為3.5 kV;輔助氣溫度為350 ℃;輔助氣流速為10 arb;鞘氣流速為35 arb;離子傳輸管溫度為320 ℃。掃描模式為全掃描/數據依賴二級掃描(Full MS/dd-MS2),一級分辨率為70 000,二級分辨率為17 500;掃描范圍為m/z100~1 500;階梯碰撞能量為20、40、60 eV。
2.4.3 對照品溶液的制備
取甜菜堿、葫蘆巴堿、熊果苷、紅景天苷、秦皮甲素、綠原酸、黃柏堿、槲皮素、山柰酚、延胡索乙素、小檗紅堿、藥根堿、巴馬汀、小檗堿、木犀草素、吳茱萸堿、檸檬苦素和黃柏酮對照品各適量,置于同一容量瓶中,加入甲醇配制成各成分質量濃度均約為100 μg/mL 的混合對照品溶液,混勻,用0.22 μm微孔濾膜過濾,即得。
2.4.4 UPLC-MS分析供試品溶液的制備
精密稱取禿葉黃檗果實粉末1.0 g,置于50 mL錐形瓶中,加入30 mL 甲醇,超聲(功率45 kHz,頻率250 W)處理30 min,過濾,濾液旋轉蒸干,加入適量甲醇溶解后,置于10 mL容量瓶中并以甲醇定容,以0.22 μm微孔濾膜過濾,即得。
2.4.5 數據處理及結果
將采集得到的原始數據導入Compound Discoverer 3.0軟件,通過其向導設置及方法模板,建立未知化合物的鑒定流程,對原始數據進行峰對齊和峰提取。通過提取得到的分子離子色譜峰、同位素峰擬合出可能的分子式,并將二級碎片實測譜圖與mzCloud網絡數據庫及本地中藥成分數據庫OTCML 進行匹配,對匹配結果設置過濾參數為:峰面積閾值80 000,一級及二級質量偏差5 ppm,匹配度分值高于80。對過濾后的離子與數據庫中的化合物信息及對照品進行比對,結合相關文獻和在線數據庫(PubChem)對化學成分進行進一步的分析鑒定。結果,通過UPLC-Q-Orbitrap HRMS技術,共從禿葉黃檗果實中鑒定出69個化合物,包括酚酸類化合物16個、生物堿類化合物13個、黃酮類化合物10個、氨基酸類化合物7個、核苷類化合物5個、香豆素類化合物3個、三萜類化合物3個、其他類化合物12個,其中18個化合物經過對照品比對確認。在正、負離子檢測模式下,禿葉黃檗果實供試品及混合對照品UPLC-Q-Orbitrap HRMS的總離子流圖見圖2,具體化合物信息見表3。
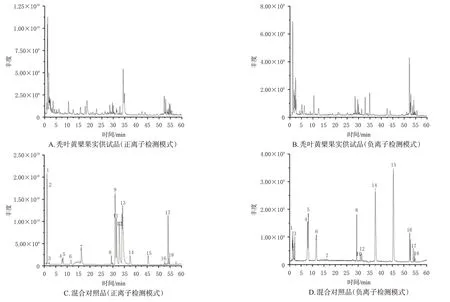
圖2 禿葉黃檗果實與混合對照品UPLC-Q-Orbitrap HRMS的總離子流圖
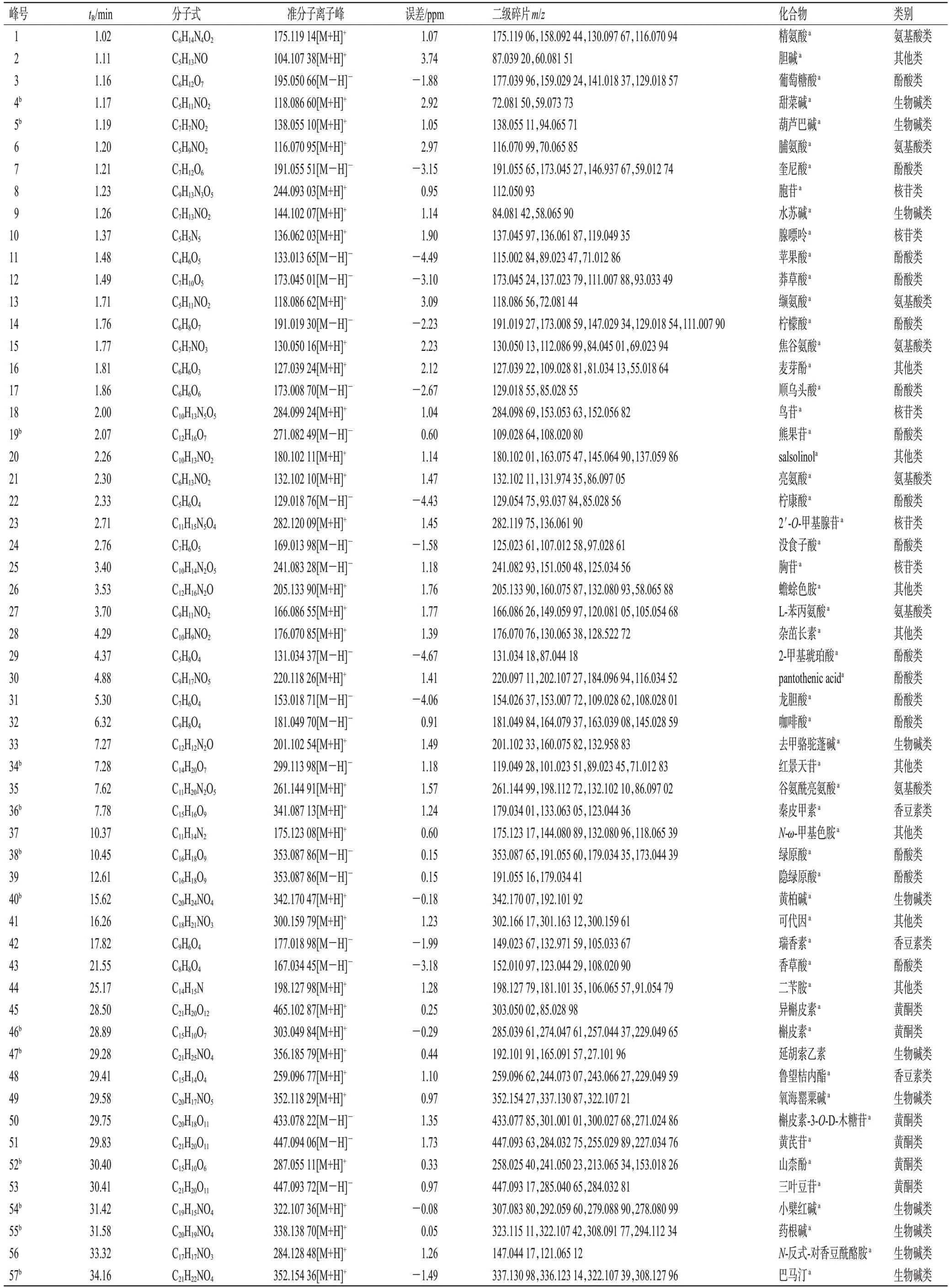
表3 禿葉黃檗果實非揮發性化學成分分析結果
2.5 網絡藥理實驗篩選禿葉黃檗果實祛痰止咳的活性成分及機制
2.5.1 活性成分的篩選
以口服生物利用度(oral bioavailability,OB)>30%和類藥性(drug-likeness,DL)>0.18 為篩選條件對“2.3”和“2.4”項下所鑒定出的禿葉黃檗果實的化學成分進行活性篩選[10]。結果顯示,滿足篩選條件的化學成分共有10個,包括槲皮素、延胡索乙素、山柰酚、小檗紅堿、藥根堿、巴馬汀、小檗堿、木犀草素、吳茱萸苦素、黃柏酮。此外,雖然所鑒定成分中α-蒎烯和月桂烯的DL 值略低于0.18,綠原酸的OB 值略低于30%,但據報道[6,11—12],三者均具有良好的祛痰止咳活性,故也納入后續研究中。因此,共篩選獲得13個活性成分。
2.5.2 潛在作用靶點預測
通過SwissTargetPrediction、TCMSP 和SuperPred 等數據庫共獲得活性成分的靶點681個,以“cough”和“expectoration”為關鍵詞,通過GeneCards 數據庫獲得與咳嗽和咳痰相關的疾病靶點378個。在Venny2.1.0在線作圖工具平臺上獲取兩者交集靶點,即為潛在作用靶點,共57個。
2.5.3 蛋白互作網絡構建和核心靶點獲取
通過String 數據庫對潛在作用靶點進行蛋白互作(protein-protein interaction,PPI)網絡關系數據分析,使用Cytoscape 3.7.1 軟件對數據結果進行可視化分析,選取連接度最大的5個節點作為核心作用靶點,結果見圖3。圖3中包含55個節點,節點的顏色由淺逐漸變深,而顏色越深表示節點的連接度越大;核心靶點為腫瘤壞死因子(tumor necrosis factor,TNF)、表皮生長因子受體(epidermal growth factor receptor,EGFR)、血管內皮生長因子A(vascular endothelial growth factor A,VEGFA)、絲氨酸/蘇氨酸蛋白激酶(serine/threonine kinase proteins,AKT1)、Toll樣受體4(Toll-like receptor 4,TLR4)。
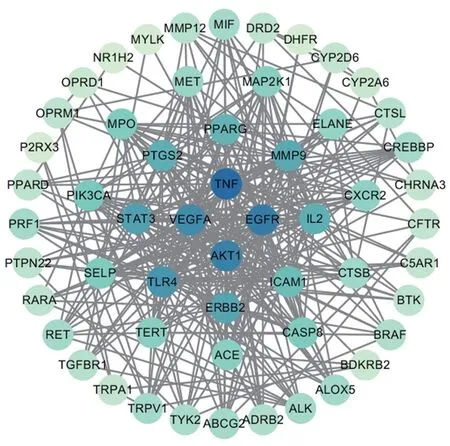
圖3 禿葉黃檗果實祛痰止咳靶點的PPI網絡圖
2.5.4 通路富集分析
利用DAVID 網站對潛在作用靶點進行GO 富集分析和KEGG信號通路富集分析,以P<0.05進行篩選,共得到生物過程通路233 條、細胞組成通路35 條、分子功能通路49條,均選擇其中P值排前10位的條目繪制GO富集分析條形圖,見圖4A。結果顯示,GO 功能條目包括對脂多糖的反應、肽基絲氨酸磷酸化的正向調節、一氧化氮生物合成過程的積極調節等生物過程。同樣選擇P值排前10 位的KEGG 信號通路繪制KEGG 分析氣泡圖,結果見圖4B。結果顯示,KEGG 信號通路包括癌癥、非小細胞肺癌、癌癥中的蛋白聚糖等信號通路。
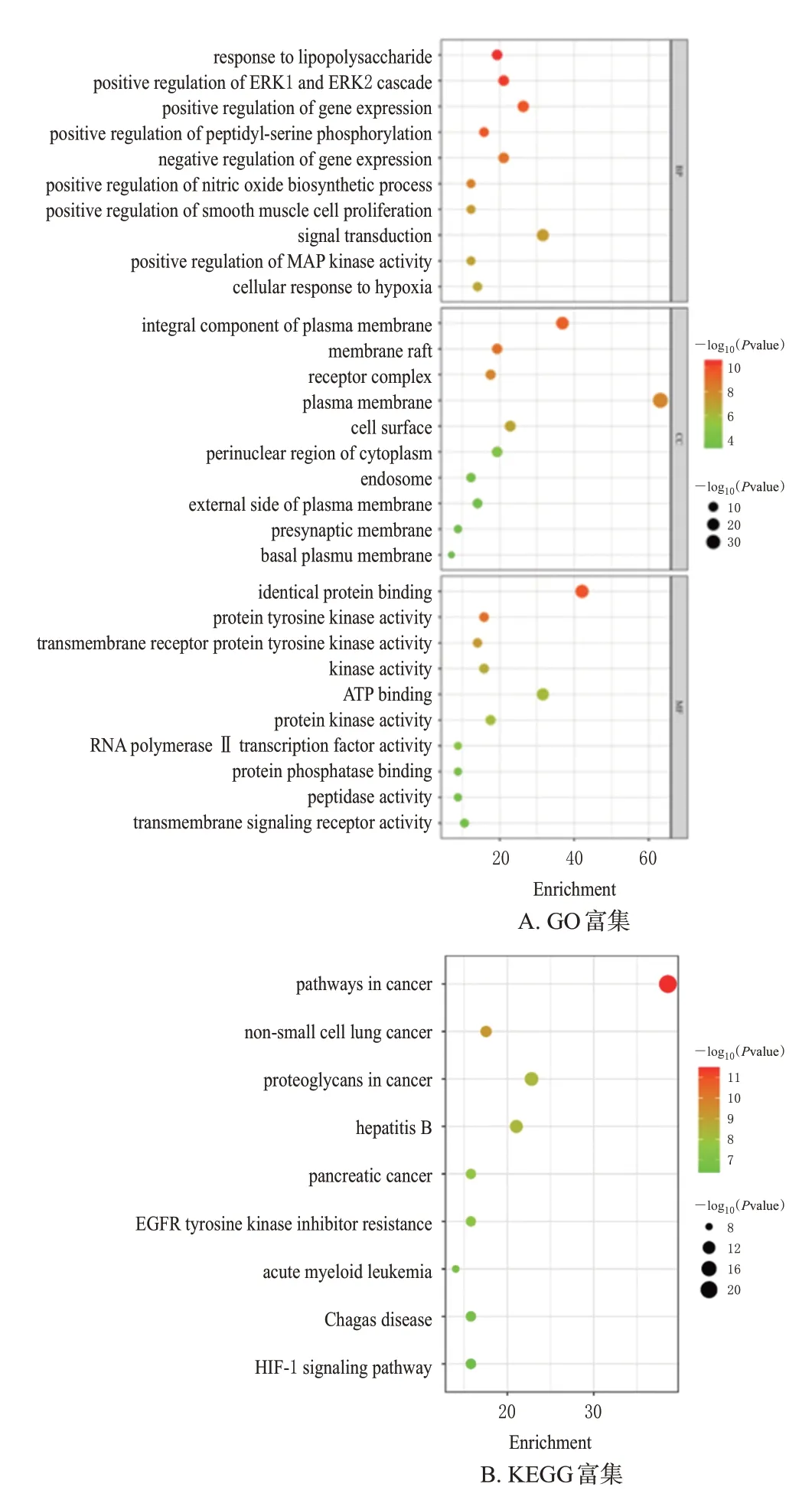
圖4 禿葉黃檗果實祛痰止咳GO 富集分析條形圖和KEGG富集分析氣泡圖
2.5.5 分子對接驗證
使用AutoDock Tools 1.5.6 軟件將“2.5.1”項下篩選獲得的活性成分、鎮咳陽性藥物右美沙芬與“2.5.3”項下分析所得的5個核心作用靶點進行分子對接,結果見表4。一般認為,對接結合能≤-5.0 kcal/mol(1 cal=4.184 J),說明兩者結合活性較好[13]。本研究中,除靶點VEGFA 與成分月桂烯和α-蒎烯的結合能略大于-5.0 kcal/mol 外,其他成分和靶點的結合能均不大于-5.0 kcal/mol,提示其均具有較好的結合能力。這說明所篩選的活性成分均有可能是禿葉黃檗果實祛痰止咳的物質基礎成分。
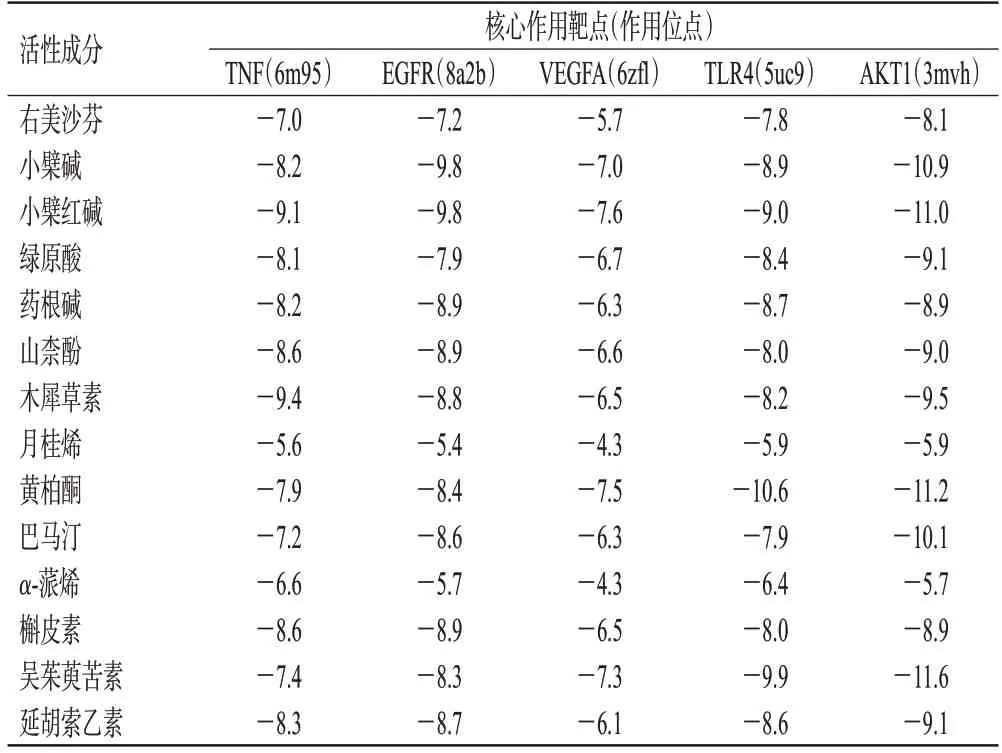
表4 右美沙芬、禿葉黃檗果實活性成分與核心靶點分子的對接結合能(kcal/mol)
3 討論
據報道,黃檗果實水煎液祛痰止咳的治療劑量以每日15 g為宜[5]。以成人體質量60 kg計,按照小鼠與人劑量的換算系數12.3計算,得到小鼠給藥劑量約為3 g/kg。另有研究表明,灌胃給予小鼠0.2~0.8 g/kg 的黃檗果實揮發油對小鼠有明顯的祛痰作用[6]。本研究參考黃檗果實的治療劑量,將12、3 g/kg 和0.8、0.2 g/kg 分別作為水煎液和揮發油祛痰止咳的高、低治療劑量。此外,氯化銨在藥物祛痰實驗研究中常被用作陽性對照藥物;右美沙芬屬于非成癮性中樞鎮咳藥,主要通過抑制延髓咳嗽中樞而發揮鎮咳作用,常被用作小鼠鎮咳實驗的陽性對照藥物。故本研究選擇右美沙芬和氯化銨作為陽性對照藥物,其給藥劑量參考文獻[9]設置。本研究結果表明,禿葉黃檗果實水煎液和揮發油均具有明顯的祛痰止咳作用,并呈明顯的劑量依賴趨勢。
晏晨等[14]研究發現,不同產地川黃檗果實的揮發油化學成分組成有較大差異。蔣太白等[8]研究表明,貴州產禿葉黃檗果實的揮發油主要成分為月桂烯(相對百分含量為66.9%)。本研究首次鑒定了四川產禿葉黃檗果實揮發油的化學成分組成,發現其主要成分同樣為月桂烯(相對百分含量為64.08%),表明不同產地禿葉黃檗果實的揮發油化學成分組成具有良好的一致性。本研究首次采用UPLC-MS技術對禿葉黃檗果實非揮發性成分進行鑒定分析,共鑒定出酚酸類、生物堿類、黃酮類等69個化合物,進一步補充完善了其化學成分的研究。
筆者查閱所鑒定出的化合物的祛痰止咳活性研究報道后發現,α-蒎烯具有祛痰止咳的活性,是祛痰藥桉檸蒎腸溶軟膠囊的指標性成分之一[11]。據《中華本草》記載,黃檗果實揮發油鎮咳作用的有效單體為月桂烯[7];綠原酸為返魂草、石韋等祛痰止咳中藥的指標成分之一[12,15];木犀草素為石韋、筋骨草和三子養親湯等祛痰止咳中藥和方劑的指標成分之一[15—16];小檗堿為藏成藥十味龍膽花顆粒的指標成分之一,適用于治療慢性支氣管炎[17]。且分子對接結果表明,上述成分與祛痰止咳核心靶點間均有較好的結合活性。因此,筆者推斷α-蒎烯、月桂烯、綠原酸、木犀草素和小檗堿等成分可能為禿葉黃檗果實祛痰止咳的物質基礎。
筆者利用網絡藥理學探究了禿葉黃檗果實祛痰止咳的作用機制,發現其核心作用靶點為TNF、EGFR、VEGFA、AKT1和TLR4。其中,TNF可誘導氧自由基的產生并導致組織損傷,還可以進一步激活核因子κB(nuclear factor kappa-B,NF-κB)通路中炎癥介質的轉錄和表達,促進炎癥的發生和發展[18]。TLR4 被激活后可通過一系列級聯反應激活NF-κB,使其入核并結合促炎基因啟動子,從而增強炎癥基因表達,釋放炎癥細胞因子[19]。AKT在細胞生長、遷移、增殖、炎癥和血管生成方面有重要作用,其亞型AKT1參與細胞的生長與存活,并在多種組織中表達[20]。咳嗽、咳痰是慢性支氣管炎患者最典型的癥狀,現代醫學認為慢性支氣管炎是因感染或其他非感染因素引起的支氣管及其周圍組織的非特異性炎癥。這說明,禿葉黃檗果實揮發油和水煎液可能主要通過緩解支氣管及其周圍組織的非特異性炎癥從而達到祛痰止咳的作用。GO分析和KEGG富集分析結果表明,禿葉黃檗果實祛痰止咳的作用機制主要是通過影響脂多糖的反應、肽基絲氨酸磷酸化的正向調節、一氧化氮生物合成過程的積極調節等生物過程,調節癌癥、非小細胞肺癌、癌癥中的蛋白聚糖等信號通路。
綜上所述,禿葉黃檗果實主要通過作用于TNF、EGFR、VEGFA、AKT1 和TLR4 等靶點及其顯著富集的信號通路發揮祛痰止咳的作用,其物質基礎可能為α-蒎烯、月桂烯、綠原酸、木犀草素和小檗堿等成分。但是,本研究僅對禿葉黃檗果實的化學成分作了GC-MS 和UPLC-MS 的定性分析,以及通過網絡藥理學分析了其祛痰止咳的物質基礎,缺乏對物質基礎化學成分的定量分析。本課題組后續將繼續開展對物質基礎成分的定量研究工作,為禿葉黃檗果實資源的進一步開發利用研究奠定理論基礎。

