釓對比劑全程化藥學服務共識
中國醫藥教育協會臨床合理用藥專業委員會,廣東省藥學會用藥評價與臨床科研專家委員會
釓對比劑(gadolinium-based contrast agent,GBCA)是磁共振成像(magnetic resonance imaging,MRI)對比劑中應用最廣泛的類型。全球首個GBCA——釓噴酸葡胺注射液[Gadopentetate acid dimeglumine salt injection,簡寫為Gd(DTPA),商品名馬根維顯]于1988 年問世,此后又有多個釓螯合物對比劑被開發并應用于臨床,涉及中樞神經系統、腹部、乳腺和心臟等身體各部位。伴隨不同釓對比劑的開發應用及對比增強磁共振成像(contrast-enhanced MRI,CE-MRI)技術的持續進步,MRI 檢查的敏感性、特異性和準確性均得到不斷提高[1—2]。
GBCA 的不同理化性質決定了其在患者體內的動力學行為及安全性、有效性[3]。雖然目前學者普遍認為釓對比劑是安全的,但仍有極少數患者會出現嚴重的不良反應[如急性不良反應和腎源性系統性纖維化(nephrogenic systemic fibrosis,NSF)等][4—5],除此之外還需考慮腦部釓沉積的風險[6]。與此同時,不同的GBCA 在特殊人群(如腎功能不全患者、妊娠期婦女、哺乳期婦女、兒童、老年人等)中的應用有不同要求,臨床應尤為關注。
對于GBCA 的安全使用和用藥監護目前尚缺乏較為系統、全面的藥學共識,本文主要從常用GBCA 的臨床合理使用與安全性管理兩個方面進行闡述并撰寫全程化的藥學服務共識,以期為該類藥物的合理使用提供依據,也為醫師處方該類藥物及藥師審核處方提供參考。
1 編制背景及工作流程
為更好地制定GBCA的全程化藥學服務共識,使醫療機構在GBCA臨床合理使用方面更具可操作性,使該類藥物的使用和管理進一步規范化、同質化,中國醫藥教育協會臨床合理用藥專業委員會聯合廣東省藥學會用藥評價與臨床科研專家委員會于2022年發起了《釓對比劑全程化藥學服務共識》編寫項目。
本共識工作組由專家組、編寫組構成。專家組由中國醫藥教育協會臨床合理用藥專業委員會、廣東省藥學會用藥評價與臨床科研專家委員會中具有副高級及以上職稱專家組成,涵蓋藥學、醫學專家,負責共識中臨床問題的確定及推薦意見的審核。編寫組設組長1名、副組長4名,主要協調共識編寫的全過程并參與臨床問題的確定和共識初稿的審核工作。具體執筆人由具有臨床合理用藥經驗及熟悉循證藥學相關工作的藥學人員組成,主要負責系統檢索已有的臨床證據及資料并形成報告以提供給專家組參考,以及完成共識初稿的編寫。
該共識的編寫框架及具體臨床問題是通過組織專家討論確定的。執筆人根據擬定的編寫框架及臨床問題開展中英文文獻檢索并撰寫共識初稿,中文數據庫包括中華醫學期刊數據庫、中國知網、萬方數據,英文數據庫包括PubMed、Cochrane 圖書館。編寫組對共識初稿開展了3輪會議討論,并廣泛收集臨床、藥學專家意見。編寫組及執筆人根據專家意見完成共識的修改及定稿。
2 GBCA概述
2.1 基本藥理作用
釓屬于稀土金屬,具有穩定的不成對電子,可形成強磁矩,通過縮短周圍水質子的T1(縱向)和T2(橫向)弛豫時間,間接產生信號增強作用,從而增強圖像對比度,可有效增強病變組織(如腫瘤)和背景組織(正常組織)之間的信號強度差。GBCA以縮短T1弛豫時間為主,在T1加權像上的增強表現為高信號,其弛豫率受溫度、磁場強度和組織環境(水、血漿或血液)的影響。經靜脈注射后,GBCA 可快速經血液循環到達全身血管,然后快速從血管進入血管外間隙;大部分GBCA通過腎臟系統排泄,因此其在腎功能不全患者體內的半衰期較長;其中釓塞酸二鈉、釓貝葡胺部分經肝膽系統排出體外[2,7],因此具有肝臟特異性。
2.2 分類
理想的MRI 對比劑必須具有出色的成像效果和特異性,能在組織中保留一段時間并顯示出良好的對比度。成像后,大部分對比劑應從靶組織排泄,具備半衰期短、化學穩定性好、清除率高、弛豫率高等特點[2]。可根據在溶液中的凈電荷將GBCA 分為離子型和非離子型,根據其螯合配體的分子結構(可能是離子性或非離子性的)分為線性和大環狀。臨床常用GBCA基本特性的比較[8—9]見表1。

表1 臨床常見GBCA基本特性的比較
2.2.1 線性常規弛豫率GBCA
線性常規弛豫率GBCA最早被開發并應用于臨床,其主要的代表藥物包括釓噴酸葡胺和釓雙胺。釓噴酸葡胺是一種釓(Gd3+)螯合物,是廣泛使用的MRI對比劑之一。1988 年,釓噴酸葡胺被最先應用于臨床研究;隨后,一系列釓螯合物也開始應用于臨床;研究者對Gd(DTPA)進行修飾,合成了很多的Gd(DTPA)的衍生物[10],其中就包括釓雙胺。
線性常規弛豫率GBCA 與潛在的生物毒性問題有關[7]。歐洲泌尿生殖放射學會(European Society of Urogenital Radiology,ESUR)的對比劑指南將釓噴酸葡胺及釓雙胺列為NSF 的高風險藥物,歐洲藥品管理局(European Medicines Agency,EMA)已經暫停其在靜脈內使用[11]。
2.2.2 大環狀常規弛豫率GBCA
大環狀常規弛豫率GBCA 以DOTA 或其衍生物作為配體,具有很高的穩定性,目前臨床應用的主要代表藥物包括釓特醇、釓布醇和釓特酸葡胺。與線性常規弛豫率GBCA相比,大環狀常規弛豫率GBCA具有更高的動力學惰性,更有助于減少GBCA 在組織中的蓄積,提高其安全性[3]。
2.2.3 線性高弛豫率、肝特異性GBCA
在正常情況下,GBCA 僅分布于細胞外間隙,不會進入細胞內。在DTPA 骨架中引入疏水性含苯環基團,能增加分子的親脂性,使其可被肝細胞選擇攝取,形成線性高弛豫率、肝特異性GBCA。
目前,肝特異性GBCA主要包括釓貝葡胺和釓塞酸二鈉,二者都能被肝細胞選擇攝取,并經膽汁排泄,具有肝臟靶向性。肝特異性GBCA 可進行動態三期增強和肝膽期成像檢查,可使肝癌及轉移瘤的檢出率顯著提高[2]。此外,最新研究表明,釓貝葡胺對于肝細胞癌的診斷敏感性要顯著高于釓塞酸二鈉[12]。
由于肝特異性GBCA 的化學結構與線性常規弛豫率GBCA不同,使得該類GBCA穩定性有所提升。已有研究證實了釓貝葡胺和釓塞酸二鈉的NSF 風險極低[13—17],故歐美監管機構均未限制其在肝臟應用。
2.2.4 大環狀高弛豫率GBCA
未來GBCA 的發展方向是追求更好的化學穩定性和更高的弛豫率。其中,釓哌啶醇(gadopiclenol)具有基于吡咯的大環狀結構,在Gd解離方面具有高度穩定性,并且表現出更高的弛豫率(是傳統釓劑的2 倍以上)[18—19]。2021年3月的一項Ⅲ期臨床研究結果顯示,與釓布醇相比,釓哌啶醇僅需一半劑量即可在多種適應證中展現更好的效果[20]。釓哌啶醇于2022 年9 月獲美國FDA 批準適用于2 歲及以上的兒童和成人患者CEMRI,并預計于近期在歐洲上市。
2.3 藥代動力學/藥效動力學
所有臨床批準的GBCA都是中性的或帶負電荷的,具有幾乎相同的生物分布特性。GBCA 通常是細胞外液對比劑,并在細胞外空間迅速平衡。反映藥物分布和消除的藥代動力學參數(清除率、分布/消除半衰期、穩態分布容積)可通過血漿濃度對時間數據擬合到標準二室開放模型來確定。
由于該類藥物的高度親水性,其在健康個體中可通過腎臟快速消除,半衰期約為90 min。此外,幾乎所有(>90%)靜脈注射的GBCA均在24 h內通過腎臟排泄,腎功能不全的患者清除速度較慢。值得注意的是,配體結構上具有疏水性芳香族取代基的藥物(包括釓貝葡胺和釓塞酸二鈉)可部分通過肝膽排泄清除,其中釓塞酸二鈉因有50%通過肝臟排泄而被廣泛用作肝特異性GBCA[3,21]。
3 GBCA的臨床合理使用
3.1 適應證和禁忌證
匯總不同GBCA 藥品說明書中的適應證和禁忌證(表2)可以發現,除釓塞酸二鈉作為肝特異性GBCA 僅用于檢測肝臟局灶性病變外,其余6種均可用于中樞神經系統和全身MRI檢查。其中,中樞神經系統包括腦及脊髓;全身檢查包括面部顱骨、頸部、含心臟的胸腔和腹腔、女性乳腺、盆腔和四肢,以及全身血管成像。
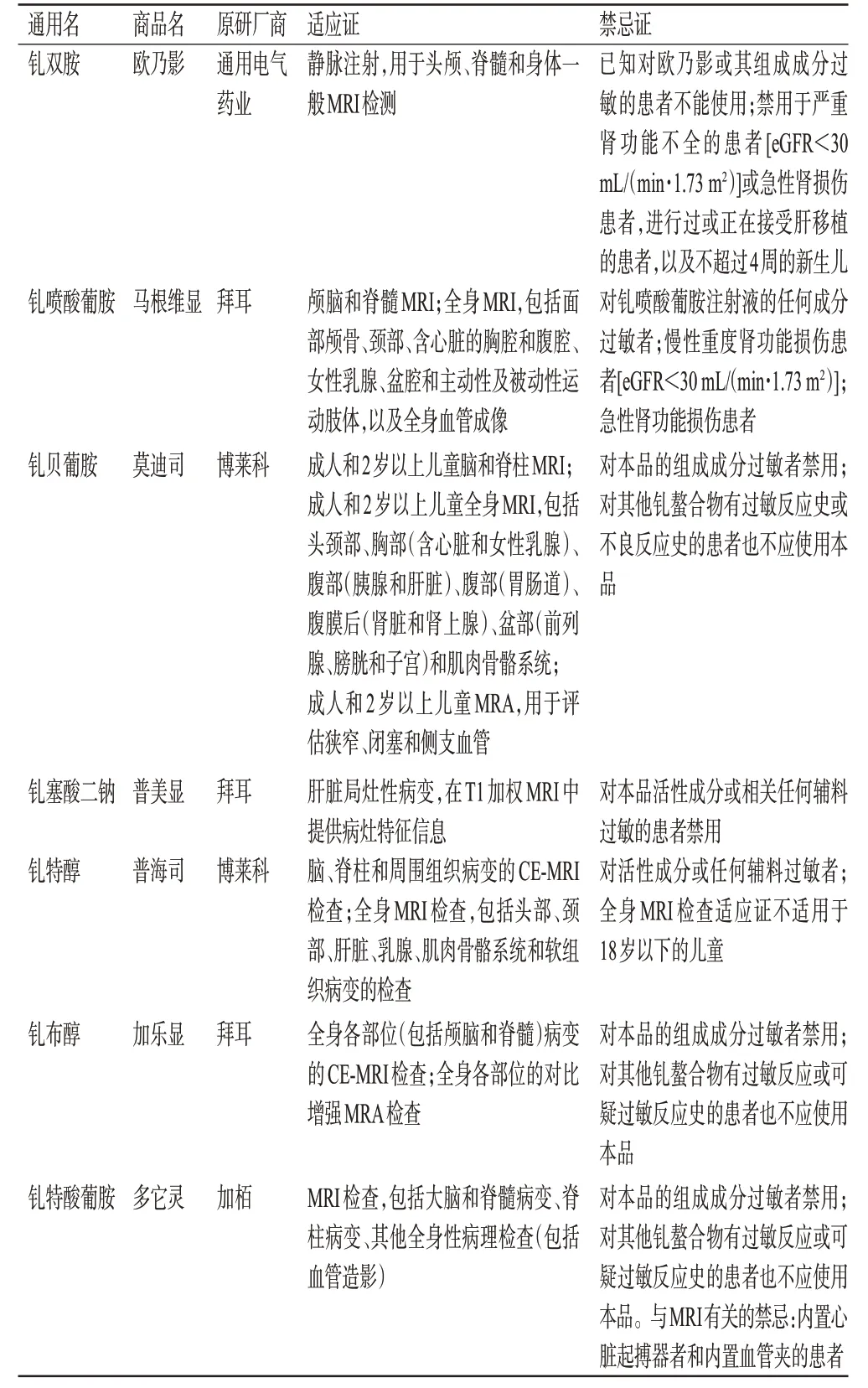
表2 不同GBCA的適應證及禁忌證比較
禁忌證方面,7 種GBCA 的藥品說明書均提示對藥物組成成分過敏者禁用;此外,釓噴酸葡胺、釓雙胺禁用于嚴重腎功能不全 [eGFR<30 mL/(min·1.73 m2)]或急性腎損傷患者。
在適用年齡范圍方面,《美國放射學會對比劑使用指南》[1](以下簡稱《ACR指南》)提到,兒童使用GBCA常存在超說明書應用。釓噴酸葡胺和釓布醇的使用范圍覆蓋了全年齡段;釓特酸葡胺除規定18歲以下兒童禁用于血管造影外,其余使用范圍覆蓋了全年齡段;釓雙胺的使用范圍包括6個月以上兒童;釓貝葡胺的適應證包含2歲以上兒童;釓特醇的使用范圍包括兒童中樞神經系統和周圍組織病變,不包含18 歲以下兒童的全身適應證。
對于腎功能不全的患者,需要進行eGFR 及臨床情況的評估,根據腎功能不全程度合理選擇GBCA。具體使用推薦[4]見表3。

表3 不同腎功能成人患者的GBCA使用推薦
由于影像對比劑的檢查人群和用途廣泛,應根據患者情況及GBCA的應用特點合理選用,避免發生不良事件后因超適應證或違反禁忌證帶來的風險。
3.2 注意事項
3.2.1 共同注意事項
使用GBCA 會增加藥物清除功能受損患者發生NSF 的風險,對于慢性重度腎功能損傷[eGFR<30 mL/(min·1.73 m2)]以及急性腎功能損傷患者應避免使用GBCA。釓雙胺和釓噴酸葡胺屬于NSF 高風險GBCA,EMA 禁止靜脈內使用[11]。《ACR 指南》推薦在特殊人群中避免使用高風險GBCA[1]。
線性GBCA 和大環狀GBCA 均會在大腦及其他組織中造成痕量釓沉積。
3.2.2 其他注意事項
特殊人群如孕婦、兒童、老年人應謹慎使用GBCA。因產品特性不同,哺乳期婦女在使用GBCA 后,建議舍去12 h 內或24 h 內的乳汁;心血管疾病患者、癲癇患者應謹慎使用釓貝葡胺、釓特醇;有對比劑過敏史的患者在使用釓特酸葡胺時,臨床應采取密切監測等特別預防措施,必須事先準備所有必要的設備和藥品以處理可能出現的抽搐。部分特殊人群在接受GBCA 后的注意事項見表4。

表4 特殊人群接受GBCA后的注意事項
3.3 用法用量
GBCA通常使用的單次標準劑量為0.1 mmol/kg,釓塞酸二鈉為0.025 mmol/kg。對于新生兒(<1 個月)和嬰幼兒(1 個月~2 歲)而言,由于其腎功能尚未發育完全,故只有在進行仔細評估后才可使用,并建議盡可能使用最低批準劑量。釓噴酸葡胺藥品說明書特別指出,新生兒和嬰幼兒所需的劑量應當手推給予,不得使用自動注射器,以免造成傷害。
關于GBCA 的注射間隔時間,各國指南推薦不一。《歐洲泌尿生殖放射學會對比劑使用指南》(以下簡稱《ESUR 指南》)推薦:正常腎功能及中度腎功能損傷[eGFR>30 mL/(min·1.73 m2)] 患者應間隔4 h;重度腎功能損傷[eGFR<30 mL/(min·1.73 m2)]或透析患者應間隔7 d[11]。《ACR 指南》推薦:對于NSF 低風險患者來說,多次注射的間隔時間應根據實際臨床需要,未特別推薦間隔時間;對于NSF高風險(中重度腎功能不全或透析)患者,建議使用低風險GBCA,未推薦間隔時間[1]。《腎病患者靜脈注射釓對比劑應用中國專家共識》推薦:所有高危患者或使用高危GBCA 的患者如需重復檢查,間隔時間應大于7 d[21]。綜合以上意見,患者接受GBCA的間隔時間推薦見表5,GBCA 的臨床合理使用推薦見表6。
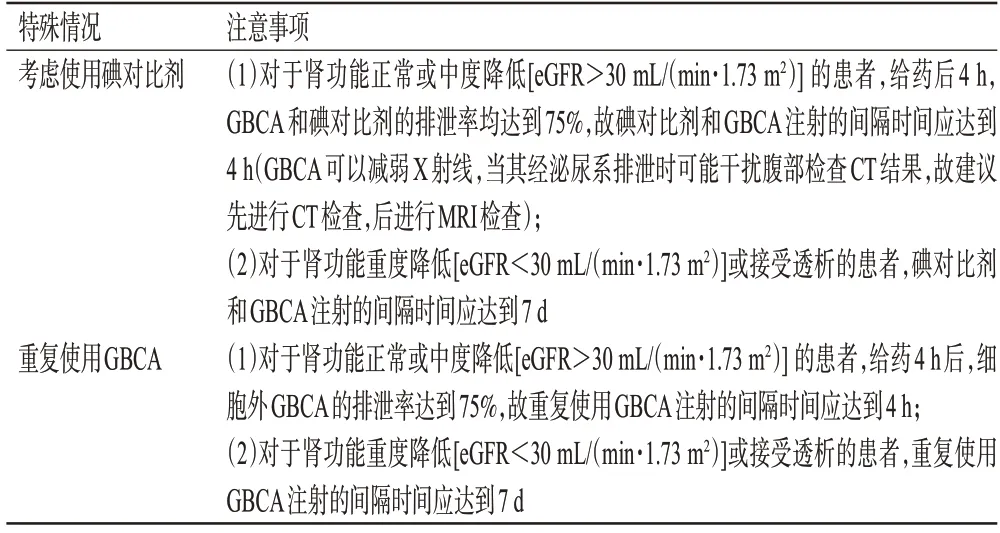
表5 患者接受GBCA的間隔時間推薦意見表

表6 GBCA的臨床合理使用推薦意見表
4 GBCA的安全性管理
4.1 過敏試驗
原則上不推薦進行GBCA過敏試驗,除非藥品說明書注明特別要求。因為過敏試驗結果呈陰性的患者也可能發生過敏樣反應甚至嚴重過敏樣反應;相反,結果呈陽性的患者也不一定會發生過敏樣反應,且過敏試驗本身也可能發生嚴重的不良反應[1]。
4.2 外滲
GBCA的外滲罕見,其發生率為0.05%(納入研究數量共28 000劑)。MRI研究中,對比劑的用量通常較小,這樣可降低筋膜室綜合征的發生概率。由于這些原因,由MRI對比劑外滲造成嚴重損傷的可能性極低[1]。
4.3 預防用藥
預防用藥只能預防急性過敏樣反應,對輕度過敏樣反應有一些預防效果[11],對血管迷走神經等生理性反應無效。
4.4 急性不良事件的鑒別、診斷與處理
對比劑急性不良反應多見于注射1 h內,無論碘劑、GBCA 還是超聲對比劑,其分類和處理原則均相同[11]。GBCA 的急性不良反應主要分為過敏樣反應和生理性反應,根據嚴重程度又分為輕度、中度和重度3 類。GBCA總體不良反應發生率較低[22]。
根據《ACR指南》,對GBCA急性不良反應的處理與碘對比劑相似。GBCA 不同類型急性不良反應的處理措施[1,11]可參考表7。

表7 GBCA常見急性不良反應及處理措施
4.5 遲發性不良反應NSF的關鍵問題
4.5.1 NSF的歷史概述
NSF 是一種以廣泛的皮膚和結締組織纖維化為特征的嚴重全身性疾病,可導致四肢皮膚增厚和硬化,造成關節固定和攣縮,嚴重者可導致死亡。我國也有NSF病例的報道,但總體數量稀少,可能與臨床對該病認識不足,且確診困難有關[11,23]。
4.5.2 歐美GBCA相關指南意見及主要風險因素
NSF 的確切致病機制尚不清楚。廣為接受的假說是由于GBCA 清除時間長及其他與腎臟疾病相關的代謝因素;在腎功能顯著退化的患者中,釓離子與GBCA中的螯合物分離,游離釓與陰離子(如磷酸鹽)結合,產生的不溶性沉淀物沉積在各種組織中,隨后出現纖維化反應。
目前至少有8 種GBCA 在全球廣泛應用,可通過其螯合劑的不同進行區分。《ACR指南》按照臨床實際NSF病例發生情況對使用GBCA 后發生NSF 風險的大小進行了相應分類[1]——(1)高風險的GBCA:釓雙胺、釓噴酸葡胺、釓弗塞胺;(2)低風險的GBCA:釓貝葡胺、釓特醇、釓布醇、釓特酸葡胺;(3)風險不明確的GBCA:釓塞酸二鈉。
GBCA 導致NSF 的風險因素包括患者和對比劑兩方面。腎功能降低,尤其是eGFR<15 mL/(min·1.73 m2)的透析患者易發生NSF。嚴重腎功能不全患者注射釓雙胺后的NSF 發生率為3%~18%;釓弗塞胺和釓噴酸葡胺也有致NSF的報道,嚴重腎功能不全患者使用釓噴酸葡胺后NSF 的發生率為0.1%~1.0%;注射劑量越大,風險越高,但也有單次劑量注射發生NSF的報道[4]。
4.6 腦沉積
研究表明,所有的GBCA即使單次暴露都可能導致患者腦深部區域的釓沉積[23—25],腎功能正常的受試者也如此[24—26]。大環狀GBCA 的沉積率比線性GBCA 低[11]。此外,一項釓雙胺的研究表明,釓沉積與使用劑量具有相關性[24]。研究證實,早期釓沉積量從小到大依次為:釓特醇<釓特酸葡胺<釓布醇<線性高弛豫率GBCA<線性常規弛豫率GBCA[25,27—28]。目前,腦內釓沉積的臨床和生物學意義仍然未知,尚未發現腦內釓沉積與任何實際臨床癥狀或疾病有關。即便如此,考慮到單劑量GBCA 可能造成釓沉積,建議只有在非CE-MRI 無法提供充分診斷信息的情況下才使用GBCA。
4.7 藥物相互作用
GBCA與其他藥物之間無已知的相互作用。GBCA的安全用藥推薦意見詳見表8。

表8 GBCA的安全用藥推薦意見表
5 GBCA的全程化藥學服務
GBCA 全程化藥學服務流程可參見圖1,其用藥監護及教育記錄可參見圖2。

圖1 GBCA全程化藥學服務流程圖
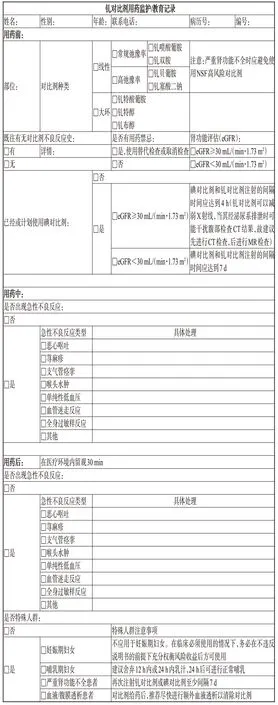
圖2 GBCA用藥監護/教育記錄
5.1 檢查前
(1)了解患者的過敏史、病史、用藥史,如患者曾有使用同類GBCA過敏史,可考慮預防用藥。
(2)對患者進行腎功能評估,如患者存在腎功能受損情況,根據表3來進行GBCA的品種選擇。
(3)核對患者所需使用的GBCA品種、劑量等。
(4)對患者進行口頭宣教,告知患者所使用的GBCA的使用目的、用法及可能出現的不良反應。
5.2 檢查中
注射GBCA過程中及注射后,密切觀察患者有無急性不良事件的發生,如有發生,根據所發生事件為過敏樣反應/生理性反應分為輕度、中度或重度,并采取相應的應急措施。
5.3 檢查后
為及時識別并處理GBCA的急性不良反應,建議患者注射后在醫療機構內留觀30 min[11]。患者出現急性不良反應時的應對措施可參見表7[11]。此外,特殊檢查人群檢查后的注意事項參見表4,GBCA 與碘對比劑或兩次GBCA之間的使用間隔時間可參照表5。
6 結語
GBCA在各醫療機構中應用廣泛,其不合理使用將導致藥物不良事件及醫療成本增加。本共識工作組通過多輪專家研討及文獻檢索形成關于GBCA 臨床合理使用的推薦意見,并基于臨床實際制定了操作性強的GBCA 全程化藥學服務流程。本共識的發布將為臨床醫生、護士合理使用該類特殊藥品提供依據,也為藥師針對該類藥物進行處方審核、用藥監護及用藥教育等藥學服務提供重要參考。
參考藥品說明書版本
釓雙胺注射液(商品名歐乃影),修改日期為2016年4月
釓噴酸葡胺注射液(商品名馬根維顯),修改日期為2019年4月11日
釓貝葡胺注射液(商品名莫迪司),修改日期為2022年1月29日
釓塞酸二鈉注射液(商品名普美顯),修改日期為2019年7月15日
釓特醇注射液(商品名普海司),修改日期為2020年12月8日
釓布醇注射液(商品名加樂顯),修改日期為2019年1月17日
釓特酸葡胺注射液(商品名多它靈),修改日期為2011年3月23日
Gadopiclenol injection(釓哌啶醇注射液,商品名Vueway),修改日期為2022年9月
編寫組成員
組 長:
王 勇(南方醫科大學珠江醫院)
副組長:
喻珊珊(南方醫科大學珠江醫院)
謝守霞(深圳市人民醫院)
黎小妍(中山大學附屬第六醫院)
劉 韜(中山大學腫瘤防治中心)
執筆人:
肖 琰(深圳市人民醫院)
覃 利(中山大學附屬第六醫院)
劉 晶(南方醫科大學珠江醫院)
鄧俊麗(南方醫科大學珠江醫院)
余柱立(中山大學腫瘤防治中心)
專家組成員(按姓氏漢語拼音排序)
蔡本志(哈爾濱醫科大學附屬第二醫院)
陳靈俊(海口市人民醫院)
戴海斌(浙江大學醫學院附屬第二醫院)
何瑞榮(東莞市人民醫院)
黃際薇(中山大學附屬第三醫院)
黃學全(中國人民解放軍陸軍軍醫大學第一附屬醫院)
季 波(中國人民解放軍南部戰區總醫院)
江東波(廣東醫科大學附屬醫院)
賴偉華(廣東省人民醫院)
李雪芹(中山市人民醫院)
李亦蕾(南方醫科大學南方醫院)
林 華(廣東省中醫院)
麥海燕(中山大學附屬第三醫院)
孟小斌(梅州市人民醫院)
潘 杰(蘇州大學附屬第二醫院)
彭曉青(廣州市第一人民醫院)
王景浩(暨南大學附屬第一醫院)
魏 理(廣州醫科大學附屬第一醫院)
溫志波(南方醫科大學珠江醫院)
吳 暉(昆明醫科大學附屬第一醫院)
吳瓊詩(海南省人民醫院)
伍俊妍(中山大學孫逸仙紀念醫院)
肖澤宇(暨南大學附屬第一醫院)
楊西曉(南方醫科大學深圳醫院)
張述耀(暨南大學附屬廣州紅十字會醫院)
張 肖(中國人民解放軍總醫院第一醫學中心)
鄭志昌(貴州醫科大學附屬醫院)

