紫花苜蓿GPAT基因家族鑒定及在鹽堿脅迫下的表達模式分析
唐 芳, 梅 亭, 高佳荷, 王佳妮, 石鳳翎, 高翠萍
(內蒙古農業大學草原與資源環境學院, 內蒙古 呼和浩特 010010)
植物脂質是生物膜的重要組成成分,在能量轉換、碳儲備、信號轉導以及脅迫應答等方面發揮著不可估量的作用[1]。植物脂質種類繁多,包括甘油磷脂類、脂肪酸類、鞘脂類、糖脂類等[2],其生物合成受到基因和蛋白質網絡的精確調控[3]。甘油-3-磷酸酰基轉移酶(Glycerol-3-phosphate acyltransferase,GPAT)催化酰基從酰基輔酶A(Acylcoenzyme A,acyl-CoA) 或酰基載體蛋白(Acyl-carrierprotein,acyl-ACP)轉移到甘油-3-磷酸(glycerin-3-phosphate,G3P) 的sn-1或sn-2位置,生成溶血磷脂酸(Lysophosphatidic acid,LPA)[4]。LPA是形成多種甘油脂的重要中間體[5],是催化甘油酯合成的第一步反應[6]。因此,GPAT是三酰甘油(Triacylglycerol,TAG)生物合成的限速酶[7],參與多種脂類的生物合成途徑。植物中至少有3類GPAT基因參與甘油酯生物合成,分別定位在質體、線粒體和內質網[8]。GPAT除參與植物角質層及軟木脂合成外,也響應植物應對非生物脅迫[7],在植物生長發育及抵御逆境脅迫中具有重要作用。
GPAT基因已在多種植物中進行了全基因組鑒定和功能分析,包括擬南芥(Arabidopsisthaliana)[7]、百合(Liliumregale)[9]、大麥(Hordeumvulgare)[10]、水稻(Oryzasativa)[11]、連翹(Forsythiasuspense)[12]和蒺藜苜蓿(Medicagotruncatula)[4]等。擬南芥的AtGPATs基因研究最為深入,目前已鑒定出10個AtGPATs基因,分別為質體ATS1、線粒體AtGPAT1,2,3和內質網AtGPAT4,5,6,7,8,9[7]。根據進化距離的遠近程度將其分為3個亞組[7],分別是ATS1,AtGPAT9以及AtGPAT1,2,3,4,5,6,7,8。GPAT基因功能研究表明,ATS1參與膜脂質合成[13],AtGPAT1是花粉發育中的關鍵基因[14],但AtGPAT3功能尚待確定[13]。AtGPAT4,6,8均與植物角質層合成有關,其中AtGPAT4和AtGPAT8屬于高度同源的功能冗余基因,是植物角質層合成過程中的關鍵酰基轉移酶[15],AtGPAT6參與萼片和花瓣中角質層的合成[16]。AtGPAT5對根和種皮中軟木脂的合成至關重要[17],AtGPAT7與AtGPAT5同源性高,功能相似,在組織受傷時被強烈誘導[18]。AtGPAT9與種子含油量呈正相關[13]。GPAT基因除直接參與油脂生物合成,還與植物響應非生物脅迫存在一定程度的正向調控關系[19]。隋娜等[20]將堿蓬(Suaedasalsa)SsGPAT基因轉入擬南芥,顯著提高了鹽脅迫下擬南芥的發芽率和根長,進一步研究表明擬南芥中過表達的SsGPAT基因提高了PG不飽和脂肪酸含量,減輕了PSII和PSI系統的光抑制,最終增強宿主耐鹽性。
紫花苜蓿(Medicagosativa)屬于豆科苜蓿屬多年生牧草,有“牧草之王”的美譽,是世界上種植面積最大,分布最廣的人工牧草[21-22],蛋白含量高、適應性強[23],且具有改良土壤鹽漬化[24-25]、豐富土壤有機質等功效[24,26]。多個紫花苜蓿基因家族已有研究,如與低木質素遺傳改良有關的MsCCoAOMT基因家族[27],與種子貯藏、發育、光信號傳導等有關的bZIP轉錄因子基因家族[28],與響應干旱脅迫有關的MsTCP轉錄因子基因家族[29],與銅轉運有關的MsCOPT基因家族[30]等。但是,目前尚沒有關于紫花苜蓿MsGPAT基因家族的報道。
我國鹽堿地約有1 000 km2,土壤鹽堿化造成土壤理化性質受到破壞,嚴重危害植物生長[31]。鑒于MsGPAT基因家族在植物生長發育與鹽堿脅迫響應中的重要作用,本研究對紫花苜蓿MsGPAT基因家族進行鑒定和分析,并研究其在鹽堿脅迫下的表達模式,為進一步研究GPAT基因在紫花苜蓿中的具體功能(如耐鹽堿性)提供理論依據和候選基因。
1 材料與方法
1.1 MsGPAT基因鑒定
查詢文獻獲取10個AtGPAT基因家族成員信息,從TAIR10擬南芥數據庫(http://plants.ensembl.org)獲取擬南芥蛋白質序列,利用紫花苜蓿基因組、蛋白質序列和注釋信息(https://figshare.com/projects/whole_genome_sequencing_and_assembly_of_Medicago_sativa/66380[32])。鑒定MsGPAT基因家族成員。具體方法為:1、以擬南芥GPAT蛋白序列為靶序列,通過Blast比對紫花苜蓿蛋白質序列,獲取紫花苜蓿GPAT候選蛋白序列;2、利用Pfam(http://pfam.xfam.org)的PF01553隱馬爾可夫模型查找紫花苜蓿蛋白質序列獲取候選蛋白序列。以上兩種方法獲取的序列取并集,并去除重復序列,利用NCBI CDD(https://www.ncbi.nlm.nih.gov/Structure/bwrpsb/bwrpsb.cgi)、Phhmer(https://www.ebi.ac.uk/Tools/hmmer/search/phmmer)、SMART(http://smart.embl-heidelberg.de/)在線結構域預測工具進行驗證,保證所有MsGPAT結構域被識別為“Glycerol-3-phosphate acyltransferase”注釋(NCBI CDD結果)或PF01553(Pfam結果)或PlsC結構域(SMART結果),再根據植物GPAT蛋白質氨基酸序列長度(237~621個氨基酸)進行篩選,最終將符合以上要求的蛋白序列歸為MsGPAT基因家族成員。
1.2 蛋白質理化性質和染色體定位分析
利用ExPasy(https://web.expasy.org/protparam/)在線蛋白質分析工具預測氨基酸數、分子量、等電點和親水性指數等信息。基因長度按照非冗余外顯子長度之和計算。根據紫花苜蓿基因注釋文件信息,提取MsGPAT基因在染色體上的位置,并利用在線工具MagGene2[33](http://mg2c.iask.in/mg2c_v2.1/index.html)繪制基因的染色體定位圖。
1.3 基因結構、蛋白質基序和順式啟動元件分析
利用在線工具GSDS2.0(http://gsds.gao-lab.org/)分析MsGPAT家族成員的基因結構。通過MEME在線軟件(https://meme-suite.org/meme/tools/meme)預測,設定最大預測值為10。利用TBTools[34]展示motif和基因結構。選取MsGPAT基因距離起始密碼子上游的2 000 bp序列,利用PlantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)的Search for care工具預測并分析啟動子順式作用元件。
1.4 系統發育樹分析
通過MEGA7[35]軟件的NJ法構建系統進化樹,采用Mega7中的MUSCLE算法對擬南芥AtGPAT、蒺藜苜蓿MtGPAT與紫花苜蓿MsGPAT基因家族成員的蛋白質序列進行多序列比對,構建系統發育樹,比較進化距離(Bootstrap測試值設定為1 000)。使用Evolview[36](https://evolgenius.info)在線進化樹注釋工具,對進化樹進行注釋。
1.5 共線性分析
構建紫花苜蓿MsGPAT基因家族數據庫,利用Blast進行物種內序列比對,再利用MCScanX[37]進行共線性分析,并利用Circos軟件[38]繪制共線性關系圖。
1.6 基因表達分析
本研究基于楊紫貽[39]紫花苜蓿耐鹽評價體系,因此脅迫濃度和脅迫后取樣時間的選擇延用其設計。以紫花苜蓿耐鹽品種‘中苜1號’簡稱ZM1和敏鹽品種‘WL323’為研究對象,對2周齡幼苗進行200 mmol·L-1NaCl單鹽脅迫、50 mmol·L-1NaHCO3單堿脅迫以及200 mmol·L-1NaCl+50 mmol·L-1NaHCO3混合鹽堿脅迫,并選擇脅迫后0 h,6 h,12 h,24 h的根部(因根系鹽脅迫下地下部分直接與鹽堿溶液接觸[40],首先受到影響[41])轉錄組測序結果進行分析。數據對原始FPKM值進行Log2(FPKM+1)變換已滿足方差分析的條件,并利用Excel軟件繪制差異基因表達模式圖。
2 結果與分析
2.1 紫花苜蓿MsGPAT基因家族鑒定
MsGPAT基因家族成員在NCBI CDD數據庫中均被注釋為“Glycerol-3-phosphate acyltransferase”,在Pfam數據庫中大部分被識別為pfam結構域(PF01553),在Smart數據庫中大部分被識別為PlsC結構域。本研究中,將存在以上3種結構域中的任意一種蛋白質序列視為MsGPAT基因家族成員。Waschburger等人分析了450個GPATs蛋白質特性,認定GPATs蛋白質結構氨基酸長度在237~621個之間[3],故剔除不符合該長度范圍內的蛋白質33個。最終從紫花苜蓿全基因組中鑒定出73個MsGPAT基因家族成員,按照其在染色體位置的先后順序,分別命名為MsGPAT1-MsGPAT73。如表1所示,MsGPAT基因家族成員的ORF長度為720 bp~1 530 bp,編碼239~509個氨基酸,其中蛋白質序列最長的是MsGPAT63,最短的是MsGPAT8。MsGPAT分子量介于26.8 kDa~57.9 kDa之間,理論等電點的變化相對較小,介于5.9~9.5之間,只有9個MsGPAT基因編碼的蛋白等電點小于7。(表1)
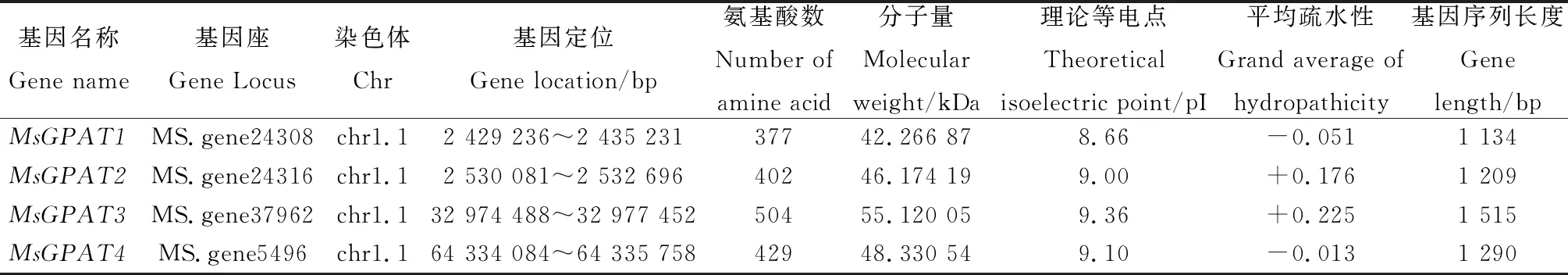
表1 紫花苜蓿MsGPAT基因家族成員信息
2.2 紫花苜蓿染色體定位分析
對MsGPAT基因家族成員進行染色體定位分析,結果表明MsGPATs的69個成員分布在紫花苜蓿26條染色體上,其余4個基因定位在scaffold上。如圖1所示,Chr1.3,Chr7.4上分布的MsGPAT基因最多,均有5個成員;Chr2.2,Chr2.4,Chr4.1,Chr8.4上的含有的MsGPAT基因家族成員最少,僅有1個;其余20條染色體上分布著2~4個MsGPAT基因家族成員。此外,scaffold 6938,10775,10776和10777上分別分布著1個MsGPAT基因家族成員。紫花苜蓿MsGPAT基因家族成員在染色體上呈不均勻分布,多分布于各染色體的兩端,且MsGPAT1和MsGPAT2,MsGPAT5和MsGPAT6,MsGPAT8至MsGPAT10,MsGPAT13和MsGPAT14、MsGPAT23和MsGPAT24,MsGPAT25和MsGPAT26呈小范圍簇狀排列。
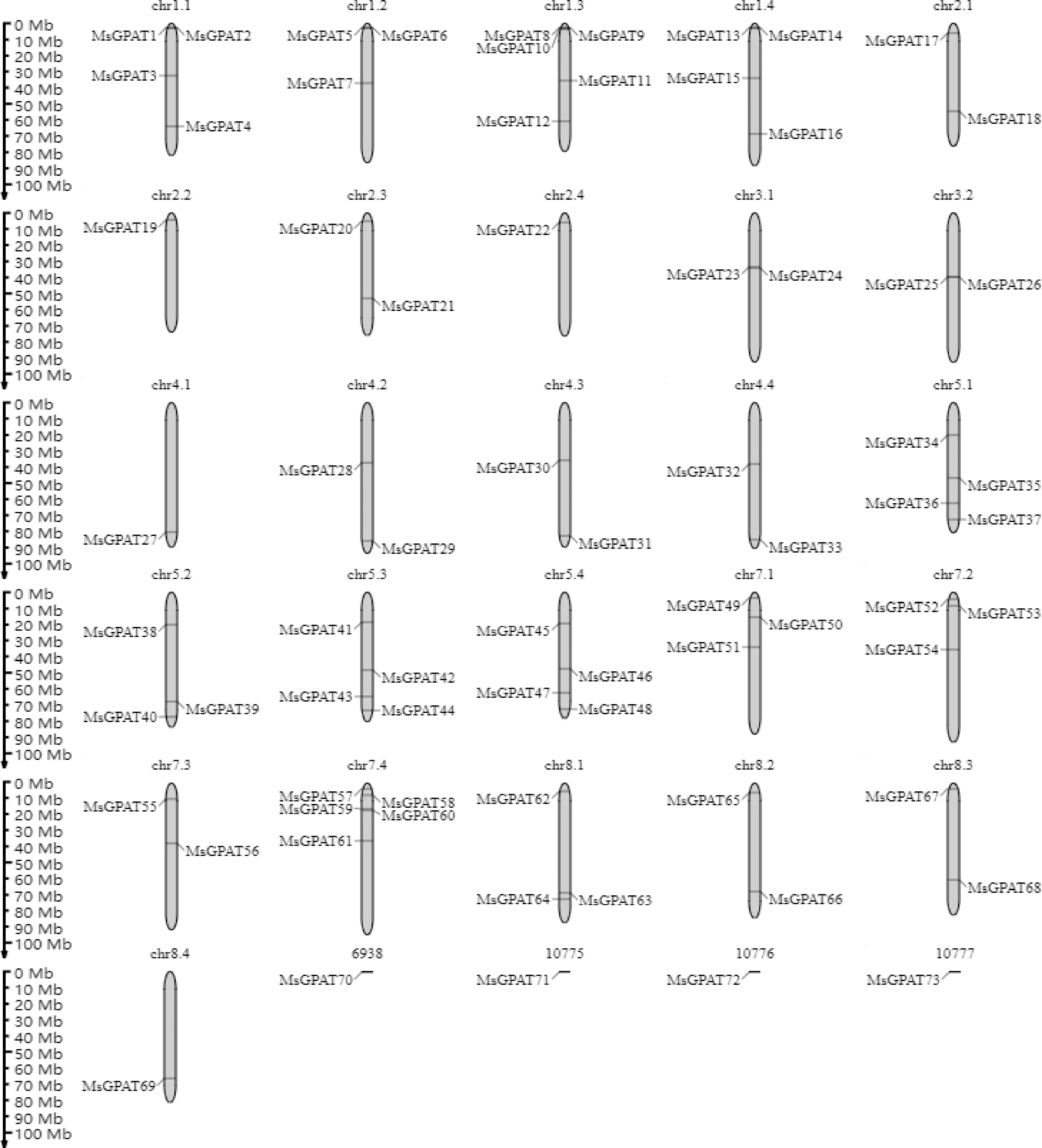
圖1 紫花苜蓿MsGPAT基因的染色體定位分析
2.3 紫花苜蓿MsGPAT基因結構分析和保守基序分析
紫花苜蓿MsGPAT基因結構分析顯示(圖2),除MsGPAT15外,其余基因家族成員均含有內含子,內含子數在1~13個之間。不同成員基因結構存在較大差異,MsGPAT63和MsGPAT68基因結構最復雜,含有14個外顯子;而MsGPAT15基因結構最簡單,僅有1個外顯子。其中,含有2~3個外顯子的成員共有38個,占比52%;含有11~12個外顯子的成員共有18個,占比25%;含有介于4~10個外顯子的成員共14個,占比19%。

圖2 紫花苜蓿MsGPAT基因結構和保守基序
利用Meme軟件對MsGPAT基因編碼蛋白的保守基序進行分析,共鑒定出10個保守基序(圖2)。其中最保守的基序是Motif8,共有70個基因家族成員含有該基序,只有MsGPAT23,25,61不含有該基序。MsGPAT基因家族成員含有1~8個保守基序,其中含有全部8個基序的成員共30個,占比41%;僅含有1個保守基序的成員有MsGPAT34,38,41,45,49,52,57占比9%。
2.4 紫花苜蓿MsGPAT基因順式啟動元件分析
基因編碼區上游區域存在多個順式作用元件,具有調控相關基因表達的特性。本研究對73個MsGPAT基因的啟動子區域進行順式作用元件分析,以用于預測MsGPAT基因的潛在功能。如圖3所示,通過對光反應元件(TCCC-motif,LAMP-element,GT1-motif)、生長素反應元件(G-Box和TGA-element)、脅迫反應元件(MYC,ABRE,MYB,W-box,GT1-motif,LTR和MBS)進行分析,MsGPAT基因成員的順式作用元件差異較大,如MsGPAT71含有上述9種類型的順式作用元件,而MsGPAT19則只有上述3種類型的順式作用元件。在脅迫反應元件的種類上,大部分基因都有4個以上的脅迫應答元件,表明MsGPAT基因廣泛參與植物響應逆境脅迫。
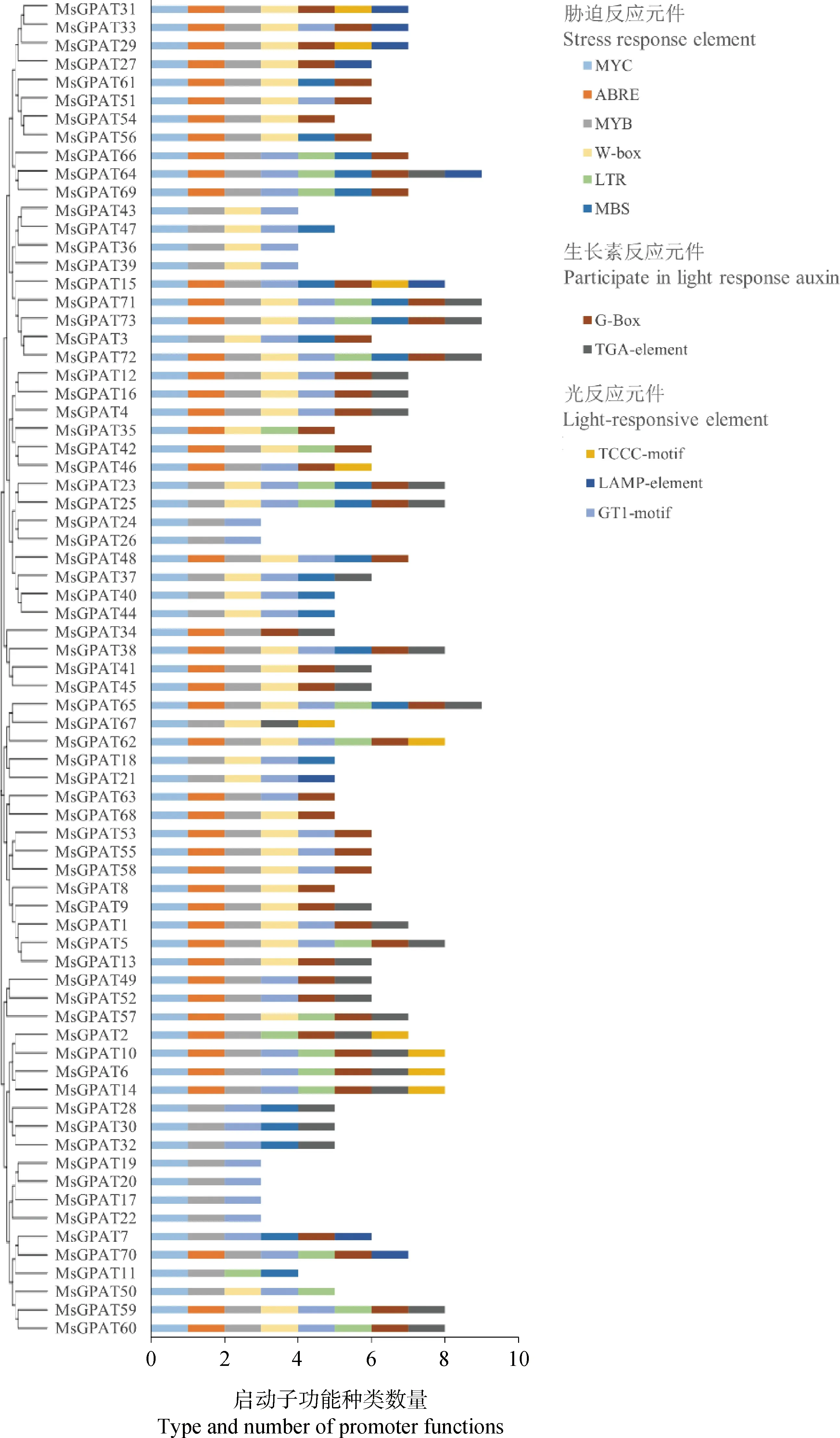
圖3 紫花苜蓿MsGPAT順式作用元件
2.5 紫花苜蓿MsGPAT基因家族系統發育分析
對10個擬南芥AtGPATs基因家族成員、24個蒺藜苜蓿MtGPATs基因家族成員和73個紫花苜蓿MsGPATs基因家族成員構建系統發育樹(圖4),結果表明73個紫花苜蓿成員分為3個亞家族,與擬南芥AtGPATs基因分組相同[4]。其中,24個MsGPATs基因、8個MtGPATs基因和擬南芥ATS1聚成第1亞族,表明該組基因與ATS1進化關系較近,與ATS1處于同一分支的MsGPAT34,38,45,41基因具有與擬南芥ATS1類似的12個外顯子結構,均只含有1個motif。其他亞組MsGPATs基因外顯子從2~11個不等。第2亞族中,15個MsGPATs基因,6個MtGPATs基因與AtGPAT9具有較近的進化距離。其中MsGPAT67,21,18與AtGPAT9基因結構類似,具有12個外顯子,以及3個motif結構。第3亞族中,共包含34個MsGPATs基因、10個MtGPATs成員和擬南芥AtGPAT1-8。該亞族中MsGPATs基因均具有2~3個外顯子,與擬南芥AtGPAT1-8的基因結構類似,并具有相似的motif結構。
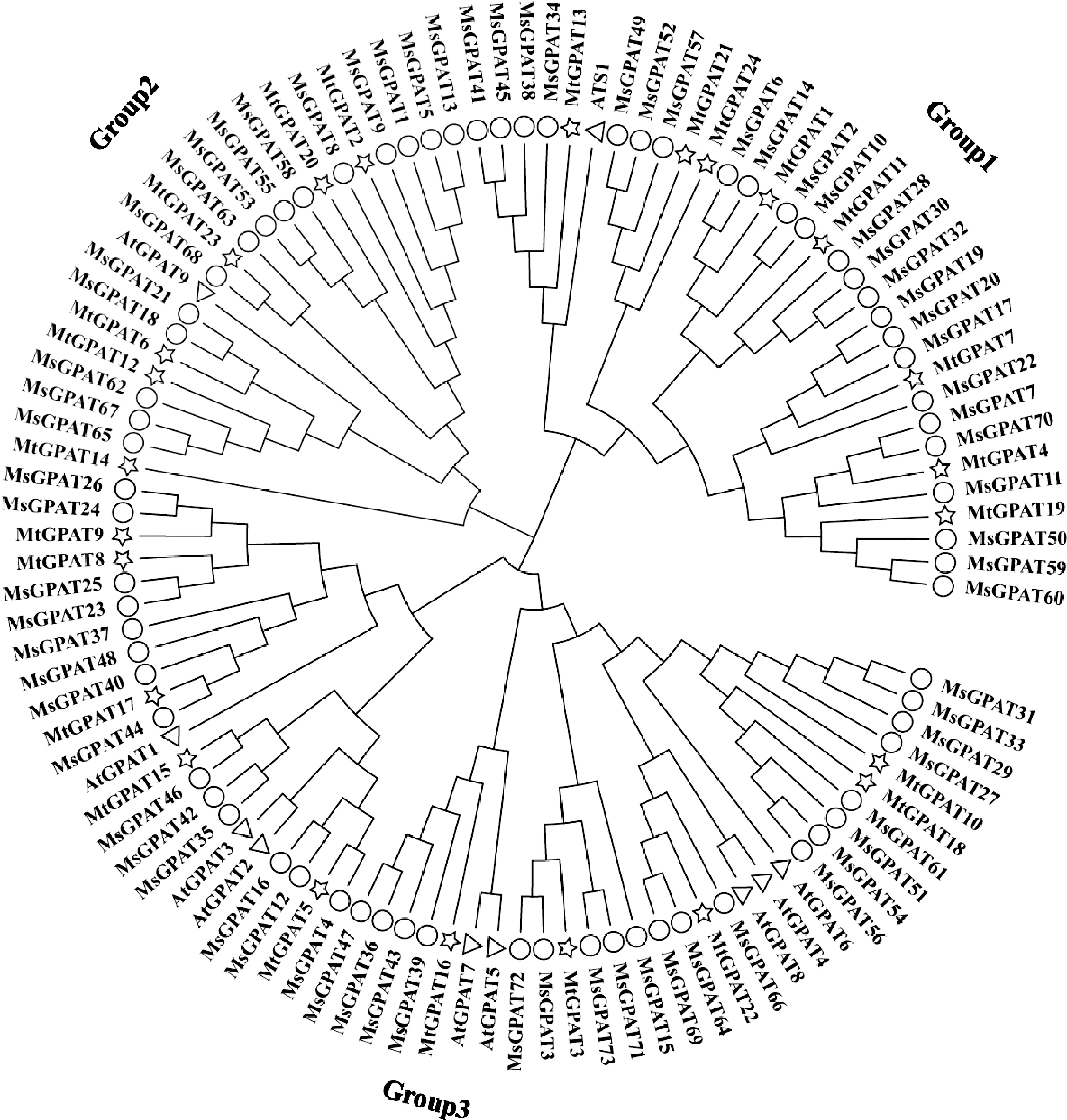
圖4 紫花苜蓿MsGPAT、蒺藜苜蓿MtGPAT和擬南芥AtGPAT基因家族系統進化分析
2.6 紫花苜蓿MsGPAT基因家族共線性分析
紫花苜蓿MsGPAT基因家族大部分成員具有共線性關系,具有高度同源性(圖5)。如同源染色體Chr1.1上的MsGPAT1與Chr1.2上的MsGPAT5,Chr1.3上的MsGPAT8與Chr1.4上的MsGPAT13均有共線性。此外,存在如Chr1.3的MsGPAT11與Chr7.1上的MsGPAT50和Chr7.4上的MsGPAT59的跨染色體大片段復制現象。
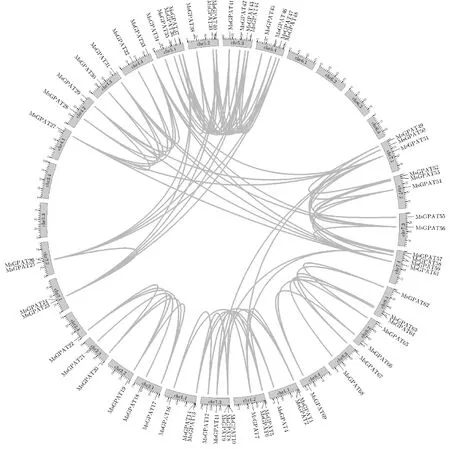
圖5 MsGPAT基因家族共線性分析
2.7 紫花苜蓿MsGPAT基因鹽堿脅迫下的表達模式分析
本研究中共篩選出19個響應鹽堿脅迫的MsGPATs基因,其中共10個MsGPATs基因參與響應單鹽脅迫(圖6),5個MsGPATs基因參與響應單堿脅迫(圖7),18個MsGPATs基因參與響應混合鹽堿脅迫(圖8)。
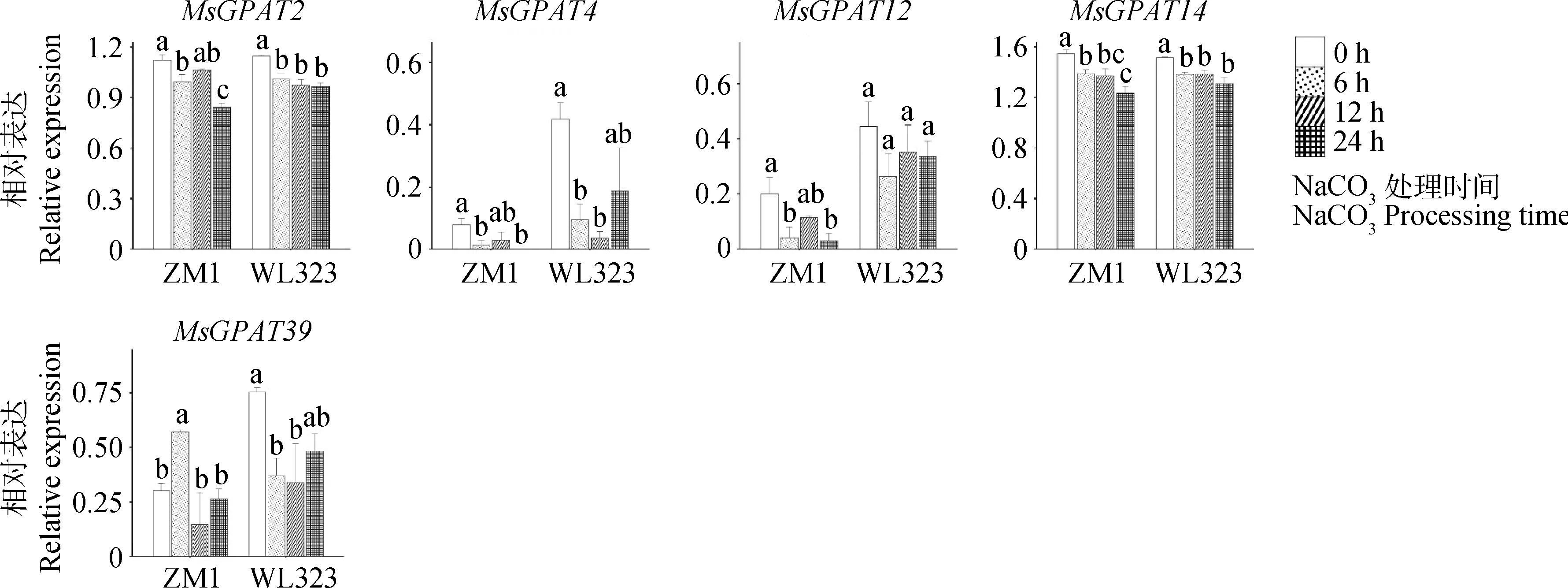
圖7 ‘ZM1’和‘WL323’紫花苜蓿品種MsGPAT基因在堿脅迫下的表達模式
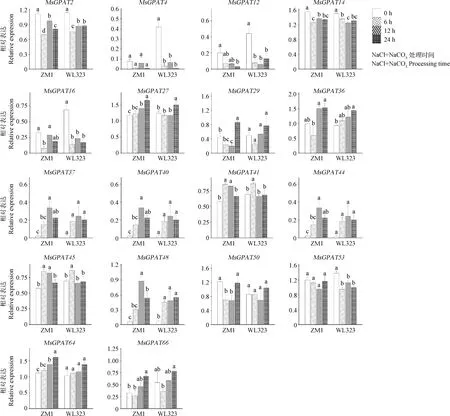
圖8 ‘ZM1’和‘WL323’紫花苜蓿品種MsGPAT基因在混合鹽堿脅迫下的表達模式
單鹽脅迫下,兩紫花苜蓿品種的大部分響應基因表現出大體相似的表達規律,MsGPAT36,37,40,44,48的相對表達量在鹽脅迫后上調,在24 h表達量回落(圖6),呈現出先增高后下降的趨勢;而MsGPAT2,16隨脅迫時間增長呈現先下降后增高的趨勢,低表達量多出現在6~12 h。MsGPAT4,12中耐鹽品種‘ZM1’和敏鹽品種‘WL323’呈現不同的表達趨勢,MsGPAT4在‘ZM1’中的表達量變化不大,而在‘WL323’中的表達量呈顯著下降(P<0.05);MsGPAT12在‘ZM1’中的表達量變化不大,而在‘WL323’中的表達量呈顯著下降(P<0.05),因此可能是調控兩品種耐鹽性差異的關鍵候選基因。
在單堿脅迫下,紫花苜蓿MsGPATs大部分基因相對表達量與0 h相比均有所下調(圖7),且成員數量上也遠小于響應單鹽脅迫的基因成員。其中,MsGPAT2,4,12,14表達量隨鹽脅迫呈下降趨勢(6~12 h)。而MsGPAT39在‘ZM1’中的表達量呈現先升高后下降的趨勢,在與‘WL323’中的表達趨勢相反(圖7),可能是不同紫花苜蓿品種響應堿脅迫的特異基因。
混合鹽堿脅迫下,共有18個MsGPATs基因家族成員的表達量在不同品種或不同脅迫時間下存在差異,其中的大部分成員的表達量隨鹽堿脅迫后上調(圖8),表達量高峰在6~24 h之間均有分布。MsGPAT4,29,37,48,50,53,64在兩品種間表達量存在顯著差異(圖8),如MsGPAT53在‘ZM1’中的表達量變化不大,而在‘WL323’中的表達量在脅迫后顯著下降(P<0.05),MsGPAT64在‘ZM1’中的表達量隨脅迫時間增長呈現顯著上升(P<0.05)的趨勢,而‘WL323’中的表達量在脅迫前后變化不大。因此MsGPAT4,29,37,48,50,53,64可能是調控苜蓿耐鹽堿性的關鍵差異基因。
3 討論
大部分植物GPAT基因的數量未超過30個,例如水稻[11]GPAT基因為26個,玉米(Zeamays)[42]為20個,大豆(Glycinemax)[3]為28個,蒺藜苜蓿為24個[4]。本研究共鑒定出73個紫花苜蓿MsGPAT基因家族成員,其數量約是蒺藜苜蓿的3倍,是目前已研究GPAT家族成員數量最多的植物,可能是由于紫花苜蓿基因組加倍造成的。在bZIP基因家族[28]研究中,紫花苜蓿共鑒定出138個bZIP基因,而蒺藜苜蓿鑒定出75個bZIP基因,紫花苜蓿的bZIP基因大約是蒺藜苜蓿的2倍,與GPAT基因家族數量的變化趨勢一致。此外,也可能是不同的研究方法導致的成員數量有差異。水稻OsGPAT基因家族在較早的研究中為18個成員,而最新的研究中為26個[11]個成員。稍早的研究中,蒺藜苜蓿僅鑒定出12個MtGPAT基因[3],而最新的研究中共鑒定出24個[4],表明研究方法的更新使得研究者可以鑒定出更多的基因家族成員。
系統發育樹中進化距離較近的MsGPAT家族成員的基因結構具有相似的外顯子和內含子數目。除MsGPAT15沒有內含子,其他MsGPATs基因均含有1個或更多數量的內含子或外顯子,即內含子或外顯子數量存在多種形式,表明MsGPATs基因結構在進化過程中的多樣性。其他植物GPAT基因結構也有類似特征,如擬南芥ATS1和AtGPAT9基因均具有12個外顯子,11個內含子,ATGPAT1-8基因具有2~4個外顯子和1~3個內含子的形式。蒺藜苜蓿MtGPATs基因最少含有1個外顯子,無內含子,最多含有14個外顯子和13個內含子的多樣化的基因結構。
紫花苜蓿MsGPAT基因家族成員系統發育樹可分為3個亞組,這與在擬南芥[7]、蒺藜苜蓿[4]、水稻[11]、棉花(Gossypium)[43]和玉米[42]等植物中的GPAT基因家族的研究一致。擬南芥ATS1基因,是一種可溶性GPAT酶,參與葉片脂質合成途徑[13],以酰基載體蛋白ACP為底物[8]。本研究中,共有24個MsGPATs基因與其聚類在一起,且MsGPAT34,38,41,45基因與擬南芥ATS1進化距離最為接近,可能具有生物膜脂質合成[13]的功能。擬南芥AtGPAT1-8,功能與花粉發育、逆境抵抗、角質層和軟木脂合成有關。本研究中,共有34個MsGPATs成員與擬南芥AtGPAT1-8聚類在一起。其中MsGPAT17,23,24,25,26,37,40,44,48與AtGPAT1進化距離最為接近,可能具有相似的功能,與絨氈層磷脂合成和花粉發育有關。AtGPAT4,6,8均與植物角質層合成有關。MsGPAT27,29,31,33,51,54,56,61與AtGPAT6在同一分支,可能參與花器官角質層的合成[44]。MsGPAT36,39,43,47與AtGPAT5,7的進化距離最為接近,可能與根和種皮的軟木脂合成有關[17]。AtGPAT9是參與生物TAG合成的重要GPAT酶,負責植物膜脂和油的合成[45]。過表達的AtGPAT9顯著提升種子中甘油三酯的積累水平,并且與ER甘油酯生物合成的其他酶相互作用。本研究中,共有15個MsGPATs成員與AtGPAT9聚類在一起,且MsGPAT18,21,62,65,67與AtGPAT9處于同一分支,推測其可能具有與AtGPAT9相似的功能。前人研究表明,過表達的AtGPAT6、7可降低幼苗在鹽脅迫下的死亡率,表明二者具有正向調控植物耐鹽性的潛力[19],且AtGPAT2與AtGPAT6類似,與鹽脅迫響應有關[20]。在本研究中,由于MsGPAT4,12,16與AtGPAT2聚類在一起,MsGPAT27,29與AtGPAT6聚類在一起,MsGPAT36,39與AtGPAT7聚類在一起,且在鹽、堿和鹽堿混合脅迫下有一定響應,因此推測以上基因在紫花苜蓿鹽堿脅迫調控中可能具有重要作用,具有提高紫花苜蓿耐鹽堿性的潛力。然而,目前沒有對紫花苜蓿MsGPAT基因家族的具體功能進行研究的報道,因此推測的功能尚待研究驗證。
4 結論
本研究表明,紫花苜蓿MsGPAT基因家族共有73個成員,大多數分布在26條染色體上,呈不均勻分布,另有4個成員分布在scoldfold上。系統發育分析顯示紫花苜蓿基因分為3個亞組。基因結構分析顯示該家族成員外顯子數在1~14之間,其中含有2~3個外顯子的成員和11~12個外顯子的成員最多。蛋白質基序分析顯示motif8是MsGPAT基因家族中最保守的基序。順式作用元件分析顯示MsGPAT基因家族成員大部分含有多種不同數量的光響應、生長素反應和脅迫應答元件。共線性分析表明MsGPAT基因家族大部分成員之間存在大片段復制現象。在18個響應鹽堿脅迫的MsGPAT基因中,大部分成員積極響應單鹽和混合鹽堿脅迫,對單堿脅迫響應的基因較少。其中,MsGPAT4/12和MsGPAT39分別可能是調控紫花苜蓿耐鹽性、堿性的關鍵差異基因。

