基于營養風險篩查下的早期腸內營養支持對食管癌光動力治療后病人營養狀態及腸黏膜屏障功能的影響
張麗娟,王改琳
對處于手術無法切除、無法耐受手術或無法耐受放化療等情況的病人,光動力療法為食管癌病人帶來新的希望。但由于腫瘤組織的蛋白質合成及分解代謝強,增加了病人營養不良風險,且光動力療法亦對機體造成損傷。腸外營養為短時間內補充營養的一種有效方法,可改善食管癌病人的營養不足,但可能出現感染。而營養風險篩查可量化病人營養狀況,利于營養方案的針對性實施[1-4]。研究表明,早期腸內營養可促進食管癌病人術后恢復,改善其生活質量[5]。本研究則在營養風險篩查的基礎上,應用早期腸內營養支持,探究該營養方式對食管癌光動力治療后病人的應用價值,具體如下。
1 資料與方法
1.1 一般資料
選取我院2020年11月—2022年6月收治的105例食管癌光動力治療后病人為研究對象。納入標準:符合食管癌的診斷標準[6];均行光動力治療;病人與家屬簽署知情同意書。排除標準:其他惡性腫瘤;消化道畸形;自身免疫性疾病;認知功能異常。依據營養方式不同分為對照組52例和觀察組53例。對照組:男30例,女22例;年齡46~69(56.83±6.84)歲;初中以下27例,初中及以上25例;鱗癌39例,腺癌13例。觀察組:男32例,女21例;年齡46~69(57.14±5.71)歲;初中以下30例,初中及以上23例;鱗癌41例,腺癌12例。兩組病人基線資料比較差異無統計學意義(P>0.05),具有可比性。本研究經我院醫學倫理委員會審核批準(倫理批號:20201109)。
1.2 干預方法
1.2.1 對照組干預方法
對照組病人給予常規營養支持,持續干預1周。術后予以病人深靜脈置管,行腸外營養,所用營養液經我院營養科醫生配制,依照50 mL/(kg·d)總入液量、104.65 kcal/(kg·d)的非蛋白質熱量、1∶1的糖脂比、150 kcal∶1 g的熱氮比、糖鹽水與中長鏈脂肪乳按照1∶2的比例為病人提供非蛋白質熱量,能量為10~25 kcal/(kg·d),待胃腸功能恢復拔除胃管,由流質飲食逐漸過渡為普食。
1.2.2 觀察組干預方法
觀察組病人給予基于營養風險篩查下的早期腸內營養支持,持續干預1周。依據相關指南[7]于術后 6 h開展腸內營養,將250~500 mL的5%葡萄糖氯化鈉注入營養管;于術后24 h內病人生命體征穩定,20~30 mL/h自鼻腸管通過腸內營養泵恒速灌注腸內營養液,根據其耐受程度逐漸增加營養液輸入量,總輸入量在1 000 mL內;于第2 天以50~60 mL/h的滴速予腸內營養液1 000 mL;于第3 天以80~100 mL/h的滴速予腸內營養液1 500~2 000 mL,達全量;之后不超過125 mL/h予全量腸內營養液。依據總熱量125.52 kJ/(kg·d)計算,初始階段靜脈補充,補充不足的液體量和熱量。依據歐洲腸外腸內營養學會(ESPEN)推薦的2002營養風險篩查簡表(NRS 2002)評分[8],行營養風險篩查,NRS 2002評分不足3分時行上述腸內營養,每隔2 d篩查1次;NRS2002評分不小于3分時依照病人的年齡、體質指數和疾病狀態對其能量需求進行精確計算,靜息狀態能量消耗、食物動力消耗與機體活動消耗之和為每日消耗總能量,對蛋白質、糖類及脂肪比例予合理調整。
1.3 觀察指標
1.3.1 營養狀態
于干預前、干預1周末清晨病人空腹時抽取其2 mL肘靜脈血,分離血清,BK-400型全自動生化分析儀測定前白蛋白(PA)、白蛋白(ALB)及血紅蛋白(Hb)含量。
1.3.2 腸黏膜屏障功能
于干預前、干預1周末抽取病人清晨空腹肘靜脈血3 mL,2 300 r/min離心10 min,取適量血清標本,酶聯免疫法測定二胺氧化酶(DAO)、腫瘤壞死因子α(TNF-α)水平;免疫透射比濁法測定C反應蛋白(CRP)水平。
1.3.3 胃腸道功能
比較兩組病人術后首次肛門排氣時間、首次腸鳴音恢復時間及首次排便時間。
1.4 統計學方法
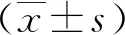
2 結果
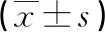
表1 兩組病人干預前、干預1周末營養狀態比較
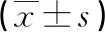
表2 兩組病人干預前、干預1周末腸黏膜屏障功能比較
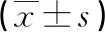
表3 兩組病人胃腸道功能比較
3 討論
3.1 基于營養風險篩查下的早期腸內營養支持可調節營養狀態
臨床上對于不能耐受手術或手術無法切除等類型的食管癌病人常應用光動力療法,但由于癌癥本身引起機體處于高代謝狀態,易引起機體能量過度消耗,造成營養不良[9-11]。常規營養支持可糾正體液丟失及電解質紊亂,可較短時間內糾正機體營養不良狀況,對營養狀態具有一定調節效果[12]。而基于營養風險篩查下的早期腸內營養支持,NRS 2002評分可針對病人情況予以量化評估,精準劃分病人所處的營養風險等級,不僅使得營養方案更具有針對性,且定期篩查可便于及時掌握其營養需求,及時調整營養方案,更高效地進行營養干預;早期進食可對腸道黏膜進行直接作用,改善腸黏膜通透性,加快腸道正常消化吸收功能的恢復進程,加快機體代謝,扭轉機體營養不良狀態[13]。與黃雙雙等[14-15]研究結果一致。本研究結果顯示,觀察組病人干預1周末PA、ALB、Hb水平高于對照組,表明基于營養風險篩查下的早期腸內營養支持可改善營養狀態。
3.2 基于營養風險篩查下的早期腸內營養支持可調節腸黏膜屏障功能
本研究結果顯示,觀察組病人干預1周末DAO、TNF-α、CRP水平低于對照組,表明基于營養風險篩查下的早期腸內營養支持可改善腸黏膜屏障功能。靜脈輸注較為方便,病人易于接受,可較快達到所需熱量,但較長時間應用,易增加腸黏膜萎縮風險,影響腸黏膜屏障功能的調節[16]。而NRS 2002評分的應用可對病人當前營養狀態予以直接評估,便于臨床醫生及時掌握其當前營養水平,利于術后營養干預方案的制訂更具有針對性及目的性,避免長時間禁食增加腸黏膜萎縮風險;當營養液通過消化道黏膜時可興奮腸黏膜感受器,推動腸黏膜生長。早期進食一方面及時為腸黏膜提供營養,提高腸道血液循環速度,利于術后機體應激反應的減輕,避免胃腸道黏膜萎縮,加快腸黏膜屏障功能恢復;另一方面,抑制內生脂肪氧化分解,改善腸道黏膜厚度及絨毛高度,利于胃腸黏膜修復[17]。楊瓊等[18]研究表明,營養篩查下的營養干預可改善病人免疫能力,便于減輕術后應激反應,對腸黏膜屏障功能具有間接改善作用。
3.3 基于營養風險篩查下的早期腸內營養支持可調節胃腸道功能
腸外營養通過靜脈途徑輸注能量和各種營養素,利于維持營養平衡,但長時間應用可使小腸黏膜細胞及營養酶系的活性退化,增加消化道負擔,造成胃腸道功能的調節效果一般[19]。NRS 2002評分具有較高的特異性,可于人群中有效檢出營養風險陽性者,提高臨床護理干預的效率,且其對評估者的專業性沒有過高要求,便于病人更好地理解營養風險篩查的重要性,促使病人更好地配合臨床干預;相對靜脈腸外營養,于早期腸內營養更安全,輸入營養液可刺激腸黏膜,加快腸黏膜的血液循環,提高腸黏膜代謝,促使腸道固有菌群得以維持正常生長,并使消化液以及胃腸道激素的分泌增多,促使胃腸逐漸恢復正常蠕動;且早期腸內營養可對消化道黏膜及時予以有效刺激,增加腸胃動力,加快腸鳴音恢復,促進術后盡早排氣[20]。與何建冰等[21]研究結果相似。本研究結果顯示,觀察組病人術后首次肛門排氣時間、首次腸鳴音恢復時間、首次排便時間短于對照組,表明基于營養風險篩查下的早期腸內營養支持可改善胃腸道功能。
綜上所述,基于營養風險篩查下的早期腸內營養支持可改善食管癌光動力治療后病人營養狀態,調節胃腸道功能,改善腸黏膜屏障功能,療效優于常規營養支持干預。本研究應用ESPEN推薦的NRS 2002評分,對病人當前營養狀況予以精準量化評估,并依據《食管癌病人營養治療指南》行早期腸內營養支持,符合機體生理狀態,利于術后盡早恢復,對食管癌病人的臨床應用干預具有重要的指導意義。但由于研究時間相對較短,入選的樣本數較有限,在所得的結果中可能存在偏倚,應擴大樣本入選量,增加研究時間,以便更深入地研究。

