基于網絡藥理學研究靈芝治療骨質疏松癥的分子機制
馮平,李曉峰,霍樂樂
河南省洛陽正骨醫院(河南省骨科醫院),鄭州 450016
近年來,骨質疏松癥已成為老年人群和絕經后婦女的重要公共衛生問題之一。骨質疏松癥會增加骨折風險,因而在世界范圍內越來越受到重視[1-2]。隨著老齡化進程的加快,我國骨質疏松癥、骨質疏松性骨折的發生率逐年上升。據報道,2016年我國60歲以上人群骨質疏松癥的患病率為36%,估計到2050年將有599萬以上的老年人出現骨質疏松性骨折,給全社會帶來巨大的經濟壓力和醫療負擔[3-4]。因此,迫切需要開發有效的治療策略來干預和治療骨質疏松癥。
中醫藥是中華民族的瑰寶,多味中藥已被證實在治療骨質疏松癥、骨折、類風濕性關節炎等多種骨科相關疾病時具有療效較佳、不良反應較少的優點[5-7]。也有大量的研究表明,有些中藥能夠通過改善腸道對鈣離子的吸收、促進成骨細胞成熟、增強細胞的成骨活性以及抑制破骨細胞的形成來預防和治療骨質疏松癥[8-9]。因此積極尋找具有治療骨質疏松癥作用的中藥并明確其有效成份是當前的研究熱點之一。
靈芝為多孔菌科真菌赤芝Ganodermalucidum(Leyss.ex Fr.)Karst.或紫芝Ganoder-masinenseZhao,Xu et Zhang 的干燥子實體,別名赤芝、木靈芝等,味甘,性平,歸心、肺、肝、腎經,具有補氣安神、止咳平喘的功效。目前已從靈芝中分離并鑒定出靈芝多糖、靈芝酮三醇等400多種化合物。現代藥理學研究表明,靈芝具有免疫調節、降血糖、抗氧化、抗衰老等多種生物學活性[10]。《神農本草經》記載其“利關節,保神,益精氣,堅筋骨……久食輕身不老,延年神仙”[11],提示其在骨質疏松癥等衰老性疾病的治療中有巨大潛力。然而靈芝的藥效物質基礎尚不明確,其抗骨質疏松作用的靶點及機制也有待深入研究,這在一定程度上限制了其在臨床上的推廣和應用。
網絡藥理學是在經典藥理學、計算機技術和生物信息學等多學科交叉融合的基礎上發展起來的一門新興學科,它可以從多個方面系統地研究藥物與人體之間的相互作用及規律。網絡藥理學有助于探索藥物發揮療效的多種作用途徑和(或)信號通路,該策略已被廣泛應用于中醫藥多成份、多靶點、多路徑、多功能研究及中藥配方分析、新藥開發等領域[7]。基于此,本研究通過運用網絡藥理學方法系統地探討了靈芝治療骨質疏松癥的生物學機制,以期為臨床應用提供理論依據。
1 資料與方法
1.1 收集、篩選靈芝的活性成份及作用靶點
利用中藥系統藥理學數據庫與分析平臺(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP,https://tcmsp-e.com/molecule.php?qn=7088),基于吸收、分布、代謝及排泄等藥代動力學參數,以口服生物利用度(oral bioavailability,OB)≥30%、藥 物 相 似 性(drug-likeness,DL)≥0.18為限定條件篩選得到靈芝中的潛在活性成份。將獲得的活性成份輸入PubChem數 據 庫(https://pubchem.ncbi.nlm.nih.gov/)得到其相應的分子結構,并保存為SMILES格式。為了確定靈芝的潛在靶標,將篩選得到的活性成份的SMILES文件逐一輸入Swiss Target Prediction數據庫(http://www.swisstargetprediction.ch/),限定物種為“homo sapiens”,通過整合去重后得到靈芝主要活性成份的預測靶點。應用Uniprot數據庫(https://www.uniprot.org/)對預測的靶點進行人類基因名轉換。
1.2 骨質疏松癥相關靶點的篩選
以“osteoporosis”為關鍵檢索詞,在DisGeNET數據庫(http://www.disgenet.org/)和OMIM數據庫(https://omim.org/)中檢索并篩選骨質疏松癥已知的疾病靶點,整合兩個數據庫的檢索結果并刪除重復靶點,得到已知的與骨質疏松癥密切相關的疾病靶點。
1.3 構建“靈芝活性成份-骨質疏松癥-共同靶點”網絡
將靈芝活性成份與骨質疏松癥的潛在作用靶點導入Cytoscape 3.2.1軟件并構建“靈芝活性成份-骨質疏松癥-共同靶點”可視化網絡。
1.4 構建蛋白質相互作用網絡(protein-protein interaction network,PPI)
通過Bioinformatics and Evolutionary Genomics在線網站(http://bioinformatics.psb.ugent.be/webtools/Venn/)將靈芝主要活性成份的潛在作用靶點與骨質疏松癥已知靶點進行映射取交集,提取共同的靶基因。將共同的靶基因上傳到String數據庫(https://string-db.org/),物種選擇“homo sapiens”,獲取蛋白質相互作用信息,并將結果導入Cytoscape 3.2.1 軟件,構建PPI并進行可視化展示,同時對網絡結構進行拓撲分析。
1.5 靈芝治療骨質疏松癥關鍵靶點通路與功能富集分析
將靈芝中活性成份和骨質疏松癥共同靶點作為關鍵靶點,通過David數據庫(https://david.ncifcrf.gov/),限定物種為“homo sapiens”,對關鍵靶點進行基因本體(gene ontology,GO)分析與京都基因與基因組百科全書(Kyoto encyclopedia of genes and genomes,KEGG)分析,得到共同靶點富集最具顯著性的生物學注釋。其中,GO分析包括生物過程、細胞組分和分子功能,以P<0.01為篩選標準;KEGG分析以P<0.05為篩選標準。
2 結果
2.1 靈芝活性成份及其作用靶點
通過TCMSP數據庫共檢索到靈芝中的242種化學成份,經篩選后得到61種靈芝活性成份。利用Swiss Target Prediction數據庫預測靈芝中所有活性成份的作用靶點,去除無效和重復靶點后,61種活性成份共涉及107個作用靶點。
2.2 靈芝治療骨質疏松癥的潛在作用靶點
通過檢索、合并、去重后共獲得478個骨質疏松癥相關靶點,將其與靈芝活性成份作用靶點相映射并繪制Venn圖(圖1),獲得21個共同靶基因,包 括NR3C1、AR、HSD11B1、PGR、NOS3、CYP19A1、TACR3、CYP17A1、LDLR、ESR1、ESR2、CNR1、CNR2、VDR、HIF1A、NR1I2、MMP1、PTPN11、GC、MAPK1、MAPK3。

圖1 靈芝活性成份作用靶點與骨質疏松癥相關靶點的交集
2.3 “靈芝活性成份-骨質疏松癥-共同靶點”網絡
將靈芝治療骨質疏松癥的活性成份及作用靶點導入Cytoscape 3.2.1軟件,得到“靈芝活性成份-骨質疏松癥-共同靶點”網絡(圖2)。結果表明,β-谷甾醇(beta-sitosterol)、環氧靈芝醇B (epoxyganoderiol B)、環氧靈芝醇C(epoxyganoderiol C)、麥角甾-4,7,22-三 烯-3,6-二 酮(ergosta-4,7,22-trien-3,6-dione)、靈芝酮三醇(ganodermatriol)、靈芝醇A(ganodermenonol)、Lucialdehyde A、Lucialdehyde B能與6個以上的靶點相連接,是靈芝治療骨質疏松癥時的主要活性成份。

圖2 “靈芝活性成份-骨質疏松癥-共同靶點”網絡
2.4 靈芝治療骨質疏松癥的關鍵靶點蛋白
將靈芝與骨質疏松癥映射得到的21個共同靶基因導入String數據庫并繪制靈芝-骨質疏松癥的PPI(圖3)。在PPI中,去除2個孤立蛋白節點后,共有21個節點通過126條邊發生相互作用。通過分析拓撲結構,篩選得到MAPK3、MAPK1、NR3C1、ESR1、AR、CYP19A1、NOS3、HIF1A等共19個靈芝治療骨質疏松癥的關鍵靶點蛋白(表1)。
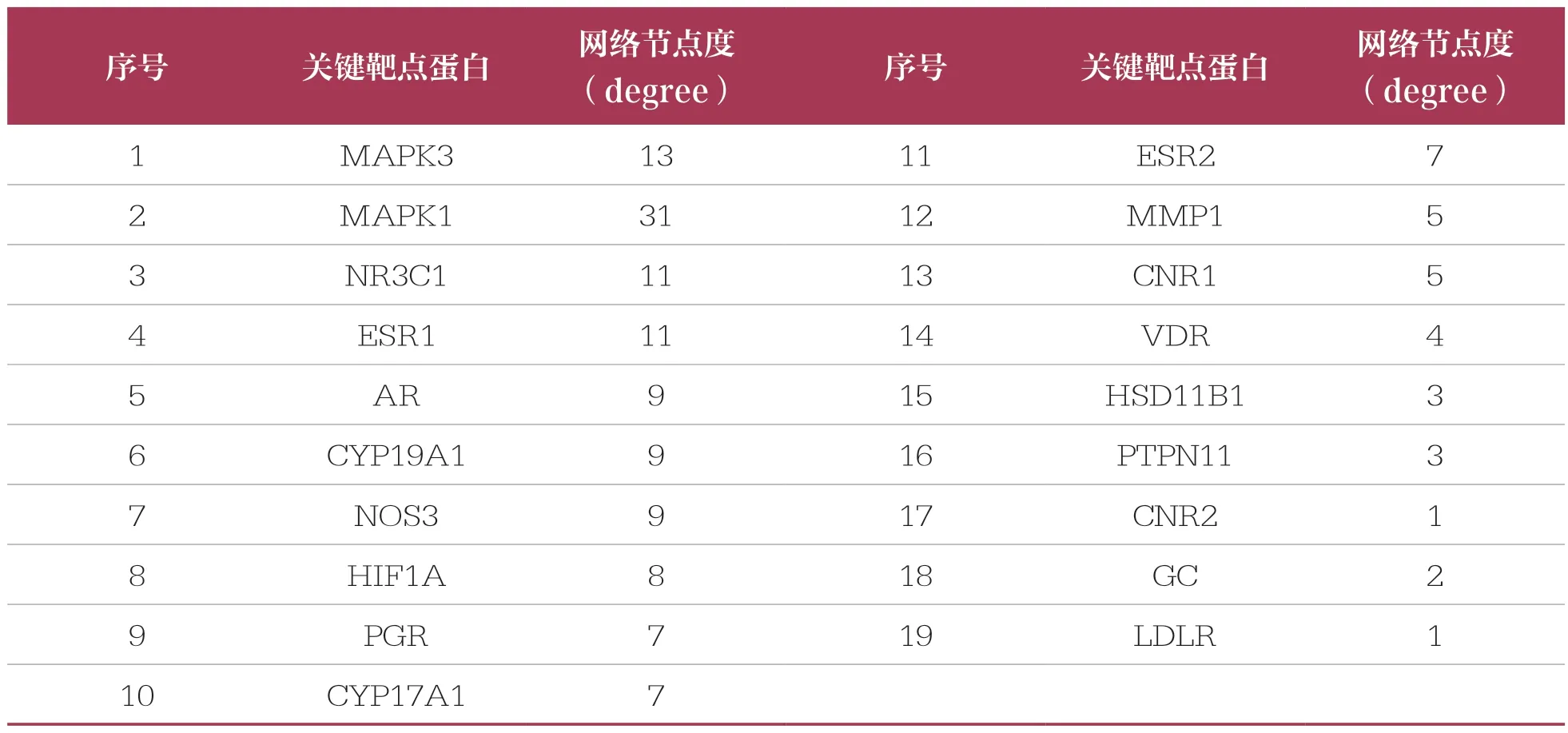
表1 靈芝治療骨質疏松癥的關鍵靶點蛋白

圖3 靈芝-骨質疏松癥的PPI圖
2.5 GO分析和KEGG分析
利用DAVID數據庫對靈芝治療骨質疏松癥的21個共同靶基因進行GO功能富集分析和KEGG通路富集分析。在GO分析中,選取富集程度最高的20個生物過程進行展示(圖4),結果顯示靈芝主要涉及核受體的活性(nuclear receptor activity)、配體激活的轉錄因子活性(ligand-activated transcription factor activity)、類固醇結合(steroid binding)、類固醇激素受體活性(steroid hormone receptor activity)、DNA結合轉錄激活劑活性(DNA-binding transcription activitor activity)、RNA特異性聚合酶Ⅱ(RNA polymerase Ⅱ-specific)等生物過程。

圖4 靈芝活性成份關鍵靶點GO生物過程富集分析
在KEGG分析中,按照P值大小進行排序,選取富集程度最高的前20條信號通路展示(圖5),結果顯示靶基因主要富集在催乳素信號通路(prolactin signaling pathway)、雌激素信號通路(estrogen signaling pathway)、腎細胞癌(renal cell carcinoma)、乳腺癌(breast cancer)等信號通路。

圖5 靈芝活性成份關鍵靶點的KEGG 代謝通路富集分析
3 討論
骨質疏松癥是一種全身性代謝性骨病,其特征在于骨密度降低和脆性骨折風險增加。隨著人類壽命延長和老齡化進程加快,骨質疏松癥已成為重要的健康問題之一[12]。目前臨床上所使用的降鈣素、雙膦酸鹽、雌激素等抗骨質疏松藥物大多數通過抑制破骨細胞活性發揮作用[13],長期應用抗骨質疏松藥物會增加乳腺癌、前列腺癌的患病風險,并易導致下頜骨壞死等不良反應[14]。因此,從中醫藥中尋找能夠有效預防和治療骨質疏松癥的提取物是一種新的治療策略。
靈芝對免疫系統、神經系統、內分泌系統以及心血管系統等都具有調節作用[10]。近年來,不少研究提示靈芝具有抗骨質疏松的作用[15],但靈芝活性成份復雜,其在體內多成份、多靶點、多途徑的藥理特征尚未得到深入研究。本研究利用系統和規范的生物信息學方法來挖掘多種數據庫,整合和分析靶蛋白和化合物的信息,對闡明靈芝抗骨質疏松的作用靶點及分子機制具有重要意義。
在本研究中,基于網絡藥理學方法,通過藥代動力學系統評估、PPI分析以及GO、KEGG分析,初步研究了靈芝治療骨質疏松癥的有效成份和潛在靶點。本研究共篩選得到61種活性成份、107個活性成份可能的作用靶點以及478個骨質疏松癥相關靶點。“靈芝活性成份-骨質疏松癥-共同靶點”網絡分析顯示β-谷甾醇、環氧靈芝醇B、環氧靈芝醇C、麥角甾-4,7,22-三烯-3,6-二酮、靈芝酮三醇、靈芝醇A、Lucialdehyde A、Lucialdehyde B等活性成份能協同作用于多個靶點,表明靈芝在治療骨質疏松癥過程中具有多成份、多靶點交互作用的特性。進一步對21個靈芝治療骨質疏松癥的共同靶基因進行PPI分析,結果表明MAPK3、MAPK1、ESR1、NR3C1、AR、CYP19A1、NOS3、HIF1A在交互網絡中具有最高權重,提示其可能是靈芝治療骨質疏松癥的關鍵靶點蛋白。MAPK3、MAPK1基因編碼的MAPK1和MAPK3屬于蛋白激酶,是MAPK信號通路中的重要分支之一,在細胞增殖、分化中起重要作用。MAPK1/MAPK3與細胞分化及骨形成密切相關。MAPK1/MAPK3被磷酸化后能夠調節成骨分化特異性轉錄因子 RUNX2及其下游OSX基因的表達,上調成骨分化標志物堿性磷酸酶(alkaline phosphatase,ALP)、骨鈣素(osteocalcin,OCN)、骨橋蛋白(osteopontin,OPN)的表達,促進成骨細胞的成熟及基質的礦化[16-17]。雌激素受體(estrogen receptor,ER)屬于核受體超家族,主要存在于細胞核中,通過與雌激素結合而參與多種生理過程的調節。ESR1是ER的一個亞型,在皮質骨中高表達。全基因組關聯研究表明,ESR1基因多態性與骨密度密切相關[18]。糖皮質激素由于具有良好的抗炎作用而被廣泛用于自身免疫性疾病和炎癥性疾病的治療,然而長期過量應用糖皮質激素會抑制成骨細胞分化、促進成骨細胞凋亡從而導致骨質疏松癥。NR3C1能夠編碼糖皮質激素受體,直接影響RANKL啟動子的活性及其轉錄調控,誘導成骨細胞凋亡,導致主要骨重塑途徑RANK/RANKL/OPG軸的失衡,骨吸收增加[19]。KEGG通路富集分析表明,靈芝中的生物活性成份可以通過多種途徑發揮抗骨質疏松作用,其核心靶點主要涉及通路包括催乳素信號通路、雌激素信號通路、腎細胞癌、乳腺癌等。雌激素主要通過與ER結合來發揮其功能和作用,雌激素信號通路通常在骨質疏松癥中出現失調,絕經后女性會由于體內雌激素水平的下降而發生骨重建失衡、骨吸收增加[20]。
綜上所述,本研究應用網絡藥理學篩選了靈芝中的活性成份及其潛在靶點,揭示了靈芝發揮抗骨質疏松作用的潛在機制可能是基于其對潛在靶點和通路的直接或間接調控,體現了靈芝多成份、多靶點、多途徑的治療特點。網絡藥理學為靈芝治療骨質疏松癥提供了新的思路和方向,但仍需相關體外的細胞功能實驗、體內的骨質疏松模型實驗進行驗證。

