電解液添加劑對高電壓LiCoO2/C電池電化學性能的影響
常海濤
(福建南平南孚電池有限公司,福建 南平 353000)
0 引言
電化學儲能技術作為一種高效、清潔的能源轉換技術,對解決快速增長的能源需求和日益突出的環境問題至關重要。鋰離子電池憑借高能量密度、高電勢、寬溫域工作、無記憶效應和使用壽命長等優勢,被廣泛應用于各種領域,如通信、運輸、儲能和航空等[1]。
商業化正極材料的比容量低于負極材料,目前對正極材料的開發仍是鋰離子電池的研究重點。已完成商業化進程的主要正極材料有鈷酸鋰(LiCoO2)、錳酸鋰(LiMn2O4)、磷酸鐵鋰(LiFePO4)、三元材料(NCA、NCM)等[2-7]。其中,LiCoO2正極材料由于能量密度高、加工工藝窗口寬、循環穩定性優良等優勢在便攜式消費電子設備領域中占據了大部分市場。自1991年索尼公司首次實現鋰離子電池的商業化應用以來,伴隨著技術的不斷改革創新,正極LiCoO2搭配負極石墨的電池體系的能量密度由最初的200 Wh/L(80 Wh/kg)跨越式提高至700 Wh/L(280 Wh/kg)。通過如Ti、Mg、Al等各類元素的摻雜,緩解LiCoO2在充電至高電壓下的結構變化[8,9]。此外,通過表面包覆手段,高電壓下過渡金屬元素溶出、電解液分解所帶來的表界面副反應等問題得到改善,LiCoO2電池的實際應用電壓已由最初的4.2 V提高至4.45 V以上[10,11]。
盡管高電壓LiCoO2電池在能量密度方面具有明顯的優勢,但是其在環境溫度適應性上仍存在不少問題。在高溫下充放電循環,正負極與電解液之間的副反應增加,引起材料結構變化并導致電池的內阻增加,從而影響鋰離子電池的循環性能。因此改善高電壓LiCoO2電池的高溫循環性能有著重要意義。在電解液中加入功能添加劑被認為是改善鋰離子電池在常溫和高溫下循環穩定性較經濟有效的策略。然而,高電壓LiCoO2電池(4.2 V以上)相比常規LiCoO2電池(4.2 V)的電化學反應更加復雜,對常規電壓體系行之有效的電解液添加劑對高電壓鈷酸鋰/石墨(LiCoO2/C)電池的改善效果可能一般。本文以高電壓LiCoO2/C電池作為研究對象,選擇不同的添加劑電解液,在常溫及45 ℃高溫充放電循環下,對比電池各方面電化學性能變化,包括充放電行為、循環性能以及阻抗等,探究電解液添加劑對高電壓LiCoO2電池的作用機理。
1 實驗部分
1.1 實驗材料
電解液A和B在珠海生產,基礎鋰鹽及溶劑由LiPF6/EC+PC+PP組成,A組電解液添加劑含有LiDFOB、FEC、PS、ADN,B組除以上四種添加劑外還添加了HTCN。從A組電解液得到的電池記為方案A,從B組電解液得到的電池記為方案B。
正極LiCoO2材料的適用電壓范圍為3.0~4.48 V,壓實密度為4.1 g/cm3。負極為快充型人造石墨,壓實密度為1.7 g/cm3。正負極活性材料參數如表1、表2所示。

表1 正極活性材料參數Table 1 Physical parameters of cathode material
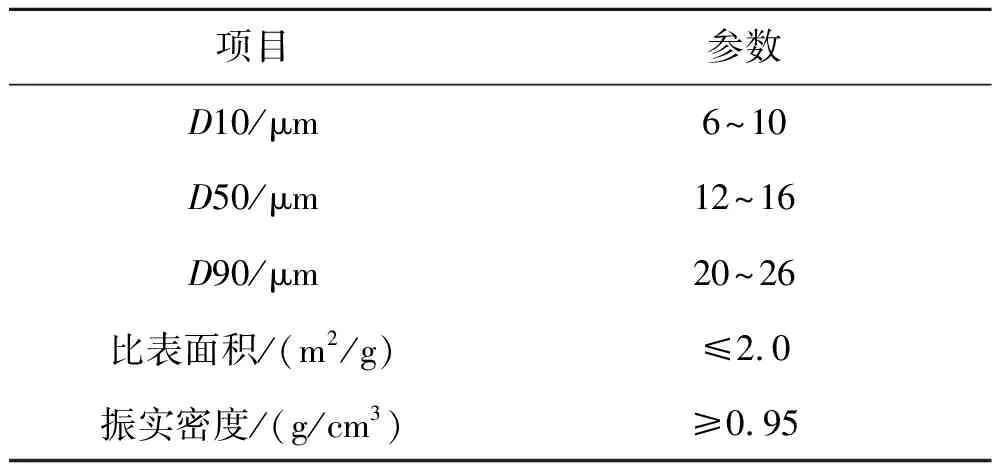
表2 負極活性材料參數Table 2 Physical parameters of anode material
1.2 漿料、正負極片制備及卷芯制備
按照97∶2∶1的質量比分別稱取LiCoO2正極材料、導電劑以及PVDF黏結劑,將材料放入攪拌鍋中進行干粉混合,混合后加入適量NMP,并持續攪拌,制備得到黏度適宜的正極漿料。負極則按照94∶3∶3的質量比分別稱取石墨、導電劑、水性黏合劑制作漿料。按照1.05的N/P設計比,進行正負極涂布,并使用相應的工藝參數對正負極片進行輥壓和分切,得到正負極耳。通過焊接機對正負極耳進行焊接,并卷繞得到直徑12 mm、高度5.4 mm的1254型卷繞電芯。接下來,將電芯送入烘箱烘烤24 h,以去除水分。烘烤結束后,分別注入A、B兩種電解液并封口,然后進行高溫老化。完成高溫老化后,進行分容測試,最后完成1254型電池的制作,并進行相關測試。
1.3 電化學性能測試
使用深圳新威(Neware)電池測試系統,對電池進行不同倍率的充放電和循環測試,電壓測試范圍為3.0~4.48 V。充電模式采用恒流恒壓的方式:在3.0~4.48 V,采用恒流限壓充電;超過4.48 V時,采用恒壓限流方式充電,截止電流為1.5 mA(0.02 C,1 C=75 mA)。倍率充電測試范圍為0.2 C、0.5 C、1 C、2 C、3 C、4 C、5 C。在不同倍率的性能測試中,放電電流都采用0.2 C。交流阻抗測試采用上海辰華CHI760E電化學工作站進行,測試頻率范圍為0.01~100 kHz。
材料的形貌表征通過日本日立公司生產的Flex-1000Ⅱ型掃描電子顯微鏡(SEM)完成;設備配有X射線能量色散譜(EDX),可以對材料進行微區元素分布分析。
2 結果與討論
2.1 電池首次庫侖效率對比
在(25±2) ℃環境溫度下,對比了方案A與方案B兩組各50只電池化成、分容后的首次庫侖效率,如表3所示。方案A中電池的首次庫侖效率均值為86.57%,而在電解液中加入1,3,6-己烷三腈(HTCN)添加劑的方案B電池的首次庫侖效率均值則達到了88.14%,這主要是由于HTCN添加劑具有高抗氧化性,并且與Co離子有強烈的相互作用。在化成充電過程中,HTCN添加劑在正極表面形成了穩定的CEI膜,從而提升了高電壓LiCoO2/C電池的首次庫侖效率[12]。
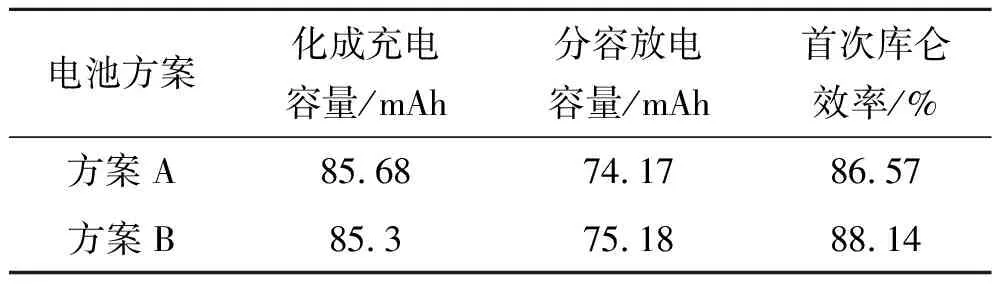
表3 方案A與方案B電池首次庫侖效率對比Table 3 Comparison of the first coulombic efficiency for scheme A and B batteries
2.2 電池的倍率充電性能
將方案A與方案B電池以0.2~5 C電流進行恒流充電至4.48 V,之后以恒壓充電至電流降低至0.02 C,靜置2 h后,以0.2 C電流恒流放電至3.0 V,進行倍率充電性能對比。
如圖1及表4所示,隨著充電電流密度的增加,含有HTCN添加劑的高電壓LiCoO2/C電池在電解液中表現出更高的恒流比和更小的極化現象。在5 C充電倍率下,與未添加HTCN組相比,電池的恒流比提高了12.34%。這表明HTCN添加劑的加入有助于高電壓下鋰離子的高速運輸,并降低電池的極化現象[12]。
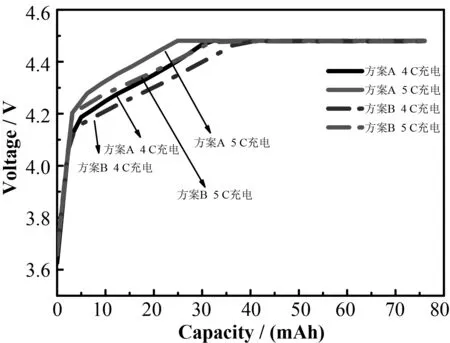
圖1 方案A與方案B電池4 C、5 C倍率充電曲線對比Fig.1 Comparison of 4 C and 5 C charging curves for scheme A and B batteries
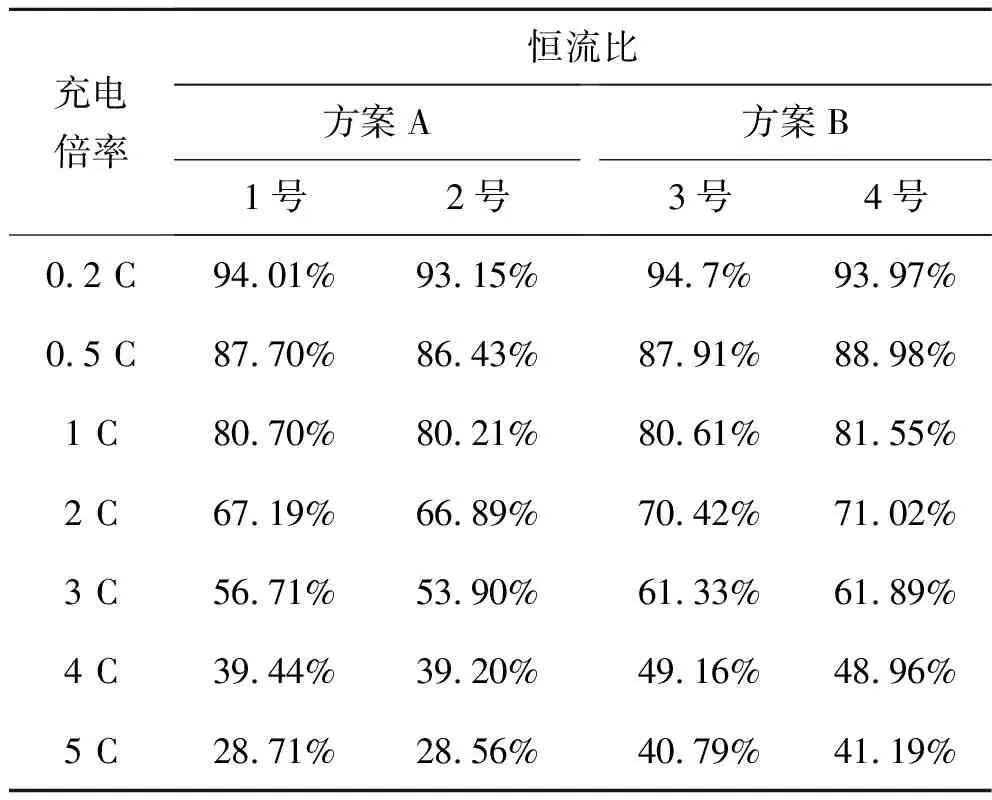
表4 方案A與方案B倍率充電性能恒流比對比Table 4 Comparison of constant current ratio of charging at different rates for scheme A and B
2.3 HTCN添加劑對高電壓LiCoO2/C電池循環性能的影響
如圖2所示,對比了常溫下方案A與方案B電池3 C/0.5 C充放電的循環穩定性,經過300周循環后,方案A電池容量保持率僅為70.99%,而方案B電池容量保持率則高達86.32%。
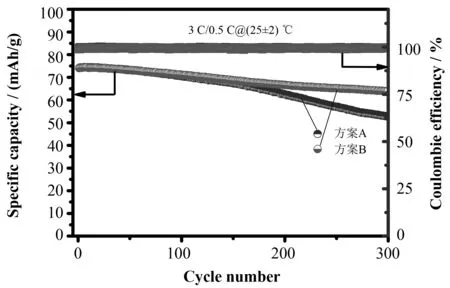
圖2 方案A與方案B常溫下充放電循環性能Fig.2 Cycling performance of scheme A and scheme B at room temperature
如圖3所示,通過SEM檢測循環后的兩組電池正極顆粒表面,可以觀察到以下現象。方案A中電解液不含HTCN添加劑的電池正極顆粒表面有明顯的裂紋[圖3(a)],而方案B中添加HTCN添加劑的電池正極顆粒表面更為光滑,并且未發現有明顯的裂紋[圖3(b)]。這表明HTCN添加劑在高電壓LiCoO2/C電池化成過程中所形成的CEI膜更加穩固,減少了高電壓下電池內部各類副反應對正極顆粒的侵蝕,抑制了材料內部的損傷和裂紋產生,從而提高了電池的循環穩定性[13]。

圖3 循環后LiCoO2顆粒SEM圖像(a)方案A;(b)方案B Fig.3 SEM images of cycled LiCoO2 particles (a) scheme A and (b) scheme B
如圖4所示,進一步對比在45 ℃高溫環境下,方案A與方案B電池3 C/0.5 C充放電的循環穩定性。經過180周循環后,方案A電池容量保持率僅為68.96%,而方案B電池容量保持率則高達91.37%,并且發現,方案A電池的庫侖效率已降低至57.15%,而方案B電池的庫侖效率仍保持在接近100%的水平。通過對高溫循環后脫鋰狀態下負極顆粒表面EDS掃描檢測發現,方案A電池負極顆粒表面檢測到Co的質量分數為0.44%,而方案B電池負極顆粒表面檢測到Co的質量分數為0.11%,具體數據見表5。Co元素的溶出會導致正極結構的坍塌、電解質鹽的不斷分解以及正極CEI膜和負極SEI膜的不斷破裂和生長。這些因素是導致方案A電池在高溫下循環壽命嚴重衰減的主要原因。這進一步證明了HTCN添加劑能夠有效地在正極顆粒表面與電解液之間形成穩固的電極-電解質界面,從而減少高溫高壓循環下Co離子的溶出[14,15]。
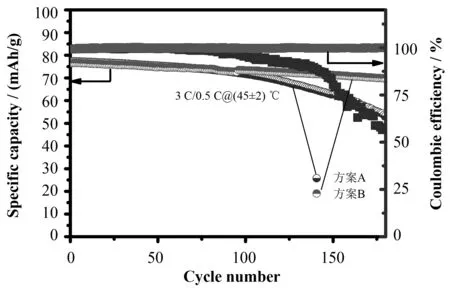
圖4 方案A與方案B在45 ℃下充放電循環性能Fig.4 Cycling performance of scheme A and scheme B at 45 ℃
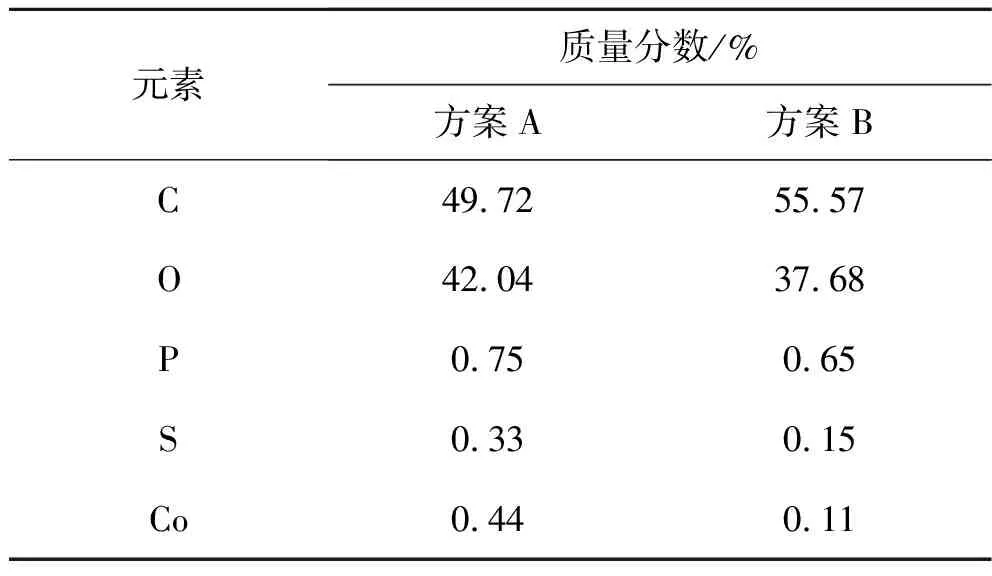
表5 方案A與方案B在45 ℃循環后負極顆粒表面元素含量EDS對比分析Table 5 EDS comparison of surface elements of anode particles for scheme A and B after cycling at 45 ℃
2.4 阻抗分析
進一步對比兩組電池在45 ℃高溫循環后的阻抗。其中,Rs是由電極材料、集流體以及隔膜等構成的接觸電阻,即歐姆電阻;RSEI與C1分別表示Li+穿過SEI膜的阻抗和電容;Rct及C2分別代表電荷轉移電阻和雙電層電容。由圖5及表6數據可看出,兩組電池在45 ℃循環前的歐姆電阻Rs沒有明顯區別。然而,方案A電池在45 ℃循環失效后,接觸電阻Rs的增加幅度明顯高于方案B電池。這意味著在高溫充放電循環過程中,方案A電池的正極材料受到破壞,導致顆粒之間接觸不良,從而使接觸電阻大幅增加。
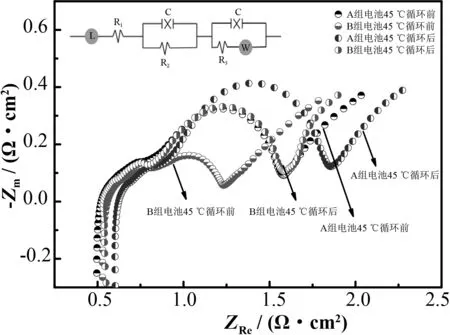
圖5 45 ℃循環前后方案A和方案B電池阻抗圖譜(內嵌圖為等效電路圖)Fig.5 Impedance spectra of scheme A and scheme B before and after cycling at 45 ℃(the embedded diagram is equivalent circuit diagram)
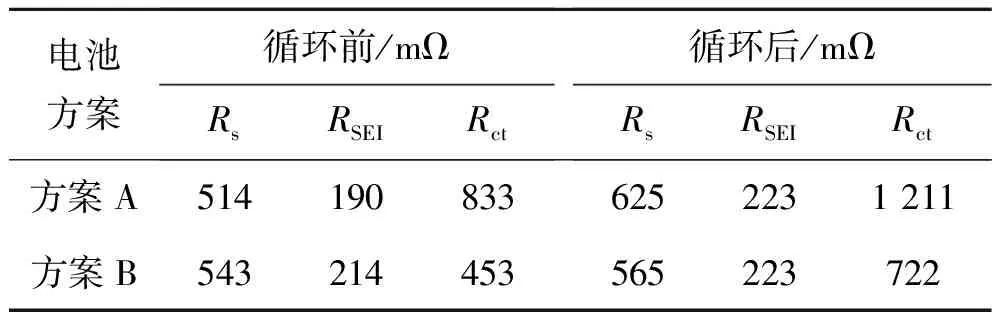
表6 方案A與方案B 45 ℃循環前后電化學阻抗數據Table 6 Electrochemical impedance data of scheme A and B before and after cycling at 45 ℃
同時,方案A電池在高溫循環后RSEI的增加幅度明顯大于方案B電池。這說明經過高溫循環后,方案A電池的正負極與電解液之間發生的副反應較多,表面形成的CEI膜及SEI膜增厚,導致阻抗大幅增大。另外,在高溫循環后,方案B電池的Rct阻抗增加幅度(269 mΩ)也小于方案A電池的Rct阻抗增加幅度(378 mΩ)。這表明HTCN添加劑能優化界面,使其形成的界面膜具有低阻抗和高穩定性的特點,從而減少高溫循環過程中對界面和材料結構的破壞[16-18]。
3 結論
通過對兩組電池常溫循環后的掃描電鏡觀察、高溫循環后負極顆粒表面的EDS測試以及電化學阻抗對比,分析結果表明:在4.48 V高電壓LiCoO2/C電池體系中,HTCN添加劑的加入能夠有效提升電池在常溫及高溫下的循環穩定性。HTCN能夠在高電壓鈷酸鋰電極表面形成穩定的電極-電解質界面,有效減少常溫循環下因LiCoO2材料電極表面的裂紋引起的電解液與界面的副反應,以及高溫循環下Co離子溶出。這樣可以提高高壓LiCoO2電池的電化學性能,對開發具有長循環壽命的高電壓和高溫LiCoO2/C電池具有重要的研究價值。

